文档内容
1.下列叙述或操作正确的是( )
A.浓硫酸具有强氧化性,稀硫酸无氧化性
B.浓硫酸不慎沾到皮肤上,立即用NaOH溶液冲洗
C.稀释浓硫酸时应将水沿着烧杯壁慢慢地注入盛有浓硫酸的烧杯中,并不断搅拌
D.浓硫酸与铜的反应中,浓硫酸不仅表现强氧化性,还表现酸性
2.下列关于鉴别1 mol·L-1稀硫酸和98%的浓硫酸的叙述正确的是( )
A.常温下测定两溶液的导电能力,导电能力强的是浓硫酸
B.常温下可以用铜片鉴别两种溶液
C.常温下不能用铝片鉴别两种溶液
D.两溶液敞口在空气中放置一段时间后质量明显增大的是浓硫酸
3.下列事实的解释错误的是( )
A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B.浓硫酸和浓盐酸混合可制氯化氢,说明浓硫酸具有吸水性
C.常温下能够用铝罐储存浓硫酸,是因为浓硫酸的强氧化性可使铝发生钝化
D.反应:C+2HSO (浓)=====CO↑+2HO+2SO ↑中,HSO 既体现酸性又体现强氧化
2 4 2 2 2 2 4
性
4.硫酸是重要的化工原料,可用于生产化肥、农药、炸药、染料和盐类。下列有关硫及其
化合物的性质与用途具有对应关系的是( )
A.硫具有还原性,可用硫黄处理洒落的汞单质
B.二氧化硫具有氧化性,可用作葡萄酒的抗氧化剂
C.稀硫酸具有酸性,可用于去除铁锈
D.浓硫酸具有脱水性,可用于干燥二氧化硫
5.下列说法正确的是( )
A.蘸有浓硫酸的玻璃棒接近浓氨水瓶口有白烟产生
B.钠、铝、铁、铜在空气中都会氧化变质生成相应的金属氧化物
C.可直接向铜与浓硫酸反应后的溶液中加入水来证明该反应有硫酸铜生成
D.实验室用乙醇和浓硫酸制乙烯、蔗糖遇浓硫酸炭化,两过程中浓硫酸都表现出脱水性
6.某同学设想用如图装置来验证浓硫酸的某些性质,其中不能达到实验目的的是( )
A B C D
实验 吸水性 脱水性 溶解放热 强氧目的
化性
实验
装置
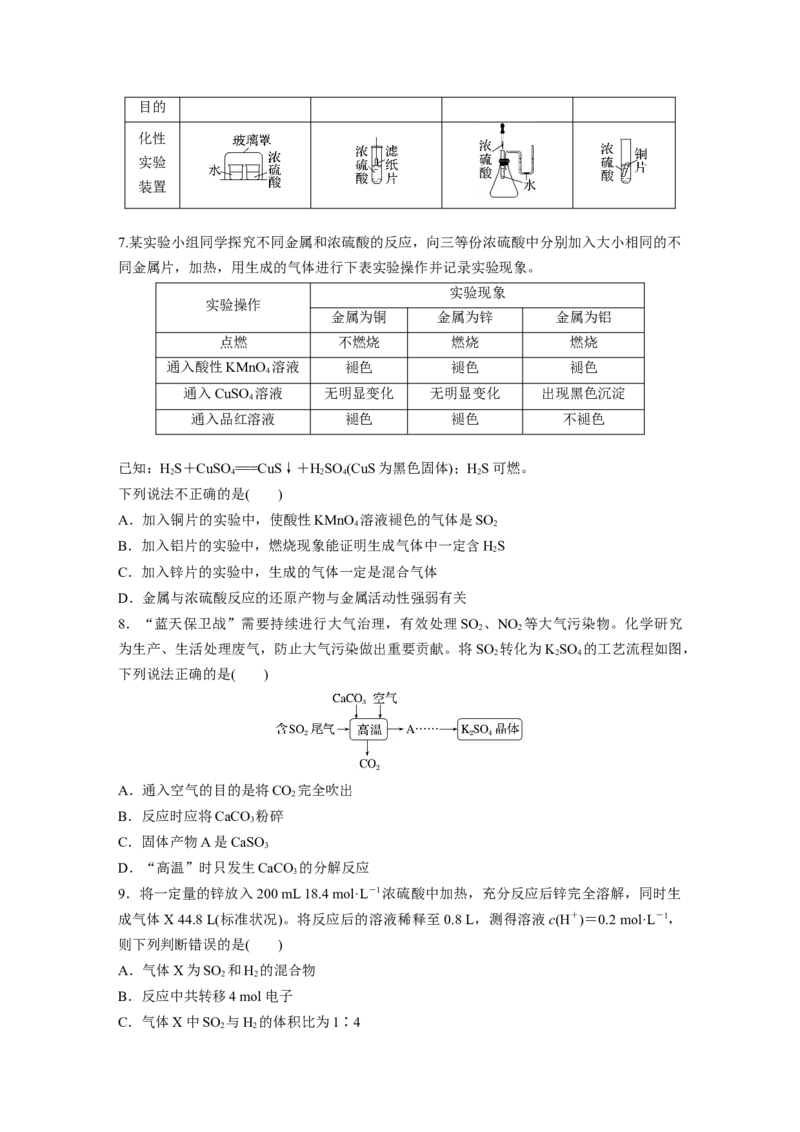
7.某实验小组同学探究不同金属和浓硫酸的反应,向三等份浓硫酸中分别加入大小相同的不
同金属片,加热,用生成的气体进行下表实验操作并记录实验现象。
实验现象
实验操作
金属为铜 金属为锌 金属为铝
点燃 不燃烧 燃烧 燃烧
通入酸性KMnO 溶液 褪色 褪色 褪色
4
通入CuSO 溶液 无明显变化 无明显变化 出现黑色沉淀
4
通入品红溶液 褪色 褪色 不褪色
已知:HS+CuSO ===CuS↓+HSO (CuS为黑色固体);HS可燃。
2 4 2 4 2
下列说法不正确的是( )
A.加入铜片的实验中,使酸性KMnO 溶液褪色的气体是SO
4 2
B.加入铝片的实验中,燃烧现象能证明生成气体中一定含HS
2
C.加入锌片的实验中,生成的气体一定是混合气体
D.金属与浓硫酸反应的还原产物与金属活动性强弱有关
8.“蓝天保卫战”需要持续进行大气治理,有效处理SO 、NO 等大气污染物。化学研究
2 2
为生产、生活处理废气,防止大气污染做出重要贡献。将SO 转化为KSO 的工艺流程如图,
2 2 4
下列说法正确的是( )
A.通入空气的目的是将CO 完全吹出
2
B.反应时应将CaCO 粉碎
3
C.固体产物A是CaSO
3
D.“高温”时只发生CaCO 的分解反应
3
9.将一定量的锌放入200 mL 18.4 mol·L-1浓硫酸中加热,充分反应后锌完全溶解,同时生
成气体X 44.8 L(标准状况)。将反应后的溶液稀释至0.8 L,测得溶液c(H+)=0.2 mol·L-1,
则下列判断错误的是( )
A.气体X为SO 和H 的混合物
2 2
B.反应中共转移4 mol电子
C.气体X中SO 与H 的体积比为1∶4
2 2D.反应中共消耗Zn 130 g
10.将Cu与CuO的混合物20.8 g加入到50 mL 18.4 mol·L-1浓HSO 中,加热充分反应至
2 4
固体物质完全溶解(产生气体全部逸出),冷却后将溶液稀释至1 000 mL,测得c(H+)=
0.84 mol·L-1;若要使稀释后溶液中的Cu2+沉淀完全,应加入6.0 mol·L-1 NaOH溶液的体积
为( )
A.100 mL B.160 mL
C.240 mL D.307 mL
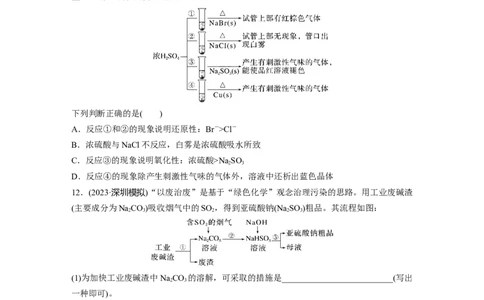
11.下列四支试管中分别盛有固体NaBr、NaCl、NaSO 、Cu,分别向这四支试管中加入适
2 3
量浓硫酸,部分现象如图所示:
下列判断正确的是( )
A.反应①和②的现象说明还原性:Br->Cl-
B.浓硫酸与NaCl不反应,白雾是浓硫酸吸水所致
C.反应③的现象说明氧化性:浓硫酸>Na SO
2 3
D.反应④的现象除产生刺激性气味的气体外,溶液中还析出蓝色晶体
12.(2023·深圳模拟)“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣
(主要成分为NaCO)吸收烟气中的SO ,得到亚硫酸钠(Na SO )粗品。其流程如图:
2 3 2 2 3
(1)为加快工业废碱渣中NaCO 的溶解,可采取的措施是__________________________(写出
2 3
一种即可)。
(2)过程①进行的操作是__________________________________________________________。
(3) 上 述 流 程 中 , 加 入 NaOH 后 , 发 生 反 应 的 化 学 方 程 式 为
______________________________。
(4)亚硫酸钠粗品中含有少量NaSO ,原因是_______________________________________。
2 4
(5)设计实验证明亚硫酸钠粗品中含有少量NaSO 的方案:在一支试管中,加入少量亚硫酸
2 4
钠粗品,用适量蒸馏水溶解,____________________________________________________
_____________________________________________________________________________,
出现白色沉淀,则证明含有NaSO 。
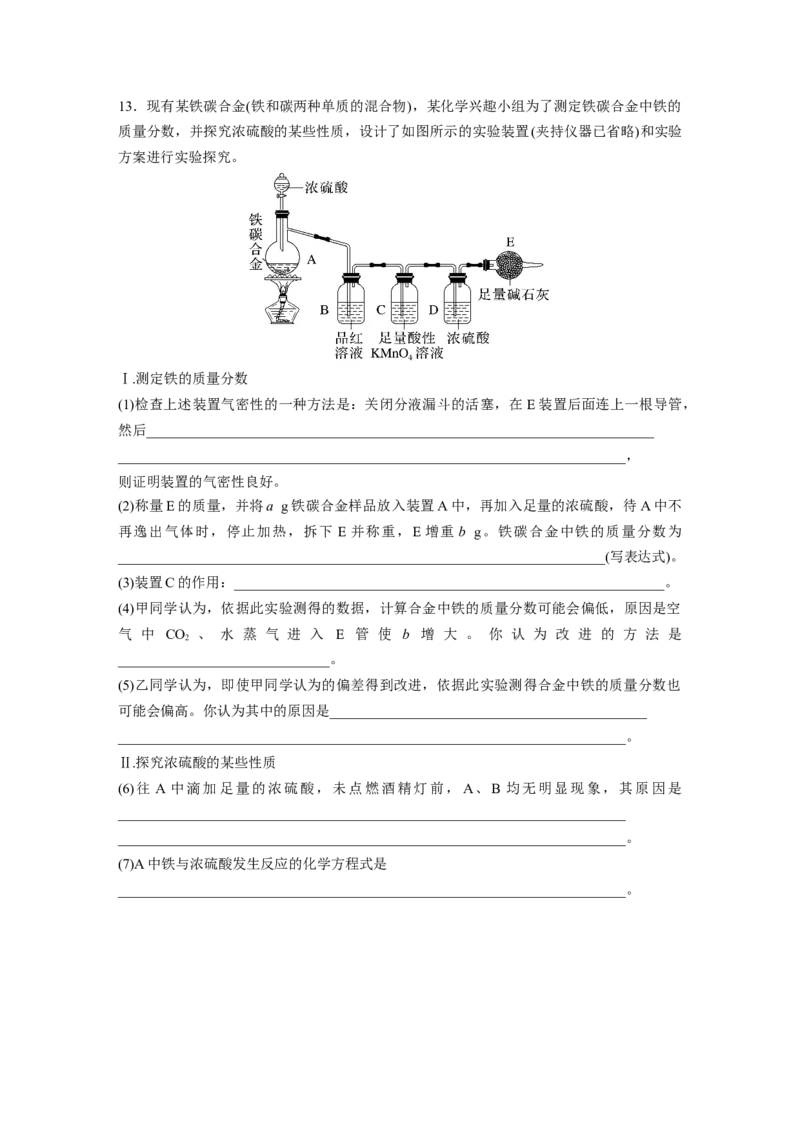
2 413.现有某铁碳合金(铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中铁的
质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置(夹持仪器已省略)和实验
方案进行实验探究。
Ⅰ.测定铁的质量分数
(1)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在E装置后面连上一根导管,
然后________________________________________________________________________
________________________________________________________________________,
则证明装置的气密性良好。
(2)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不
再逸出气体时,停止加热,拆下 E 并称重,E 增重 b g。铁碳合金中铁的质量分数为
_____________________________________________________________________(写表达式)。
(3)装置C的作用:_____________________________________________________________。
(4)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,原因是空
气 中 CO 、 水 蒸 气 进 入 E 管 使 b 增 大 。 你 认 为 改 进 的 方 法 是
2
______________________________。
(5)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分数也
可能会偏高。你认为其中的原因是_____________________________________________
________________________________________________________________________。
Ⅱ.探究浓硫酸的某些性质
(6)往 A 中滴加足量的浓硫酸,未点燃酒精灯前,A、B 均无明显现象,其原因是
________________________________________________________________________
________________________________________________________________________。
(7)A中铁与浓硫酸发生反应的化学方程式是
________________________________________________________________________。