文档内容
第四章 物质结构 元素周期律
第二节 元素周期律 课时作业
第二课时 元素周期表和元素周期律的应用
基础达标
1.下列说法正确的是 ( )
A.在元素周期表中金属与非金属分界线左边的元素均为金属元素
B.Na、Mg、Al的还原性依次减弱
C.F、Cl、Br的非金属性依次增强
D.NaOH、KOH、Mg(OH) 的碱性依次减弱
2
2.运用元素周期律分析下面的推断,其中不正确的是( )
A.锂(Li)与水反应比钠与水反应剧烈
B.氢氧化镁的碱性强于氢氧化铝
C.在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂
D. 的酸性比 的酸性强
3.某元素X的气态氢化物与该元素的最高价氧化物对应的水化物反应生成盐,则该
元素不可能具有的性质是( )
A.在周期表中处于第三周期ⅦA族 B.在周期表中处于第二周期ⅤA族
C.该氢化物比PH 稳定 D.常见化合价有-3、+2、+3、+5等
3
4.部分元素在周期表中的分布如图所示(虚线为金属元素与非金属元素的分界线),下
列说法不正确的是 ( )
A.虚线左侧是金属元素
B.At处于第六周期ⅥA族
C.Si、Ge可作半导体材料
D.As既有金属性又有非金属性
5.某短周期主族元素R的最高正价与最低负价的代数和为4,下列叙述中不正确的是
( )
A.R是第ⅣA族元素 B.R的气态氢化物化学式为HR
2
C.R能形成两种氧化物RO 和RO D.R的气态氢化物的水溶液显酸性
2 3
6.已知砷元素符号为As,原子结构示意图如下,则下列对砷的结构及性质的说法错
误的是( )
A.砷元素的原子序数是33
B.砷的最高价氧化物对应水化物是一种强酸C.三氧化二砷既有氧化性又有还原性
D.砷的非金属性比溴弱
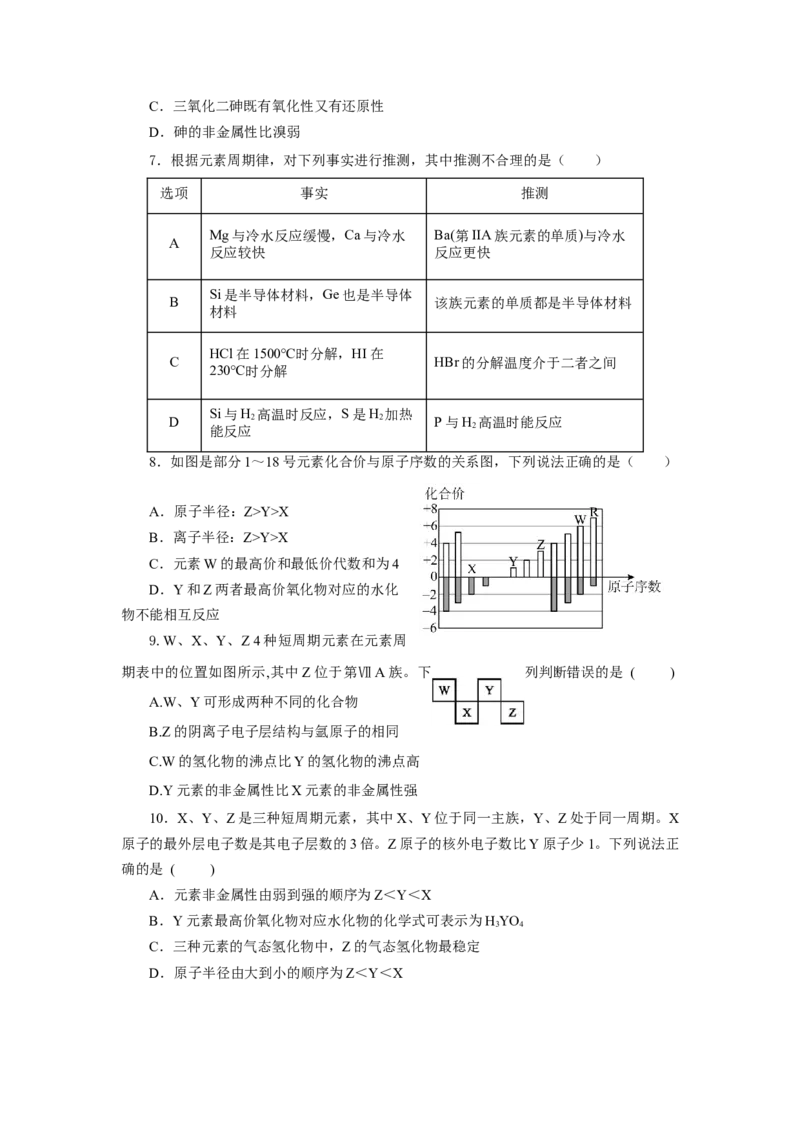
7.根据元素周期律,对下列事实进行推测,其中推测不合理的是( )
选项 事实 推测
Mg与冷水反应缓慢,Ca与冷水 Ba(第IIA族元素的单质)与冷水
A
反应较快 反应更快
Si是半导体材料,Ge也是半导体
B 该族元素的单质都是半导体材料
材料
HCl在1500℃时分解,HI在
C HBr的分解温度介于二者之间
230℃时分解
Si与H 高温时反应,S是H 加热
D 2 2 P与H 高温时能反应
能反应 2
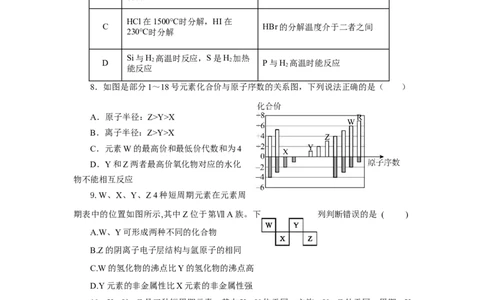
8.如图是部分1~18号元素化合价与原子序数的关系图,下列说法正确的是( )
A.原子半径:Z>Y>X
B.离子半径:Z>Y>X
C.元素W的最高价和最低价代数和为4
D.Y和Z两者最高价氧化物对应的水化
物不能相互反应
9.W、X、Y、Z 4种短周期元素在元素周
期表中的位置如图所示,其中Z位于第ⅦA族。下 列判断错误的是 ( )
A.W、Y可形成两种不同的化合物
B.Z的阴离子电子层结构与氩原子的相同
C.W的氢化物的沸点比Y的氢化物的沸点高
D.Y元素的非金属性比X元素的非金属性强
10.X、Y、Z是三种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X
原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正
确的是 ( )
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为HYO
3 4
C.三种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z<Y<X能力提升
11.碱金属元素钫(Fr)具有放射性。下列对其性质的预言中,不正确的是( )
A.它的金属性比Na强,跟水反应更剧烈
B.它的原子半径比Na大,离子半径也比Na+大
C.它与硫酸铜溶液发生置换反应得到金属铜
D.它的氢氧化物(FrOH)是一种强碱,使酚酞溶液变红
12.X、Y、Z是三种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子
的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的
是 ( )
A.元素非金属性由弱到强的顺序为ZY>Z
13.元素周期表可以指导人们进行规律性的推测和判断,下列说法不正确的是( )
A.若 X2+和 Y-的核外电子层结构相同,则原子序数:a=b+3
a b
B.由水溶液的酸性:HCl>HF,可推断出元素的非金属性:Cl>F
C.锗与硅位于金属元素与非金属元素的分界处,都能作半导体材料
D.S和Se分别位于第ⅥA的第三、四周期,则氢化物的热稳定性:H S>HSe
2 2
14.如图是元素周期表的一部分,回答下列问题:
(1)元素Ga在元素周期表中的位置为:第
_______周期第_______族。
(2)Sn的最高正价为_______,Cl的最高价氧化
物对应的水化物的化学式为____________,Bi的最
高价氧化物的化学式为___________________。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
_______(填元素符号)。
②H AsO 、HSeO 的酸性强弱:HAsO _______HSeO(填“>”或“<”下同)。
3 4 2 4 3 4 2 4
③氢化物的还原性:HO_______H S。
2 2直 击 高 考