文档内容
第二节 元素周期律
第2课时 元素周期表和元素周期律的应用
基础巩固
1.关于元素周期表和元素周期律的应用有如下叙述,其中正确的是( )。
①元素周期表是学习化学知识的一种重要工具;②利用元素周期表可以预测新元素的原子结构和性质;③利
用元素周期表和元素周期律可以预言新元素;④利用元素周期表可以指导人们寻找某些特殊的材料。
A.①②③④ B.②③④ C.③④ D.①②
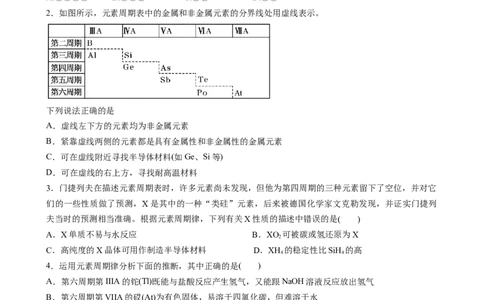
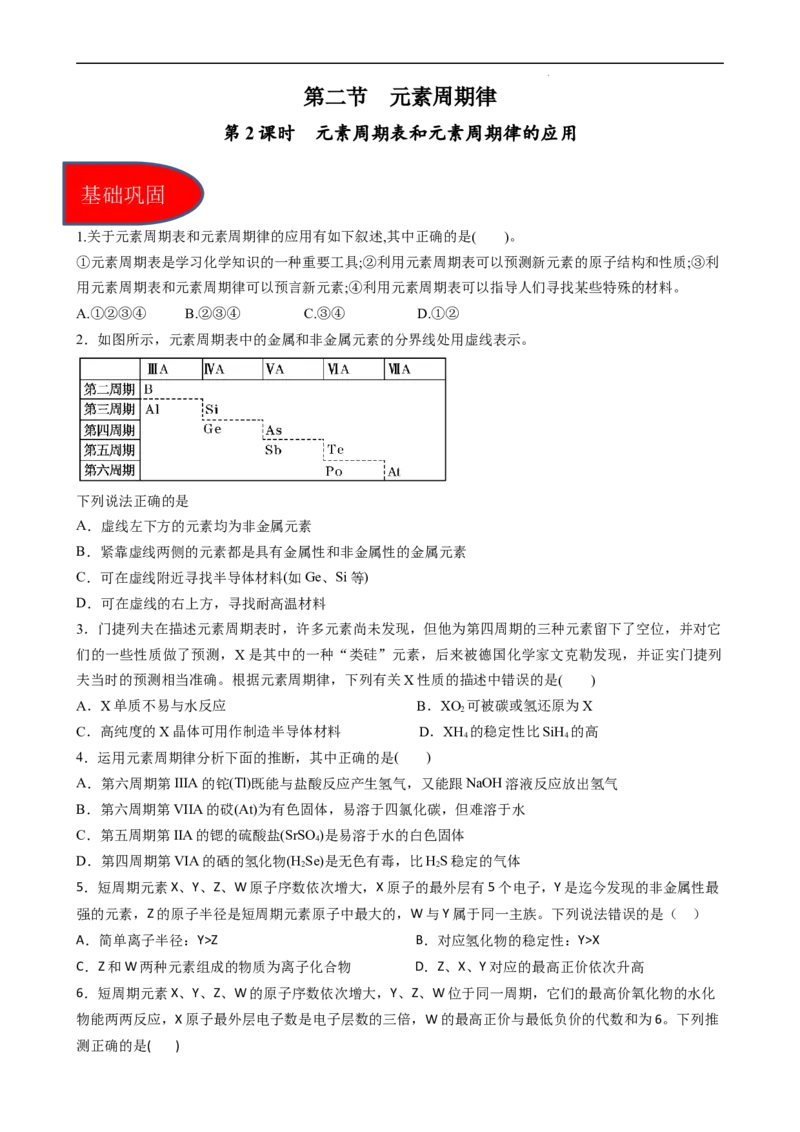
2.如图所示,元素周期表中的金属和非金属元素的分界线处用虚线表示。
下列说法正确的是
A.虚线左下方的元素均为非金属元素
B.紧靠虚线两侧的元素都是具有金属性和非金属性的金属元素
C.可在虚线附近寻找半导体材料(如Ge、Si等)
D.可在虚线的右上方,寻找耐高温材料
3.门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它
们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列
夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是( )
A.X单质不易与水反应 B.XO 可被碳或氢还原为X
2
C.高纯度的X晶体可用作制造半导体材料 D.XH 的稳定性比SiH 的高
4 4
4.运用元素周期律分析下面的推断,其中正确的是( )
A.第六周期第IIIA的铊(Tl)既能与盐酸反应产生氢气,又能跟NaOH溶液反应放出氢气
B.第六周期第VIIA的砹(At)为有色固体,易溶于四氯化碳,但难溶于水
C.第五周期第IIA的锶的硫酸盐(SrSO )是易溶于水的白色固体
4
D.第四周期第VIA的硒的氢化物(H Se)是无色有毒,比HS稳定的气体
2 2
5.短周期元素X、Y、Z、W原子序数依次增大,X原子的最外层有5个电子,Y是迄今发现的非金属性最
强的元素,Z的原子半径是短周期元素原子中最大的,W与Y属于同一主族。下列说法错误的是( )
A.简单离子半径:Y>Z B.对应氢化物的稳定性:Y>X
C.Z和W两种元素组成的物质为离子化合物 D.Z、X、Y对应的最高正价依次升高
6.短周期元素X、Y、Z、W的原子序数依次增大,Y、Z、W位于同一周期,它们的最高价氧化物的水化
物能两两反应,X原子最外层电子数是电子层数的三倍,W的最高正价与最低负价的代数和为6。下列推
测正确的是( )
学科网(北京)股份有限公司A.Y、Z、W三种元素的简单离子半径:Y>Z>W B.X与Y可形成Y X 和Y X两种离子化合物
2 2 2
C.W元素最高价氧化物对应水化物的化学式为H WO D.Y、Z单质的还原性:Z>Y
2 4
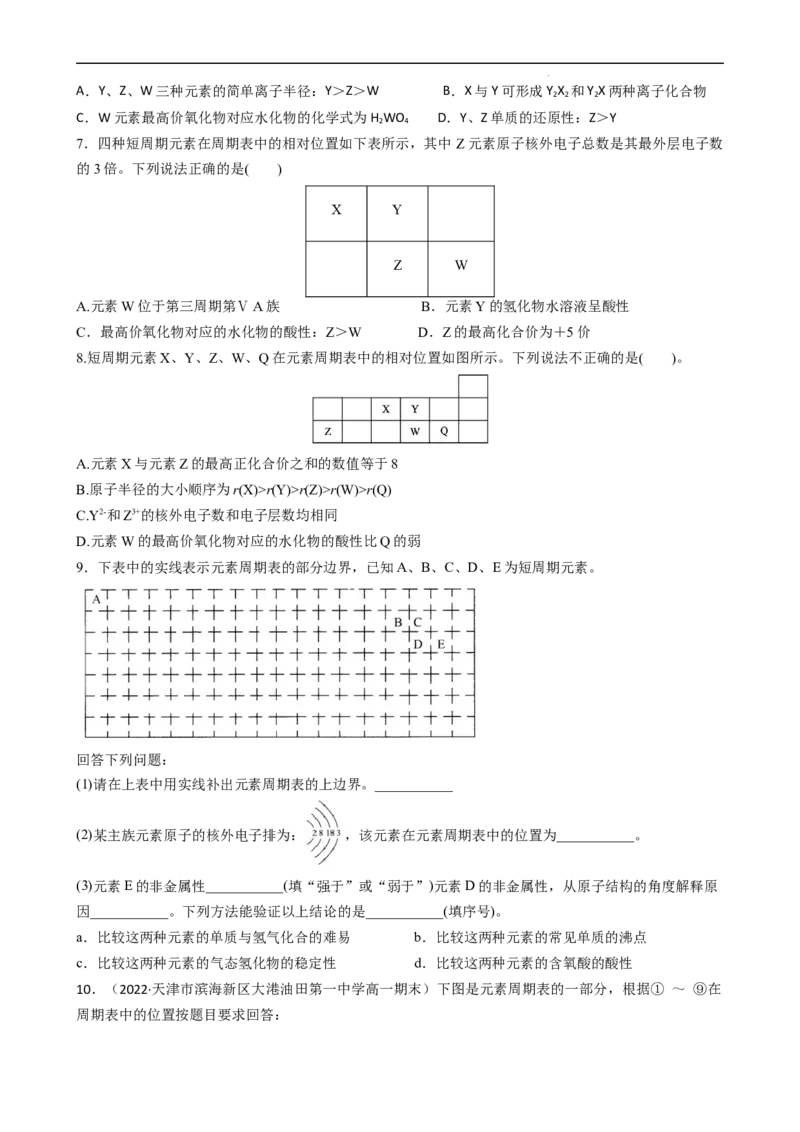
7.四种短周期元素在周期表中的相对位置如下表所示,其中 Z元素原子核外电子总数是其最外层电子数
的3倍。下列说法正确的是( )
X Y
Z W
A.元素W位于第三周期第ⅤA族 B.元素Y的氢化物水溶液呈酸性
C.最高价氧化物对应的水化物的酸性:Z>W D.Z的最高化合价为+5价
8.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是( )。
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为r(X)>r(Y)>r(Z)>r(W)>r(Q)
C.Y2-和Z3+的核外电子数和电子层数均相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的弱
9.下表中的实线表示元素周期表的部分边界,已知A、B、C、D、E为短周期元素。
回答下列问题:
(1)请在上表中用实线补出元素周期表的上边界。___________
(2)某主族元素原子的核外电子排为: ,该元素在元素周期表中的位置为___________。
(3)元素E的非金属性___________(填“强于”或“弱于”)元素D的非金属性,从原子结构的角度解释原
因___________。下列方法能验证以上结论的是___________(填序号)。
a.比较这两种元素的单质与氢气化合的难易 b.比较这两种元素的常见单质的沸点
c.比较这两种元素的气态氢化物的稳定性 d.比较这两种元素的含氧酸的酸性
10.(2022·天津市滨海新区大港油田第一中学高一期末)下图是元素周期表的一部分,根据① ~ ⑨在
周期表中的位置按题目要求回答:
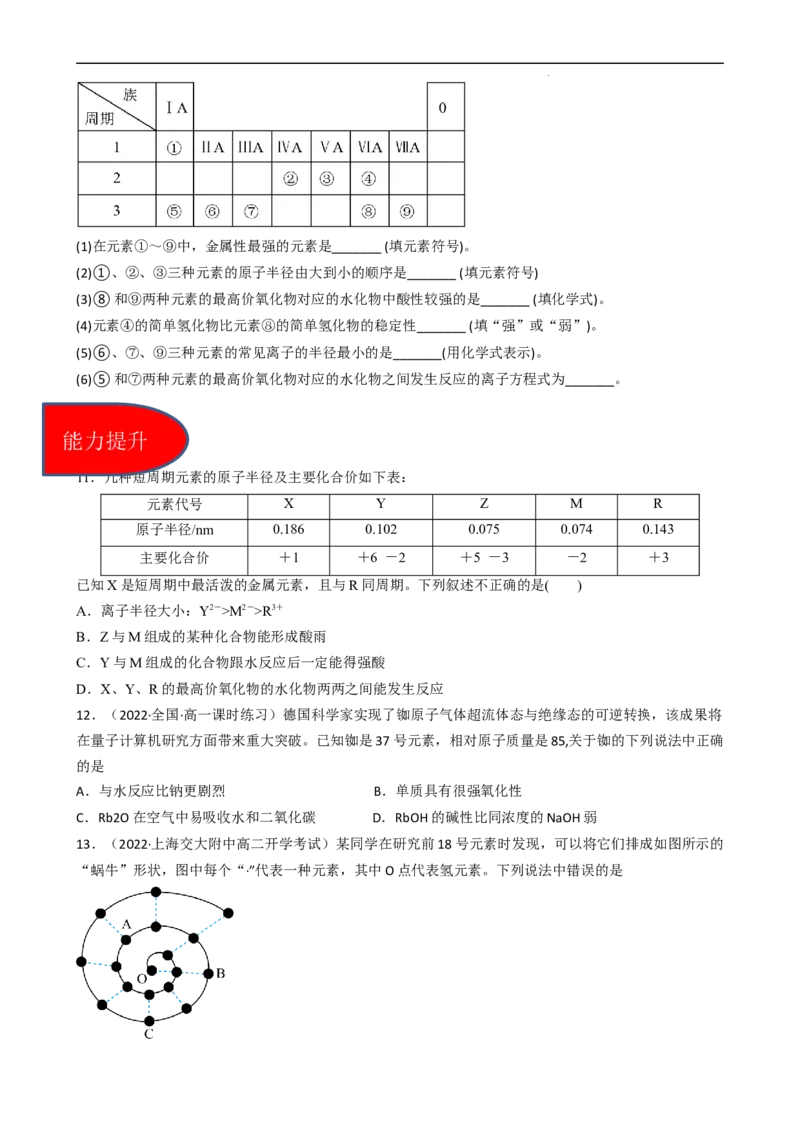
学科网(北京)股份有限公司(1)在元素①~⑨中,金属性最强的元素是_______ (填元素符号)。
(2)①、②、③三种元素的原子半径由大到小的顺序是_______ (填元素符号)
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是_______ (填化学式)。
(4)元素④的简单氢化物比元素⑧的简单氢化物的稳定性_______ (填“强”或“弱”)。
(5)⑥、⑦、⑨三种元素的常见离子的半径最小的是_______(用化学式表示)。
(6)⑤和⑦两种元素的最高价氧化物对应的水化物之间发生反应的离子方程式为_______。
能力提升
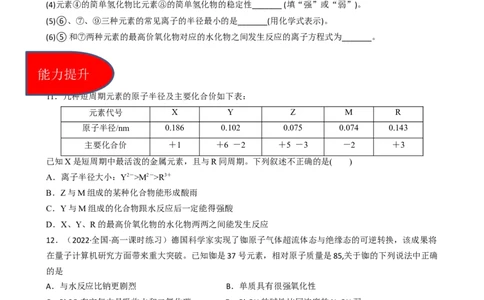
11.几种短周期元素的原子半径及主要化合价如下表:
元素代号 X Y Z M R
原子半径/nm 0.186 0.102 0.075 0.074 0.143
主要化合价 +1 +6 -2 +5 -3 -2 +3
已知X是短周期中最活泼的金属元素,且与R同周期。下列叙述不正确的是( )
A.离子半径大小:Y2->M2->R3+
B.Z与M组成的某种化合物能形成酸雨
C.Y与M组成的化合物跟水反应后一定能得强酸
D.X、Y、R的最高价氧化物的水化物两两之间能发生反应
12.(2022·全国·高一课时练习)德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将
在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85,关于铷的下列说法中正确
的是
A.与水反应比钠更剧烈 B.单质具有很强氧化性
C.Rb2O在空气中易吸收水和二氧化碳 D.RbOH的碱性比同浓度的NaOH弱
13.(2022·上海交大附中高二开学考试)某同学在研究前18号元素时发现,可以将它们排成如图所示的
“蜗牛”形状,图中每个“·”代表一种元素,其中O点代表氢元素。下列说法中错误的是
学科网(北京)股份有限公司A.离O点越远的元素原子半径越大 B.虚线相连的元素处于同一族
C.B元素是图中金属性最强的元素 D.A、B组成的化合物中可能含有共价键
14.镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素。镓的原子序数为 31,
属ⅢA族。镓的熔点为29.78 ℃,沸点高达2 403 ℃。镓有过冷现象(即冷至熔点下不凝固),它可过冷到
-120 ℃。由此判断下列有关镓的性质及其用途的叙述不正确的是( )
A.镓是制造高温温度计的上佳材料
B.镓能溶于强酸和强碱中
C.镓与锌、锡、铟等金属制成的合金,可用在自动救火的水龙头中
D.近年来镓成为电子工业的新宠,其主要用途是制造半导体材料,被誉为“半导体家族的新成员”,这
是利用了镓的导电性介于导体和绝缘体之间的性质
15.(2022·全国·高一课时练习)联合国大会将2019年定为“化学元素周期表国际年”,表明了元素周
期律的重要性。以下短周期主族元素中,含元素a的化合物被广泛用于制作手机电池,古迪纳夫因在该领
域做出了杰出贡献荣获2019年诺贝尔化学奖。
a … b c d
e … g h j
(1)a原子结构示意图为_______。
(2)d在周期表中的位置是_______。
(3)元素g的单质与NaOH溶液反应的离子方程式为_______。
(4)由单质a制成的电池需要注意防水,其原因用化学反应方程式表示为_______。
(5)科学家在研究元素周期表时,预言了在元素h的下一周期存在一种“类h”元素,该元素多年后被德国
化学家文克勒发现,命名为锗(Ge),锗在周期表的位置为_______。
(6)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”、Mc可由反应 Am+ Ca→Mc+3
n得到。Mc用核素符号表示为_______。
学科网(北京)股份有限公司学科网(北京)股份有限公司