文档内容
第四章《化学反应与电能》导学案
第二节 电解池
第一课时 电解池
【学习目标】
1.掌握电解池的基本原理和概念,包括阴阳极反应类型等应用;
2.理解离子移动和电极反应过程,包括微观粒子的运动和电极反应的微观解释;
3.培养实验安全意识和环保意识,注重实验操作规范;
4.通过实验演示和案例分析,增强学生对电解池的理解和记忆;
【学习重难点】
重点:理解电解池的工作原理:即电流通过电解质溶液时,在阴阳两极上发生的氧化还原
反应。这需要学生具备基本的电化学知识。
难点:掌握阴、阳极反应过程:电解池的阴阳极反应复杂,涉及到氧化还原反应的原理,
并能够根据实际情况进行判断和书写。
【课前预习】
旧知回顾
二次电池(铅酸蓄电池)
1.二次电池又称可充电电池或蓄电池,放电后可以再充电使活性物质获得再生,是一类放
电后可以再充电而反复使用的电池。
2.铅酸蓄电池的构成;
铅酸蓄电池是一种常见的二次电池,深灰色所示的正极板,板上覆盖有二氧化铅。浅
灰色所示的负极板上覆盖有铅单质。硫酸作为电解质溶液。
2.正负极分判断:铅蓄电池是最常见的二次电池,负极材料是Pb,正极材料是PbO 。
2
3.二次电池的充电规律
a.充电时电极的连接:充电的目的是使电池恢复其供电能力,是原电池的逆反应,因此负
极应与电源的负极相连得电子,称阴极,正极接电源的正极后作阳极。
b.工作时的电极反应式:同一电极上的电极反应式,在充电与放电时,形式上恰好是相反
的;同一电极周围的溶液,充电与放电时pH的变化趋势也恰好相反。
4.图解二次电池的的工作原理5.电极反应式的书写
①放电时的反应
负极:_____________________________
正极:_____________________________
总反应式:Pb(s)+PbO (s)+2HSO (aq) ==2PbSO (s)+2HO(l)
2 2 4 4 2
②充电时的反应
阴极:______________________________
阳极:______________________________
总反应:2PbSO + 2HO === Pb + PbO +4H+ +
2SO2-
4 2 2 4
【总结】铅酸蓄电池是二次可充电电池,引导学生熟悉铅酸蓄电池的整体工作原理的总反应式。
Pb(s)+PbO (s)+2HSO (aq) 2PbSO (s)+2HO(l)
2 2 4 4 2
【课中探究】
情境导入:解密电解水骗局
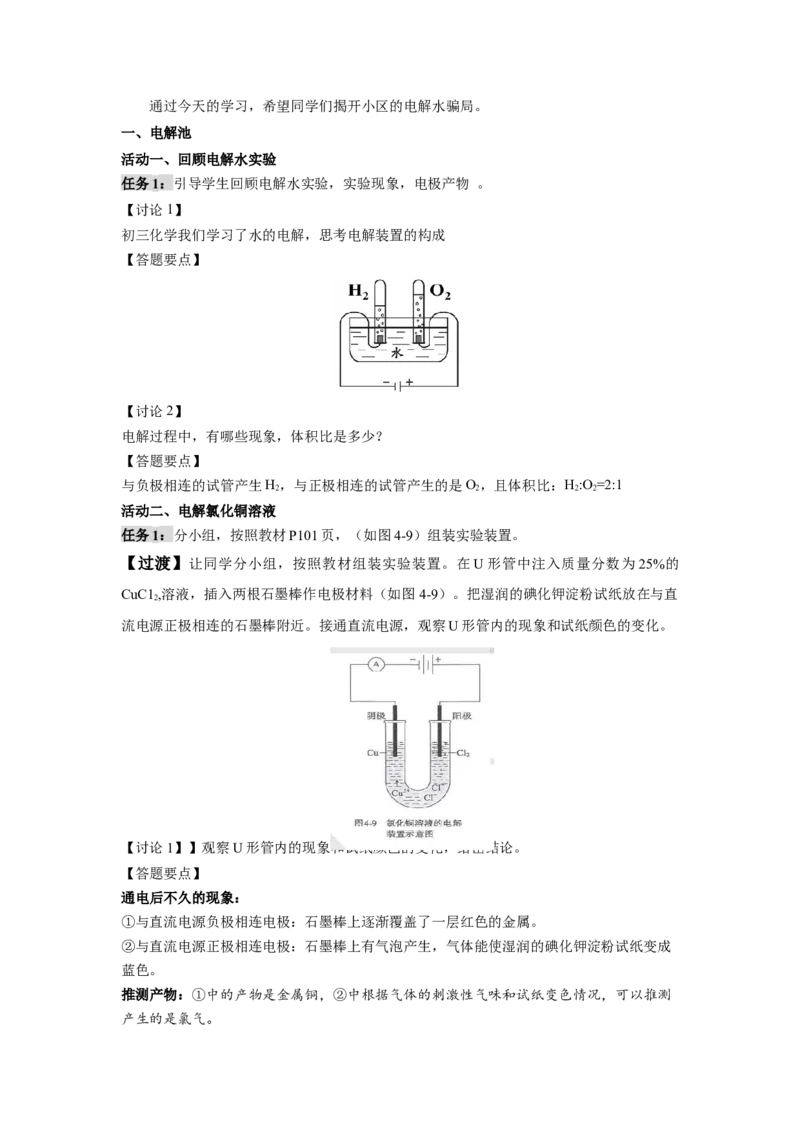
随着生活品质的提高,现在每个家庭对饮用水也有了严格的标准,所以市场上出现了
琳琅满目的各种净水器,价位不等,形式各样,为我们提供了很多的选择,下图是我们常
见的几个类型的净水器。
由于净水器的价位不同,选择过多,也被一些不良商家钻了空子。但也有些不良商家
在小区内推销自制,无品牌的净水器。电解两杯不同的水,一杯是自来水,一杯是通过商
家净水器净化后的饮用水。实验的现象是,没有净化的自来水出现了严重的污浊,而通过
商家净化后的水仍是清澈的。
这是为什么呢?难道是我们的自来水真的这么不堪吗?通过今天的学习,希望同学们揭开小区的电解水骗局。
一、电解池
活动一、回顾电解水实验
任务1:引导学生回顾电解水实验,实验现象,电极产物 。
【讨论1】
初三化学我们学习了水的电解,思考电解装置的构成
【答题要点】
【讨论2】
电解过程中,有哪些现象,体积比是多少?
【答题要点】
与负极相连的试管产生H,与正极相连的试管产生的是O,且体积比:H:O =2:1
2 2 2 2
活动二、电解氯化铜溶液
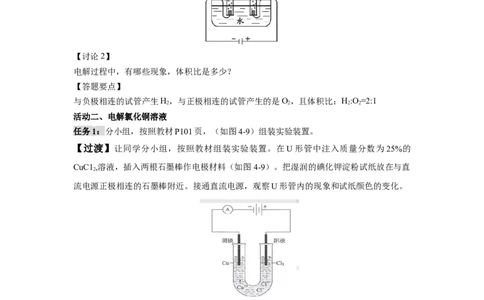
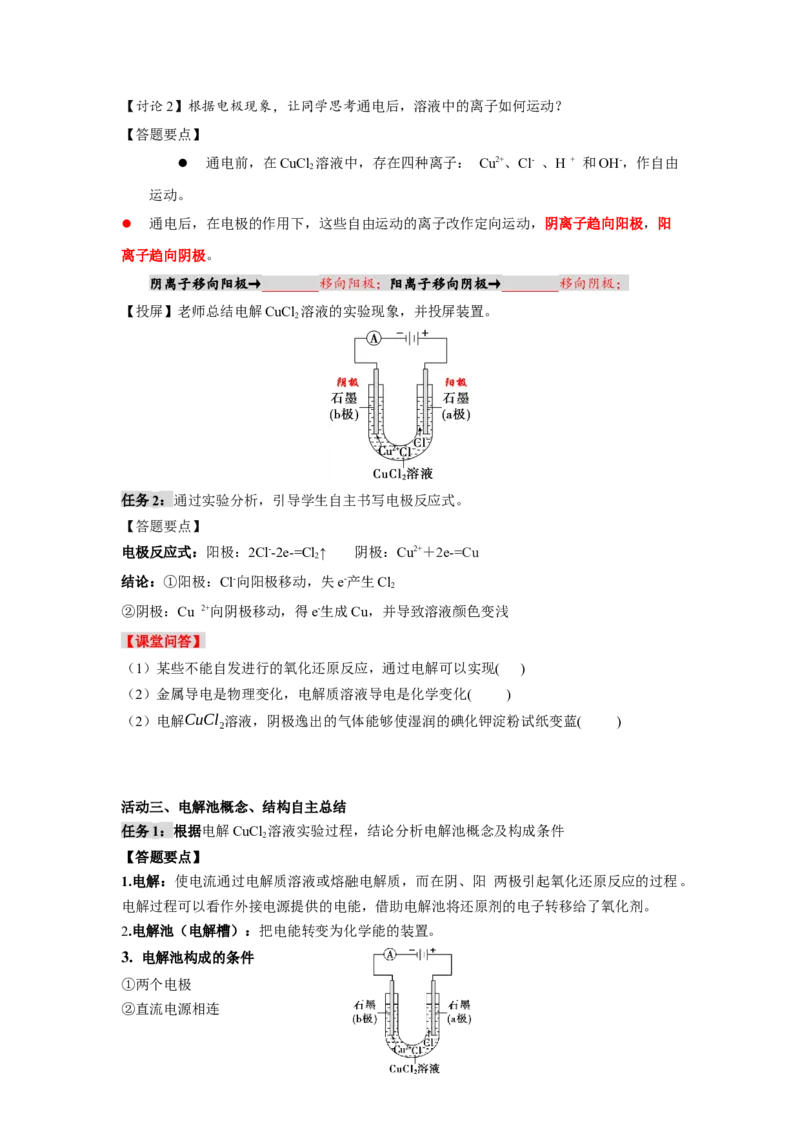
任务1:分小组,按照教材P101页,(如图4-9)组装实验装置。
【过渡】让同学分小组,按照教材组装实验装置。在U形管中注入质量分数为25%的
CuC1 ,溶液,插入两根石墨棒作电极材料(如图4-9)。把湿润的碘化钾淀粉试纸放在与直
2
流电源正极相连的石墨棒附近。接通直流电源,观察U形管内的现象和试纸颜色的变化。
【讨论1】】观察U形管内的现象和试纸颜色的变化,给出结论。
【答题要点】
通电后不久的现象:
①与直流电源负极相连电极:石墨棒上逐渐覆盖了一层红色的金属。
②与直流电源正极相连电极:石墨棒上有气泡产生,气体能使湿润的碘化钾淀粉试纸变成
蓝色。
推测产物:①中的产物是金属铜,②中根据气体的刺激性气味和试纸变色情况,可以推测
产生的是氯气。【讨论2】根据电极现象,让同学思考通电后,溶液中的离子如何运动?
【答题要点】
通电前,在CuCl 溶液中,存在四种离子: Cu2+、Cl- 、H + 和OH-,作自由
2
运动。
通电后,在电极的作用下,这些自由运动的离子改作定向运动,阴离子趋向阳极,阳
离子趋向阴极。
阴离子移向阳极→________移向阳极;阳离子移向阴极→________移向阴极;
【投屏】老师总结电解CuCl 溶液的实验现象,并投屏装置。
2
任务2:通过实验分析,引导学生自主书写电极反应式。
【答题要点】
电极反应式:阳极:2Cl--2e-=Cl ↑ 阴极:Cu2++2e-=Cu
2
结论:①阳极:Cl-向阳极移动,失e-产生Cl
2
②阴极:Cu 2+向阴极移动,得e-生成Cu,并导致溶液颜色变浅
【课堂问答】
(1)某些不能自发进行的氧化还原反应,通过电解可以实现( )
(2)金属导电是物理变化,电解质溶液导电是化学变化( )
(2)电解CuCl 溶液,阴极逸出的气体能够使湿润的碘化钾淀粉试纸变蓝( )
2
活动三、电解池概念、结构自主总结
任务1:根据电解CuCl 溶液实验过程,结论分析电解池概念及构成条件
2
【答题要点】
1.电解:使电流通过电解质溶液或熔融电解质,而在阴、阳 两极引起氧化还原反应的过程。
电解过程可以看作外接电源提供的电能,借助电解池将还原剂的电子转移给了氧化剂。
2.电解池(电解槽):把电能转变为化学能的装置。
3. 电解池构成的条件
①两个电极
②直流电源相连③电解质溶液或熔融电解质
④形成闭合回路。
三、电解池的工作原理
活动一、电解池工作原理的总结
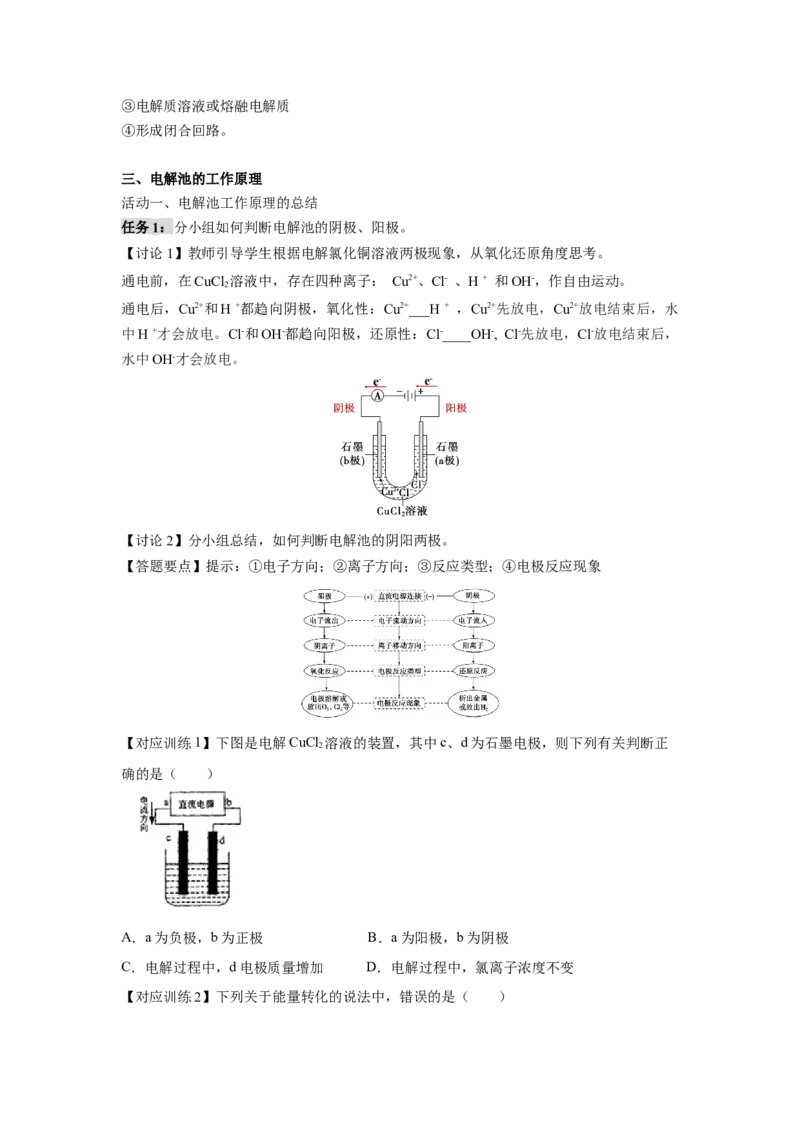
任务1:分小组如何判断电解池的阴极、阳极。
【讨论1】教师引导学生根据电解氯化铜溶液两极现象,从氧化还原角度思考。
通电前,在CuCl 溶液中,存在四种离子: Cu2+、Cl- 、H + 和OH-,作自由运动。
2
通电后,Cu2+和H +都趋向阴极,氧化性:Cu2+___H + ,Cu2+先放电,Cu2+放电结束后,水
中H +才会放电。Cl-和OH-都趋向阳极,还原性:Cl-____OH-, Cl-先放电,Cl-放电结束后,
水中OH-才会放电。
【讨论2】分小组总结,如何判断电解池的阴阳两极。
【答题要点】提示:①电子方向;②离子方向;③反应类型;④电极反应现象
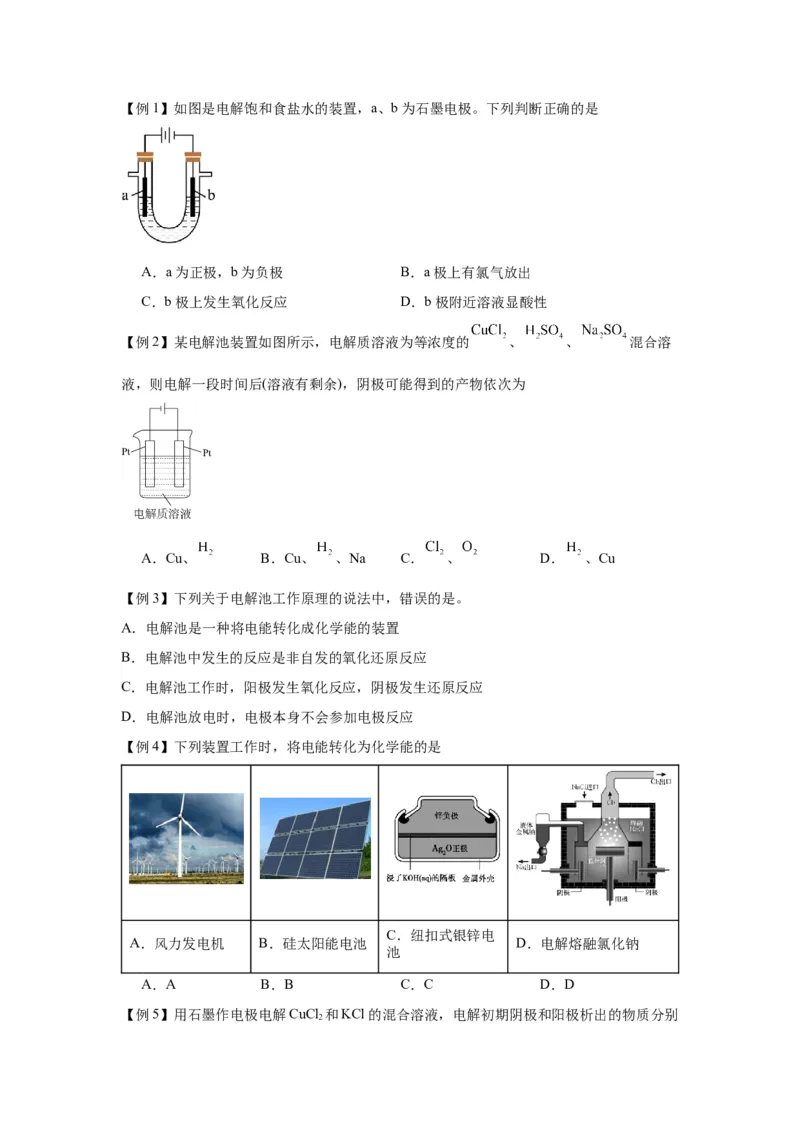
【对应训练1】下图是电解CuCl 溶液的装置,其中c、d为石墨电极,则下列有关判断正
2
确的是( )
A.a为负极,b为正极 B.a为阳极,b为阴极
C.电解过程中,d电极质量增加 D.电解过程中,氯离子浓度不变
【对应训练2】下列关于能量转化的说法中,错误的是( )A.电解水生成氢气和氧气时,电能转化为化学能
B.绿色植物进行光合作用时,太阳能转化为化学能
C.白炽灯工作时,电能全部转化为光能
D.煤燃烧时,化学能主要转化为热能
二、电解规律
活动一、探究惰性电极电解池电解规律
任务1:在电解氯化铜溶液的学习基础上,探究离子在阴阳极的放电顺序。
【答题要点】
阳极:失电子,发生氧化反应—比较——还原性(失电子能力)强弱
阴离子的放电顺序是:
金属电极>S 2->SO2->I ->Br->Cl->OH->NO ->SO2-(等含氧酸根离子)>F-
3 3 4
惰性电极
阴极:得电子,发生还原反应—比较——氧化性(得电子能力)强弱
阳离子在阴极上放电顺序是:
Ag+> Fe 3+ >Cu2+>H+ >Pb2+>Sn2+>Fe2+>Zn2+>H+ > Al3+>Mg2+>Na+>Ca2+>K+
(酸) (水)
任务2:分小组总结电解池中电极反应式的书写规则及方法。
【答题要点】
(1)明确电解池的电极材料;
阳极如果是金属电极,首先金属电极先失电子。
(2)明确溶液中存在哪些离子
电解氯化钠溶液实验中,电解质溶液中存在Cl-、OH-、Na+、H+四种离子
(2)离子的移动方向;阴阳两极附近有哪些离子
阴离子移向阳极→Cl-、OH-移向阳极;阳离子移向阴极→Na+、H+移向阴极;
(4)根据阳极氧化、阴极还原以及氧化性、还原性强弱判断反应的离子先后,
最后分析得出产物
阳离子的放电顺序是:Cl->OH- 阴离子在阴极上放电顺序是: H+> Na+
阳极:2Cl- - 2 e- = Cl ↑ 阴极:2H+ + 2e-= H2↑
2
【对应训练3】下列用惰性电极电解不同物质的电极反应式中,错误的是
A.电解饱和食盐水 阴极:
B.电解 溶液 阴极:C.电解熔融 阳极:
D.电解 溶液 阳极:
【对应训练4】用惰性电极电解饱和食盐水的反应原理为
2NaCl+2H O 2NaOH+H ↑+Cl↑,下列说法错误的是
2 2 2
A.阳极反应式为:2Cl--2e-=Cl↑
2
B.HO为还原剂,得到电子
2
C.电解一段时间后,溶液的pH变大
D.NaOH既不是氧化产物也不是还原产物
活动二、酸、碱、盐溶液电解规律(惰性电极)
任务1:探究含氧酸的电解规律,如电解HSO 、HNO 等溶液;
2 4 3
【讨论】①根据电解规律,思考电解HSO 、HNO 溶液的电极反应式;②思考电解一段时
2 4 3
间后,溶液溶度如何变化,pH值如何变化,若要恢复原溶液,可通过什么方法?
【答题要点】
1.电极反应式:
阳极 :2HO-4e-= 4H+ +O ↑; 阴极: 4H+ +4e-=2H ↑
2 2 2
总反应:2HO 电==解== O ↑ +2H ↑
2 2 2
2. 电解后溶液中溶质的质量分数增大,若要恢复原来的浓度,电解的是酸,由于溶剂水的
量变小,所以pH变小,若想恢复原溶液,只需加入一定量的水即可。
任务2:探究含氧酸的电解规律,如电解NaOH,KOH等溶液;
【讨论】①根据电解规律,思考电解NaOH,KOH溶液的电极反应式;②思考电解一段时
间后,溶液溶度如何变化,pH值如何变化,若要恢复原溶液,可通过什么方法?
【答题要点】
1.电极反应式:
阳极 :2HO-4e-= 4H+ +O ↑; 阴极: 4H+ +4e-=2H ↑
2 2 2
电解
总反应:2HO ==== O ↑ +2H ↑
2 2 2
2. 电解后溶液中溶质的质量分数增大,若要恢复原来的浓度,电解的是酸,由于溶剂水的
量变小,所以pH变大,若想恢复原溶液,只需加入一定量的水即可。
任务3:通过电解池电解规律的学习,引导学生独立书写氢前金属含氧酸盐的电解规律,
如电解NaSO 、KCO 等溶液;
2 4 3【投屏】阳极 : 2HO-4e-= 4H+ +O ↑ 阴极: 4HO +4e-=2H ↑+ 4OH-
2 2 2 2
电解
总反应:2HO ==== O ↑ +2H ↑
2 2 2
【总结】通过以上四种溶液的电解电极反应式的书写,总结规律,属于电解水型,若要恢
复原溶液,只需要加入HO即可。
2
【自主学习】
任务1:总结书写电解HCl、CuCl 溶液的电解规律;
2
【答题要点】
(1)电解HCl溶液
阳极: 2Cl -- 2e-=Cl↑ 阴极: 2H+ + 2e-= H ↑
2 2
电解
总反应:2HCl==== Cl ↑ + H ↑
2 2
(2)电解CuCl 溶液
2
阳极: 2Cl -- 2e-=Cl↑ 阴极: Cu2+ + 2e-=Cu
2
总反应:CuCl 电==解== Cl ↑ + Cu
2 2
任务2:写出电极反应式后,学生总结电解类型
【答题要点】① 属于电解电解质本身型;
② 电解后溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入一定量的溶质
任务3:将学生分为两大组,自主总结书写电解下列溶液的电解规律。
【小组1】电解NaCl、KCl、MgCl 、AlCl 溶液的电解规律;
2 3
【答题要点】电解NaCl溶液时其电极反应式为:
阳极 : 2Cl -- 2e-=Cl↑ 阳极 : 2Cl -- 2e-=Cl↑
2 2
电解
总反应:2NaCl+2H O ===== 2NaOH+ Cl ↑ + H ↑
2 2 2
【总结】
① 电解后原溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需通入一定量的
HCl气体。② 属于放氢生碱型
【小组2】电解CuSO 溶液、AgNO 溶液的电解规律;
4 3
【答题要点】电解CuSO 溶液时其电极反应式为:
4
阳极 : 4OH--4e-=2HO +O ↑ 阴极: 2Cu2+ +4e-=2Cu
2 2
总反应: 2CuSO +2H O 电==解==== 2Cu+O ↑ +2H SO
4 2 2 2 4
【总结】①电解后原溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入一
定量金属氧化物。②属于放氧生酸型。
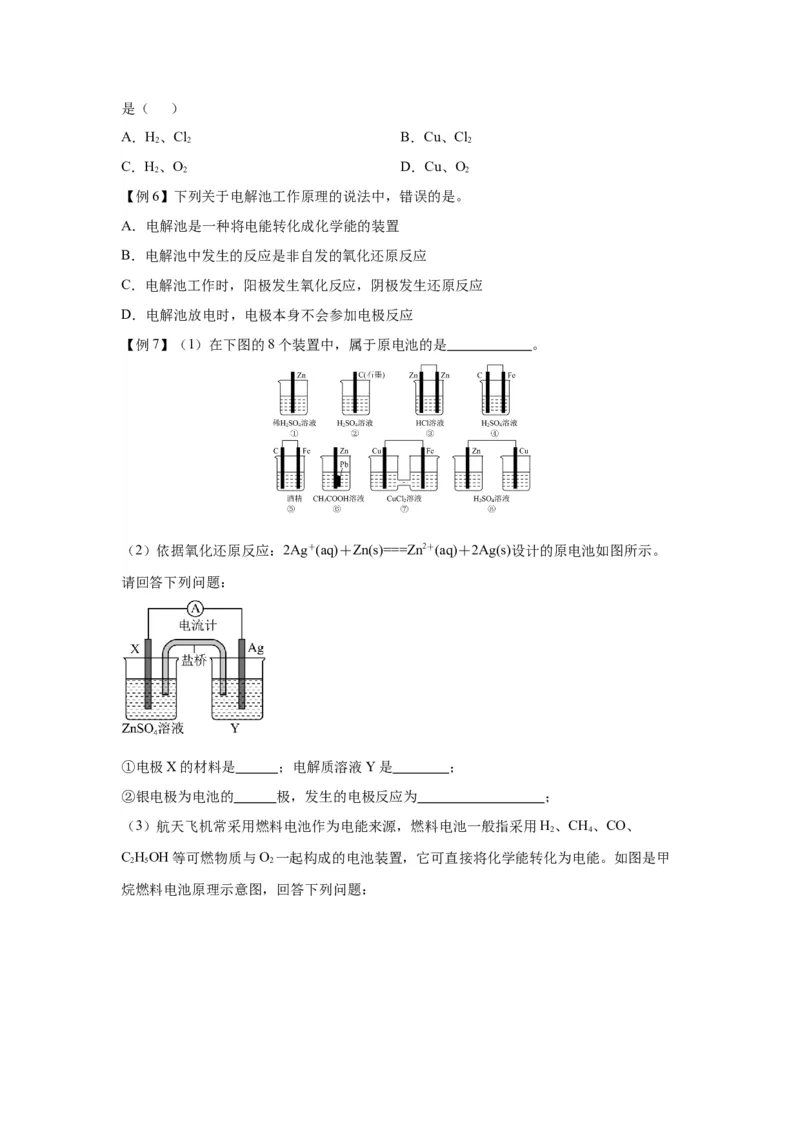
课 后 作 业 练 习【例1】如图是电解饱和食盐水的装置,a、b为石墨电极。下列判断正确的是
A.a为正极,b为负极 B.a极上有氯气放出
C.b极上发生氧化反应 D.b极附近溶液显酸性
【例2】某电解池装置如图所示,电解质溶液为等浓度的 、 、 混合溶
液,则电解一段时间后(溶液有剩余),阴极可能得到的产物依次为
A.Cu、 B.Cu、 、Na C. 、 D. 、Cu
【例3】下列关于电解池工作原理的说法中,错误的是。
A.电解池是一种将电能转化成化学能的装置
B.电解池中发生的反应是非自发的氧化还原反应
C.电解池工作时,阳极发生氧化反应,阴极发生还原反应
D.电解池放电时,电极本身不会参加电极反应
【例4】下列装置工作时,将电能转化为化学能的是
C.纽扣式银锌电
A.风力发电机 B.硅太阳能电池 D.电解熔融氯化钠
池
A.A B.B C.C D.D
【例5】用石墨作电极电解CuCl 和KCl的混合溶液,电解初期阴极和阳极析出的物质分别
2是( )
A.H、Cl B.Cu、Cl
2 2 2
C.H、O D.Cu、O
2 2 2
【例6】下列关于电解池工作原理的说法中,错误的是。
A.电解池是一种将电能转化成化学能的装置
B.电解池中发生的反应是非自发的氧化还原反应
C.电解池工作时,阳极发生氧化反应,阴极发生还原反应
D.电解池放电时,电极本身不会参加电极反应
【例7】(1)在下图的8个装置中,属于原电池的是 。
(2)依据氧化还原反应:2Ag+(aq)+Zn(s)===Zn2+(aq)+2Ag(s)设计的原电池如图所示。
请回答下列问题:
①电极X的材料是 ;电解质溶液Y是 ;
②银电极为电池的 极,发生的电极反应为 ;
(3)航天飞机常采用燃料电池作为电能来源,燃料电池一般指采用H、CH、CO、
2 4
C HOH等可燃物质与O 一起构成的电池装置,它可直接将化学能转化为电能。如图是甲
2 5 2
烷燃料电池原理示意图,回答下列问题:①电池的负极是 (填“a”或“b”),该极的电极反应是 。
②消耗标准状况下5.6 L O 时,有 mol电子发生转移。
2
③开始放电时,正极附近溶液的pH (填“增大”“减小”或“不变”)
④以铜为电极,用此电池作电源,电解以下溶液,开始阶段发生反应Cu+
2HO===Cu(OH) +H↑的有 。
2 2 2