文档内容
第四章《化学反应与电能》教学设计
第二节 电解池
第一课时 电解池
课题: 4.2.1 电解池 课时 1 授课年级 高二
内容要求:掌握电解池的工作原理和基本概念,包括阴阳极、电子转移、离子移动等。理解电
课标
解池中的离子移动和电极反应过程,包括阳极氧化反应、阴极还原反应等。
要求 学业要求: 培养实验设计和操作能力,能够设计和实施简单的电解实验,观察并记录实验现
象,并能够分析和解释实验结果。
本节内容是高中化学人教版(2019版)选择性必修1第四章第二节《电解池》内容。电
解池是高中化学中的一个重要部分,涵盖了电解池的工作原理、离子移动和电极反应过程、电
解池的应用以及实验设计和操作等。
在本章节中,我们将介绍电解池的基本概念、工作原理和阴阳极反应类型。通过这部分
内容的学习,学生可以了解电解池的基本性质和运作方式,为后续学习打下基础。
内容的组织方面,教材通过由浅入深、由理论到实践的方式,逐步展开电解池的教学内
容。从基本原理到应用实例,从理论知识的讲解到实验操作的演示,逐步深入,有助于学生更
好地理解和掌握电解池。同时,通过实验设计和操作等实践性教学环节,增强学生的理解和记
教材 忆,培养学生的实验设计和操作能力。
教材的重点落在电解池的工作原理、阴阳极反应过程等基本概念的理解和应用。而教学
分析
难点则在于如何将理论知识与实验操作相结合,以及如何让学生理解和掌握一些抽象概念和反
应过程。教师需要通过生动的实验教学、案例分析和互动讨论等教学方法,帮助学生加深理解
电解池是高中化学中的一个重要部分,与我们的日常生活和工业生产有着密切的联系。
通过本章的学习,学生可以更好地理解电解池的基本原理和性质,为后续学习打下坚实的基
础。同时,电解池的应用实例也与其他章节的内容相呼应,有助于构建化学学科的整体知识体
系。
1.掌握电解池的基本原理和概念,包括阴阳极反应类型等应用;
教学
2.理解离子移动和电极反应过程,包括微观粒子的运动和电极反应的微观解释;
目标 3.培养实验安全意识和环保意识,注重实验操作规范;
4.通过实验演示和案例分析,增强学生对电解池的理解和记忆;
重点:理解电解池的工作原理:即电流通过电解质溶液时,在阴阳两极上发生的氧化还原反
重点
应。这需要学生具备基本的电化学知识。
难点 难点:掌握阴、阳极反应过程:电解池的阴阳极反应复杂,涉及到氧化还原反应的原理,并能
够根据实际情况进行判断和书写。
宏观辨识与微观探析:宏观上通过学生对电解氯化铜溶液的实验现象的观察,得出有效实
核心 验信息加以分析;微观角度理解电解池工作原理反。科学探究与创新意识:通过实验探究,初步体验有序、全面、敏锐观察实验现象的方法,
并能准确地用语言描述,尝试对现象进行分析、归纳,培养初步的科学探究能力。
素养
科学精神与社会责任:通过对电解池的探究分析,学习电解池的工作原理,结合工作生产
与生活应该。理解科学认识来源于实践的科学精神,科学认识的方法之一是定性与定量相结
合。
从学生的知识认知看,在上一节我们已经学过原电池,所以学生对电化学领域的知识已
经有了初步的了解,但对电解池的学习还处于起步阶段。大部分学生对于电解池的基本原理和
过程在化学电源中的“二次电池”的学习过程中有简单的了解。 本节的学习带领学生深入学
习电解池工作原理,并能够初步理解阳极和阴极反应。然而,他们在面对一些复杂问题时可能
会感到困惑。因此,在电解池的学习中,教师应注重循序渐进的引导和讲解,使学生逐渐理解
学情
并掌握电解池的相关知识。
分析 另一方面,高二学生对实践操作和实验技能的需求也较高。通过实验教学和案例分析,学
生可以更好地理解电解池的实际应用,并提高实验操作技能。教师需要关注学生的学习习惯和
方法,提供适当的指导和帮助,以促进学生的学习效果。
总的来说,高二学生对电解池的学习处于起步阶段,需要教师在教学过程中注重基础知识
的教学和实践操作的引导,同时也需要关注学生的学习态度和方法问题。只有这样,才能帮助
学生更好地掌握电解池的知识和应用,提高他们的化学素养和综合素质。
教学过程
教学 设计意
教学活动
环节 图
【导入】解密电解水骗局
随着生活品质的提高,现在每个家庭对饮用水也有了严格的标准,所以市场上出
根据
环
现了琳琅满目的各种净水器,价位不等,形式各样,为我们提供了很多的选择,下图
节
创设生
一 是我们常见的几个类型的净水器。
活中电
、
解池的
生 应用,
创
活 激发探
设
情 究欲
情
境 望。
境
、
,
引
激
入
发
电
兴 由于净水器的价位不同,选择过多,也被一些不良商家钻了空子。但也有些不良
解
趣
池 商家在小区内推销自制,无品牌的净水器。电解两杯不同的水,一杯是自来水,一杯
的
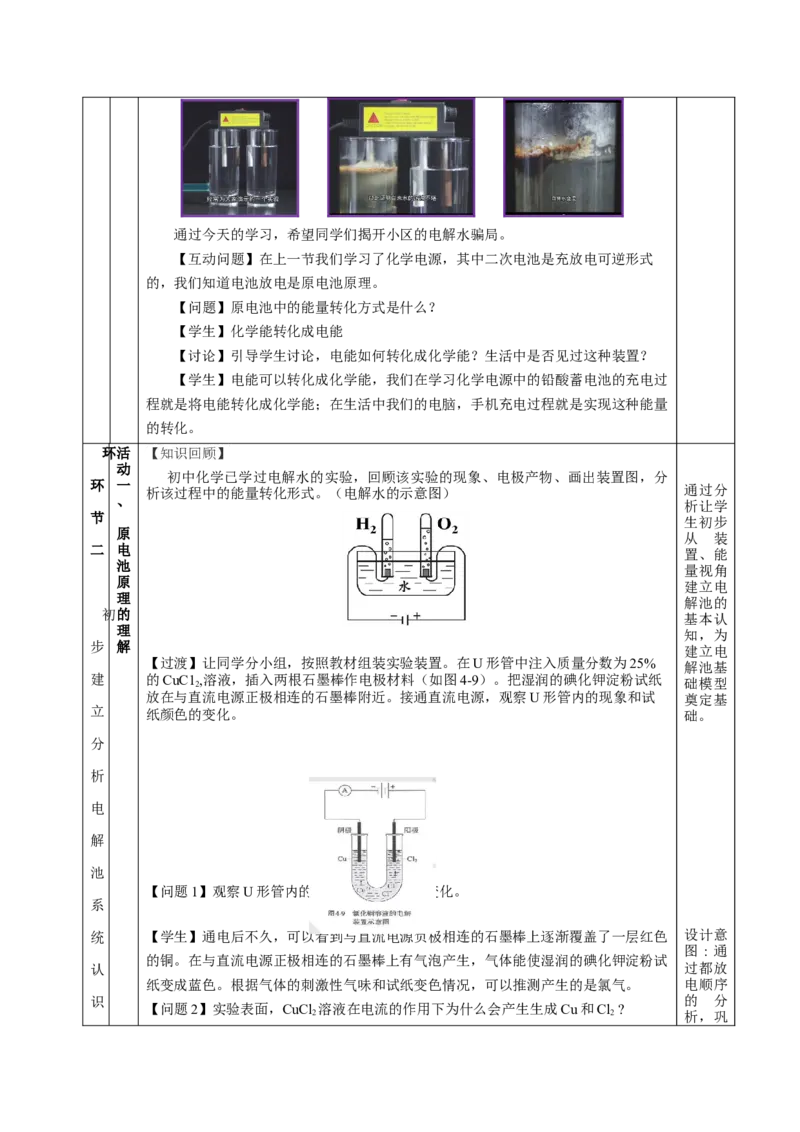
是通过商家净水器净化后的饮用水。实验的现象是,没有净化的自来水出现了严重的
概
念 污浊,而通过商家净化后的水仍是清澈的。
这是为什么呢?难道是我们的自来水真的这么不堪吗?通过今天的学习,希望同学们揭开小区的电解水骗局。
【互动问题】在上一节我们学习了化学电源,其中二次电池是充放电可逆形式
的,我们知道电池放电是原电池原理。
【问题】原电池中的能量转化方式是什么?
【学生】化学能转化成电能
【讨论】引导学生讨论,电能如何转化成化学能?生活中是否见过这种装置?
【学生】电能可以转化成化学能,我们在学习化学电源中的铅酸蓄电池的充电过
程就是将电能转化成化学能;在生活中我们的电脑,手机充电过程就是实现这种能量
的转化。
环活 【知识回顾】
动
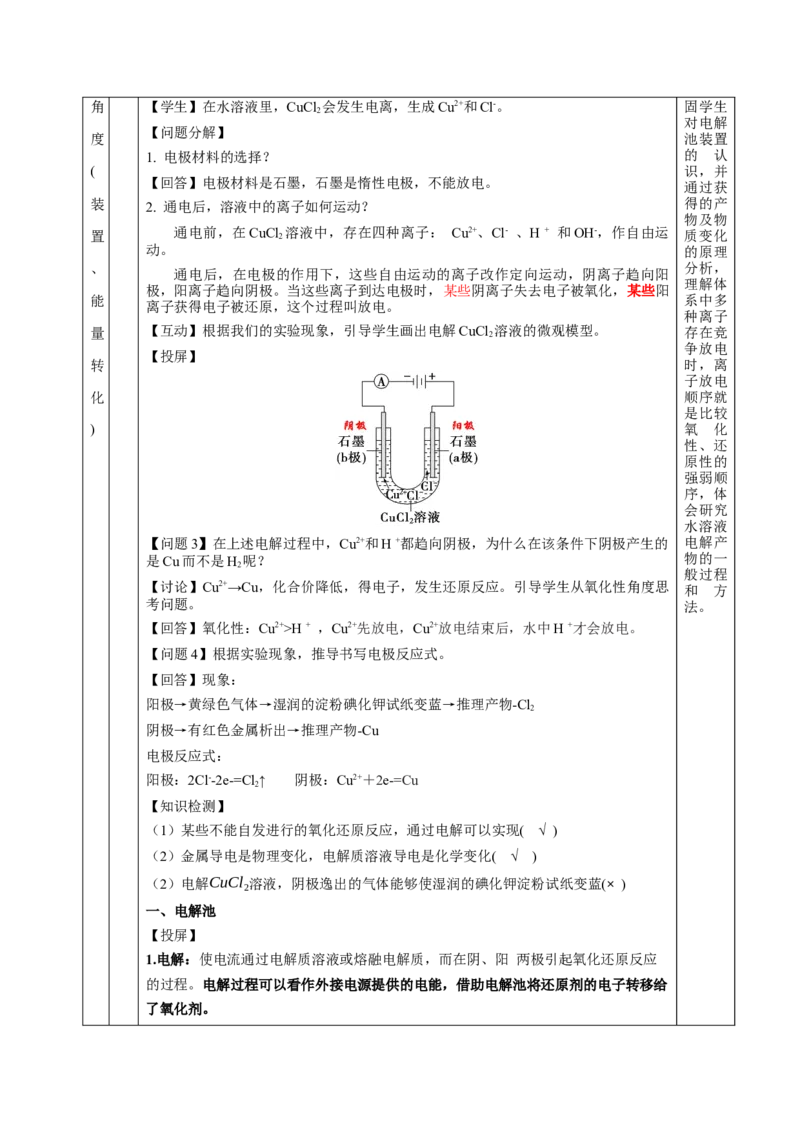
初中化学已学过电解水的实验,回顾该实验的现象、电极产物、画出装置图,分
环 一
析该过程中的能量转化形式。(电解水的示意图) 通过分
、
析让学
节
生初步
原
从 装
二 电
置、能
池
量视角
原
建立电
理
解池的
初的
基本认
理
知,为
步 解
建立电
【过渡】让同学分小组,按照教材组装实验装置。在U形管中注入质量分数为25%
解池基
建 的CuC1 2 ,溶液,插入两根石墨棒作电极材料(如图4-9)。把湿润的碘化钾淀粉试纸 础模型
放在与直流电源正极相连的石墨棒附近。接通直流电源,观察U形管内的现象和试 奠定基
立 纸颜色的变化。 础。
分
析
电
解
池
【问题1】观察U形管内的现象和试纸颜色的变化。
系
统 【学生】通电后不久,可以看到与直流电源负极相连的石墨棒上逐渐覆盖了一层红色 设计意
图 : 通
的铜。在与直流电源正极相连的石墨棒上有气泡产生,气体能使湿润的碘化钾淀粉试
认 过都放
纸变成蓝色。根据气体的刺激性气味和试纸变色情况,可以推测产生的是氯气。 电顺序
识 的 分
【问题2】实验表面,CuCl 溶液在电流的作用下为什么会产生生成Cu和Cl ?
2 2 析,巩角 【学生】在水溶液里,CuCl 会发生电离,生成Cu2+和Cl-。 固学生
2
对电解
【问题分解】
度 池装置
1. 电极材料的选择? 的 认
( 识,并
【回答】电极材料是石墨,石墨是惰性电极,不能放电。
通过获
装 2. 通电后,溶液中的离子如何运动? 得的产
物及物
置 通电前,在CuCl 2 溶液中,存在四种离子: Cu2+、Cl- 、H + 和OH-,作自由运 质变化
动。 的原理
、 分析,
通电后,在电极的作用下,这些自由运动的离子改作定向运动,阴离子趋向阳
理解体
极,阳离子趋向阴极。当这些离子到达电极时,某些阴离子失去电子被氧化,某些阳
能 系中多
离子获得电子被还原,这个过程叫放电。
种离子
量 【互动】根据我们的实验现象,引导学生画出电解CuCl 溶液的微观模型。 存在竞
2
争放电
【投屏】
转 时,离
子放电
化 顺序就
是比较
) 氧 化
性、还
原性的
强弱顺
序,体
会研究
水溶液
【问题3】在上述电解过程中,Cu2+和H +都趋向阴极,为什么在该条件下阴极产生的 电解产
是Cu而不是H 呢? 物的一
2
般过程
【讨论】Cu2+→Cu,化合价降低,得电子,发生还原反应。引导学生从氧化性角度思
和 方
考问题。 法。
【回答】氧化性:Cu2+>H + ,Cu2+先放电,Cu2+放电结束后,水中H +才会放电。
【问题4】根据实验现象,推导书写电极反应式。
【回答】现象:
阳极→黄绿色气体→湿润的淀粉碘化钾试纸变蓝→推理产物-Cl
2
阴极→有红色金属析出→推理产物-Cu
电极反应式:
阳极:2Cl--2e-=Cl ↑ 阴极:Cu2++2e-=Cu
2
【知识检测】
(1)某些不能自发进行的氧化还原反应,通过电解可以实现( √ )
(2)金属导电是物理变化,电解质溶液导电是化学变化( √ )
(2)电解CuCl 溶液,阴极逸出的气体能够使湿润的碘化钾淀粉试纸变蓝(× )
2
一、电解池
【投屏】
1.电解:使电流通过电解质溶液或熔融电解质,而在阴、阳 两极引起氧化还原反应
的过程。电解过程可以看作外接电源提供的电能,借助电解池将还原剂的电子转移给
了氧化剂。2.电解池(电解槽):把电能转变为化学能的装置。
【讨论】分小组讨论电解池构成的条件。
【老师】电解池构成的条件
①两个电极
②直流电源相连
③电解质溶液或熔融电解质
④形成闭合回路。
二、电解池的工作原理
【讨论】分小组讨论,根据对电解CuCl 溶液的学习总结电解池工作原理。
2
【问题1】如何判断电解池的阴极、阳极。
【投屏】
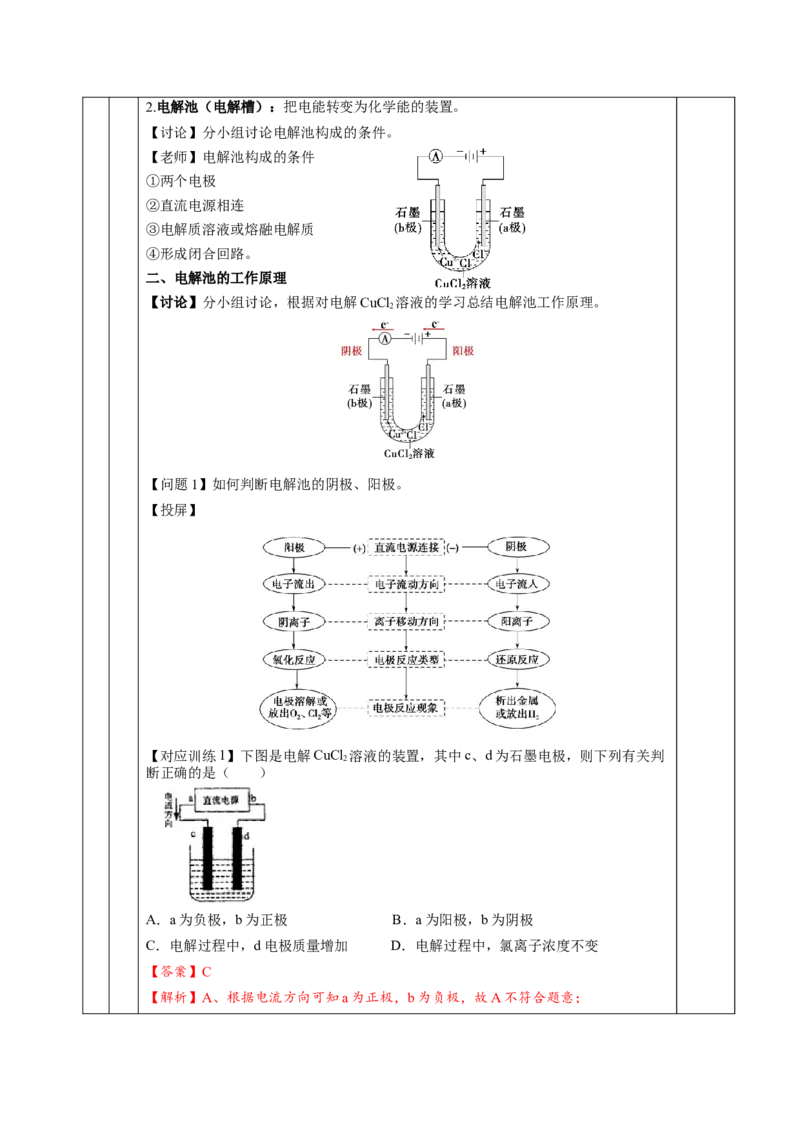
【对应训练1】下图是电解CuCl 溶液的装置,其中c、d为石墨电极,则下列有关判
2
断正确的是( )
A.a为负极,b为正极 B.a为阳极,b为阴极
C.电解过程中,d电极质量增加 D.电解过程中,氯离子浓度不变
【答案】C
【解析】A、根据电流方向可知a为正极,b为负极,故A不符合题意;B、根据电流方向可知a为正极,b为负极,故B不符合题意;
C、根据电流方向可知a为正极,b为负极,c为阳极,d为阴极,电解过程中,d电
极铜离子得到电子变为铜单质,质量增加,故C符合题意;
D、电解过程中,c极氯离子失去电子变为氯气,因此浓度减小,故D不符合题意;
故答案为:C。
【对应训练2】下列关于能量转化的说法中,错误的是( )
A.电解水生成氢气和氧气时,电能转化为化学能
B.绿色植物进行光合作用时,太阳能转化为化学能
C.白炽灯工作时,电能全部转化为光能
D.煤燃烧时,化学能主要转化为热能
【答案】C
【解析】A.电解水生成氢气和氧气的电解装置是将电能转化为化学能的装置,故不符
合题意;
B.绿色植物进行光合作用时,太阳能转化为化学能,故不符合题意;
C.白炽灯工作时电能转化为光能和热能,故符合题意;
D.物质的燃烧将化学能转化为热能和光能,主要是热能,故不符合题意。
故答案为:C。
二、电解规律
【思考】电解氯化铜溶液实验中,电解质溶液中存在Cl-、OH-、Cu2+、H+四种离子,
为什么阳极反应为Cl-失去电子生成Cl 而不是OH-失去电子生成O 呢?为什么阴极
2, 2
反应为Cu2+得到电子生成Cu单质 而不是H+得到电子生成H 呢?
, 2
【老师】点解产物是由溶液中的离子的放电顺序所决定的,那么我们来总结一下:
阳极:失电子,发生氧化反应—比较——还原性(失电子能力)强弱
①若为金属(非惰性)电极,电极失电子,金属在阳极失电子被氧化成阳离子进入溶
液,阴离子不容易在电极上放电。
②若为惰性电极,电解质溶液中阴离子“争”失电子 。
阴离子的放电顺序是:
S2->SO2->I ->Br->Cl->OH->NO ->SO2-(等含氧酸根离子)>F-
3 3 4
阴极:得电子,发生还原反应—比较——氧化性(得电子能力)强弱
① 电极本身不参加反应
②一定是电解质溶液中阳离子“争”得电子
阳离子在阴极上放电顺序是:
Ag+> Fe 3+ >Cu2+>H+ >Pb2+>Sn2+>Fe2+>Zn2+>H+ > Al3+>Mg2+>Na+>Ca2+>K+
(酸) (水)
【问题】根据学习的电解规律,分小组讨论书写电解池的电极反应式的方法。
【学生】分析电解反应(用惰性电极时)的一般思路,以“电解氯化铜溶液”为例:
(1)明确溶液中存在哪些离子
电解氯化铜溶液实验中,电解质溶液中存在Cl-、OH-、Cu2+、H+四种离
子(2)离子的移动方向;
阴离子移向阳极;阳离子移向阴极;
(3)阴阳两极附近有哪些离子
阴离子移向阳极→Cl-、OH-移向阳极;阳离子移向阴极→Cu2+、H+移向
阴极;
(4)根据阳极氧化、阴极还原以及氧化性、还原性强弱判断反应的离子先后,
最后分析得出产物
阳离子的放电顺序是:Cl->OH- 阴离子在阴极上放电顺序是:Cu2+>H+
阳极:2Cl- - 2 e- = Cl ↑ 阴极:Cu2+ + 2e-= Cu
2
【对应训练3】下列用惰性电极电解不同物质的电极反应式中,错误的是
A.电解饱和食盐水 阴极:
B.电解 溶液 阴极:
C.电解熔融 阳极:
D.电解 溶液 阳极:
【答案】A
【详解】A.电解饱和食盐水阴极水电离出的氢离子放电,即 ,
A错误;
B.电解 溶液阴极铜离子得电子生成铜单质,电极反应正确,B正确;
C.电解熔融 阳极氯离子放电生成氯气,电极反应正确,C正确;
D.电解 溶液阳极氢氧化钠电离的氢氧根放电生成氧气,电极反应正确,D正
确;
【对应训练4】用惰性电极电解饱和食盐水的反应原理为2NaCl+2H O
2
2NaOH+H ↑+Cl↑,下列说法错误的是
2 2
A.阳极反应式为:2Cl--2e-=Cl↑
2
B.HO为还原剂,得到电子
2
C.电解一段时间后,溶液的pH变大
D.NaOH既不是氧化产物也不是还原产物
【答案】B
【详解】A.根据惰性电极电解饱和食盐水的总反应可知,阳极氯气发生失电子的氧
化反应,其电极反应式为:2Cl--2e-=Cl↑,A正确;
2
B.阴极水得电子转化为氢气,水为氧化剂,B错误;
C.根据总反应可知,电解一段时间后,生成的氢氧化钠使溶液的pH增大,C正
确;
D.上述反应中,氢气为还原产物,氯气为氧化产物,氢氧化钠既不是氧化产物也不
是还原产物,D正确;活 一、 酸、碱、盐溶液电解规律(惰性电极) 利用已
动 有知
(一)电解水型
二 识,预
、 【过渡】已经掌握了电解池(惰性电极)工作时的电解规律; 测物质
电 的性
【互动】与学生互动问答,提问阴极,阳极离子放电顺序,可以实现课堂效果,同时
解 质,培
又可以强化基础知识。
质 养利用
溶 【讨论1】分小组讨论,含氧酸的电解规律,如电解HSO 、HNO 等溶液; 所学解
2 4 3
液 决实际
【投屏】阳极 :2HO-4e-= 4H+ +O ↑; 阴极: 4H+ +4e-=2H ↑
用 2 2 2 问题的
惰 能力。
总反应:2HO ==== O ↑ +2H ↑
2 2 2
性
电 【问题1】电解一段时间后,溶液的浓度如何变化?通过什么方法可以恢复溶液状
极 态?
电
【学生】电解后溶液中溶质的质量分数增大,若要恢复原来的浓度,只需加入一定量
解
的水即可。
的
示 【讨论2】分小组讨论,的电解强碱规律,如电解NaOH、KOH等溶液;
例
【投屏】阳极 : 4OH--4e-=2HO +O ↑ 阴极: 4HO +4e-=2H ↑+ 4OH-
2 2 2 2
总反应:2HO ==== O ↑ +2H ↑
2 2 2
【问题2】电解一段时间后,溶液的浓度如何变化?通过什么方法可以恢复溶液状
态?
【学生】电解后溶液中溶质的质量分数增大,若要恢复原来的浓度,只需加入一定量
的水即可。
【讨论3】分小组讨论,氢前金属含氧酸盐的电解规律,如电解 NaSO 、KCO 等溶
2 4 3
液;
【投屏】阳极 : 2HO-4e-= 4H+ +O ↑ 阴极: 4HO +4e-=2H ↑+ 4OH-
2 2 2 2
总反应:2HO ==== O ↑ +2H ↑
2 2 2
(二)电解电解质本身
【讨论】分小组讨论,含电解HCl、CuCl 等溶液的电解规律;
2
【老师】根据电极离子的放电顺序,同学们可以直接写出电极反应式。
【投屏】
(1)电解HCl溶液
阳极: 2Cl -- 2e-=Cl↑ 阴极: 2H+ + 2e-= H ↑
2 2
总反应:2HCl==== Cl ↑ + H ↑
2 2
(2)电解CuCl 溶液
2
阳极: 2Cl -- 2e-=Cl↑ 阴极: Cu2+ + 2e-=Cu
2
总反应:CuCl ==== Cl ↑ + Cu
2 2
【老师】电解后溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入一
定量的溶质(加入一定量的HCl气体,CuCl 固体)
2
(三)放氢生碱型
【讨论】分小组讨论,含电解NaCl、KCl、MgCl 、AlCl 溶液的电解规律;
2 3
【投屏】电解NaCl溶液时其电极反应式为:
阳极 : 2Cl -- 2e-=Cl↑ 阳极 : 2Cl -- 2e-=Cl↑
2 2总反应:2NaCl+2H O ===== 2NaOH+ Cl ↑ + H ↑
2 2 2
【总结】 电解后原溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需通
入一定量的HCl气体。
(四)放氧生酸型
【讨论】分小组讨论,含电解CuSO 溶液、AgNO 溶液的电解规律;
4 3
【投屏】电解CuSO 溶液时其电极反应式为:
4
阳极 : 4OH--4e-=2HO +O ↑ 阴极: 2Cu2+ +4e-=2Cu
2 2
总反应: 2CuSO +2H O ====== 2Cu+O ↑ +2H SO
4 2 2 2 4
【总结】电解后原溶液中溶质的质量分数减小,若要恢复原来的组成和浓度,需加入
一定量金属氧化物。
电解规律总结
阳极:失电子,发生氧化反应—比较——还原性(失电子能力)强弱
①若为金属(非惰性)电极,电极失电子,金属在阳极失电子被氧化成阳离子进入溶液,阴离
子不容易在电极上放电。
②若为惰性电极,电解质溶液中阴离子“争”失电子 。
课堂 阴离子的放电顺序是:
总结
S2->SO2->I ->Br->Cl->OH->NO ->SO2-(等含氧酸根离子)>F-
3 3 4
阴极:得电子,发生还原反应—比较——氧化性(得电子能力)强弱
② 电极本身不参加反应
②一定是电解质溶液中阳离子“争”得电子
阳离子在阴极上放电顺序是:
Ag+> Fe 3+ >Cu2+>H+ >Pb2+>Sn2+>Fe2+>Zn2+>H+ > Al3+>Mg2+>Na+>Ca2+>K+
(酸) (水)
第四章 化学能与电能
第二节 电解池
一、电解池
1.定义:
2.电解池构成的条件:
二、电解原理
1.电解CuCl 溶液
2
2.惰性电极电解酸碱盐溶液
板书
(1)电解水型
设计
(2)电解电解质本身
教学方法:在教学中,我注重学生的实践操作和观察能力,通过演示实验和分组实验等方
式,让学生亲自动手操作,观察电解池的工作原理和过程。但是,在讲解理论知识时,应该更加注重学生的基础知识的掌握,加强讲解和讨论,让学生更好地理解电解池的基本概念、工作
原理和影响因素。
学生反馈:在教学过程中,我关注了学生的反馈和问题,并及时调整教学策略和方法。但
教学
是,还应该更加注重学生的个体差异,根据不同学生的学习特点和需求,制定不同的教学计划
反思
和方法,帮助他们更好地理解和掌握电解池知识。
实验安全和环保:在电解池实验教学中,我注重实验安全和环保,确保学生正确使用实验
器材和试剂,避免发生意外事故。但是,还应该加强实验废弃物的处理和管理,减少实验废弃
物的产生和对环境的影响。
联系实际:在教学中,我注重将电解池知识与实际生活和工业应用联系起来,让学生了解
电解池在生活和工业中的应用。但是,还应该更加注重将电解池知识应用到实际问题中,提高
学生的解决实际问题的能力。
总的来说,高二电解池的教学需要注重学生的实践操作、基础知识掌握、实验安全和环保
以及联系实际等方面。通过不断反思和改进,提高教学质量和效果,帮助学生更好地理解和掌
握电解池知识。
课后
作业 【练习1】用惰性电极电解饱和食盐水的反应原理为2NaCl+2H O 2NaOH+H ↑+Cl↑,下列
2 2 2
说法错误的是
A.阳极反应式为:2Cl--2e-=Cl↑
2
B.HO为还原剂,得到电子
2
C.电解一段时间后,溶液的pH变大
D.NaOH既不是氧化产物也不是还原产物
【答案】B
【详解】A.根据惰性电极电解饱和食盐水的总反应可知,阳极氯气发生失电子的氧化反应,
其电极反应式为:2Cl--2e-=Cl↑,A正确;
2
B.阴极水得电子转化为氢气,水为氧化剂,B错误;
C.根据总反应可知,电解一段时间后,生成的氢氧化钠使溶液的pH增大,C正确;
D.上述反应中,氢气为还原产物,氯气为氧化产物,氢氧化钠既不是氧化产物也不是还原产
物,D正确;
【练习2】根据电解饱和食盐水的工作原理回答下列问题:(1)阳极:优先放电的离子: ,电极反应式: ,反应类型: 反应。
(2)阴极:优先放电的离子: ,电极反应式: ,反应类型: 反应。
(3)阳极产物为 ,阴极产物为: 。
【答案】(1) Cl- 2Cl--2e-=Cl↑ 氧化
2
(2) H O的H+ (或H+) 2H O+2e-=H ↑+2OH-或(2 H++2e-=H ↑ ) 还原
2 2 2 2
(3) Cl NaOH、H
2 2
【解析】(1)根据电解池中阳极的放电顺序(电极本身>S2->I->Br->Cl->OH->含氧酸根离子>
F-)可知:Cl-优先于OH-放电,电极反应式为:2Cl--2e-=Cl↑,阳极发生氧化反应,故答案为:
2
Cl-;2Cl--2e-=Cl↑;氧化反应;
2
(2)根据电解池中阴极的放电顺序(Ag+>Fe3+>Hg2+>Cu2+>H+(酸)>Pb2+ >Sn2+>Fe2+>Zn2+>H+
(水)>Al3+>Mg2+>Na+ >Ca2+>K+)可知,H+优先Na+放电,电极反应式为:2HO+2e-=H ↑+2OH-或(2
2 2
H++2e-=H ↑ ),阴极发生还原反应,故答案为:HO的H+ (或H+);2HO+2e-=H ↑+2OH-或(2 H+
2 2 2 2
+2e-=H ↑ );还原;
2
(3)根据上述分析可知,阳极产物为Cl,阴极产物为H,剩余的OH-与从阳极室通过离子交换
2 2
膜过来的Na+形成NaOH溶液,故阴极产物为:NaOH、H,故答案为:Cl;NaOH、H。
2 2 2