文档内容
4.2.2 电解原理的应用(学案)
1.理解并掌握电解规律和电解产物的判断方法.
2.理解并掌握电解饱和食盐水、电镀、电解精炼铜,电冶金的原理,会书写电极反应式及化
学方程式。
1.电解池原理的应用。
电解饱和食盐水的化学方程式:_________________________________________。
知识点一、电解原理的应用
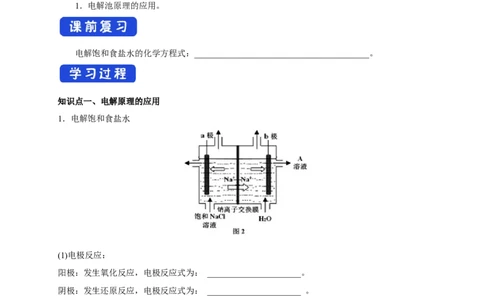
1.电解饱和食盐水
(1)电极反应:
阳极:发生氧化反应,电极反应式为: ______________________。
阴极:发生还原反应,电极反应式为: ______________________ 。
(2)总反应式:
化学方程式:________________________________________________
离子方程式:________________________________________________
工业上习惯把电解饱和食盐水叫做氯碱工业。
电解饱和食盐水时阴极区溶液变红,检验阳极产物
(1)因为电解饱和食盐水时,由于H+在阴极上得到电子而生成H ,破坏了附近的水的电离平衡,促
2
进了水的继续电离,结果阴极区溶液中的OH-的浓度增大而呈碱性。
(2)把湿润的KI淀粉试纸靠近阳极“U”形管口,若变蓝,证明有Cl 产生。
22.电镀
(1)根据图示,书写电极反应式:
阳极:______________________________
阴极:______________________________。
(2)电镀的概念是应用电解原理在某些金属或非金属材料表面镀上一薄层其他金属或合金的过程。
(3)电镀池的构成:一般都是用含有镀层金属离子的电解质溶液作电镀液;把镀层金属浸入电镀液中
与直流电源的正极相连,作为阳极;待镀金属制品与直流电源的负极相连,作阴极。
(4)电镀的目的主要是增强材料抗腐蚀能力,也有许多电镀是为了美观或增加表面硬度。
电镀过程中,铜离子的浓度_______________。
3.电解精炼铜
电解精炼铜时,粗铜中的Zn、Fe、Ni、Ag、Au等杂质:
电解精炼过程中,铜离子的浓度_______________。
当粗铜在阳极不断溶解时,位于金属活动顺序表中铜以前的金属杂质如 Zn、Fe、Ni等,也会同时
失去电子,如Zn-2e-===Zn2+、Fe-2e-===Fe2+、Ni-2e-===Ni2+。但是Zn2+、Ni2+、Fe2+比Cu2
+更难被还原,所以它们并不在阴极获得电子析出,而只是留在电解质溶液里。而位于金属活动性
顺序表中铜之后的金属如银、金等杂质,因为失电子能力比铜弱,难以在阳极失去电子变成阳离子
溶解下来,而是以金属单质的形式沉积在电解槽底,形成阳极泥(阳极泥可作为提炼金、银等贵重
金属的原料)。
4.电冶金
(1)金属冶炼的本质:使矿石中的金属离子获得电子,从它们的化合物中还原出来。如 Mn++ne-
===M。
(2)电解熔融的氯化钠可制取金属钠:
阳极反应式:__________________
阴极反应式:_______________总反应:______________________________
5.冶炼镁和铝,写出电极反应式。
在工业上用电解熔融的MgCl ,熔融的Al O 的方法制得镁和铝,其电极反应式分别为:
2 2 3
冶炼镁:
阳极:__________________
阴极:______________________________
冶炼铝:
阳极:______________________________
阴极:______________________________
【练习】1.氯碱工业中的某生成物,在一定条件下与另外两种生成物均能发生反应,该生成物的
结构和性质错误的是( )
A.该生成物中含有极性键,且溶于水或呈酸性
B.该生成物分子中,所含微粒均达到8电子稳定结构
C.该生成物可以使淀粉KI溶液变蓝
D.该生成物属于氧化产物
【练习】2.氯碱工业的原理示意图如图。下列说法正确的是( )
A.M为负极
B.出口c收集到的物质是氢气
C.该装置使用阴离子交换膜
D.通电一段时间后,阴极区pH升高
【练习】3.下列叙述错误的是( )
A.在铁件上镀铜时,金属铜作阳极
B.电解精炼粗铜时,电解质 CuSO 溶液加少量硫酸是抑制 CuSO 水解
4 4
C.纯锌与稀硫酸反应时,加入少量 CuSO ,可使反应速率加快
4
D.甲醇和氧气以及 KOH 溶液构成的新型燃料电池中,其负极上发生的反应为:CH OH+6OH
3
﹣+6e﹣═CO 2﹣+5H O
3 2
【练习】4.下列叙述不正确的是( )A.在铁件上镀铜时,金属铜作阳极
B.实验室制氢气用粗锌比用纯锌速率快
C.电解精炼铜时,粗铜电极上每转移0.2 mol e﹣,阴极析出6.4 g Cu(忽略能量损失)
D.甲醇和氧气以及KOH溶液构成的新型燃料电池中,负极反应为:CH OH+6OH﹣﹣6e﹣
3
═CO +5H O
2 2
【练习】5 .下列描述不正确的是( )
A.在镀件上电镀铜时,可用金属铜作阳极
B.工业制硫酸,需要在接触室的两层催化剂之间装上一个热交换器
C.在氯碱工业,电解槽被离子交换膜隔成阴极室和阳极室,避免阳极产生的气体与烧碱反应
D.用铂电极电解CuSO 溶液,当Cu2+浓度降低至原来一半时,停止通电,若加入适量Cu
4
(OH) 能使溶液恢复成原来浓度
2
【练习】6.某小组用如图装置模拟电镀铜和精炼铜。下列说法不正确的是( )
A.电镀铜和精炼铜时,Y上的电极反应都是:Cu2++2e﹣═Cu
B.电镀铜时,Y电极为待镀的金属制品
C.精炼铜时,X电极是粗铜,比铜活泼的金属最终变成阳极泥
D.电镀铜时,X电极是铜,溶液中的Cu2+浓度保持不变
【练习】7.下列有关钢片镀银的说法不正确的是( )
A.阳极反应式为Ag﹣e﹣═Ag+
B.钢片应与电源正极相连
C.电解液为AgNO 溶液
3
D.镀银过程中电能转化为化学能
【练习】8.关于电解精炼铜的说法不正确的是( )
A.粗铜作阳极、纯铜作阴极
B.电解液一定含有Cu2+
C.阳极反应只有Cu﹣2e﹣═Cu2+
D.阴极反应只有Cu2++2e﹣═Cu1.1.工业上以食盐为原料不能制取( )
A.Cl B.NaOH C.HCl D.H SO
2 2 4
2.氯碱工业的基本原理就是电解饱和食盐水。下列关于实验室电解饱和食盐水的说法中正确的说
法是( )
A.可以选用炭棒作为阴、阳极材料,但阳极材料也可以用铁棒
B.用湿润的淀粉KI试纸靠近阴极区域,试纸变蓝
C.电解过程中,在阴极区域溶液中滴加酚酞,溶液变红色
D.实验结束后将溶液搅拌,然后用pH试纸检验,溶液呈中性
3.下列有关氯碱工业的描述,正确的是( )
A.氯碱工业是指电解熔融氯化钠制取氯气的方法
B.氯碱工业只能得到氯气和氢氧化钠两种有价值的产品
C.实验室模拟氯碱工业制取氯气后所得溶液呈碱性
D.实验室模拟氯碱工业所得氯气不能直接排放,应用澄清石灰水吸收
4.下列关于铜电极的叙述正确的是( )
A.用电解法精炼铜时,粗铜作阴极、精铜作阳极
B.在镀件上电镀铜时,用金属铜作阳极
C.在电解池中,铜作电极时,溶液中的阴离子在铜极上失电子
D.电解饱和食盐水制Cl 、H 时,可用金属铜作阳极
2 2
5.下列关于铜的说法正确的是( )
A.用电解法精炼粗铜时粗铜作阳极
B.在镀件上镀铜时纯铜作阴极
C.在海轮的外壳上装上铜块可以减缓船体的腐蚀
D.铜的金属活动性比铁弱,因此可用铜罐代替铁罐储运浓硝酸
6.关于镀铜和电解精炼铜,下列说法中正确的是( )
A.都用粗铜做阳极、纯铜做阴极
B.电解液的成分都保持不变
C.阳极反应都只有Cu﹣2e﹣═Cu2+
D.阴极反应都只有Cu2++2e﹣═Cu
7.下列叙述中正确的是( )
A.电解饱和食盐水可以得到金属钠
B.电解法精炼粗铜,粗铜作阳极C.在铁制品上镀上一定厚度的锌层,可用锌做阴极,铁制品做阳极
D.用惰性电极电解Na SO 溶液,一段时间后再加入硫酸,能使溶液恢复到电解前的状态
2 4
8.关于电解法精炼铜的下列说法正确的是( )
A.电解结束后,在阳极底部会有阳极泥产生,主要成分是铁、金和银
B.电解结束后,溶液中Cu2+浓度变大
C.纯铜作阳极,粗铜作阴极,硫酸铜为电解质溶液
D.粗铜作阳极,纯铜作阴极,硫酸铜为电解质溶液
9.下列有关工业生产的叙述正确的是( )
A.合成氨生产过程中将NH 液化分离,可加快正反应速率,提高N 、H 的转化率
3 2 2
B.硫酸工业中,为了提高SO 的转化率,用五氧化二钒作催化剂
2
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C1 进入阳极室
2
D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
【课前复习答案】2NaCl+2H O+2e-=2NaOH+H +Cl;
2 2 2
【知识点填空答案】
2Cl——2e-=Cl;2HO+2e-=2OH-+H ;2NaCl+2H O+2e-=2NaOH+H +Cl;2Cl—+2H O+2e-=2OH-
2 2 2 2 2 2 2
+H +Cl;Cu-2e-===Cu2+;Cu2++2e-===Cu;不变;减小;2Cl——2e-=Cl;2Na++2e-===2Na;
2 2 2
2NaCl(熔融)=====2Na+Cl↑;2Cl——2e-=Cl;Mg2++2e-===Mg;2O2--4e-===O↑;Al3++
2 2 2
3e-===Al。
【练习答案】ADDDDCBC
【检测反馈答案】DCCBADBDD