文档内容
第 23 讲 硫酸、酸雨及防治
[复习目标] 1.掌握硫酸的性质及应用,掌握SO的检验。2.了解硫酸型酸雨的形成及防治方
法。
考点一 硫酸、硫酸根离子的检验
1.硫酸的物理性质
HSO 是无色液体,能与水以任意比互溶,稀释时可放出大量的热,浓 HSO 稀释的方法是
2 4 2 4
____________________________________________________________________________。
2.稀硫酸的性质
硫酸是二元强酸,稀硫酸具有酸的通性,请列举实例加以概括总结。
________________________________________________________________________
________________________________________________________________________
3.浓硫酸的特性
(1)填写下表:
实验 实验现象 浓硫酸的特性
少量胆矾加入浓硫酸中
用玻璃棒蘸取浓硫酸滴在滤纸上
将铜片加入盛有浓硫酸的试管中,加热
(2)分别写出浓HSO 与Cu、C反应的化学方程式: ____________________________
2 4
________________________________________________________________________。
(3)常温下,Fe、Al遇浓HSO ________,可用铝槽车装运浓HSO 。
2 4 2 4
4.硫酸的工业制备流程
完成相关反应的化学方程式:
①________________________________________________________________________,
________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。思考 吸收塔中真的是用水吸收SO 吗?为什么?
3
________________________________________________________________________
________________________________________________________________________
5.SO的检验
检验SO的正确操作方法:被检液――――――――→取清液―――――→有无白色沉淀产生(判断有无
SO)。
先加稀盐酸的目的是________________________________,再加BaCl 溶液,有白色沉淀产
2
生 。 整 个 过 程 中 可 能 发 生 反 应 的 离 子 方 程 式 : ________________________ 、
________________________、_______________________________________________、
________________________________________________________________________。
1.用硫酸清洗锅炉中的水垢( )
2.向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,说明该溶液中一定有SO( )
3 2
3.50 mL 18.4 mol·L-1浓硫酸与足量的铜反应,可产生SO 的物质的量为0.46 mol( )
2
4.HSO 是难挥发性强酸,HS是挥发性弱酸,所以可用浓硫酸与 FeS反应制取HS气体(
2 4 2 2
)
5.在实验室中,可用浓HSO 分别与NaCl、NaBr、NaI反应制取HCl、HBr、HI气体(
2 4
)
一、浓HSO 的特性及应用
2 4
1.下列有关硫酸的实验或用途中用了硫酸的哪些性质?
(1)用浓硫酸作干燥剂干燥CO、SO 、Cl 等气体: _____________________________。
2 2
(2)分别用浓硫酸与NaCl(s)、NaNO (s)反应制取HCl、HNO: ___________________。
3 3
(3)用铝或铁制容器贮存或运输浓硫酸: _____________________________________。
(4)工业上用硫酸与磷酸钙反应制取磷酸: ____________________________________
___________________________________________________________________________。
(5)实验室用铜与浓硫酸反应制取SO : ______________________________________
2
__________________________________________________________________________。
(6)实验室用甲酸与浓硫酸作用制取CO:HCOOH――――→CO+HO:_________________。
2
(7)浓硫酸与蔗糖的制取“黑面包”实验:___________________________________________。
2.下列有机反应中都要使用硫酸。其中哪些使用的是浓硫酸?哪些使用的是稀硫酸?
(1)苯的硝化 (2)乙醇的消去
(3)乙醇与乙酸的酯化 (4)乙酸乙酯的水解
(5)糖类物质的水解 (6)蛋白质的水解
(7)油脂的水解________________________________________________________________________
3.某化学兴趣小组的同学将一定量的铁与浓硫酸加热,发现铁完全溶解,并产生大量的气
体X。该兴趣小组的同学猜测气体X的成分如下:
(1)甲同学认为气体X为SO 。
2
(2)乙同学认为气体X为H。
2
(3)丙同学认为气体X为___________________________________________________。
猜测含有氢气的理由是: __________________________________________________
________________________________________________________________________。
二、SO的检验
4.有一瓶NaSO 溶液,试设计实验探究NaSO 的氧化程度。
2 3 2 3
________________________________________________________________________
________________________________________________________________________
5.下列过程中,最终的白色沉淀物不一定是BaSO 的是( )
4
A.Fe(NO ) 溶液―――――――――――――――→白色沉淀
3 2
B.Ba(NO ) 溶液―――――――――――――――→白色沉淀
3 2
C.无色溶液―――――――――――→白色沉淀
D.无色溶液―――――-→无色溶液――――――→白色沉淀
SO检验的易错点
(1)误将Ag+、Pb2+判断成SO。如向待测液中滴加BaCl 溶液,再加稀盐酸有白色沉淀便断
2
定含SO,其错误是未注意溶液中不含SO,而含Ag+或Pb2+时也会产生同样的现象:
Ag++Cl-===AgCl↓(白色),Pb2++2Cl-===PbCl ↓(白色)。
2
(2)误将SO判断成SO。如向待测液中滴加用稀盐酸酸化的Ba(NO ) 溶液生成白色沉淀,便
3 2
误以为有 SO,该错误是未注意 NO 在酸性环境中具有强氧化性,发生反应:Ba2++
SO===BaSO ↓(白色),3BaSO+2H++2NO===3BaSO (白色)+2NO↑+HO。
3 3 4 2
考点二 含硫化合物对环境的污染及治理
1.硫的氧化物的来源、危害及治理2.硫酸型酸雨的形成过程
1.酸雨的形成是一种复杂的大气化学和光学化学过程,在清洁空气、污染空气中形成硫酸
型酸雨的过程如图,下列有关说法错误的是( )
A.光照能引发酸雨的形成
B.所涉及的变化均为氧化还原反应
C.污染空气能加快酸雨的形成
D.优化能源结构能有效遏制酸雨污染
2.环保是21世纪人类社会的主要课题之一。火电厂、燃煤锅炉是SO 污染集中、规模较大
2
的行业,石灰石—石膏烟脱硫是除去SO 的一种常用方法。其过程如图1。
2
研究发现:pH和温度会对石灰石浆液的脱硫效率产生一定影响;当烟气通入速度一定时,
石灰石浆液的脱硫效率与浆液pH的关系如图2,下列有关说法正确的是( )
A.烟气通入石灰石浆液时的温度越高吸收越快,吸收率越高
B.石灰石浆液pH>5.7时,烟气脱硫效率降低的原因是石灰石的溶解度增大
C.将脱硫后的气体通入KMnO 溶液,可粗略判断烟气脱硫效率的高低
4
D.上述方法中用石灰石浆液吸收64 g SO 理论生成22 g CO
2 23.在工业上SO 尾气的处理方法一般有四种。
2
(1)钙基固硫法
为防治酸雨,工业上常用生石灰和含硫的煤混合后燃烧,燃烧时硫、生石灰、O 共同反应
2
生成硫酸钙,从而使硫转移到煤渣中,用化学方程式表示其原理。
①S的燃烧:S+O=====SO ;
2 2
②SO 转化为CaSO: ____________________________________________________;
2 3
③CaSO 转化为CaSO: __________________________________________________。
3 4
(2)氨水脱硫法
该脱硫法采用喷雾吸收法,雾化的氨水与烟气中的SO 直接接触吸收SO ,用化学方程式表
2 2
示其原理。
①SO 转化为(NH )SO : __________________________________________________
2 4 2 3
________________________________________________________________________;
②(NH )SO 转化为(NH )SO : ___________________________________________
4 2 3 4 2 4
________________________________________________________________________。
(3)钠碱脱硫法
钠碱脱硫法是用NaOH/Na CO 吸收烟气中的SO ,得到NaSO 和NaHSO ,用化学方程式
2 3 2 2 3 3
表示其原理。
①SO 和NaOH反应生成NaSO : _________________________________________
2 2 3
________________________________________________________________________;
②SO 和NaCO 反应生成NaSO : ________________________________________
2 2 3 2 3
________________________________________________________________________;
③NaSO 转化为NaHSO: _________________________________________________
2 3 3
________________________________________________________________________。
(4)双碱脱硫法
双碱脱硫法是指先用烧碱吸收SO ,再利用熟石灰浆液进行再生,再生后的NaOH碱液可循
2
环利用,用化学方程式表示其原理。
①NaOH吸收SO : ______________________________________________________;
2
②NaSO 被O 氧化:_______________________________________________________;
2 3 2
③NaSO 和Ca(OH) 反应: ________________________________________________
2 4 2
________________________________________________________________________ 。
1.正误判断,正确的打“√”,错误的打“×”。
(1)温室气体是形成酸雨的主要物质(2022·全国甲卷,7B)( )(2)用石灰石—石膏法对燃煤烟气进行脱硫,同时可得到石膏(2022·浙江6月选考,8D)( )
(3)燃煤中加入CaO可以减少酸雨的形成及温室气体的排放(2017·全国卷Ⅲ,7C)( )
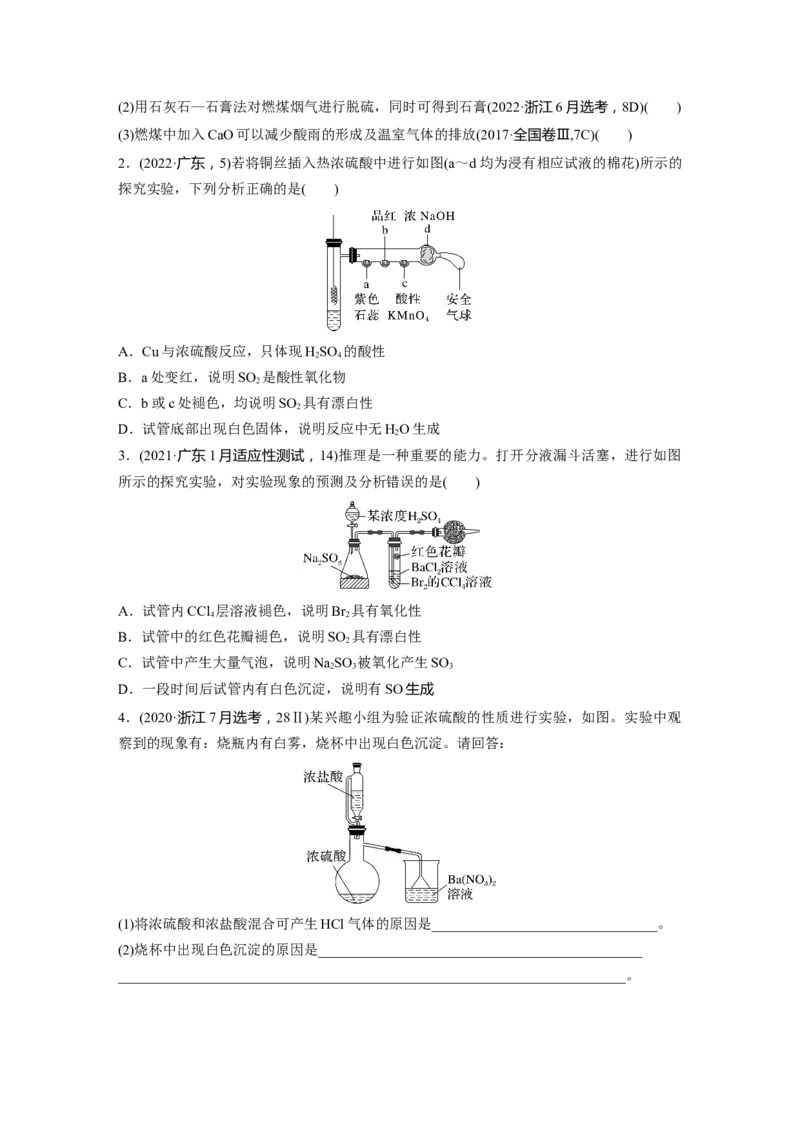
2.(2022·广东,5)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的
探究实验,下列分析正确的是( )
A.Cu与浓硫酸反应,只体现HSO 的酸性
2 4
B.a处变红,说明SO 是酸性氧化物
2
C.b或c处褪色,均说明SO 具有漂白性
2
D.试管底部出现白色固体,说明反应中无HO生成
2
3.(2021·广东1月适应性测试,14)推理是一种重要的能力。打开分液漏斗活塞,进行如图
所示的探究实验,对实验现象的预测及分析错误的是( )
A.试管内CCl 层溶液褪色,说明Br 具有氧化性
4 2
B.试管中的红色花瓣褪色,说明SO 具有漂白性
2
C.试管中产生大量气泡,说明NaSO 被氧化产生SO
2 3 3
D.一段时间后试管内有白色沉淀,说明有SO生成
4.(2020·浙江7月选考,28Ⅱ)某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观
察到的现象有:烧瓶内有白雾,烧杯中出现白色沉淀。请回答:
(1)将浓硫酸和浓盐酸混合可产生HCl气体的原因是________________________________。
(2)烧杯中出现白色沉淀的原因是______________________________________________
________________________________________________________________________。