文档内容
第 29 讲 化学键 分子的空间结构
复习目标 1.了解化学键的定义,了解离子键、共价键的形成。2.了解共价键的类型、共价
键的参数及作用。3.掌握电子式的书写。4.了解价层电子对互斥模型和杂化轨道理论的内容
并能用其推测简单分子或离子的空间结构。
考点一 化学键 电子式
1.化学键
(1)化学键的定义及分类
(2)离子键、共价键的比较
离子键 共价键
成键粒子 阴、阳离子 原子
成键实质 阴、阳离子的静电作用 共用电子对与成键原子间的静电作用
活泼金属与活泼非金属经电子得
同种元素原子之间成 不同种元素原子
形成条件 失,形成离子键;铵根离子与酸根
键 之间成键
离子之间形成离子键
非金属单质(稀有气
形成的 共价化合物或某
离子化合物 体除外);某些共价
物质 些离子化合物
化合物或离子化合物
2.共价键
(1)特征
具有饱和性和方向性。
(2)分类
分类依据 类型
形成共价键的原子轨 σ 键 轨道“头碰头”重叠
道重叠方式 π 键 轨道“肩并肩”重叠
形成共价键的电子对 极性键 共用电子对发生偏移是否偏移 非极性键 共用电子对不发生偏移
单键 原子间有一对共用电子对
原子间共用电子对的
双键 原子间有两对共用电子对
数目
三键 原子间有三对共用电子对
(3)键参数
①概念
②键参数对分子性质的影响
a.键能越大,键长越短,分子越稳定。
b.
3.化学键的表示方法——电子式
(1)概念:在元素符号周围用“·”或“×”来表示原子的最外层电子的式子。
(2)电子式书写常见的6大误区
内容 实例
漏写未参与成键的
误区1 N 的电子式误写为 ,应写为
2
电子
化合物类型不清
NaCl误写为 ,应写为 ;
误区2 楚,漏写或多写[
]及错写电荷数
HF误写为 ,应写为
书写不规范,错写
误区3
共用电子对 N 2 的电子式误写为 或 或
不考虑原子间的结
误区4
合顺序
HClO的电子式误写为 ,应写为
不考虑原子最外层
误区5 有几个电子,均写
CH的电子式误写为 ,应写为
成8电子结构不考虑AB 型离子
2
CaBr 的电子式为 ;
误区6 化合物中2个B是 2
分开写还是一起写 CaC 的电子式为
2
(3)用电子式表示化合物的形成过程
①离子化合物
如NaCl: 。
②共价化合物
如HCl: 。
1.所有物质中都存在化学键( )
2.AsH 的电子式: ( )
3
3.某元素的原子最外层只有一个电子,它跟卤素原子结合时,所形成的化学键一定是离子
键( )
4.共价键的成键原子只能是非金属原子( )
5.共价键键长是成键的两个原子半径之和( )
6.所有的共价键都有方向性( )
7.σ键能单独形成,而π键一定不能单独形成( )
8.σ键可以绕键轴旋转,π键一定不能绕键轴旋转( )
答案 1.× 2.× 3.× 4.× 5.× 6.× 7.√ 8.√
一、化学键与物质类别的关系
1.现有下列物质:①NaCl ②NaO ③NaO
2 2 2
④NaOH ⑤AlCl ⑥HO ⑦N ⑧NH Cl ⑨CO ○HO
3 2 2 4 2 2 2
(1)只含离子键的物质有________(填序号,下同),只含共价键的物质有__________。
(2)属于离子化合物的有__________,其中含非极性键的离子化合物有__________,含有非
极性键的共价化合物有__________。
答案 (1)①② ⑤⑥⑦⑨○ (2)①②③④⑧ ③ ○
判断离子化合物和共价化合物的三种方法二、共价键类型及数目的判断
2.CH 中的化学键从形成过程来看,属于________(填“σ”或“π”)键,从其极性来看属于
4
________键。
答案 σ 极性
3.已知CN-与N 结构相似,推算HCN分子中σ键与π键数目之比为________。
2
答案 1∶1
4.C 分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足 8
60
电子稳定结构,则一个C 分子中π键的数目为________。
60
答案 30
5.利用CO可以合成化工原料COCl ,COCl 分子的结构式为 ,每个COCl 分子
2 2 2
内含有的σ键、π键数目为________(填字母)。
A.4个σ键 B.2个σ键、2个π键
C.2个σ键、1个π键 D.3个σ键、1个π键
答案 D
6.1 mol丙酮分子中含有的σ键数目为__________。
答案 9N
A
通过物质的结构式,可以快速有效地判断键的种类及数目;判断成键方式时,需掌握:共价
单键全为σ键,共价双键中有一个σ键和一个π键,共价三键中有一个σ键和两个π键。
三、电子式的书写
7.(1)—OH______________,OH-______________,
HO+______________,NH______________;
3
(2)HClO______________,CCl ______________,
4CO______________,NH______________;
2 2 4
(3)Na S______________,NaH______________,
2
NaBH ______________,NaO______________。
4 2 2
答案 (1)
(2)
(3) Na+[H]-
电子式书写方法
考点二 分子的空间结构
1.价层电子对互斥模型
(1)理论要点
①价层电子对在空间上彼此相距最远时,排斥力最小,体系的能量最低。
②孤电子对的排斥力较大,孤电子对越多,排斥力越强,键角越小。
(2)用价层电子对互斥模型推测分子的空间结构的关键是判断分子中的中心原子上的价层电
子对数。其中:a是中心原子的价电子数(阳离子要减去电荷数、阴离子要加上电荷数),b是与中心
原子结合的原子最多能接受的电子数,x是与中心原子结合的原子数。
2.杂化轨道理论
(1)理论要点:中心原子上若干不同类型(主要是s、p轨道)、能量相近的原子轨道混合起来,
重新组合成同等数目、能量完全相同的新轨道。
(2)杂化轨道的类型
(3)中心原子的杂化轨道数和杂化类型判断
杂化轨道用来形成σ键和容纳孤电子对,所以有关系式:
杂化轨道的数目=中心原子上的孤电子对数+中心原子的 σ键电子对数(与中心原子直接相
连的原子个数)=中心原子的价层电子对数
(4)分子(AB 型)、离子(AB型)的空间结构分析示例
n
价层电子 中心原子
σ键电 孤电子 分子或离子的空
实例 对数(杂化 的杂化轨 VSEPR模型
子对数 对数 间结构
轨道数) 道类型
BeCl 直线形 直线形
2
2 2 0 sp
CO 直线形 直线形
2
BF 3 0 平面三角形
3
3 sp 2 平面三角形
SO 2 1 V 形
2
CH 4 0 正四面体形
4
NH 4 3 1 sp 3 四面体形 三角锥形
3
HO 2 2 V 形
2
CO 3 3 0 sp 2 平面三角形 平面三角形
NH 4 4 0 sp 3 四面体形 正四面体形1.价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数( )
2.分子中的中心原子若通过sp3杂化轨道成键,则该分子一定为正四面体结构( )
3.NH 分子为三角锥形,N原子发生sp2杂化( )
3
4.只要分子的空间结构为平面三角形,中心原子均为sp2杂化( )
5.中心原子是sp杂化的,其分子空间结构不一定为直线形( )
6.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对( )
答案 1.√ 2.× 3.× 4.√ 5.× 6.√
一、杂化类型和分子空间结构的判断
1.(1)AsCl 分子的空间结构为______________,其中As的杂化轨道类型为________。
3
(2)乙醛中碳原子的杂化轨道类型为________。
(3)在硅酸盐中,SiO四面体[如图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网
状四大类结构形式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化轨道类型
为________,Si与O的原子数之比为______,化学式为______。
答案 (1)三角锥形 sp3 (2)sp3、sp2 (3)sp3 1∶3 [SiO](或SiO)
3
解析 (1)AsCl 的中心原子(As原子)的价层电子对数为3+×(5-1×3)=4,所以是sp3杂化,
3
AsCl 分子的空间结构为三角锥形。(3)依据图(a)可知,SiO的空间结构类似于甲烷分子,为
3
正四面体形,硅原子的杂化轨道类型和甲烷分子中碳原子的杂化轨道类型相同,为 sp3;图
(b)是一种无限长单链结构的多硅酸根,每个结构单元中两个氧原子被两个结构单元顶角共
用,所以每个结构单元含有1个Si原子、3个O原子,Si原子和O原子数之比为1∶3,化
学式可表示为[SiO]或SiO。
3
判断分子中中心原子的杂化轨道类型的方法
(1)根据VSEPR模型、中心原子价层电子对数判断
如(AB 型)中心原子的价层电子对数为4,中心原子的杂化轨道类型为sp3;价层电子对数为
m
3,中心原子的杂化轨道类型为sp2;价层电子对数为2,中心原子的杂化轨道类型为sp。
(2)根据分子或离子中有无π键及π键数目判断
没有π键的为sp3杂化,如CH 中的C原子;含1个π键的为sp2杂化,如甲醛中的C原子以
4及苯环中的C原子;含2个π键的为sp杂化,如二氧化碳分子和乙炔分子中的碳原子。
二、键角的大小比较
2.(1)比较下列分子或离子中的键角大小(填“>”“<”或“=”):
①BF________NCl ,HO________CS 。
3 3 2 2
②HO________NH________CH,SO ________SO。
2 3 4 3
③HO________H S,NCl ________PCl 。
2 2 3 3
④NF ________NCl ,PCl ________PBr 。
3 3 3 3
(2)在 分子中,键角∠HCO________(填“>”“<”或“=”)∠HCH。理由是
________________________________________________________________________。
答案 (1)①> < ②< < > ③> > ④< < (2)> π键斥力大于σ键斥力
比较键角大小的三种思维模型
(1)杂化轨道类型不同:sp>sp2>sp3。
(2)
(3)在同一分子中,π键电子斥力大,键角大。
1.(2021·浙江1月选考,1)下列含有共价键的盐是( )
A.CaCl B.HSO
2 2 4
C.Ba(OH) D.NaCO
2 2 3
答案 D
解析 CaCl 只含有离子键,不含有共价键,故A错误;HSO 中只含有共价键,属于酸,
2 2 4
不是盐,B错误;Ba(OH) 既含有离子键又含有共价键,属于碱,不是盐,C错误;NaCO
2 2 3
中既含有离子键又含有共价键而且属于盐,D正确。
2.下列有关电子式表示正确的是( )
①次氯酸的电子式: (2019·浙江4月选考,7A)
②甲醛的电子式: (2021·浙江1月选考,5D改编)
③HCl的电子式: (2018·江苏,2B)④由Na和Cl形成离子键的过程: (2018·北京,8C)
A.①③ B.①④ C.②③ D.②④
答案 D
解析 HClO的电子式应为 ,①错误;HCl的电子式为 ,③错误;Na和Cl
形成离子键时,Na失去1个电子,Cl得到1个电子,且NaCl中存在离子键,④正确。
3.(2019·江苏,2)反应NH Cl+NaNO ===NaCl+N↑+2HO放热且产生气体,可用于冬天
4 2 2 2
石油开采。下列表示反应中相关微粒的化学用语正确的是( )
A.中子数为18的氯原子:Cl
B.N 的结构式:N==N
2
C.Na+的结构示意图:
D.HO的电子式:
2
答案 D
解析 A项,中子数为18的氯原子应表示为Cl,错误;B项,N 分子中N与N之间形成三
2
键,结构式为N≡N,错误;C项,Na+的结构示意图为 ,错误;D项,HO为共价
2
化合物,每个H原子和O原子之间共用一个电子对,正确。
4.(1)[2020·浙江7月选考,26(2)]CaCN 是离子化合物,各原子均满足8电子稳定结构,
2
CaCN 的电子式是________。
2
(2)[2021·天津,16(1)节选]CH 的电子式为__________________________________________。
4
(3)[2018·海南,13(3)]CO 的电子式为____________。
2
(4)[2017·海南,13(1)]PH 的电子式为_____________________________________________。
3
(5)[2016·全国卷Ⅱ,26(1)节选]联氨(N H)分子的电子式为__________________。
2 4
答案 (1) (2)
(3) (4)
(5)5.[2021·河北,17(4)]已知KH PO 是次磷酸的正盐,HPO 的结构式为__________________,
2 2 3 2
其中P采取______________杂化方式。
答案 sp3
解析 (4)含氧酸分子中只有羟基上的H可以电离;由KH PO 是次磷酸的正盐可知,HPO
2 2 3 2
为一元酸,其分子中只有一个羟基,另外2个H与P成键,还有一个O与P形成双键,故
其结构式为 ,其中P共形成4个σ键、没有孤电子对,故其价层电子对数为
4,采取sp3杂化。
6.[2021·山东,16(2)(3)](2)OF 分子的空间结构为________。
2
(3)Xe是第五周期的稀有气体元素,与F形成的XeF 室温下易升华。XeF 中心原子的价层电
2 2
子对数为____________,下列对XeF 中心原子杂化方式推断合理的是______________(填字
2
母)。
A.sp B.sp2
C.sp3 D.sp3d
答案 (2)角(V)形 (3)5 D
解析 (2)中心原子O的价层电子对数为+2=4,则OF 分子的空间结构是角(V)形。(3)XeF
2 2
易升华,所以是分子晶体,其中心原子的价层电子对数为2+=5,其中心原子的杂化方式
应为sp3d。
课时精练
1.在NH 和NH Cl存在的条件下,以活性碳为催化剂,用HO 氧化CoCl 溶液来制备化工
3 4 2 2 2
产品[Co(NH )]Cl ,下列表述正确的是( )
3 6 3
A.中子数为32,质子数为27的钴原子:Co
B.HO 的电子式:
2 2
C.NH 和NH Cl化学键类型相同
3 4
D.[Co(NH )]Cl 中Co的化合价是+3
3 6 3
答案 D
解析 A项,中子数为32,质子数为27的元素,质量数为27+32=59,表示为Co,错误;B项,HO 为共价化合物,电子式为 ,错误;C项,NH 中只存在共价键,
2 2 3
NH Cl中既存在离子键又存在共价键,二者化学键类型不同,错误;D项,[Co(NH )]Cl 中,
4 3 6 3
NH 整体为0价,Cl为-1价,所以Co的化合价为+3,正确。
3
2.下列关于化学键和化合物的说法正确的是( )
A.NaO、NaOH、CaCl 三种化合物含有相同的化学键
2 2 2
B.金属元素和非金属元素形成的化合物一定是离子化合物
C.非金属元素组成的化合物一定是共价化合物
D.HCl、HS溶于水时只破坏了共价键
2
答案 D
3.下列反应中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
A.NH HCO =====NH ↑+CO↑+HO
4 3 3 2 2
B.NH +HCl===NH Cl
3 4
C.2KOH+Cl===KCl+KClO+HO
2 2
D.2KO+2CO===2KCO+O
2 2 2 2 3 2
答案 D
4.下列分子中所有原子都满足最外层8电子稳定结构的是( )
A.六氟化氙(XeF ) B.次氯酸(HClO)
6
C.二氧化碳(CO) D.三氟化硼(BF)
2 3
答案 C
解析 XeF 中Xe不是8电子稳定结构,A错误;HClO中氢原子为2电子结构,B错误;
6
CO 中所有原子都满足最外层8电子稳定结构,C正确;BF 中硼原子不是8电子稳定结构,
2 3
D错误。
5.下列说法正确的是( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.NH NO 晶体中含共价键,是共价化合物
4 3
C.HO、NH 分子中只含有极性共价键
2 2 2 4
D.某化合物熔融状态能导电,可以证明该化合物内一定存在离子键
答案 D
解析 离子键是阴、阳离子间的静电作用,包括引力和斥力,故 A错误;硝酸铵是离子化
合物,含有离子键和共价键,故B错误;HO 的结构式为H—O—O—H,含有极性共价键
2 2
和非极性共价键,NH 中也是含有极性共价键和非极性共价键,故 C错误;离子化合物在
2 4
熔融状态下导电,共价化合物在熔融状态下不导电,故D正确。
6.(2022·大连期末)下列说法正确的是( )
A.PCl 分子的空间结构是三角锥形,这是因为P原子是以sp2杂化的结果
3B.sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道
C.凡中心原子采取sp3杂化的分子,其VSEPR模型都是四面体形
D.AB 型分子的空间结构必为平面三角形
3
答案 C
解析 A项,PCl 分子的中心原子P含有3个成键电子对和1个孤电子对,为sp3杂化,空
3
间结构为三角锥形,错误;B项,能量相近的s轨道和p轨道形成杂化轨道,错误;C项,
凡中心原子采取sp3杂化的分子,其VSEPR模型都是四面体形,而分子的空间结构还与含有
的孤电子对数有关,正确;D项,AB 型分子的空间结构与中心原子的孤电子对数也有关,
3
如BF 中B原子没有孤电子对,为平面三角形,NH 中N原子有1个孤电子对,为三角锥形,
3 3
错误。
7.下列有关描述正确的是( )
A.NO为V形分子
B.ClO的空间结构为平面三角形
C.NO的VSEPR模型、空间结构均为平面三角形
D.ClO的VSEPR模型、空间结构相同
答案 C
解析 NO中N原子的价层电子对数为3+×(5+1-2×3)=3,没有孤电子对,空间结构为
平面三角形,A项错误,C项正确;ClO中氯原子的价层电子对数为3+×(7+1-3×2)=
4,有1个孤电子对,VSEPR模型为四面体形,而空间结构为三角锥形,B、D项错误。
8.下列说法正确的是( )
①S 分子中S原子采用的杂化轨道类型为sp3
8
②C H 分子中只有以s轨道与sp2杂化轨道“头碰头”方式重叠而成的σ键
2 4
③SnBr 分子中Br—Sn—Br的键角<120°
2
④HO+中H—O—H的键角比HO中H—O—H的键角大
3 2
A.①② B.③④
C.①②③ D.①③④
答案 D
解析 ①S 是一个环形分子,每个S与两个其他S原子相连,S原子形成两个孤电子对,两
8
个σ键,所以S是sp3杂化,正确;②碳碳双键中一个是σ键,还有一个是π键,错误;
③SnBr 分子中,Sn原子的价层电子对数是×(4-2×1)+2=3,含有1个孤电子对,SnBr
2 2
的空间结构为V形,根据价层电子对互斥模型可以判断其键角小于120°,正确;④HO+、
3
HO的价层电子对互斥模型为四面体形,氧原子采取 sp3杂化,HO中O原子有两个孤电子
2 2
对,HO+
3
中O原子有1个孤电子对,导致HO+中H—O—H的键角比HO中H—O—H的键角大,正
3 2确。
9.缺电子化合物是指电子数不符合路易斯结构(一个原子通过共享电子使其价层电子数达到
8,H原子达到2所形成的稳定分子结构)要求的一类化合物。下列说法错误的是( )
A.NH 、BF、BF中只有BF 是缺电子化合物
3 3 3
B.BF、BF中心原子的杂化方式分别为sp2、sp3
3
C.BF 与NH 反应时有配位键生成
3 3
D.BF的键角小于NH
3
答案 D
解析 NH 的电子式为 ,BF 的电子式为 ,BF的电子式为 ,只
3 3
有BF 是缺电子化合物,故A正确;BF 中心原子B的价层电子对数为3+×(3-1×3)=3,
3 3
则杂化方式为sp2;BF中心原子B的价层电子对数为4+×(3+1-4×1)=4,则杂化方式为
sp3,故B正确;BF 与NH 反应时,NH 中N原子有孤电子对,BF 中B有空轨道,可生成
3 3 3 3
配位键,故C正确;BF和NH 均为sp3杂化,BF中心原子无孤电子对,NH 有1个孤电子
3 3
对,根据价层电子对互斥模型,孤电子对数增多,对成键电子的斥力增大,键角减小,则
BF的键角大于NH ,故D错误。
3
10.CH、—CH、CH都是重要的有机反应中间体,下列有关它们的说法错误的是( )
3
A.CH与HO+的空间结构均为三角锥形
3
B.它们的C均采取sp2杂化
C.CH中的所有原子均共面
D.CH与OH-形成的化合物中不含有离子键
答案 B
解析 CH与HO+中C原子与O原子价层电子对数都是4,且都含有1个孤电子对,均为三
3
角锥形结构,A项正确;CH、—CH 、CH中C的价层电子对数分别是3、4、4,根据价层
3
电子对互斥模型知,C原子杂化类型分别是sp2、sp3、sp3,B项错误;CH中的碳原子采取
sp2杂化,所有原子均共面,C项正确;CH与OH-形成的化合物是CHOH,属于共价化合
3
物,不含离子键,D项正确。
11.(2022·黄石模拟)下列说法错误的是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱与化学键的强弱有关
B.三硫化磷(P S)分子结构如图: ,1 mol P S 分子中含有9 mol共价键
4 3 4 3C.丙烯腈 分子中,碳原子的杂化方式有sp3、sp2
D.CO的结构可以表示为 ,所以CO分子中有一个π键是配位键
答案 C
解析 键能:H—F>H—Cl>H—Br>H—I,其热稳定性:HF>HCl>HBr>HI,A项正确;
由题图可知,1个PS 分子中有6个P—S、3个P—P共价键,则1 mol P S 分子中含有9
4 3 4 3
mol共价键,B项正确;由丙烯腈的结构可知,碳原子的杂化方式有sp、sp2,C项错误。
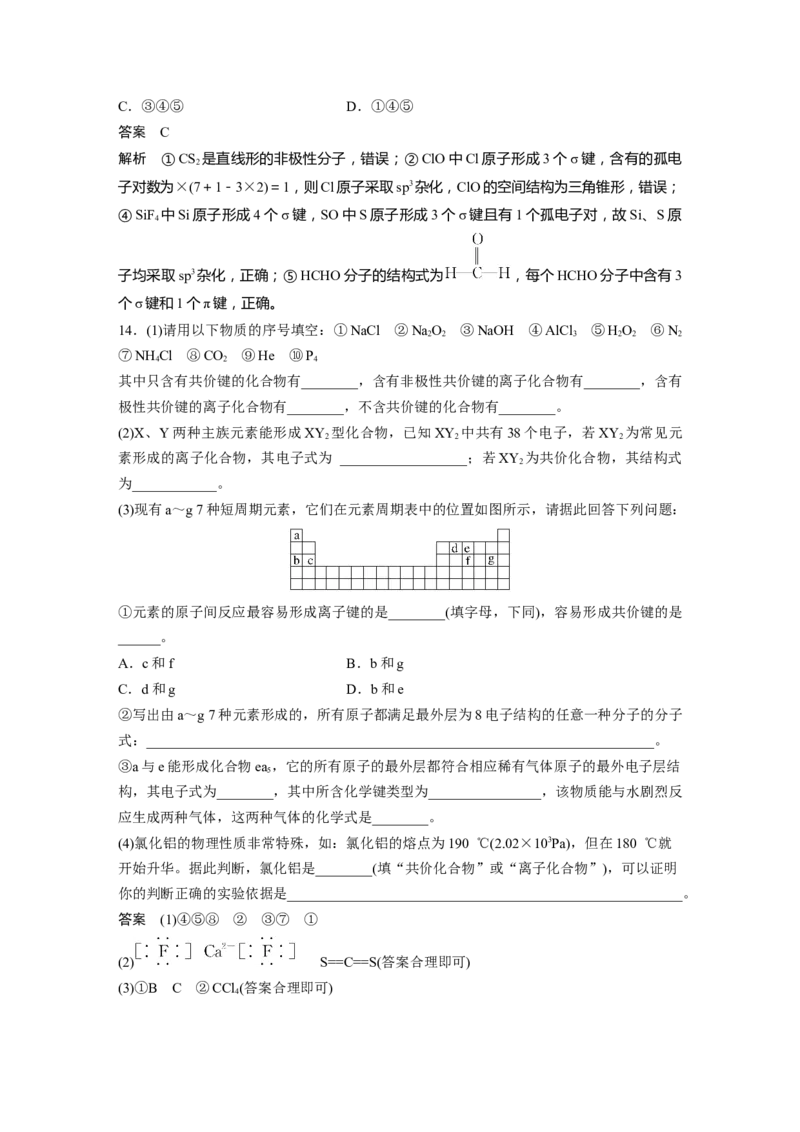
12.(2022·东营联考)氨基氰(CHN)中C、N原子均满足8电子稳定结构,福州大学王新晨
2 2
教授以其为原料制得类石墨相氮化碳(g-C N),其单层结构如图所示。下列说法错误的是(
3 4
)
A.氨基氰的结构式:
B.氮化碳的单层结构中,所有原子可能共平面
C.氨基氰易溶于水,氮化碳能导电
D.氨基氰和氮化碳中,N原子杂化方式均为sp2和sp3
答案 D
解析 氨基氰(CHN)中C、N原子均满足8电子稳定结构,每个N原子形成3个共价键、C
2 2
原子形成4个共价键,则该分子的结构式为 ,故A正确;类比石墨结构可知,
氮化碳的单层结构中,所有原子可能共平面,故B正确;氨基氰易与水形成氢键,则易溶
于水,类比石墨能导电,则氮化碳也能导电,故 C正确;氨基氰的结构式为 ,
碳氮三键中N原子采取sp杂化、氨基中N原子采取sp3杂化,故D错误。
13.下列描述正确的是( )
①CS 为V形的极性分子 ②ClO的空间结构为平面三角形 ③SF 中有6个完全相同的成
2 6
键电子对 ④SiF 和SO的中心原子均为sp3杂化 ⑤HCHO分子中既含σ键又含π键
4
A.①②③ B.②③④C.③④⑤ D.①④⑤
答案 C
解析 ①CS 是直线形的非极性分子,错误;②ClO中Cl原子形成3个σ键,含有的孤电
2
子对数为×(7+1-3×2)=1,则Cl原子采取sp3杂化,ClO的空间结构为三角锥形,错误;
④SiF 中Si原子形成4个σ键,SO中S原子形成3个σ键且有1个孤电子对,故Si、S原
4
子均采取sp3杂化,正确;⑤HCHO分子的结构式为 ,每个HCHO分子中含有3
个σ键和1个π键,正确。
14.(1)请用以下物质的序号填空:①NaCl ②NaO ③NaOH ④AlCl ⑤HO ⑥N
2 2 3 2 2 2
⑦NH Cl ⑧CO ⑨He ⑩P
4 2 4
其中只含有共价键的化合物有________,含有非极性共价键的离子化合物有________,含有
极性共价键的离子化合物有________,不含共价键的化合物有________。
(2)X、Y两种主族元素能形成XY 型化合物,已知XY 中共有38个电子,若XY 为常见元
2 2 2
素形成的离子化合物,其电子式为 __________________;若XY 为共价化合物,其结构式
2
为____________。
(3)现有a~g 7种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:
①元素的原子间反应最容易形成离子键的是________(填字母,下同),容易形成共价键的是
______。
A.c和f B.b和g
C.d和g D.b和e
②写出由a~g 7种元素形成的,所有原子都满足最外层为8电子结构的任意一种分子的分子
式:________________________________________________________________________。
③a与e能形成化合物ea,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结
5
构,其电子式为________,其中所含化学键类型为________________,该物质能与水剧烈反
应生成两种气体,这两种气体的化学式是________。
(4)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190 ℃(2.02×103Pa),但在180 ℃就
开始升华。据此判断,氯化铝是________(填“共价化合物”或“离子化合物”),可以证明
你的判断正确的实验依据是________________________________________________________。
答案 (1)④⑤⑧ ② ③⑦ ①
(2) S==C==S(答案合理即可)
(3)①B C ②CCl (答案合理即可)
4③ 极性共价键、离子键 NH 、H
3 2
(4)共价化合物 氯化铝在熔融状态下不导电
15.(2022·晋江模拟)(1)Cu2+处于[Cu(NH )]2+的中心,若将配离子[Cu(NH )]2+中的2个NH
3 4 3 4 3
换为CN-,则有2种结构,则Cu2+是否为sp3杂化?________(填“是”或“否”),理由为
______________________________________________________________________________。
(2)用价层电子对互斥模型推断甲醛中 H—C—H的键角________120°(填“>”“<”或
“=”)。
(3)SO Cl 和SO F 都属于AX E 型分子,S与O之间以双键结合,S与Cl、S与F之间以单
2 2 2 2 4 0
键结合。请你预测SO Cl 和SO F 分子的空间结构为__________________。SO Cl 分子中
2 2 2 2 2 2
∠Cl—S—Cl________SO F 分子中∠F—S—F(填“<”“>”或“=”)。
2 2
(4)抗坏血酸的分子结构如图所示,该分子中碳原子的杂化轨道类型为______________。
答案 (1)否 若是sp3杂化,[Cu(NH )]2+的空间结构为正四面体形,将配离子[Cu(NH )]2+
3 4 3 4
中的2个NH 换为CN-,则只有1种结构 (2)< (3)四面体形 > (4)sp2、sp3
3
解析 (2)甲醛分子中,碳氧之间为双键,根据价层电子对互斥模型可知双键与单键之间的
斥力大于单键与单键之间的斥力,所以H—C—H的键角小于120°。(3)当中心原子的价层电
子对数为4时,VSEPR模型为四面体形,硫原子无孤电子对,所以空间结构为四面体形;X
原子得电子能力越弱,A—X形成的共用电子对之间的斥力越强,F原子的得电子能力大于
氯原子,所以SO Cl 分子中∠Cl—S—Cl>SO F 分子中∠F—S—F。
2 2 2 2