文档内容
0
C.v
M正
>v
N逆
D.K
M
>K
N
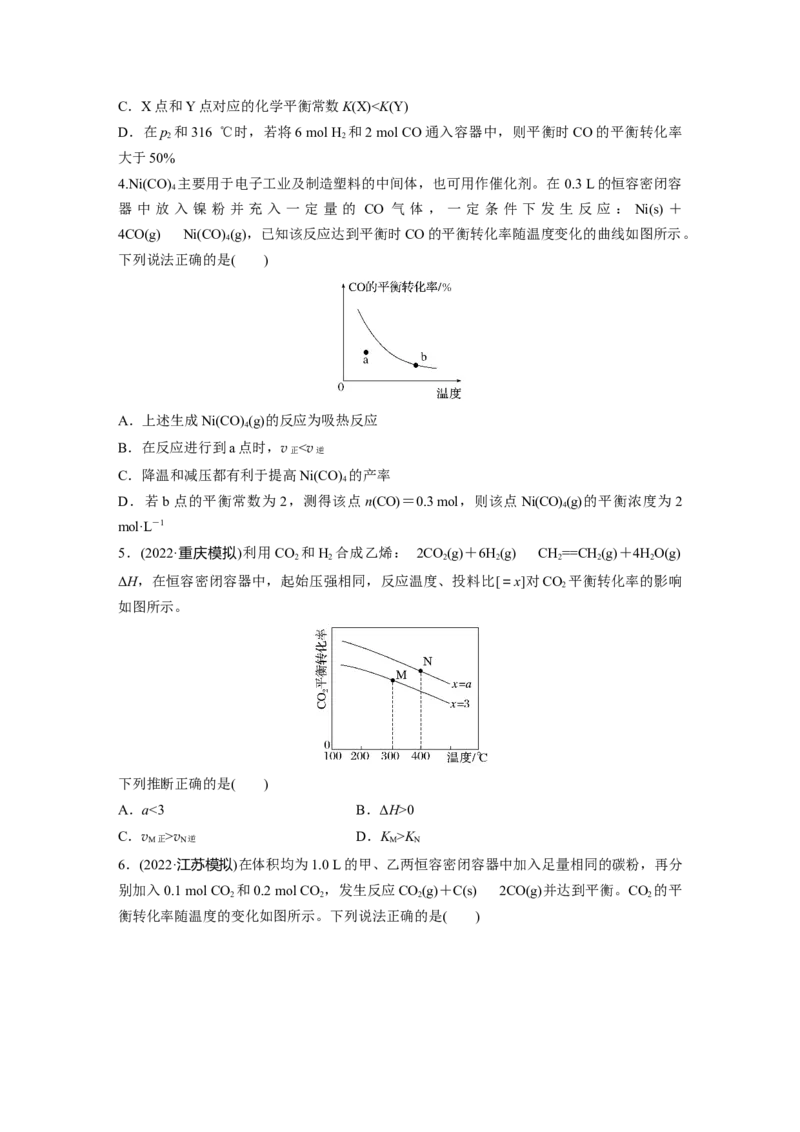
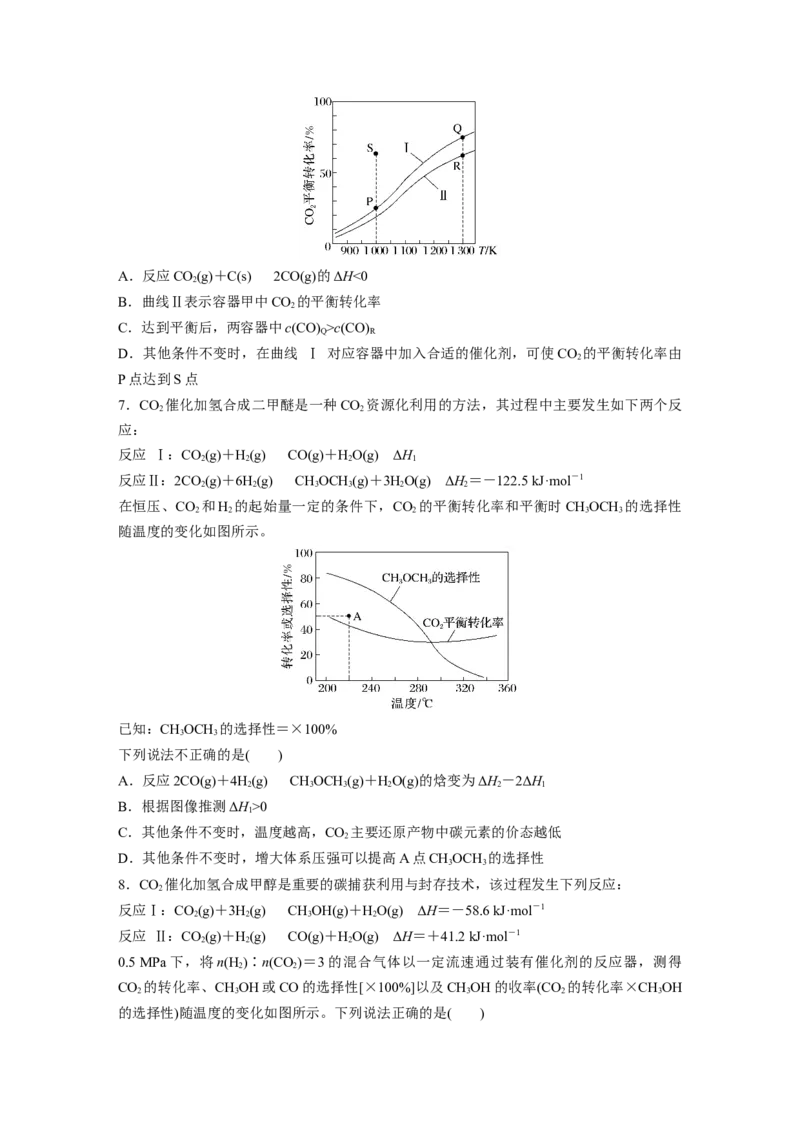
6.(2022·江苏模拟)在体积均为1.0 L的甲、乙两恒容密闭容器中加入足量相同的碳粉,再分
别加入0.1 mol CO 和0.2 mol CO ,发生反应CO(g)+C(s)2CO(g)并达到平衡。CO 的平
2 2 2 2
衡转化率随温度的变化如图所示。下列说法正确的是( )A.反应CO(g)+C(s)2CO(g)的ΔH<0
2
B.曲线Ⅱ表示容器甲中CO 的平衡转化率
2
C.达到平衡后,两容器中c(CO) >c(CO)
Q R
D.其他条件不变时,在曲线 Ⅰ 对应容器中加入合适的催化剂,可使CO 的平衡转化率由
2
P点达到S点
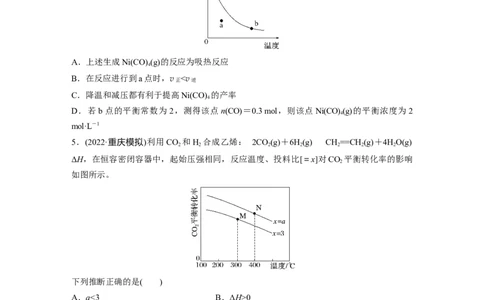
7.CO 催化加氢合成二甲醚是一种CO 资源化利用的方法,其过程中主要发生如下两个反
2 2
应:
反应 Ⅰ:CO(g)+H(g)CO(g)+HO(g) ΔH
2 2 2 1
反应Ⅱ:2CO(g)+6H(g)CHOCH (g)+3HO(g) ΔH=-122.5 kJ·mol-1
2 2 3 3 2 2
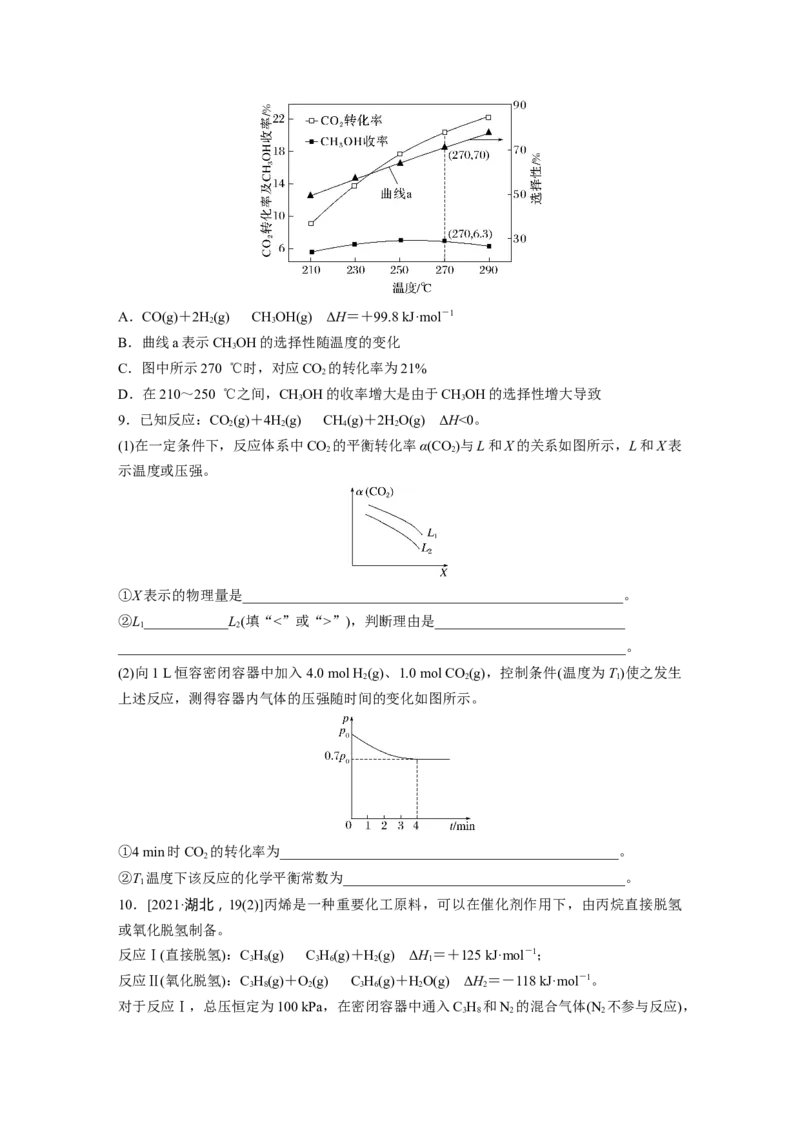
在恒压、CO 和H 的起始量一定的条件下,CO 的平衡转化率和平衡时CHOCH 的选择性
2 2 2 3 3
随温度的变化如图所示。
已知:CHOCH 的选择性=×100%
3 3
下列说法不正确的是( )
A.反应2CO(g)+4H(g)CHOCH (g)+HO(g)的焓变为ΔH-2ΔH
2 3 3 2 2 1
B.根据图像推测ΔH>0
1
C.其他条件不变时,温度越高,CO 主要还原产物中碳元素的价态越低
2
D.其他条件不变时,增大体系压强可以提高A点CHOCH 的选择性
3 3
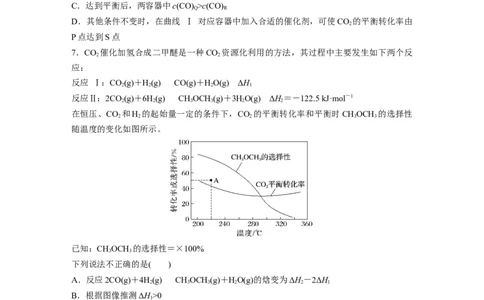
8.CO 催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程发生下列反应:
2
反应Ⅰ:CO(g)+3H(g)CHOH(g)+HO(g) ΔH=-58.6 kJ·mol-1
2 2 3 2
反应 Ⅱ:CO(g)+H(g)CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2
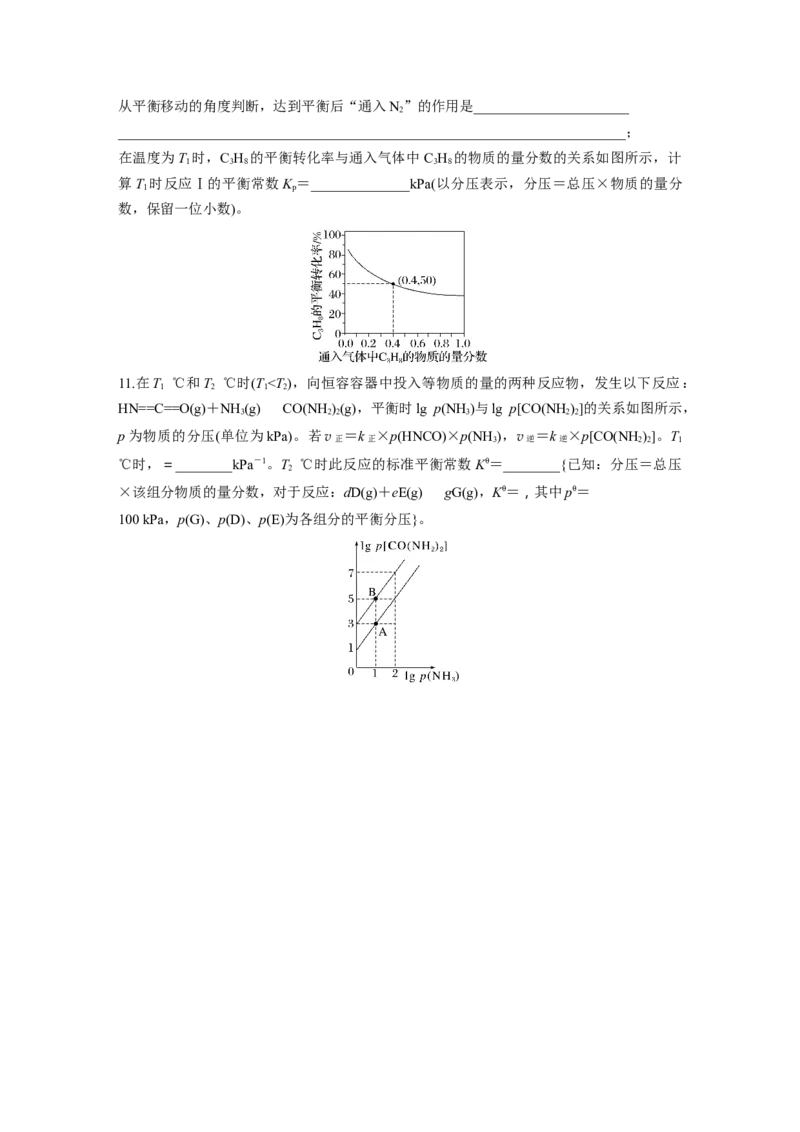
0.5 MPa下,将n(H )∶n(CO)=3的混合气体以一定流速通过装有催化剂的反应器,测得
2 2
CO 的转化率、CHOH或CO的选择性[×100%]以及CHOH的收率(CO 的转化率×CHOH
2 3 3 2 3
的选择性)随温度的变化如图所示。下列说法正确的是( )A.CO(g)+2H(g)CHOH(g) ΔH=+99.8 kJ·mol-1
2 3
B.曲线a表示CHOH的选择性随温度的变化
3
C.图中所示270 ℃时,对应CO 的转化率为21%
2
D.在210~250 ℃之间,CHOH的收率增大是由于CHOH的选择性增大导致
3 3
9.已知反应:CO(g)+4H(g)CH(g)+2HO(g) ΔH<0。
2 2 4 2
(1)在一定条件下,反应体系中CO 的平衡转化率α(CO)与L和X的关系如图所示,L和X表
2 2
示温度或压强。
①X表示的物理量是______________________________________________________。
②L____________L(填“<”或“>”),判断理由是___________________________
1 2
________________________________________________________________________。
(2)向1 L恒容密闭容器中加入4.0 mol H (g)、1.0 mol CO (g),控制条件(温度为T)使之发生
2 2 1
上述反应,测得容器内气体的压强随时间的变化如图所示。
①4 min时CO 的转化率为________________________________________________。
2
②T 温度下该反应的化学平衡常数为________________________________________。
1
10.[2021·湖北,19(2)]丙烯是一种重要化工原料,可以在催化剂作用下,由丙烷直接脱氢
或氧化脱氢制备。
反应Ⅰ(直接脱氢):C H(g)C H(g)+H(g) ΔH=+125 kJ·mol-1;
3 8 3 6 2 1
反应Ⅱ(氧化脱氢):C H(g)+O(g)C H(g)+HO(g) ΔH=-118 kJ·mol-1。
3 8 2 3 6 2 2
对于反应Ⅰ,总压恒定为100 kPa,在密闭容器中通入C H 和N 的混合气体(N 不参与反应),
3 8 2 2从平衡移动的角度判断,达到平衡后“通入N”的作用是______________________
2
________________________________________________________________________;
在温度为T 时,C H 的平衡转化率与通入气体中C H 的物质的量分数的关系如图所示,计
1 3 8 3 8
算T 时反应Ⅰ的平衡常数K =______________kPa(以分压表示,分压=总压×物质的量分
1 p
数,保留一位小数)。
11.在T ℃和T ℃时(T