文档内容
第 50 讲 常考化学反应速率和化学平衡图像的分析
[复习目标] 学会分析与化学反应速率和化学平衡相关的图像,能解答化学反应原理的相
关问题。
类型一 速率-时间图像
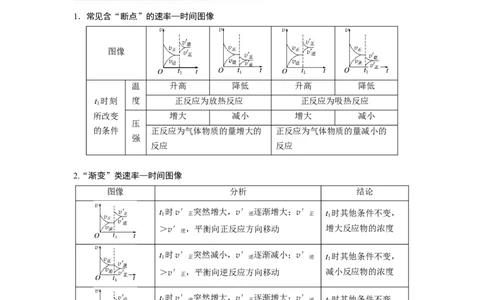
1.常见含“断点”的速率—时间图像
图像
温 升高 降低 升高 降低
t 时刻 度 正反应为放热反应 正反应为吸热反应
1
所改变 增大 减小 增大 减小
压
的条件 正反应为气体物质的量增大的 正反应为气体物质的量减小的
强
反应 反应
2.“渐变”类速率—时间图像
图像 分析 结论
t 1 时v′ 正 突然增大,v′ 逆 逐渐增大;v′ 正 t 1 时其他条件不变,
>v′
逆
,平衡向正反应方向移动 增大反应物的浓度
t 1 时v′ 正 突然减小,v′ 逆 逐渐减小;v′ 逆 t 1 时其他条件不变,
>v′
正
,平衡向逆反应方向移动 减小反应物的浓度
t 1 时v′ 逆 突然增大,v′ 正 逐渐增大;v′ 逆 t 1 时其他条件不变,
>v′
正
,平衡向逆反应方向移动 增大生成物的浓度
t 1 时v′ 逆 突然减小,v′ 正 逐渐减小;v′ 正 t 1 时其他条件不变,
>v′
逆
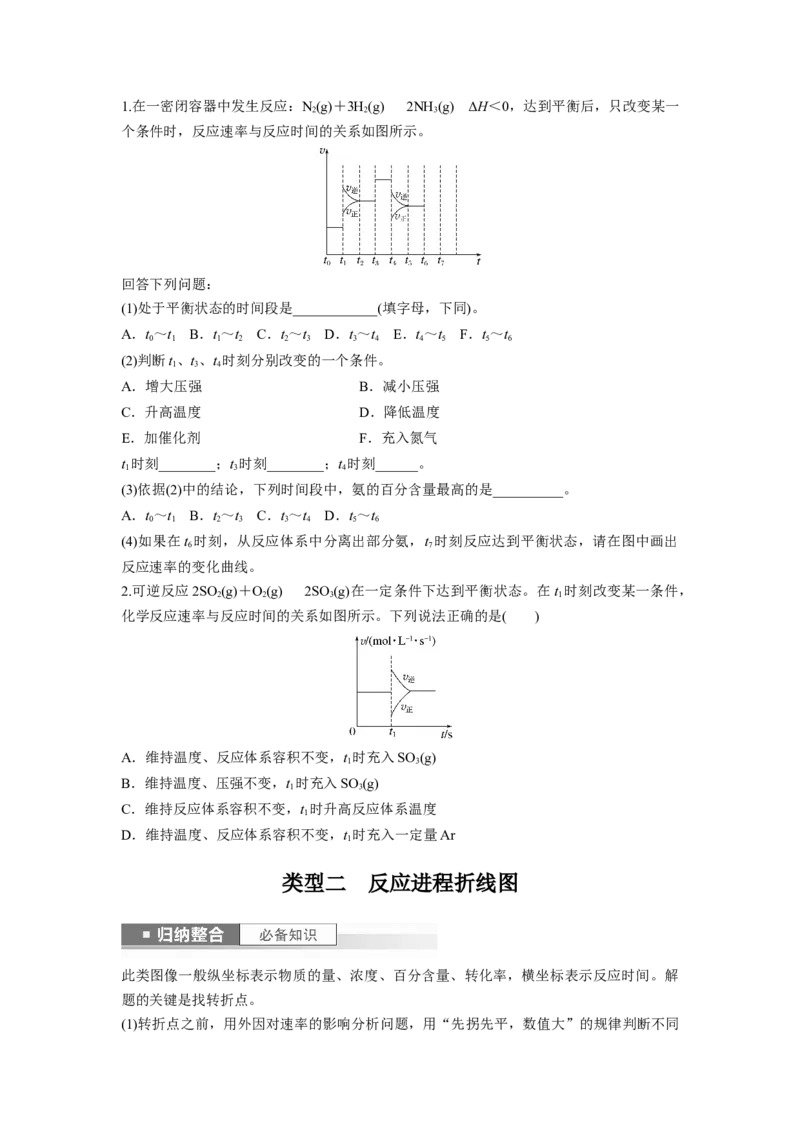
,平衡向正反应方向移动 减小生成物的浓度1.在一密闭容器中发生反应:N(g)+3H(g)2NH (g) ΔH<0,达到平衡后,只改变某一
2 2 3
个条件时,反应速率与反应时间的关系如图所示。
回答下列问题:
(1)处于平衡状态的时间段是____________(填字母,下同)。
A.t~t B.t~t C.t~t D.t~t E.t~t F.t~t
0 1 1 2 2 3 3 4 4 5 5 6
(2)判断t、t、t 时刻分别改变的一个条件。
1 3 4
A.增大压强 B.减小压强
C.升高温度 D.降低温度
E.加催化剂 F.充入氮气
t 时刻________;t 时刻________;t 时刻______。
1 3 4
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是__________。
A.t~t B.t~t C.t~t D.t~t
0 1 2 3 3 4 5 6
(4)如果在t 时刻,从反应体系中分离出部分氨,t 时刻反应达到平衡状态,请在图中画出
6 7
反应速率的变化曲线。
2.可逆反应2SO (g)+O(g)2SO (g)在一定条件下达到平衡状态。在t 时刻改变某一条件,
2 2 3 1
化学反应速率与反应时间的关系如图所示。下列说法正确的是( )
A.维持温度、反应体系容积不变,t 时充入SO (g)
1 3
B.维持温度、压强不变,t 时充入SO (g)
1 3
C.维持反应体系容积不变,t 时升高反应体系温度
1
D.维持温度、反应体系容积不变,t 时充入一定量Ar
1
类型二 反应进程折线图
此类图像一般纵坐标表示物质的量、浓度、百分含量、转化率,横坐标表示反应时间。解
题的关键是找转折点。
(1)转折点之前,用外因对速率的影响分析问题,用“先拐先平,数值大”的规律判断不同曲线表示温度或压强的大小。
(2)转折点之后是平衡状态或平衡移动,解题时要抓住量的变化,找出平衡移动的方向,利
用化学平衡移动原理推理分析。
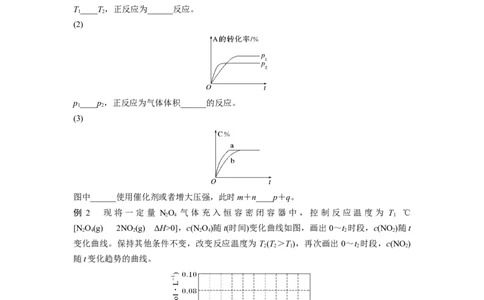
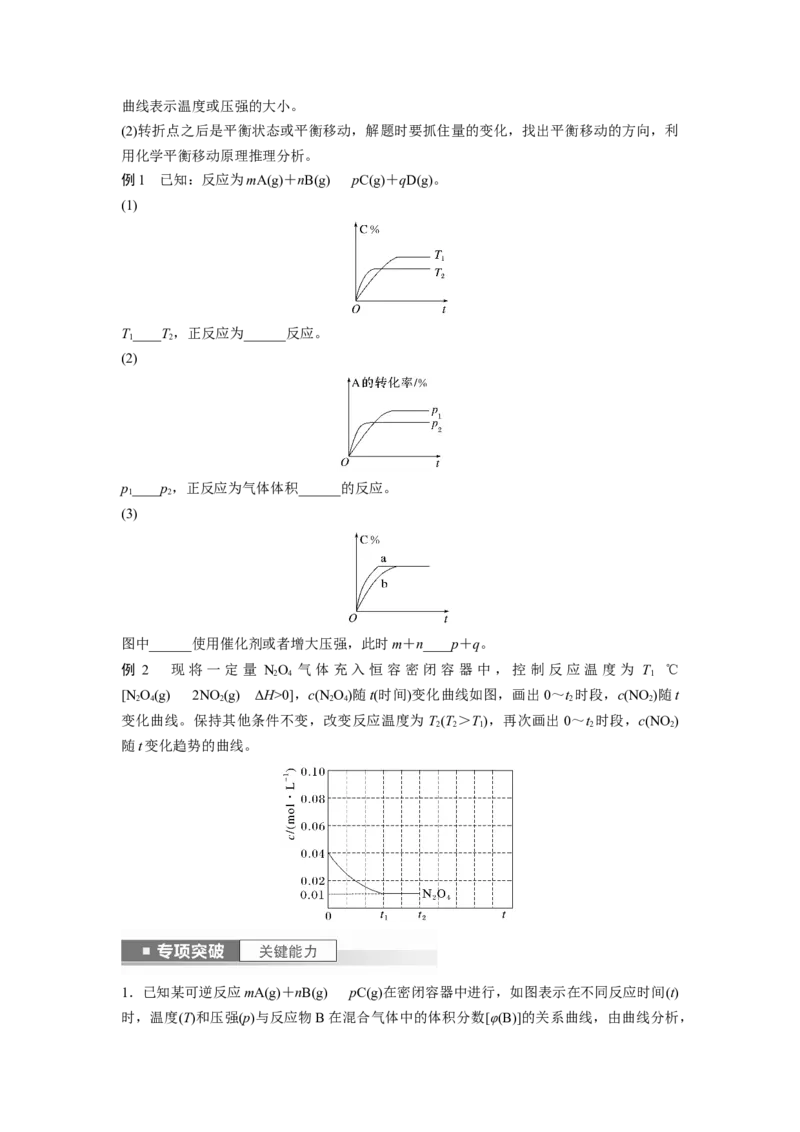
例1 已知:反应为mA(g)+nB(g)pC(g)+qD(g)。
(1)
T____T,正反应为______反应。
1 2
(2)
p____p,正反应为气体体积______的反应。
1 2
(3)
图中______使用催化剂或者增大压强,此时m+n____p+q。
例 2 现将一定量 NO 气体充入恒容密闭容器中,控制反应温度为 T ℃
2 4 1
[N O(g)2NO (g) ΔH>0],c(N O)随t(时间)变化曲线如图,画出0~t 时段,c(NO )随t
2 4 2 2 4 2 2
变化曲线。保持其他条件不变,改变反应温度为 T(T >T),再次画出0~t 时段,c(NO )
2 2 1 2 2
随t变化趋势的曲线。
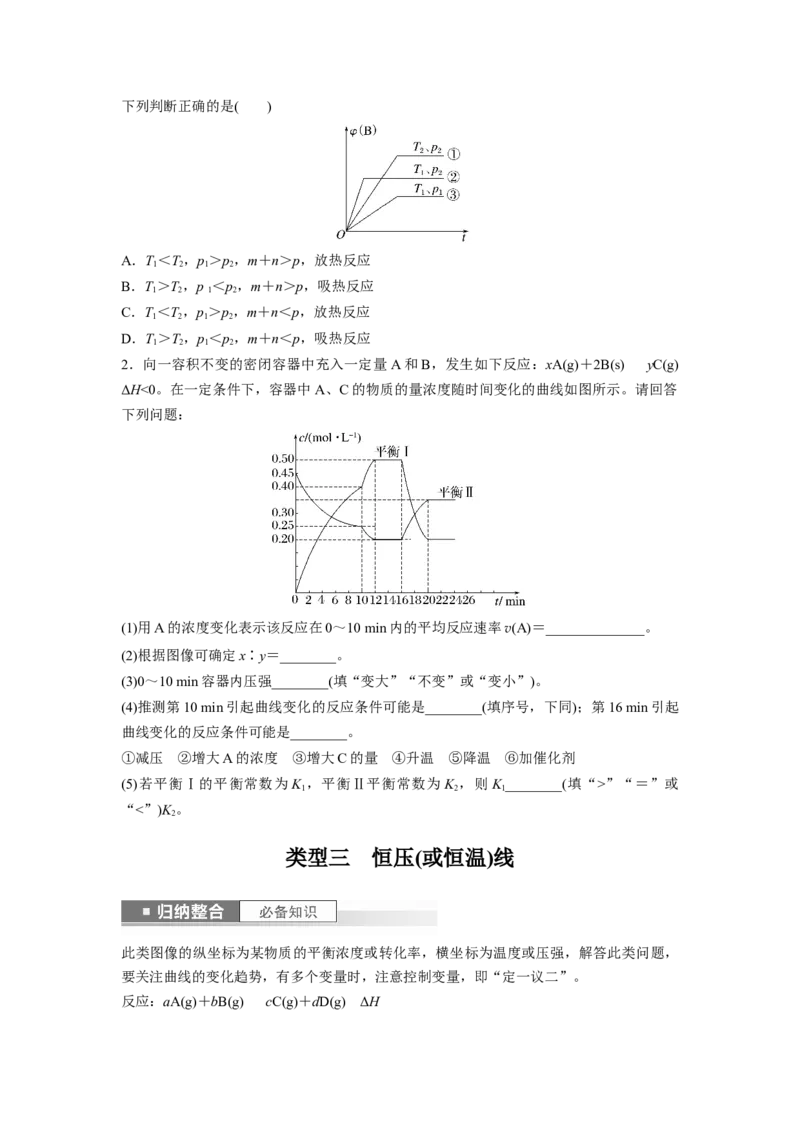
1.已知某可逆反应mA(g)+nB(g)pC(g)在密闭容器中进行,如图表示在不同反应时间(t)
时,温度(T)和压强(p)与反应物B在混合气体中的体积分数[φ(B)]的关系曲线,由曲线分析,下列判断正确的是( )
A.T<T,p>p,m+n>p,放热反应
1 2 1 2
B.T>T,p <p,m+n>p,吸热反应
1 2 1 2
C.T<T,p>p,m+n<p,放热反应
1 2 1 2
D.T>T,p<p,m+n<p,吸热反应
1 2 1 2
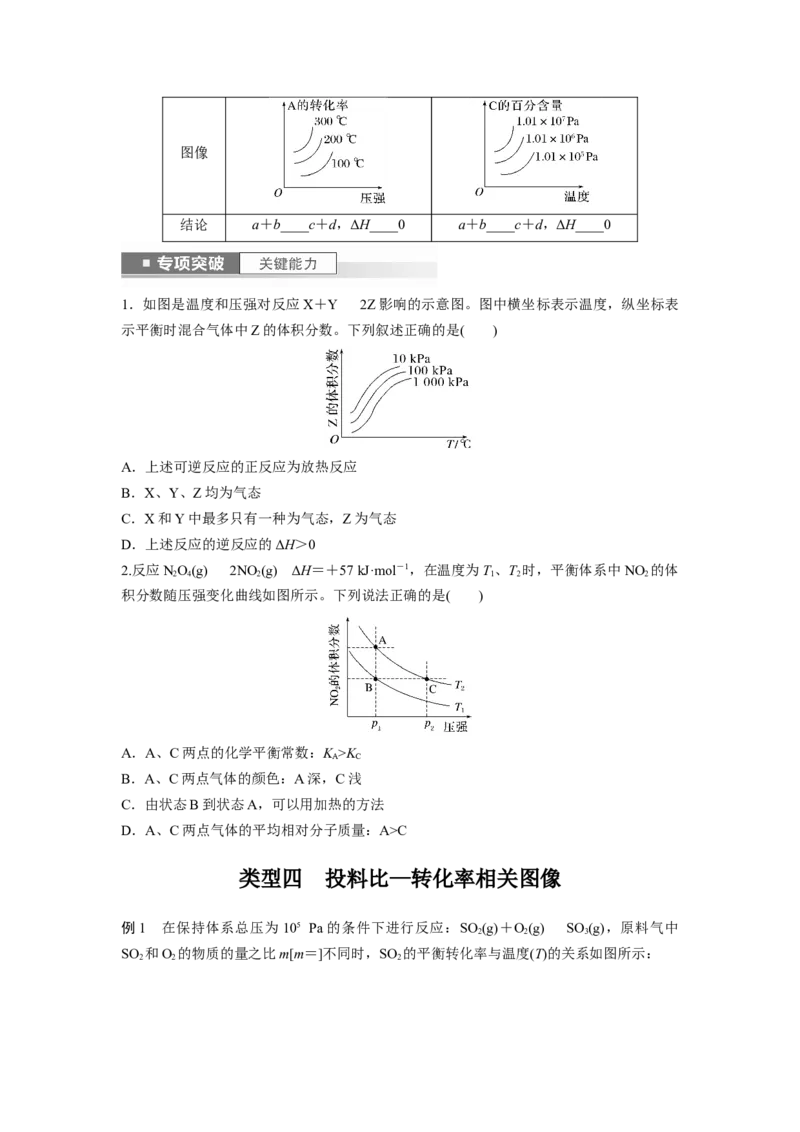
2.向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+2B(s)yC(g)
ΔH<0。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答
下列问题:
(1)用A的浓度变化表示该反应在0~10 min内的平均反应速率v(A)=______________。
(2)根据图像可确定x∶y=________。
(3)0~10 min容器内压强________(填“变大”“不变”或“变小”)。
(4)推测第10 min引起曲线变化的反应条件可能是________(填序号,下同);第16 min引起
曲线变化的反应条件可能是________。
①减压 ②增大A的浓度 ③增大C的量 ④升温 ⑤降温 ⑥加催化剂
(5)若平衡Ⅰ的平衡常数为K ,平衡Ⅱ平衡常数为K ,则K ________(填“>”“=”或
1 2 1
“<”)K 。
2
类型三 恒压(或恒温)线
此类图像的纵坐标为某物质的平衡浓度或转化率,横坐标为温度或压强,解答此类问题,
要关注曲线的变化趋势,有多个变量时,注意控制变量,即“定一议二”。
反应:aA(g)+bB(g)cC(g)+dD(g) ΔH图像
结论 a+b____c+d,ΔH____0 a+b____c+d,ΔH____0
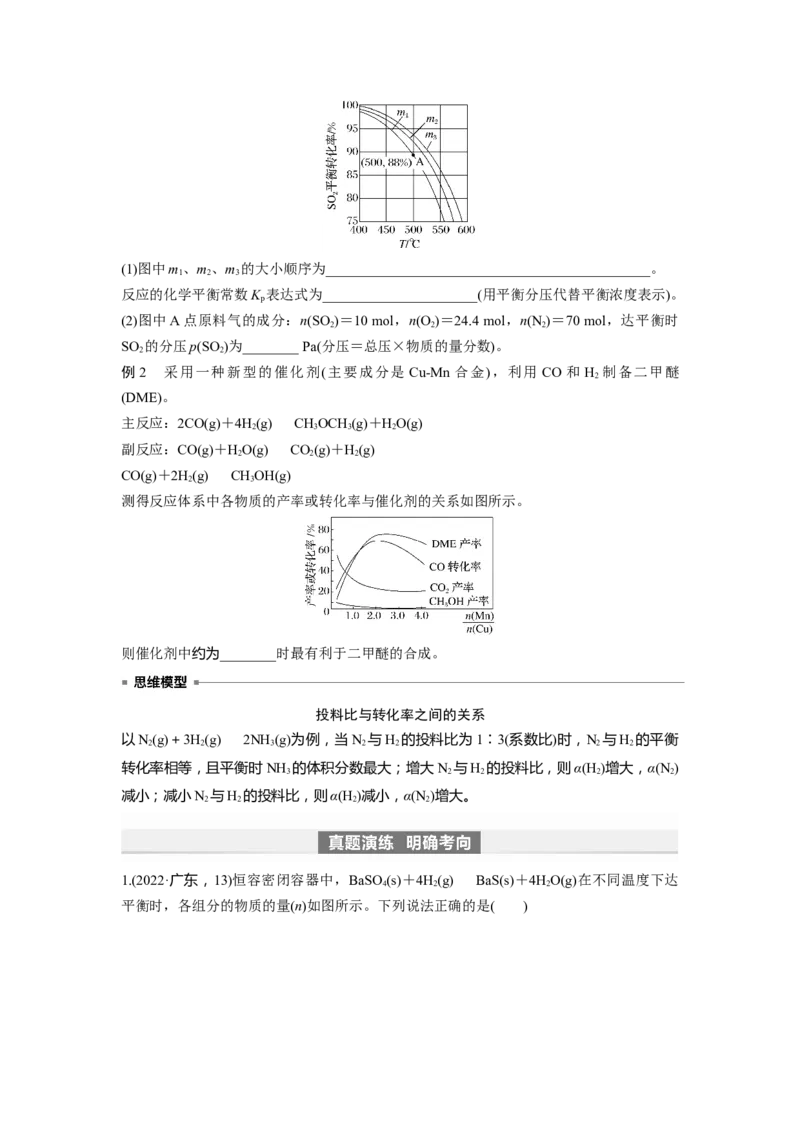
1.如图是温度和压强对反应X+Y2Z影响的示意图。图中横坐标表示温度,纵坐标表
示平衡时混合气体中Z的体积分数。下列叙述正确的是( )
A.上述可逆反应的正反应为放热反应
B.X、Y、Z均为气态
C.X和Y中最多只有一种为气态,Z为气态
D.上述反应的逆反应的ΔH>0
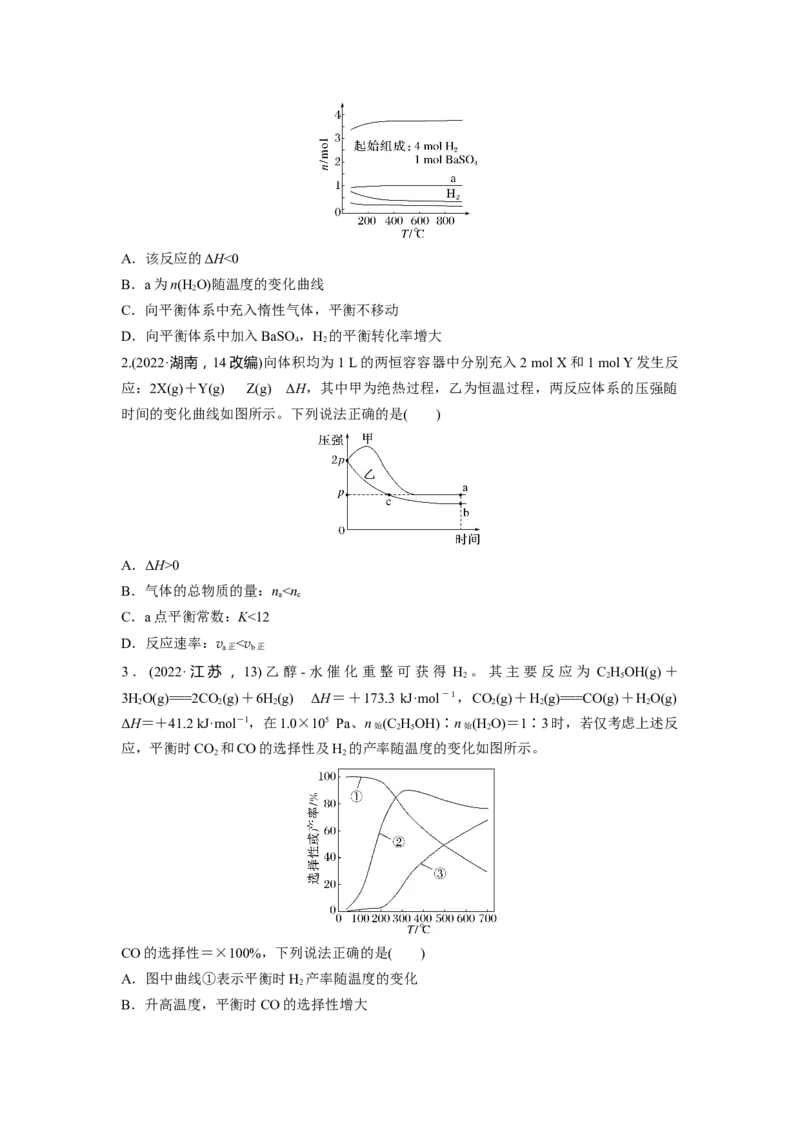
2.反应NO(g)2NO (g) ΔH=+57 kJ·mol-1,在温度为T 、T 时,平衡体系中NO 的体
2 4 2 1 2 2
积分数随压强变化曲线如图所示。下列说法正确的是( )
A.A、C两点的化学平衡常数:K >K
A C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
类型四 投料比—转化率相关图像
例1 在保持体系总压为 105 Pa的条件下进行反应:SO (g)+O(g)SO (g),原料气中
2 2 3
SO 和O 的物质的量之比m[m=]不同时,SO 的平衡转化率与温度(T)的关系如图所示:
2 2 2(1)图中m、m、m 的大小顺序为______________________________________________。
1 2 3
反应的化学平衡常数K 表达式为______________________(用平衡分压代替平衡浓度表示)。
p
(2)图中A点原料气的成分:n(SO )=10 mol,n(O )=24.4 mol,n(N )=70 mol,达平衡时
2 2 2
SO 的分压p(SO )为________ Pa(分压=总压×物质的量分数)。
2 2
例 2 采用一种新型的催化剂(主要成分是 Cu-Mn 合金),利用 CO 和 H 制备二甲醚
2
(DME)。
主反应:2CO(g)+4H(g)CHOCH (g)+HO(g)
2 3 3 2
副反应:CO(g)+HO(g)CO(g)+H(g)
2 2 2
CO(g)+2H(g)CHOH(g)
2 3
测得反应体系中各物质的产率或转化率与催化剂的关系如图所示。
则催化剂中约为________时最有利于二甲醚的合成。
投料比与转化率之间的关系
以N(g)+3H(g)2NH (g)为例,当N 与H 的投料比为1∶3(系数比)时,N 与H 的平衡
2 2 3 2 2 2 2
转化率相等,且平衡时NH 的体积分数最大;增大N 与H 的投料比,则α(H )增大,α(N )
3 2 2 2 2
减小;减小N 与H 的投料比,则α(H )减小,α(N )增大。
2 2 2 2
1.(2022·广东,13)恒容密闭容器中,BaSO(s)+4H(g)BaS(s)+4HO(g)在不同温度下达
4 2 2
平衡时,各组分的物质的量(n)如图所示。下列说法正确的是( )A.该反应的ΔH<0
B.a为n(H O)随温度的变化曲线
2
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入BaSO,H 的平衡转化率增大
4 2
2.(2022·湖南,14改编)向体积均为1 L的两恒容容器中分别充入2 mol X和1 mol Y发生反
应:2X(g)+Y(g)Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随
时间的变化曲线如图所示。下列说法正确的是( )
A.ΔH>0
B.气体的总物质的量:n