文档内容
第3讲 电解池、金属的腐蚀与防护
【2020·备考】
最新考纲:1.理解电解池的构成、工作原理及应用。2.能书写电极反应和总反应方
程式。3.了解金属发生电化学腐蚀的原因、金属腐蚀的危害以及防止金属腐蚀的措
施。
核心素养:1.变化观念与平衡思想:认识化学变化的本质是有新物质生成,并伴有
能量的转化;能多角度、动态地分析电解池中发生的反应,并运用电解池原理解决
实际问题。2.科学精神与社会责任:肯定电解原理对社会发展的重大贡献,具有可
持续发展意识和绿色化学观念,能对与电解有关的社会热点问题做出正确的价值
判断。考点一 电解原理
(频数:★★★ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 电
解原理是电化学重要的理论基础,掌握好放电顺序,总结好电解规律,是解答好电
解原理应用题的前提。另外对于设题方式多且灵活多变的实物图分析问题,应加
以关注。
1.电解定义
在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。
2.能量转化形式
电能转化为化学能。
3.电解池
(1)构成条件
①有与电源相连的两个电极。
②电解质溶液(或熔融盐)。
③形成闭合电路。
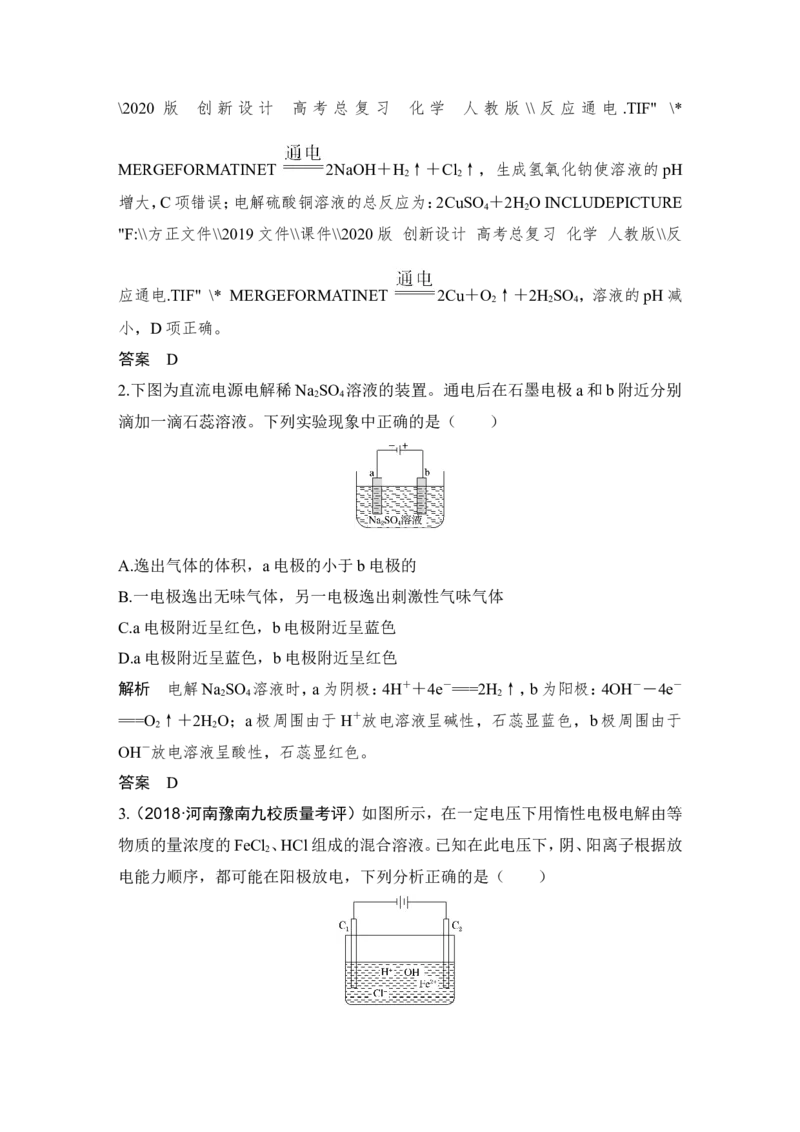
(2)电极名称及电极的反应式(如图)
(3)电子和离子的移动方向(惰性电极)4.电解过程
(1)首先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。
(2)再分析电解质水溶液的组成,找全离子并分阴、阳两组。
(3)然后排出阴、阳两极的放电顺序
阴极:阳离子放电顺序 Ag + >Fe 3 + >Cu 2 + >H +( 酸) >Fe 2 + >Zn 2 + >H +( 水) >Al 3 + >Mg 2 +
>Na + >Ca 2 + >K + 。
阳极:活泼电极> S 2 - >I - >Br - >Cl - >OH - >最高价含氧酸根离子。
(4)分析电极反应,判断电极产物,写出电极反应式,要注意遵循原子守恒和电荷
守恒。
(5)最后写出电解反应的总化学方程式或离子方程式。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.不要忘记水溶液中的H+和OH-,不要把H+、OH-误加到熔融电解质中。
2.最常用的放电顺序:阳极:活泼金属(一般指Pt、Au以外的金属)>Cl->OH-;阴
极:Ag+>Fe3+>Cu2+>H+,但如果离子浓度相差十分悬殊,离子浓度大的也可以先
放电,如理论上H+的放电能力大于Zn2+,由于溶液中c(Zn2+)≥c(H+),则先在
阴极上放电的是Zn2+,例如铁上镀锌时,放电顺序:Zn2+>H+。
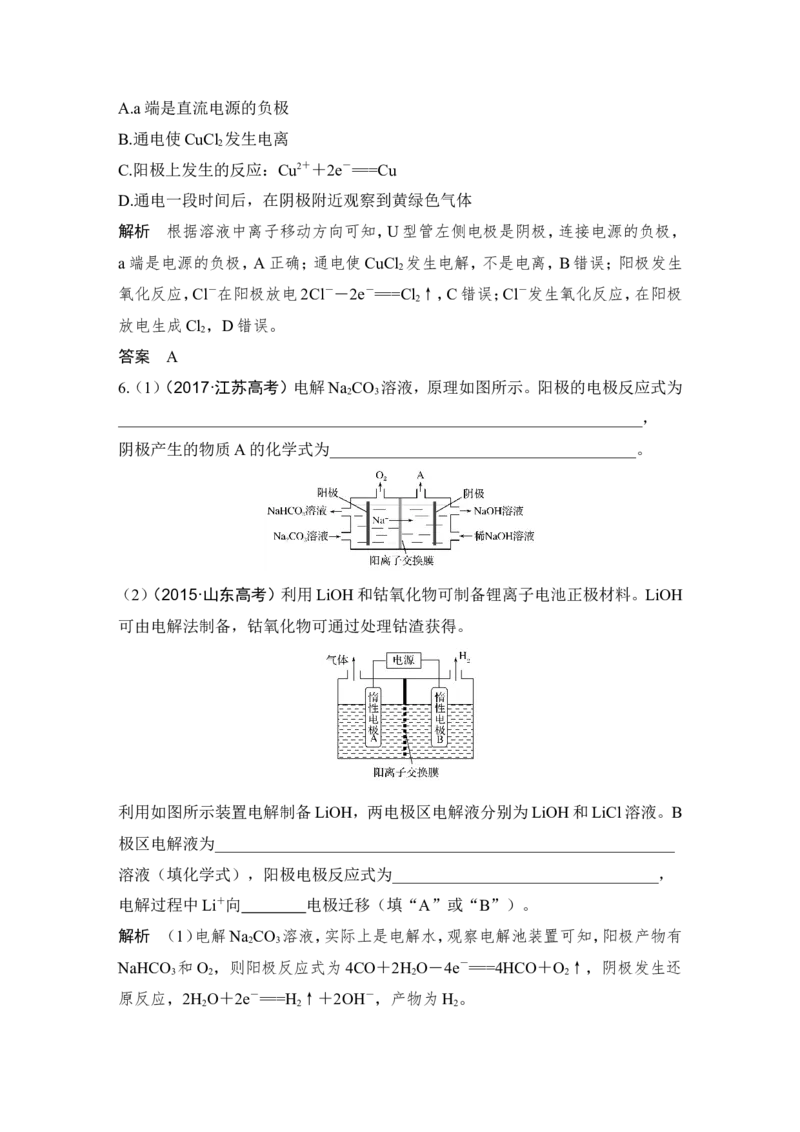
5.惰性电极电解电解质溶液的产物判断(图示)
[速查速测]1.(易混点排查)正确的打“√”,错误的打“×”
(1)电解质溶液的导电过程就是电解质溶液被电解的过程(√)
(2)电解CuCl 溶液,阴极逸出的气体能够使湿润的淀粉碘化钾试纸变蓝色(×)
2
(3)电解时,电子的移动方向为:电源负极→阴极→阳极→电源正极(×)
(4)电解盐酸、硫酸等溶液,H+放电,溶液的pH逐渐增大(×)
(5)用惰性电极电解CuSO 溶液一段时间后,加入Cu(OH)可使电解质溶液恢
4 2
复到电解前的情况(×)
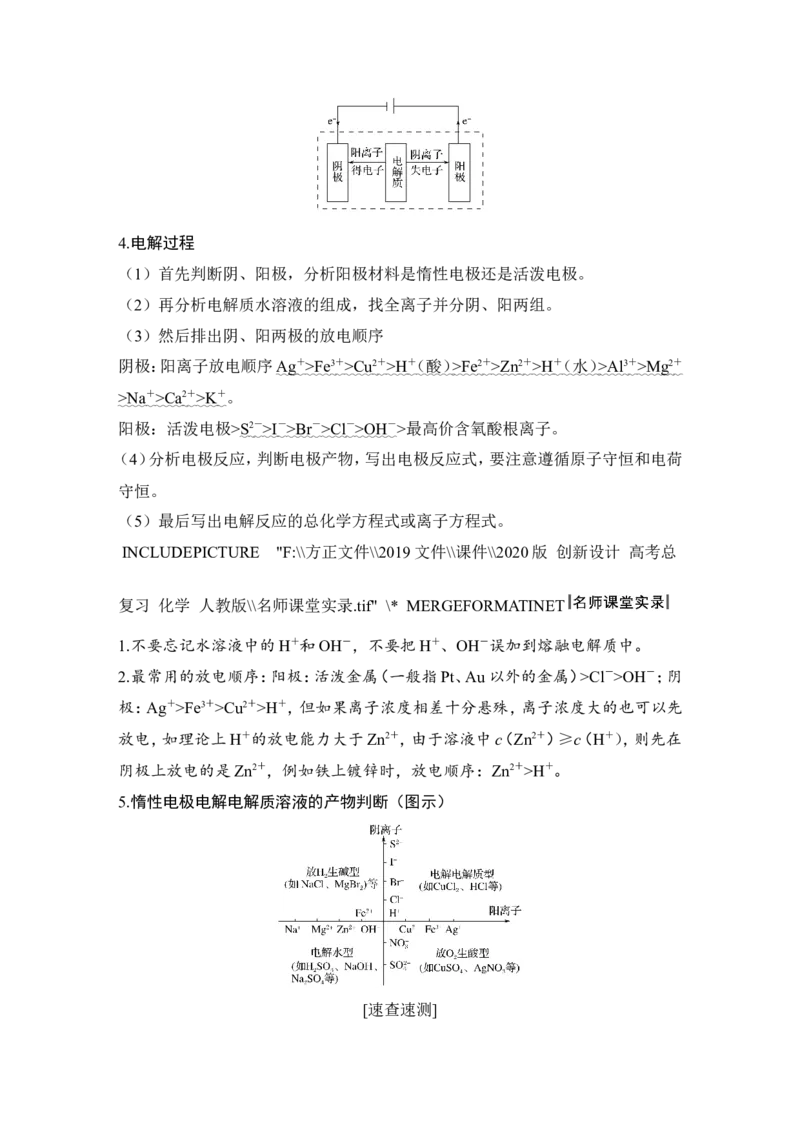
2(. 教材知识拓展题)要实现反应:Cu+2HCl===CuCl +H ↑,设计了下列四个实
2 2
验,你认为可行的是( )
解析 铜与盐酸不能直接发生反应,由于不是能自发进行的氧化还原反应,故不
能设计成原电池,即A、B选项不符合;由于铜失去电子,故铜作阳极,与电源的正
极相连,选项C符合。
答案 C
3(. 探究思考题)用惰性电极电解2 mol·L-1 NaCl和1 mol·L-1 CuSO 的混合溶液,
4
可看做两个电解阶段,试判断在两个阶段中阴、阳两极得到的产物是什么?并写
出相应的电极反应式。
第 一 阶 段 : 阳 极 产 物 , 电 极 反 应
_____________________________________________________________________;
阴 极 产 物 , 电 极 反 应
_____________________________________________________________________。
第 二 阶 段 : 阳 极 产 物 , 电 极 反 应
_____________________________________________________________________。阴 极 产 物 , 电 极 反 应
_____________________________________________________________________。
答案 Cl 2Cl--2e-===Cl ↑
2 2
Cu Cu2++2e-===Cu
O 4OH--4e-===2H O+O ↑
2 2 2
H 4H++4e-===2H ↑
2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.下列装置的线路接通后,经过一段时间,溶液的pH明显减小的是( )
解析 A项,该装置是原电池装置,H+放电生成氢气,溶液的pH增大,A项错误;
B项,阳极:Cu-2e-+2OH-===Cu(OH)↓,阴极:2H O+2e-===H ↑+2OH-,
2 2 2
总反应为:Cu+2H O INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020
2
版 创 新 设 计 高 考 总 复 习 化 学 人 教 版 \\ 反 应 通 电 .TIF" \*
MERGEFORMATINET Cu(OH)+H ↑,pH增大,B项错误;电解食盐水,
2 2
总反应为:2NaCl+2H O INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\
2\2020 版 创 新 设 计 高 考 总 复 习 化 学 人 教 版 \\ 反 应 通 电 .TIF" \*
MERGEFORMATINET 2NaOH+H ↑+Cl ↑,生成氢氧化钠使溶液的pH
2 2
增大,C项错误;电解硫酸铜溶液的总反应为:2CuSO +2H O INCLUDEPICTURE
4 2
"F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\反
应通电.TIF" \* MERGEFORMATINET 2Cu+O ↑+2H SO ,溶液的pH减
2 2 4
小,D项正确。
答案 D
2.下图为直流电源电解稀Na SO 溶液的装置。通电后在石墨电极a和b附近分别
2 4
滴加一滴石蕊溶液。下列实验现象中正确的是( )
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
解析 电解Na SO 溶液时,a为阴极:4H++4e-===2H ↑,b为阳极:4OH--4e-
2 4 2
===O ↑+2H O;a极周围由于H+放电溶液呈碱性,石蕊显蓝色,b极周围由于
2 2
OH-放电溶液呈酸性,石蕊显红色。
答案 D
3.(2018·河南豫南九校质量考评)如图所示,在一定电压下用惰性电极电解由等
物质的量浓度的FeCl 、HCl组成的混合溶液。已知在此电压下,阴、阳离子根据放
2
电能力顺序,都可能在阳极放电,下列分析正确的是( )A.C 电极上的电极反应式为2H O+2e-===2OH-+H ↑
1 2 2
B.C 电极处溶液首先变黄色
1
C.C 电极上可依次发生的电极反应为Fe2+-e-===Fe3+、2Cl--2e-===Cl ↑
2 2
D.当C 电极上有2 g物质生成时,就会有2N 个电子通过溶液发生转移
1 A
解析 C 电极与电源的负极相连,作阴极,溶液中的H+在阴极放电,电极反应式
1
为2H++2e-===H ↑,A错误;C 电极上H+放电生成H ,C 电极与电源的正极相
2 1 2 2
连,作阳极,Fe2+的还原性强于Cl-,则依次发生的电极反应为Fe2+-e-===
Fe3+、2Cl--2e-===Cl ↑,故C 电极处溶液首先变黄色,B错误,C正确;电子只
2 2
能通过导线传递,不能通过溶液传递,D错误。
答案 C
【原创总结】
以惰性电极电解电解质溶液的类型和规律
类型 放电规律 电解质(水溶液)
含氧酸(如H SO )
2 4
H+、OH-放电,电解质形成的阳离子要么
是H+,要么是放电顺序排在H+之后的活
电解水型 泼性较强的金属对应的阳离子;阴离子要
么是OH-,要么是放电顺序排在OH-之 强碱(如NaOH)
后的含氧酸根等。
活泼金属的含氧酸盐
电解质形成的阴、阳离子放电,电解质电
无氧酸(如HCl),除HF
电解电
离形成的阴、阳离子要么是H+、OH-,要 外么是放电顺序排在H+、OH-之前的对应
解质型 不活泼金属的无氧酸盐
离子。
(如CuCl ),除氟化物外
2
阳离子为放电顺序排在H+之后的金属阳
放H 生 活泼金属的无氧酸盐(如
2 离子;阴离子为放电顺序排在OH-之前的
碱型 NaCl)
阴离子。
阳离子为放电顺序排在H+之前的金属阳
放O 生 不活泼金属的含氧酸盐
2 离子;阴离子为放电顺序排在OH-之后的
酸型 (如CuSO )
阴离子。 4
说明:请同学们写出上述实例中的半反应和总反应的离子方程式,并分析电解后
溶液的pH变化。
[B组 考试能力过关]
4(. 海南高考)以石墨为电极,电解KI溶液(其中含有少量酚酞和淀粉)。下列说法
错误的是( )
A.阴极附近溶液呈红色 B.阴极逸出气体
C.阳极附近溶液呈蓝色 D.溶液的pH变小
解 析 以 石 墨 为 电 极 , 电 解 KI 溶 液 , 发 生 的 反 应 为 2KI + 2H O
2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\反应通电.TIF" \* MERGEFORMATINET 2KOH+
H ↑+I(类似于电解饱和食盐水),阴极产物是H 和KOH,阳极产物是I 。由于
2 2 2 2
溶液中含有少量的酚酞和淀粉,所以阳极附近的溶液会变蓝(淀粉遇碘变蓝),阴
极附近的溶液会变红(溶液呈碱性),A、B、C正确;由于电解产物有KOH生成,所
以溶液的pH逐渐增大,D错误。
答案 D
5.(北京高考)用石墨电极电解CuCl 溶液(见图)。下列分析正确的是( )
2A.a端是直流电源的负极
B.通电使CuCl 发生电离
2
C.阳极上发生的反应:Cu2++2e-===Cu
D.通电一段时间后,在阴极附近观察到黄绿色气体
解析 根据溶液中离子移动方向可知,U型管左侧电极是阴极,连接电源的负极,
a端是电源的负极,A正确;通电使CuCl 发生电解,不是电离,B错误;阳极发生
2
氧化反应,Cl-在阳极放电2Cl--2e-===Cl ↑,C错误;Cl-发生氧化反应,在阳极
2
放电生成Cl ,D错误。
2
答案 A
6.(1)(2017·江苏高考)电解Na CO 溶液,原理如图所示。阳极的电极反应式为
2 3
_________________________________________________________________,
阴极产生的物质A的化学式为______________________________________。
(2)(2015·山东高考)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH
可由电解法制备,钴氧化物可通过处理钴渣获得。
利用如图所示装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B
极区电解液为_________________________________________________________
溶液(填化学式),阳极电极反应式为_________________________________,
电解过程中Li+向 电极迁移(填“A”或“B”)。
解析 (1)电解Na CO 溶液,实际上是电解水,观察电解池装置可知,阳极产物有
2 3
NaHCO 和O ,则阳极反应式为4CO+2H O-4e-===4HCO+O ↑,阴极发生还
3 2 2 2
原反应,2H O+2e-===H ↑+2OH-,产物为H 。
2 2 2(2)根据电解装置图,两电极区电解液分别为LiOH和LiCl溶液,B极区产生H ,
2
电极反应式为2H O+2e-===H ↑+2OH-,OH-与Li+结合生成LiOH,所以B极
2 2
区电解液应为LiOH溶液,B电极为阴极,则A电极应为阳极,阳极区电解液应为
LiCl溶液,电极反应式为2Cl--2e-===Cl ↑。电解过程中,阳离子向阴极迁移,则
2
Li+向B电极迁移。
答案 (1)4CO+2H O-4e-===4HCO+O ↑ H
2 2 2
(2)LiOH 2Cl--2e-===Cl ↑ B
2考点二 电解原理的应用
(频数:★★★ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 电
解原理的综合应用是高考考查的重要内容,在掌握好电解原理基本应用的基础上,
要特别关注电解在物质制备、污水处理等方面的拓展应用,在分析电解装置时,应
注意半透膜的作用。
1.电解饱和食盐水
(1)电极反应
阳极反应式: 2Cl - - 2e - == =Cl ↑(氧化反应)
2
阴极反应式: 2H + + 2e - == =H ↑(还原反应)
2
(2)总反应方程式
2NaCl+2H O=====2NaOH+H ↑+Cl ↑
2 2 2
离子反应方程式: 2Cl - + 2H O ===== 2OH - + H ↑ + C l ↑
2 2 2
(3)应用:氯碱工业制烧碱、氢气和氯气
阳极:钛网(涂有钛、钌等氧化物涂层)。
阴极:碳钢网。
阳离子交换膜:
①只允许阳离子通过,能阻止阴离子和气体通过。
②将电解槽隔成阳极室和阴极室。2.电解精炼铜
3.电镀铜
4.电冶金
利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等
总方程式 阳极、阴极反应式
2Cl--2e-===Cl ↑
2
冶炼钠 2NaCl(熔融)=====2Na+Cl ↑
2
2Na++2e-===2Na
2Cl--2e-===Cl ↑
2
冶炼镁 MgCl (熔融)=====Mg+Cl ↑
2 2
Mg2++2e-===Mg
6O 2 - - 12e - == =3O ↑
2
冶炼铝 2Al O(熔融)=====4Al+3O ↑
2 3 2
4Al 3 + + 12e - == =4Al
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
由于AlCl 为共价化合物熔融状态下不导电,所以电解冶炼铝时,电解的为熔点很
3高的氧化铝,为降低熔点,加入了助熔剂冰晶石(Na AlF );而且电解过程中,阳极
3 6
生成的氧气与石墨电极反应,所以石墨电极需不断补充。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)电镀铜和电解精炼铜时,电解质溶液中c(Cu2+)均保持不变(×)
(2)电解饱和食盐水时,两个电极均不能用金属材料(×)
(3)电解冶炼镁、铝通常电解MgCl 和Al O ,也可以电解MgO和AlCl (×)
2 2 3 3
(4)电解精炼时,阳极泥可以作为提炼贵重金属的原料(√)
(5)用Zn作阳极,Fe作阴极,ZnCl 作电解质溶液,由于放电顺序H+>Zn2+,不可
2
能在铁上镀锌(×)
2.(教材改编题)(1)(LK选修4·P 3改编)电解精炼铜时,如果转移0.04 mol电
18
子,阴极材料的质量将增加1.28 g。
(2)(RJ选修4·P 4改编)电解饱和食盐水时,从阴极逸出2.24 L氢气,从阳极逸
83
出Cl 气体,逸出气体的体积为2.24 L(在标准状况下,不考虑气体溶解)。
2
3.(思维探究题)比较下列两种装置有哪些不同?
(1)请分析两装置中各电极的质量变化?
____________________________________________________________________。
(2)请分析两装置中电解质溶液浓度的变化?
____________________________________________________________________。
答案 (1)甲图中铜片质量减小,铁制品质量增加;乙图中粗铜质量减小,精铜质
量增加
(2)甲图中CuSO 溶液浓度几乎未变化,因为阳极溶解多少铜,阴极就析出多少铜;
4
乙图中CuSO 溶液浓度逐渐变小,因为粗铜中混有Zn、Fe等杂质,放电后转化成
4
Zn2+、Fe2+等离子,此时Cu2+会转化为Cu,造成CuSO 溶液浓度减小
4INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.利用如图所示装置模拟电解原理在工业生产上的应用。下列说法正确的是
( )
A.氯碱工业中,X电极上反应式是4OH--4e-===2H O+O ↑
2 2
B.电解精炼铜时,Z溶液中的Cu2+浓度不变
C.在铁片上镀铜时,Y是纯铜
D.制取金属镁时,Z是熔融的氯化镁
解析 氯碱工业中阳极是Cl-放电生成Cl ;电解精炼铜时阳极粗铜溶解,粗铜中
2
混有Zn、Fe等杂质,放电后转化为Zn2+、Fe2+,阴极Cu2+放电析出Cu,溶液中Cu2
+浓度变小;铁片上镀铜时,阴极应该是铁片,阳极是纯铜。
答案 D
2(. 物质制备)(2018·武汉市部分学校调研)在电解液不参与反应的情况下,采用
电化学法还原CO 可制备ZnC O ,原理如图所示。下列说法正确的是( )
2 2 4A.电解结束后电解液Ⅱ中c(Zn2+)增大
B.电解液Ⅰ应为ZnSO 溶液
4
C.Pt极反应式为2CO +2e-===C O
2 2
D.当通入44 g CO 时,溶液中转移1 mol电子
2
解析 因为右室Zn失去电子生成Zn2+,溶液中的Zn2+通过阳离子交换膜进入左
室,根据电荷守恒,阴离子浓度不变,c(Zn2+)不变,A项错误;右室生成的Zn2+通
过阳离子交换膜进入左室与生成的C O结合为ZnC O ,因此,电解液Ⅰ为稀的
2 2 4
ZnC O 溶液,不含杂质,电解液Ⅱ只要是含Zn2+的易溶盐溶液即可,B项错误;Pt
2 4
极反应式为2CO +2e-===C O,C项正确;当通入44 g CO 时,外电路中转移1
2 2 2
mol电子,溶液中不发生电子转移,D项错误。
答案 C
3.(废气处理)(2018·湖南三湘名校教育联盟第三次大联考)[Fe(CN) ]3-
6
可将气态废弃物中的硫化氢氧化为可利用的硫,自身被还原为[Fe(CN)]4-。工业
6
上常采用如图所示的电解装置,通电电解,然后通入H S加以处理。下列说法不正
2
确的是( )
A.电解时,阳极反应式为[Fe(CN) ]4--e-===[Fe(CN) ]3-
6 6
B.电解时,阴极反应式为2HCO+2e-===H ↑+2CO
2
C.当电解过程中有标准状况下22.4 L H 生成时,溶液中有32 g S析出(溶解忽略
2
不计)
D.整个过程中需要不断补充K [Fe(CN) ]与KHCO
4 6 3
解析 电解时,阳极上[Fe(CN)]4-失去电子,阳极的电极反应式为[Fe(CN)]4--
6 6e-===[Fe(CN)]3-,A正确;阴极上HCO放电,发生还原反应,阴极反应式为
6
2HCO+2e-===H ↑+2CO,B正确;标准状况下22.4 L H 的物质的量为1 mol,则
2 2
转移2 mol 电子。H S失去2 mol电子,生成1 mol单质S,即析出32 g S,C正确;
2
根据以上分析可知,反应的结果相当于是H S被电解生成H 和S,所以不需要补
2 2
充K [Fe(CN) ]和KHCO ,D错误。
4 6 3
答案 D
【方法技巧】
电化学中定量计算方法
1.根据电子守恒计算
用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是
电路中转移的电子数相等。
2.根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
3.根据关系式计算
根据得失电子守恒定律关系建立起已知量与未知量之间的桥梁,构建计算所需的
关系式。
[B组 考试能力过关]
4(. 2018·课标全国Ⅰ,13)最近我国科学家设计了一种CO +H S协同转化装置,
2 2
实现对天然气中 CO 和 H S 的高效去除。示意图如图所示,其中电极分别为
2 2
ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTAFe2+-e-===EDTAFe3+
②2EDTAFe3++H S===2H++S+2EDTAFe2+
2
该装置工作时,下列叙述错误的是( )A.阴极的电极反应:CO +2H++2e-===CO+H O
2 2
B.协同转化总反应:CO +H S===CO+H O+S
2 2 2
C.石墨烯上的电势比ZnO@石墨烯上的低
D.若采用Fe3+/Fe2+取代EDTAFe3+/EDTAFe2+,溶液需为酸性
解析 阴极发生还原反应,氢离子由交换膜右侧向左侧迁移,阴极的电极反应式
为CO +2e-+2H+===CO+H O,A项正确;结合阳极区发生的反应,可知协同转
2 2
化总反应为CO +H S===S+CO+H O,B项正确;石墨烯作阳极,其电势高于
2 2 2
ZnO@石墨烯的,C项错误;Fe3+、Fe2+在碱性或中性介质中会生成沉淀,它们只稳
定存在于酸性较强的介质中,D项正确。
答案 C
5(. 2016·课标全国Ⅰ,11)三室式电渗析法处理含Na SO 废水的原理如图所示,采
2 4
用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO
可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
下列叙述正确的是( )
A.通电后中间隔室的SO离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na SO 废水时可以得到NaOH和H SO 产品
2 4 2 4
C.负极反应为2H O-4e-===O +4H+,负极区溶液pH降低
2 2
D.当电路中通过1 mol电子的电量时,会有0.5 mol的O 生成
2
解析 电解池中阴离子向正极移动,阳离子向负极移动,即SO离子向正极区移动
Na+ 向负极区移动,正极区水电离的OH-发生氧化反应生成氧气,H+留在正极区,
该极得到H SO 产品,溶液pH减小,负极区水电离的H+发生还原反应生成氢气,
2 4
OH-留在负极区,该极得到NaOH产品,溶液pH增大,故A、C项错误,B正确;该
电解池相当于电解水,根据电解水的方程式可计算出当电路中通过1 mol电子的
电量时,会有0.25 mol的O 生成,错误。
2
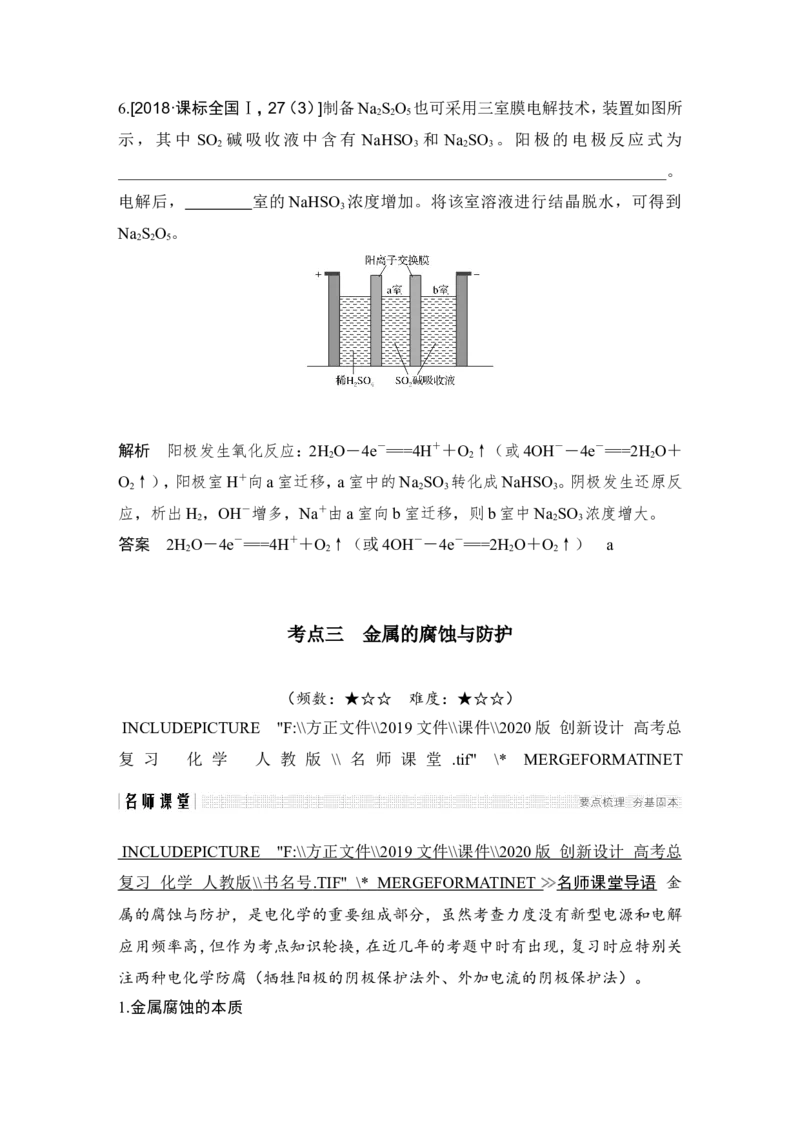
答案 B6.[2018·课标全国Ⅰ,27(3)]制备Na S O 也可采用三室膜电解技术,装置如图所
2 2 5
示,其中 SO 碱吸收液中含有 NaHSO 和 Na SO 。阳极的电极反应式为
2 3 2 3
____________________________________________________________________。
电解后, 室的NaHSO 浓度增加。将该室溶液进行结晶脱水,可得到
3
Na S O 。
2 2 5
解析 阳极发生氧化反应:2H O-4e-===4H++O ↑(或4OH--4e-===2H O+
2 2 2
O ↑),阳极室H+向a室迁移,a室中的Na SO 转化成NaHSO 。阴极发生还原反
2 2 3 3
应,析出H ,OH-增多,Na+由a室向b室迁移,则b室中Na SO 浓度增大。
2 2 3
答案 2H O-4e-===4H++O ↑(或4OH--4e-===2H O+O ↑) a
2 2 2 2
考点三 金属的腐蚀与防护
(频数:★☆☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 金
属的腐蚀与防护,是电化学的重要组成部分,虽然考查力度没有新型电源和电解
应用频率高,但作为考点知识轮换,在近几年的考题中时有出现,复习时应特别关
注两种电化学防腐(牺牲阳极的阴极保护法外、外加电流的阴极保护法)。
1.金属腐蚀的本质金属原子失去电子变为金属阳离子,金属发生氧化反应。
2.金属腐蚀的类型
(1)化学腐蚀与电化学腐蚀
类型 化学腐蚀 电化学腐蚀
金属与干燥气体(如O 、Cl 、
2 2 不纯金属或合金跟电解质溶液
条件 SO 等)或非电解质液体(如石
2 接触
油)等接触
现象 无电流产生 有微弱电流产生
本质 金属被氧化 较活泼金属被氧化
联系 两者往往同时发生,电化学腐蚀更普遍
(2)析氢腐蚀与吸氧腐蚀
以钢铁的腐蚀为例进行分析:
类型 析氢腐蚀 吸氧腐蚀
条件 水膜酸性较强( pH ≤ 4. 3 ) 水膜酸性很弱或呈中性
电极材 负极 Fe: Fe - 2e - == =Fe 2 +
料及反
应 正极 C: 2H + + 2e - == =H 2 ↑ C:O 2 + 2H 2 O + 4e - == =4OH -
总反应式 Fe + 2H + == =Fe 2 + + H ↑ 2Fe + O + 2H O == =2Fe ( OH )
2 2 2 2
联系 吸氧腐蚀更普遍
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.电解质所处环境决定金属的腐蚀方式:若电解质酸性较强,如NH Cl、H SO 等,
4 2 4
则发生析氢腐蚀,相当于金属与酸构成原电池;若电解质为弱酸、中性、弱碱,则发
生吸氧腐蚀,相当于金属、氧气构成燃料电池。
2.两种腐蚀正极的现象不同:析氢腐蚀正极产生H ,气体压强变大,pH增大;吸氧
2
腐蚀正极吸收O ,气体压强变小,pH增大。
23.金属的防护
(1)电化学防护
①牺牲阳极的阴极保护法——原电池原理
a.负极:比被保护金属活泼的金属;
b.正极:被保护的金属设备。
②外加电流的阴极保护法——电解原理
a.阴极:被保护的金属设备;
b.阳极:惰性金属。
(2)改变金属的内部结构组成,如制成合金、不锈钢等。
(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
我们通常把原电池的两极叫做正极和负极,电解池的两极叫做阳极和阴极,但实
际上,我们把失电子发生氧化反应的电极都统称为阳极,即原电池的负极也称为
阳极,这种叫法在教材上也有所体现。
LK选修4P 铜锌原电池装置(2)示意图
21
RJ选修4P 牺牲阳极的阴极保护法示意图
86
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)Al、Fe、Cu在潮湿空气中腐蚀均生成氧化物(×)(2)钢铁发生电化学腐蚀的负极反应式为Fe-3e-===Fe3+(×)
(3)在潮湿空气中,钢铁表面形成水膜,金属发生的一定是吸氧腐蚀(×)
(4)所有金属纯度越大,越不易被腐蚀(×)
(5)黄铜(铜锌合金)制作的铜锣不易产生铜绿(√)
(6)生铁比纯铁容易生锈(√)
2.(教材改编题)如图所示,各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序
为( )
A.②①③④⑤⑥ B.⑤④③①②⑥
C.⑤④②①③⑥ D.⑤③②④①⑥
解析 ①是铁发生化学腐蚀。②③④均为构成原电池,由金属的活动性可知,③中
铁作正极,受到保护;②、④中铁作负极受到腐蚀,由于Fe和Cu的金属活泼性相
差较Fe和Sn的大,故Fe-Cu原电池中Fe被腐蚀更快。⑤⑥为电解池,⑤中铁作
阳极,加快了Fe的腐蚀,⑥中铁作阴极受到保护。根据以上分析可知,铁在其中被
腐蚀由快到慢的顺序为⑤>④>②>①>③>⑥。
答案 C
3.(思维探究题)写出钢铁、铜制品在潮湿的空气中发生吸氧腐蚀生成铁锈、铜绿
的原理。
(1)铁锈的形成
负极:_______________________________________________________________
_____________________________________________________________________
正极:_____________________________________________________________
___________________________________________________________________
(2)铜锈的形成
负极:________________________________________________________________
_____________________________________________________________________正极:_______________________________________________________________
____________________________________________________________________。
解析 (1)铁锈的形成
负极:2Fe-4e-===2Fe2+
正极:O +4e-+2H O===4OH-
2 2
2Fe+O +2H O===2Fe(OH)
2 2 2
4Fe(OH) +O +2H O===4Fe(OH)
2 2 2 3
2Fe(OH) ===Fe O ·xH O(铁锈)+(3-x)H O
3 2 3 2 2
(2)铜锈的形成
负极:2Cu-4e-===2Cu2+
正极:O +2H O+4e-===4OH-
2 2
2Cu+2H O+O ===2Cu(OH)
2 2 2
2Cu(OH) +CO ===Cu (OH) CO (铜绿)+H O
2 2 2 2 3 2
答案 见解析
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2018·郑州高三模拟)一定条件下,碳钢腐蚀与溶液pH的关系如下表:
pH 2 4 6 6.5 8 13.5 14
腐蚀快慢 较快 慢 较快
主要产物 Fe2+ Fe O Fe O FeO
3 4 2 3
下列说法错误的是( )
A.当pH<4时,碳钢主要发生析氢腐蚀
B.当pH>6时,碳钢主要发生吸氧腐蚀
C.当pH>14时,正极反应为O +4H++4e-===2H O
2 2
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓
解析 C项正极反应为O +4e-+2H O===4OH-。
2 2
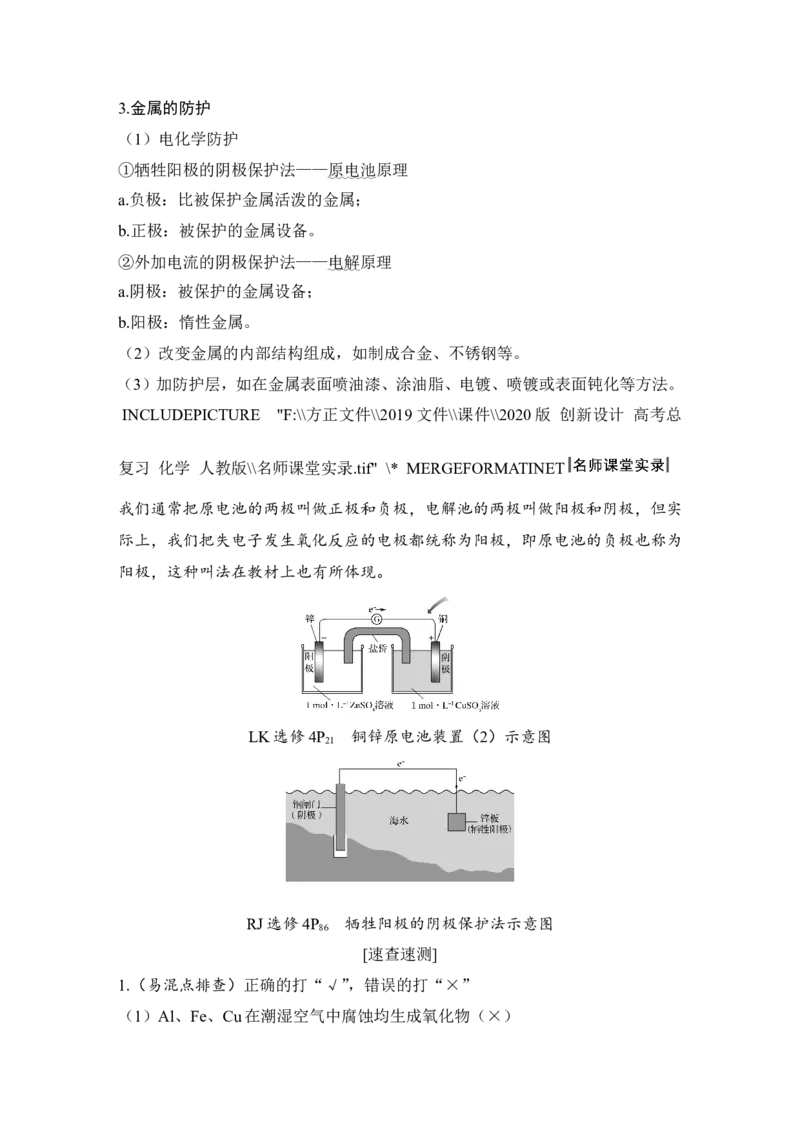
答案 C2.钢铁的防护有多种方法,下列对于图中的方法描述错误的是( )
A.a、b以导线连接,辅助电极发生氧化反应
B.a、b以导线连接或以电源连接,辅助电极的材料可能都含有Zn
C.a、b分别连接直流电源,通电后外电路电子被强制从辅助电极流向钢铁闸门
D.a、b分别连接直流电源的负极、正极,该方法是牺牲阳极的阴极保护法
解析 a、b以导线连接,即为牺牲阳极的阴极保护法,则辅助电极要作负极,发生
氧化反应,A项正确;a、b以导线连接或以电源连接,辅助电极都是发生氧化反应,
Zn比较活泼,要失去电子,B项正确;通电后,被保护的钢铁闸门作阴极,辅助电
极作阳极,因此通电后外电路电子被强制从辅助电极流向钢铁闸门,C项正确;由
于有外加电源,故此方法为外加电流的阴极保护法,D项错误。
答案 D
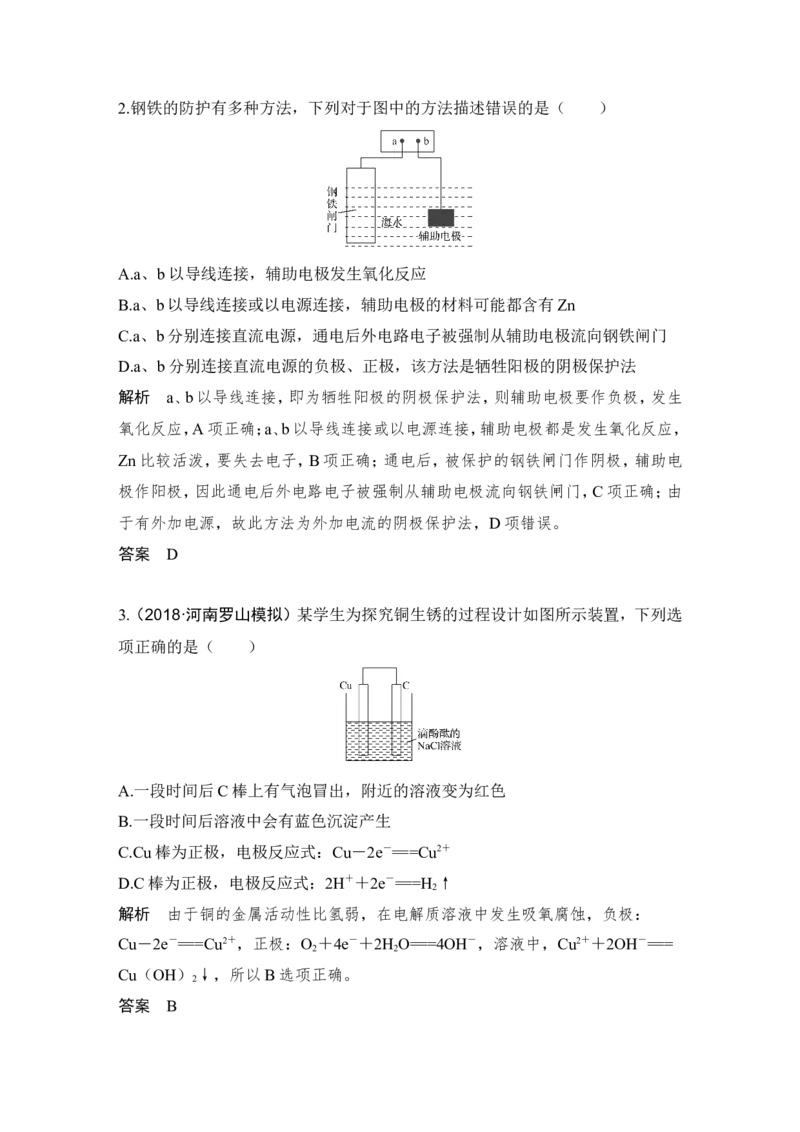
3.(2018·河南罗山模拟)某学生为探究铜生锈的过程设计如图所示装置,下列选
项正确的是( )
A.一段时间后C棒上有气泡冒出,附近的溶液变为红色
B.一段时间后溶液中会有蓝色沉淀产生
C.Cu棒为正极,电极反应式:Cu-2e-===Cu2+
D.C棒为正极,电极反应式:2H++2e-===H ↑
2
解析 由于铜的金属活动性比氢弱,在电解质溶液中发生吸氧腐蚀,负极:
Cu-2e-===Cu2+,正极:O +4e-+2H O===4OH-,溶液中,Cu2++2OH-===
2 2
Cu(OH) ↓,所以B选项正确。
2
答案 B【规律总结】
电化学腐蚀规律
1.对同一种金属来说,腐蚀的快慢:强电解质溶液中>弱电解质溶液中>非电解质
溶液中;活动性不同的两金属,活动性差别越大,活动性强的金属腐蚀越快。
2.对同一种电解质溶液来说,电解质溶液浓度越大,腐蚀越快,且氧化剂的浓度越
高,氧化性越强,腐蚀越快。
3.从防腐措施方面分析,腐蚀的由慢到快的顺序为:外加电流的阴极保护法防腐<
牺牲阳极的阴极保护法防腐<有一般防护条件的防腐<无防护条件的防腐。
4.不同类型腐蚀快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀
>有防护措施的腐蚀。
[B组 考试能力过关]
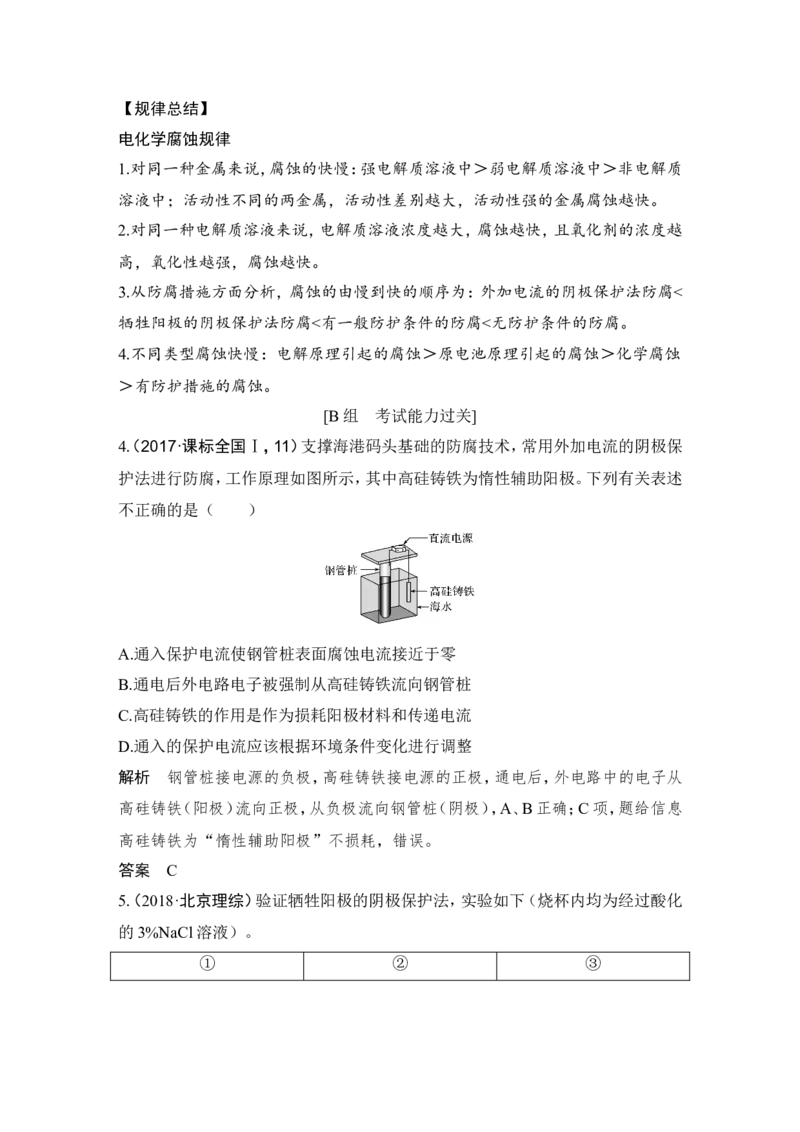
4(. 2017·课标全国Ⅰ,11)支撑海港码头基础的防腐技术,常用外加电流的阴极保
护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述
不正确的是( )
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
解析 钢管桩接电源的负极,高硅铸铁接电源的正极,通电后,外电路中的电子从
高硅铸铁(阳极)流向正极,从负极流向钢管桩(阴极),A、B正确;C项,题给信息
高硅铸铁为“惰性辅助阳极”不损耗,错误。
答案 C
5(. 2018·北京理综)验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化
的3%NaCl溶液)。
① ② ③在Fe表面生成蓝色沉淀 试管内无明显变化 试管内生成蓝色沉淀
下列说法不正确的是( )
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K [Fe(CN) ]可能将Fe氧化
3 6
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
解析 ②中Zn作负极,发生氧化反应生成Zn2+,Fe作正极被保护,所以取出的少
量Fe附近的溶液中滴入铁氰化钾溶液,试管内无明显变化。但③中没有Zn保护
Fe,Fe在酸性环境中发生析氢腐蚀,Fe作负极被氧化生成Fe2+,所以取出的少量
Fe附近的溶液中滴入铁氰化钾溶液,生成蓝色沉淀,对比②③可知Zn保护了Fe,
A项正确;①与②的区别在于:前者是将铁氰化钾溶液直接滴入烧杯中,而后者是
在取出的少量Fe附近的溶液中滴加铁氰化钾溶液,①中出现了蓝色沉淀,说明有
Fe2+生成。对比分析可知,可能是铁氰化钾氧化Fe生成了Fe2+,B项正确;通过上
述分析可知,验证Zn保护Fe时不能用①的方法,C项正确;若将Zn换成Cu,铁氰
化钾仍会将Fe氧化为Fe2+,在铁的表面同样会生成蓝色沉淀,所以无法判断Fe2+
是不是负极产物,即无法判断Fe与Cu的活泼性,D项错误。
答案 D
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET
[A级 全员必做题]
1.下列防止金属腐蚀的做法不可行的是( )
A.军事演习期间给坦克的履带上刷上油漆以防止生锈
B.地下钢管道每隔一段距离就连接一定数量镁块
C.在轮船外壳水线以下部分装上一定数量的锌块D.洗衣机的滚筒采用不锈钢材料,既耐磨又耐腐蚀
解析 油漆经不住高温,军事演习期间,坦克高速行驶履带会发热,油漆很快脱落,
故A项错;B、C项均属于牺牲阳极的阴极保护法,正确;D项滚筒采用的不锈钢材
料既耐磨又耐腐蚀,正确。
答案 A
2.某溶液中含有Cu2+、Fe2+、Al3+、Cl-、NO,且浓度均大于0.1 mol/L,用石墨作电
极进行电解时,肯定得不到的产物是( )
A.Cl B.Al
2
C.Cu D.H
2
解析 阴极上Al3+、Fe2+的放电能力弱于H+,而Cu2+的放电能力比水电离出的H
+的放电能力强,阳极上Cl-放电能力强于OH-。
答案 B
3.在酸性或碱性较强的溶液中,铝均溶解。用食盐腌制的食品也不能长期存放在铝
制品中,其主要原因是( )
A.铝能与NaCl直接发生反应而被腐蚀
B.长期存放的NaCl发生水解,其水溶液不再呈中性,可与铝发生反应
C.铝与铝制品中的杂质(碳)、NaCl溶液形成原电池,发生析氢腐蚀
D.铝与铝制品中的杂质(碳)、NaCl溶液形成原电池,发生吸氧腐蚀
解析 铝不能与NaCl直接发生反应,选项A错误;氯化钠是强酸强碱盐,不发生
水解,选项B错误;铝制品不能长时间存放食盐腌制的食品,是因为氯离子对氧化
膜有破坏作用,若氧化膜被破坏,则由于铝制品不纯,铝与其中的杂质、氯化钠溶
液形成原电池,铝失去电子,被氧化,发生吸氧腐蚀,选项C错误,选项D正确。
答案 D
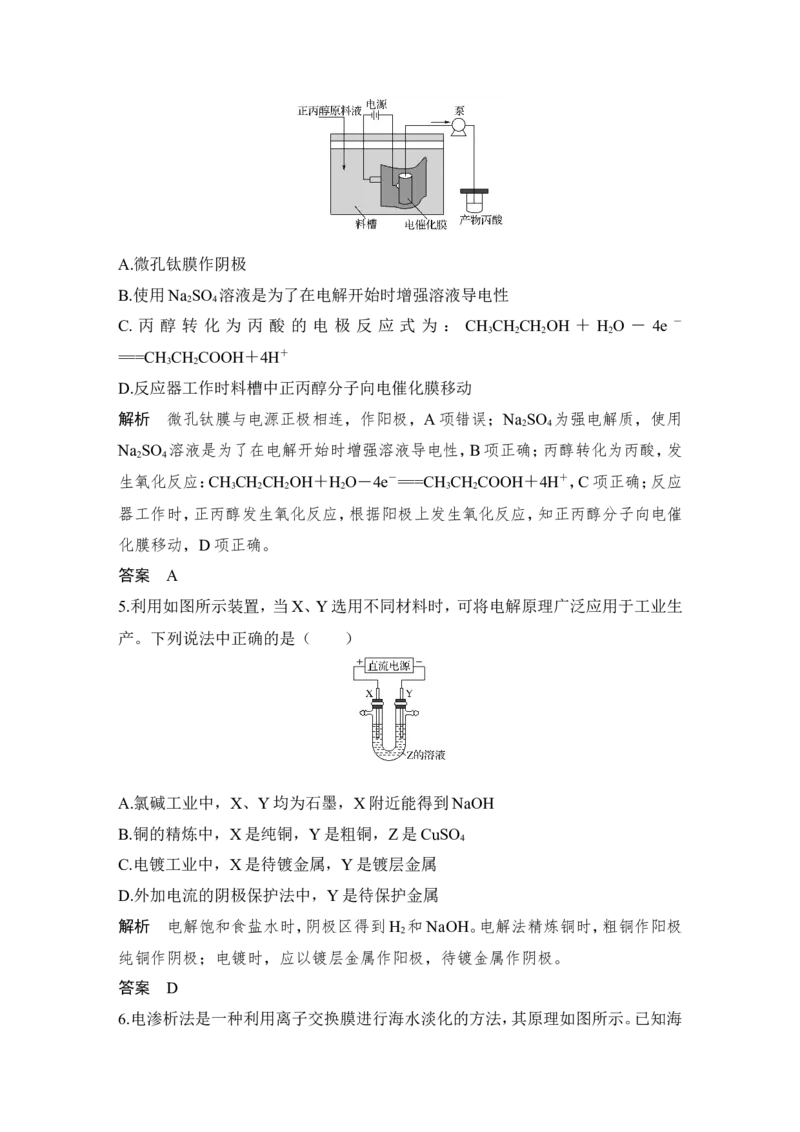
4.(2018·福州毕业班质检,12)科研人员设计一种电化学反应器,以Na SO 溶液
2 4
为电解质,负载纳米MnO 的导电微孔钛膜和不锈钢为电极材料。这种电催化膜反
2
应器可用于正丙醇合成丙酸,装置示意图如图。以下叙述错误的是( )A.微孔钛膜作阴极
B.使用Na SO 溶液是为了在电解开始时增强溶液导电性
2 4
C. 丙 醇 转 化 为 丙 酸 的 电 极 反 应 式 为 : CH CH CH OH + H O - 4e -
3 2 2 2
===CH CH COOH+4H+
3 2
D.反应器工作时料槽中正丙醇分子向电催化膜移动
解析 微孔钛膜与电源正极相连,作阳极,A项错误;Na SO 为强电解质,使用
2 4
Na SO 溶液是为了在电解开始时增强溶液导电性,B项正确;丙醇转化为丙酸,发
2 4
生氧化反应:CH CH CH OH+H O-4e-===CH CH COOH+4H+,C项正确;反应
3 2 2 2 3 2
器工作时,正丙醇发生氧化反应,根据阳极上发生氧化反应,知正丙醇分子向电催
化膜移动,D项正确。
答案 A
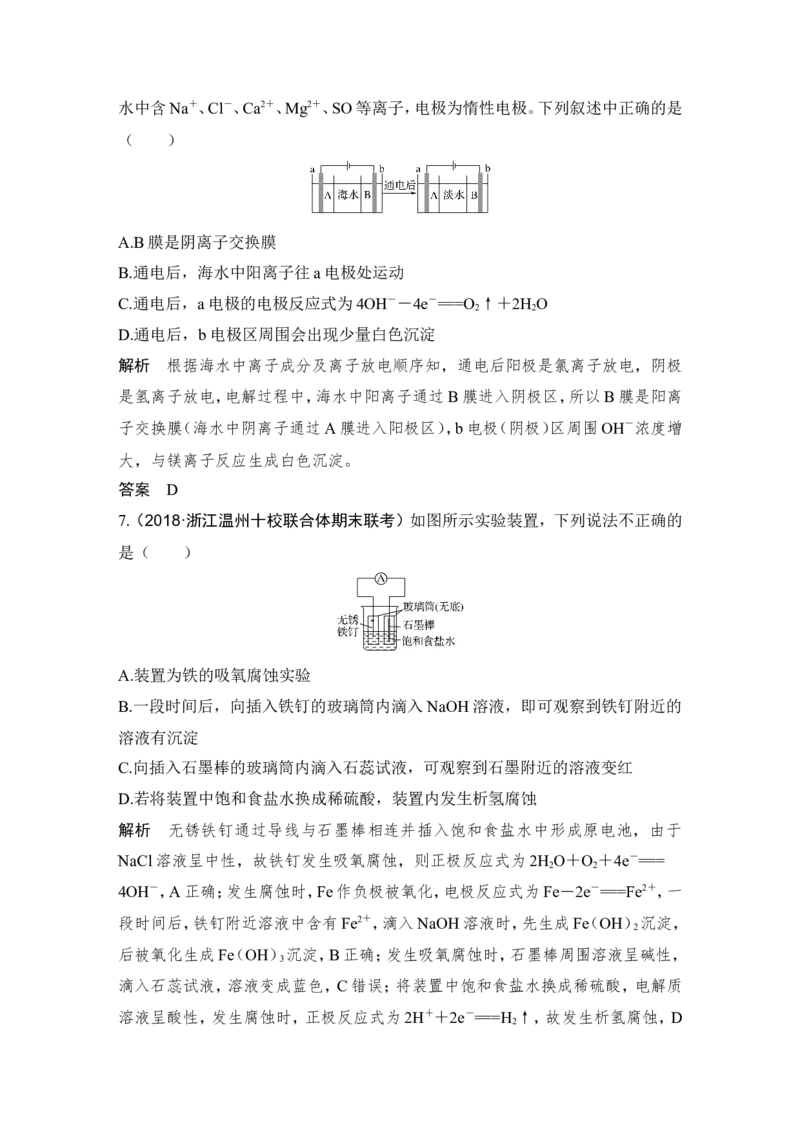
5.利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生
产。下列说法中正确的是( )
A.氯碱工业中,X、Y均为石墨,X附近能得到NaOH
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO
4
C.电镀工业中,X是待镀金属,Y是镀层金属
D.外加电流的阴极保护法中,Y是待保护金属
解析 电解饱和食盐水时,阴极区得到H 和NaOH。电解法精炼铜时,粗铜作阳极
2
纯铜作阴极;电镀时,应以镀层金属作阳极,待镀金属作阴极。
答案 D
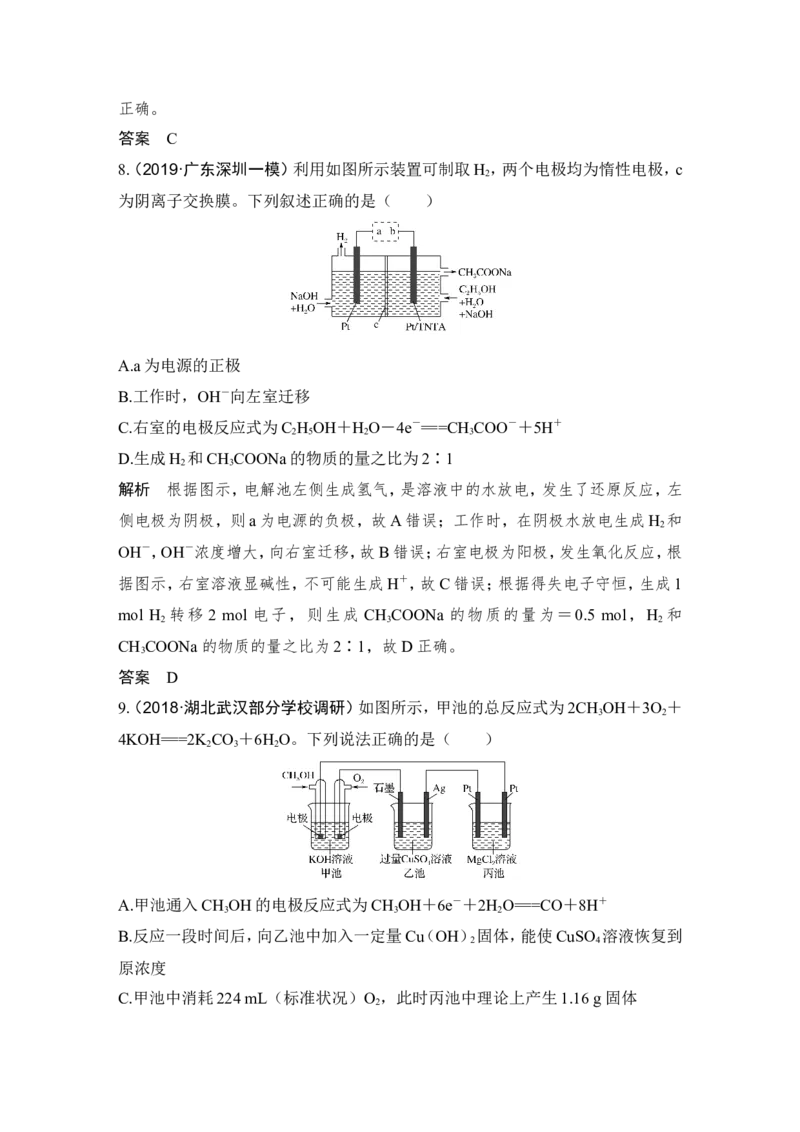
6.电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO等离子,电极为惰性电极。下列叙述中正确的是
( )
A.B膜是阴离子交换膜
B.通电后,海水中阳离子往a电极处运动
C.通电后,a电极的电极反应式为4OH--4e-===O ↑+2H O
2 2
D.通电后,b电极区周围会出现少量白色沉淀
解析 根据海水中离子成分及离子放电顺序知,通电后阳极是氯离子放电,阴极
是氢离子放电,电解过程中,海水中阳离子通过B膜进入阴极区,所以B膜是阳离
子交换膜(海水中阴离子通过A膜进入阳极区),b电极(阴极)区周围OH-浓度增
大,与镁离子反应生成白色沉淀。
答案 D
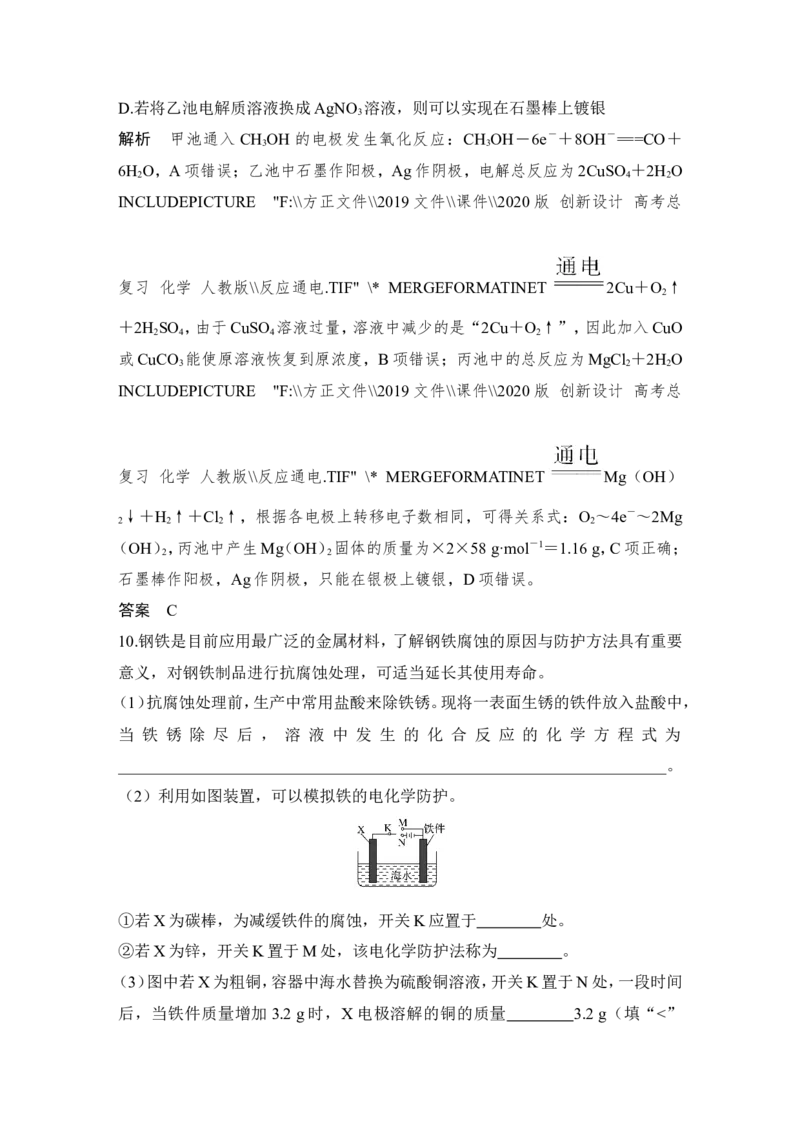
7.(2018·浙江温州十校联合体期末联考)如图所示实验装置,下列说法不正确的
是( )
A.装置为铁的吸氧腐蚀实验
B.一段时间后,向插入铁钉的玻璃筒内滴入NaOH溶液,即可观察到铁钉附近的
溶液有沉淀
C.向插入石墨棒的玻璃筒内滴入石蕊试液,可观察到石墨附近的溶液变红
D.若将装置中饱和食盐水换成稀硫酸,装置内发生析氢腐蚀
解析 无锈铁钉通过导线与石墨棒相连并插入饱和食盐水中形成原电池,由于
NaCl溶液呈中性,故铁钉发生吸氧腐蚀,则正极反应式为2H O+O +4e-===
2 2
4OH-,A正确;发生腐蚀时,Fe作负极被氧化,电极反应式为Fe-2e-===Fe2+,一
段时间后,铁钉附近溶液中含有Fe2+,滴入NaOH溶液时,先生成Fe(OH)沉淀,
2
后被氧化生成Fe(OH)沉淀,B正确;发生吸氧腐蚀时,石墨棒周围溶液呈碱性,
3
滴入石蕊试液,溶液变成蓝色,C错误;将装置中饱和食盐水换成稀硫酸,电解质
溶液呈酸性,发生腐蚀时,正极反应式为2H++2e-===H ↑,故发生析氢腐蚀,D
2正确。
答案 C
8.(2019·广东深圳一模)利用如图所示装置可制取H ,两个电极均为惰性电极,c
2
为阴离子交换膜。下列叙述正确的是( )
A.a为电源的正极
B.工作时,OH-向左室迁移
C.右室的电极反应式为C H OH+H O-4e-===CH COO-+5H+
2 5 2 3
D.生成H 和CH COONa的物质的量之比为2∶1
2 3
解析 根据图示,电解池左侧生成氢气,是溶液中的水放电,发生了还原反应,左
侧电极为阴极,则a为电源的负极,故A错误;工作时,在阴极水放电生成H 和
2
OH-,OH-浓度增大,向右室迁移,故B错误;右室电极为阳极,发生氧化反应,根
据图示,右室溶液显碱性,不可能生成H+,故C错误;根据得失电子守恒,生成1
mol H 转移 2 mol 电子,则生成 CH COONa 的物质的量为=0.5 mol,H 和
2 3 2
CH COONa的物质的量之比为2∶1,故D正确。
3
答案 D
9.(2018·湖北武汉部分学校调研)如图所示,甲池的总反应式为2CH OH+3O +
3 2
4KOH===2K CO +6H O。下列说法正确的是( )
2 3 2
A.甲池通入CH OH的电极反应式为CH OH+6e-+2H O===CO+8H+
3 3 2
B.反应一段时间后,向乙池中加入一定量Cu(OH)固体,能使CuSO 溶液恢复到
2 4
原浓度
C.甲池中消耗224 mL(标准状况)O ,此时丙池中理论上产生1.16 g 固体
2D.若将乙池电解质溶液换成AgNO 溶液,则可以实现在石墨棒上镀银
3
解析 甲池通入CH OH的电极发生氧化反应:CH OH-6e-+8OH-===CO+
3 3
6H O,A项错误;乙池中石墨作阳极,Ag作阴极,电解总反应为2CuSO +2H O
2 4 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\反应通电.TIF" \* MERGEFORMATINET 2Cu+O ↑
2
+2H SO ,由于CuSO 溶液过量,溶液中减少的是“2Cu+O ↑”,因此加入CuO
2 4 4 2
或CuCO 能使原溶液恢复到原浓度,B项错误;丙池中的总反应为MgCl +2H O
3 2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\反应通电.TIF" \* MERGEFORMATINET Mg(OH)
↓+H ↑+Cl ↑,根据各电极上转移电子数相同,可得关系式:O ~4e-~2Mg
2 2 2 2
(OH),丙池中产生Mg(OH)固体的质量为×2×58 g·mol-1=1.16 g,C项正确;
2 2
石墨棒作阳极,Ag作阴极,只能在银极上镀银,D项错误。
答案 C
10.钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要
意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。
(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,
当 铁 锈 除 尽 后 , 溶 液 中 发 生 的 化 合 反 应 的 化 学 方 程 式 为
____________________________________________________________________。
(2)利用如图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于 处。
②若X为锌,开关K置于M处,该电化学防护法称为 。
(3)图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间
后,当铁件质量增加3.2 g时,X电极溶解的铜的质量 3.2 g(填“<”“>”或“=”)。
(4)图中若X为铜,容器中海水替换为FeCl 溶液,开关K置于M处,铜电极发生
3
的 反 应 是 , 若 将 开 关 K 置 于 N 处 , 发 生 的 总 反 应 是
____________________________________________________________________。
解析 (1)铁锈的成分为Fe O ,能和盐酸反应生成FeCl 和水,当铁锈除尽后,溶
2 3 3
液中发生的化合反应的化学方程式为Fe+2FeCl ===3FeCl 。
3 2
(2)①若X为碳棒,由于Fe比较活泼,为减缓铁的腐蚀,应使Fe为电解池的阴极
即连接电源的负极,故K连接N处。②若X为锌,开关K置于M处,Zn为阳极被
腐蚀,Fe为阴极被保护,该防护法称为牺牲阳极的阴极保护法。
(3)若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,
当铁件质量增加3.2 g时,由于粗铜中有杂质参加反应,所以X电极溶解的铜的质
量<3.2 g。
(4)若X为铜,容器中海水替换为FeCl 溶液,开关K置于M处,此时构成原电池
3
装置,铜电极为正极,发生的反应是2Fe3++2e-===2Fe2+;若将开关K置于N处,
此时构成电解池装置,铜为阳极,铜本身被氧化而溶解,阴极铁离子被还原,发生
的总反应是:Cu+2Fe3+===2Fe2++Cu2+。
答案 (1)Fe+2FeCl ===3FeCl
3 2
(2)①N ②牺牲阳极的阴极保护法 (3)<
(4)2Fe3++2e-===2Fe2+ Cu+2Fe3+===2Fe2++Cu2+
11(. 2018·石景山高三上学期期末考试)知识的梳理和感悟是有效学习的方法之一。
某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显
示的电极均为石墨)。
(1)图1中,电解一段时间后,气球b中的气体是 (填化学式),U形管
(填“左”或“右”)边的溶液变红。
(2)利用图2制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成
分,则 c 为电源的 极;该发生器中反应的总离子方程式为______________________________________________________________________
_____________________________________________________________________
。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节
(电)能30%以上。该工艺的相关物质运输与转化关系如图3所示(其中的电极未
标出,所用的离子膜都只允许阳离子通过)。
①燃料电池B中的电极反应式分别为
负极________________________________________________________________,
正极________________________________________________________________。
②分析图3可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
。
解析 (1)图1中,根据电子流向知,左边电极是电解池阳极,右边电极是电解池
阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以气球a中气
体是氯气,气球b中的气体是氢气,同时阴极附近有NaOH生成,溶液呈碱性,无
色酚酞遇碱变红色,所以U形管右边溶液变红色。
(2)利用图2制作一种环保型消毒液发生器,阳极上氯离子放电生成氯气,阴极上
氢离子放电生成氢气,同时阴极有NaOH生成,氯气和氢氧化钠反应生成NaClO,
次氯酸钠具有漂白性,为了使反应更充分,则下边电极生成氯气,上边电极附近有
NaOH生成,上边电极生成氢气,为阴极,则c为负极,d为正极,其电池反应式为
Cl-+H O=====ClO-+H ↑。
2 2
(3)①B是燃料电池,右边电池中通入空气,左边原电池中通入气体Y,则Y是氢
气,则电解池中左边电极是阳极,右边电极是阴极,阳极上氯离子放电,阴极上氢
离子放电;燃料电池中通入氧化剂的电极是正极,通入氢气的电极是负极,正极上
氧气得电子和水反应生成氢氧根离子,负极上氢气失电子和氢氧根离子反应生成
水,负极、正极反应式分别为2H -4e-+4OH-===4H O、O +4e-+2H O===4OH
2 2 2 2-。②图3电解池中加入NaOH目的是增大溶液导电性,通入电解池后生成氢氧化
钠,所以加入的NaOH浓度小于出来的NaOH浓度;原电池中,正极上生成氢氧化
钠,且其浓度大于加入的氢氧化钠,所以氢氧化钠浓度大小顺序是b%>a%>c%。
答案 (1)H 右
2
(2)负 Cl-+H O=====ClO-+H ↑
2 2
(3)①2H -4e-+4OH-===4H O
2 2
O +4e-+2H O===4OH-
2 2
②b%>a%>c%
[B级 拔高选做题]
12.某同学进行下列实验:
操作 现象
放置一段时间后,生铁片上出现如图所
示“斑痕”。其边缘处为红色,中心区域
取一块打磨过的生铁片,在其表面滴1
为蓝色,在两色环交界处出现铁锈
滴含酚酞和K [Fe(CN) ]的食盐水
3 6
下列说法不合理的是( )
A.生铁片发生吸氧腐蚀
B.中心区:Fe-2e-===Fe2+
C.边缘处:O +2H O+4e-===4OH-
2 2
D.交界处:4Fe2++O +10H O===4Fe(OH) +8H+
2 2 3
解析 生铁片边缘处为红色,说明生成了氢氧根离子,O +2H O+4e-===4OH-,
2 2
生铁片发生吸氧腐蚀,故A、C合理;根据实验现象,中心区域为蓝色,说明生成了
亚铁离子,Fe-2e-===Fe2+,故B合理;在两色环交界处出现铁锈,是因为生成的
氢氧化亚铁被氧气氧化生成了氢氧化铁,故D不合理。
答案 D
13(. 2018·湖北八校第二次联考)H BO 可以通过电解NaB(OH)溶液的方法制备
3 3 4
其工作原理如图所示,下列叙述错误的是( )A.M室发生的电极反应为2H O-4e-===O ↑+4H+
2 2
B.N室中:a%