文档内容
第六章能力提升检测卷
完卷时间:90分钟
可能用到的相对原子质量:Li7
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2021·山东淄博市·高三三模)我国古代典籍中记载了许多劳动人民对化学知识的认识。下列有关
说法正确的是
A.“丹砂烧之成水银,积变又还成丹砂”中“烧”的过程有单质硫生成
B.“凡石灰经火焚炼为用。成质之后,入水永劫不坏”中所有反应均为放热反应
C.“胡粉(碱式碳酸铅)投火中,色坏还为铅”中“色坏还为铅”过程为分解反应
D.“以火烧之,紫青烟起,乃真硝石也”中的“硝石”主要成分为NaNO
3
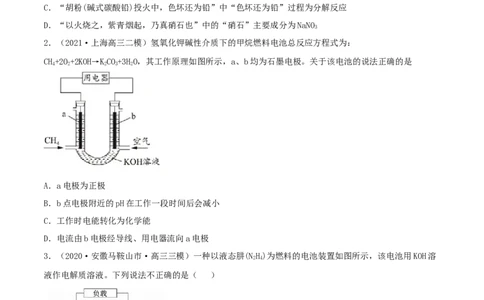
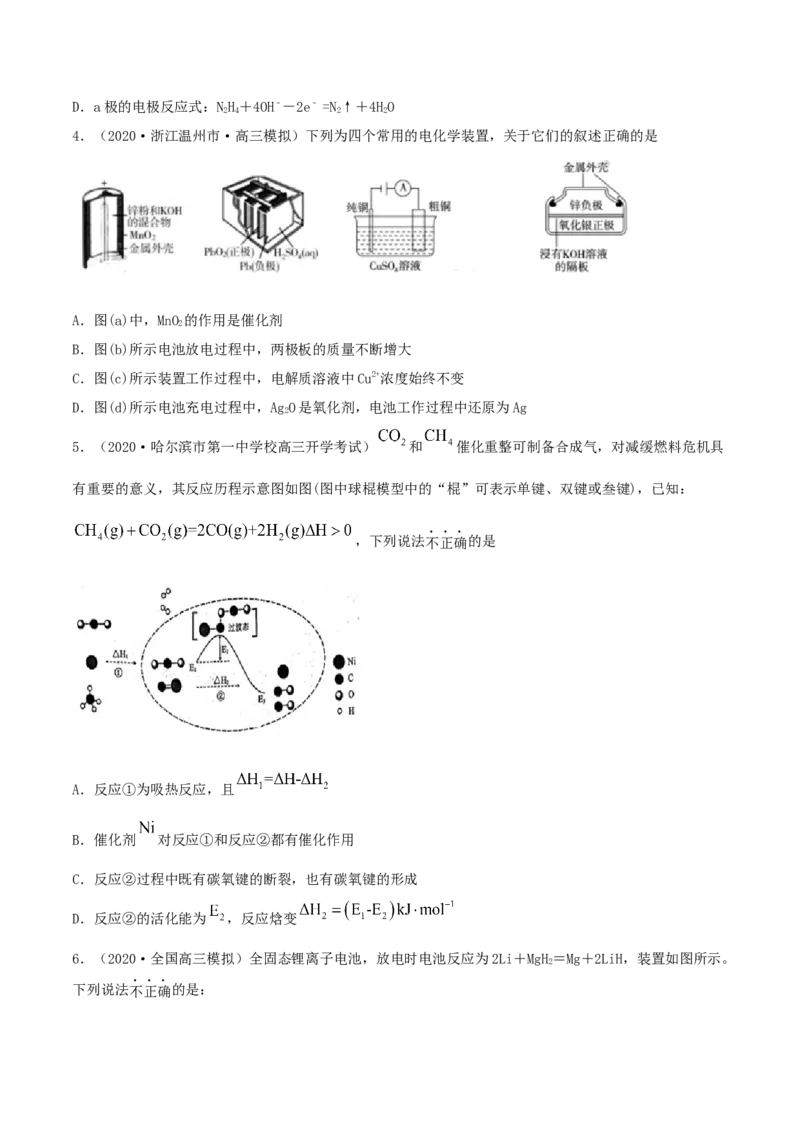
2.(2021·上海高三二模)氢氧化钾碱性介质下的甲烷燃料电池总反应方程式为:
CH+2O+2KOH→KCO+3HO,其工作原理如图所示,a、b均为石墨电极。关于该电池的说法正确的是
4 2 2 3 2
A.a电极为正极
B.b点电极附近的pH在工作一段时间后会减小
C.工作时电能转化为化学能
D.电流由b电极经导线、用电器流向a电极
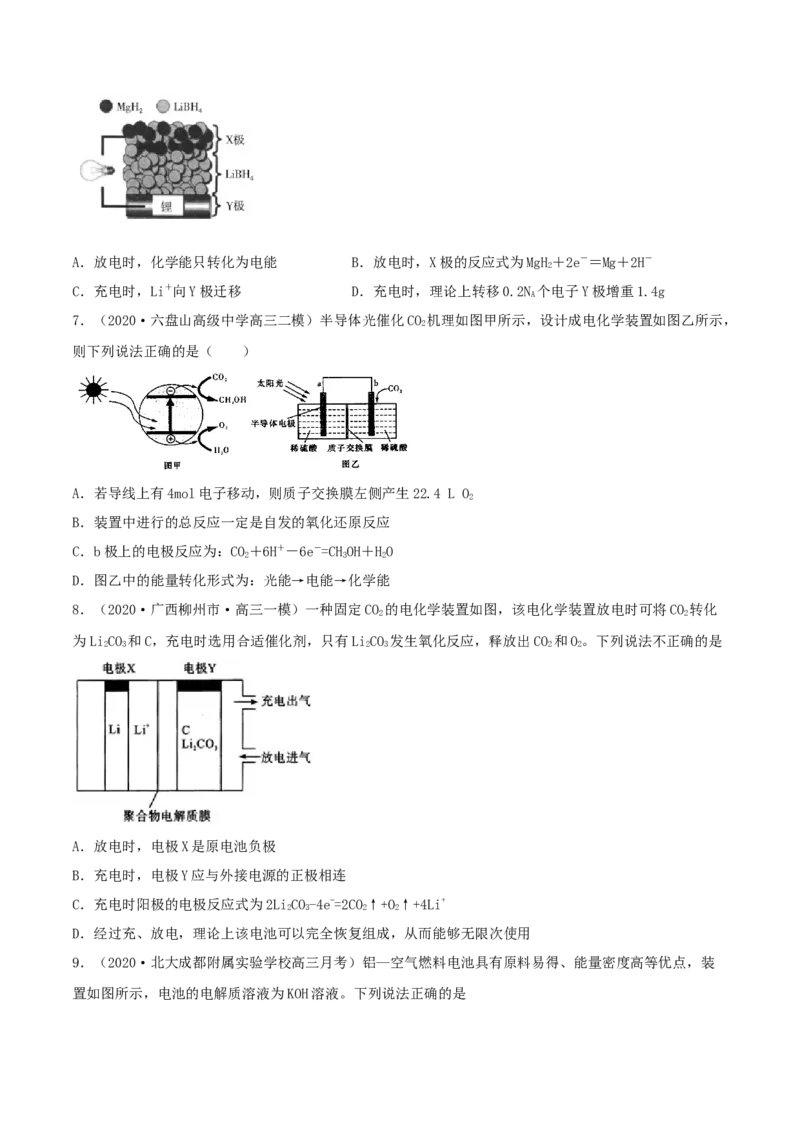
3.(2020·安徽马鞍山市·高三三模)一种以液态肼(NH)为燃料的电池装置如图所示,该电池用KOH溶
2 4
液作电解质溶液。下列说法不正确的是( )
A.b为正极,发生还原反应
B.放电时,电子从a极经负载流向b极
C.其中的离子交换膜需选用阴离子交换膜D.a极的电极反应式:NH+4OH–-2e– =N↑+4HO
2 4 2 2
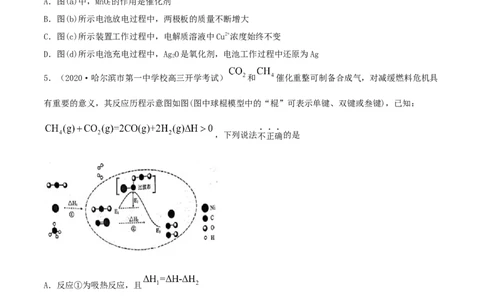
4.(2020·浙江温州市·高三模拟)下列为四个常用的电化学装置,关于它们的叙述正确的是
A.图(a)中,MnO 的作用是催化剂
2
B.图(b)所示电池放电过程中,两极板的质量不断增大
C.图(c)所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图(d)所示电池充电过程中,AgO是氧化剂,电池工作过程中还原为Ag
2
5.(2020·哈尔滨市第一中学校高三开学考试) 和 催化重整可制备合成气,对减缓燃料危机具
有重要的意义,其反应历程示意图如图(图中球棍模型中的“棍”可表示单键、双键或叁键),已知:
,下列说法不正确的是
A.反应①为吸热反应,且
B.催化剂 对反应①和反应②都有催化作用
C.反应②过程中既有碳氧键的断裂,也有碳氧键的形成
D.反应②的活化能为 ,反应焓变
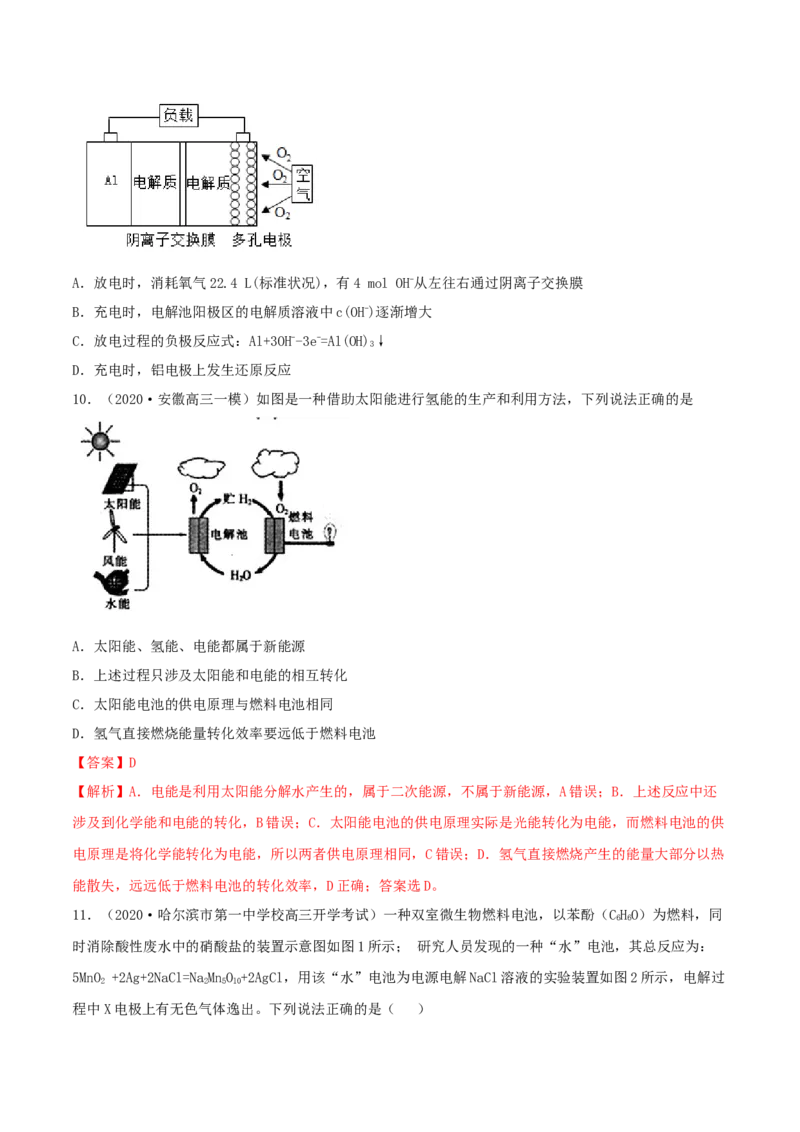
6.(2020·全国高三模拟)全固态锂离子电池,放电时电池反应为2Li+MgH=Mg+2LiH,装置如图所示。
2
下列说法不正确的是:A.放电时,化学能只转化为电能 B.放电时,X极的反应式为MgH+2e-=Mg+2H-
2
C.充电时,Li+向Y极迁移 D.充电时,理论上转移0.2N 个电子Y极增重1.4g
A
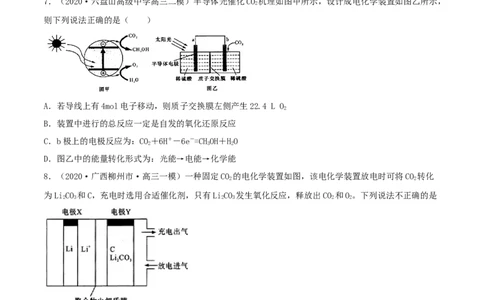
7.(2020·六盘山高级中学高三二模)半导体光催化CO 机理如图甲所示,设计成电化学装置如图乙所示,
2
则下列说法正确的是( )
A.若导线上有4mol电子移动,则质子交换膜左侧产生22.4 L O
2
B.装置中进行的总反应一定是自发的氧化还原反应
C.b极上的电极反应为:CO+6H+-6e-=CHOH+HO
2 3 2
D.图乙中的能量转化形式为:光能→电能→化学能
8.(2020·广西柳州市·高三一模)一种固定CO 的电化学装置如图,该电化学装置放电时可将CO 转化
2 2
为LiCO 和C,充电时选用合适催化剂,只有LiCO 发生氧化反应,释放出CO 和O。下列说法不正确的是
2 3 2 3 2 2
A.放电时,电极X是原电池负极
B.充电时,电极Y应与外接电源的正极相连
C.充电时阳极的电极反应式为2LiCO-4e-=2CO↑+O↑+4Li+
2 3 2 2
D.经过充、放电,理论上该电池可以完全恢复组成,从而能够无限次使用
9.(2020·北大成都附属实验学校高三月考)铝—空气燃料电池具有原料易得、能量密度高等优点,装
置如图所示,电池的电解质溶液为KOH溶液。下列说法正确的是A.放电时,消耗氧气22.4 L(标准状况),有4 mol OH-从左往右通过阴离子交换膜
B.充电时,电解池阳极区的电解质溶液中c(OH-)逐渐增大
C.放电过程的负极反应式:Al+3OH--3e-=Al(OH)↓
3
D.充电时,铝电极上发生还原反应
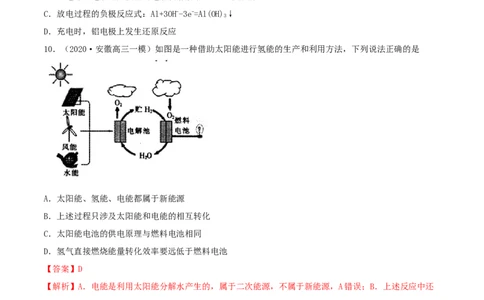
10.(2020·安徽高三一模)如图是一种借助太阳能进行氢能的生产和利用方法,下列说法正确的是
A.太阳能、氢能、电能都属于新能源
B.上述过程只涉及太阳能和电能的相互转化
C.太阳能电池的供电原理与燃料电池相同
D.氢气直接燃烧能量转化效率要远低于燃料电池
【答案】D
【解析】A.电能是利用太阳能分解水产生的,属于二次能源,不属于新能源,A错误;B.上述反应中还
涉及到化学能和电能的转化,B错误;C.太阳能电池的供电原理实际是光能转化为电能,而燃料电池的供
电原理是将化学能转化为电能,所以两者供电原理相同,C错误;D.氢气直接燃烧产生的能量大部分以热
能散失,远远低于燃料电池的转化效率,D正确;答案选D。
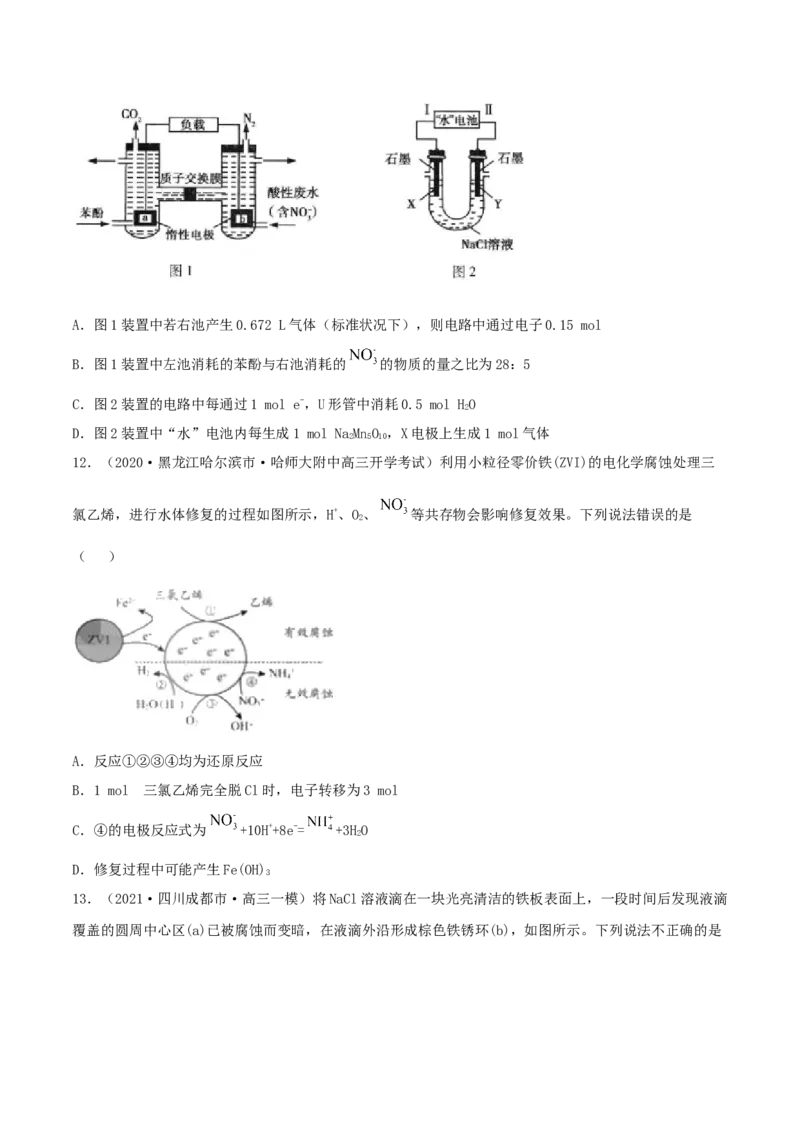
11.(2020·哈尔滨市第一中学校高三开学考试)一种双室微生物燃料电池,以苯酚(CHO)为燃料,同
6 6
时消除酸性废水中的硝酸盐的装置示意图如图1所示; 研究人员发现的一种“水”电池,其总反应为:
5MnO +2Ag+2NaCl=NaMnO +2AgCl,用该“水”电池为电源电解NaCl溶液的实验装置如图2所示,电解过
2 2 5 l0
程中X电极上有无色气体逸出。下列说法正确的是( )A.图1装置中若右池产生0.672 L气体(标准状况下),则电路中通过电子0.15 mol
B.图1装置中左池消耗的苯酚与右池消耗的 的物质的量之比为28:5
C.图2装置的电路中每通过1 mol e-,U形管中消耗0.5 mol HO
2
D.图2装置中“水”电池内每生成1 mol NaMnO ,X电极上生成1 mol气体
2 5 10
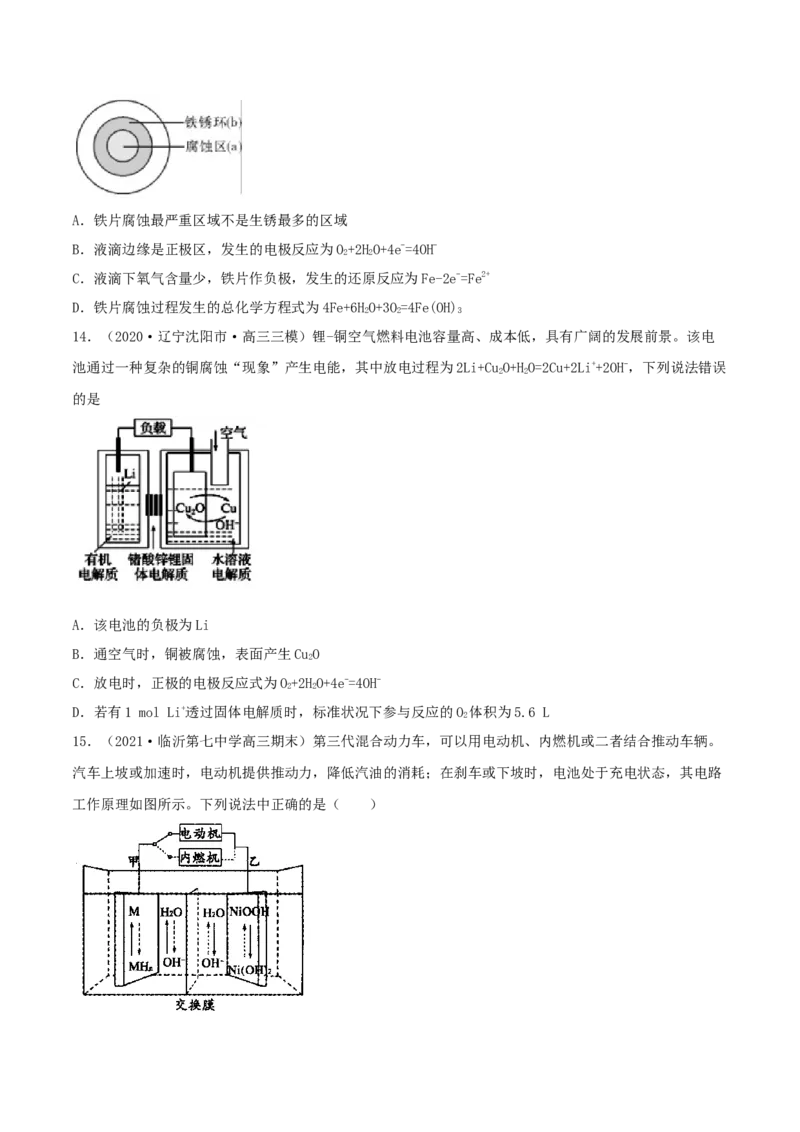
12.(2020·黑龙江哈尔滨市·哈师大附中高三开学考试)利用小粒径零价铁(ZVI)的电化学腐蚀处理三
氯乙烯,进行水体修复的过程如图所示,H+、O、 等共存物会影响修复效果。下列说法错误的是
2
( )
A.反应①②③④均为还原反应
B.1 mol 三氯乙烯完全脱Cl时,电子转移为3 mol
C.④的电极反应式为 +10H++8e-= +3HO
2
D.修复过程中可能产生Fe(OH)
3
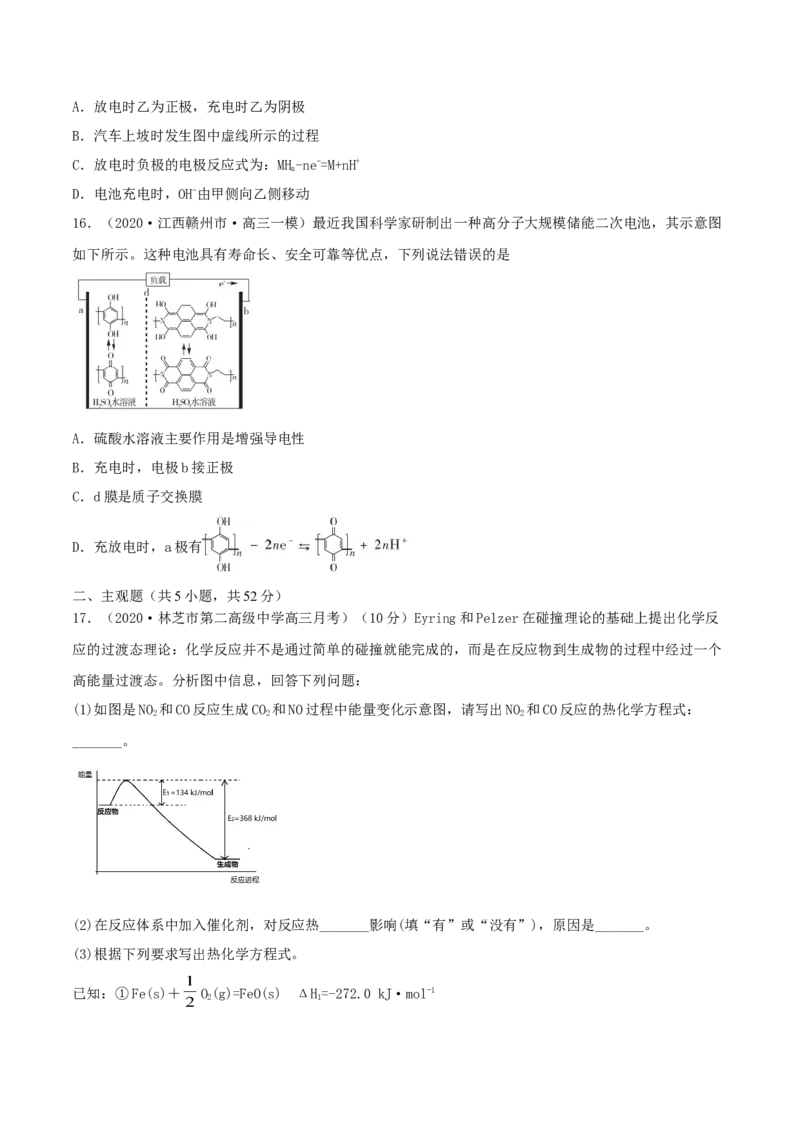
13.(2021·四川成都市·高三一模)将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴
覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。下列说法不正确的是A.铁片腐蚀最严重区域不是生锈最多的区域
B.液滴边缘是正极区,发生的电极反应为O+2HO+4e-=4OH-
2 2
C.液滴下氧气含量少,铁片作负极,发生的还原反应为Fe-2e-=Fe2+
D.铁片腐蚀过程发生的总化学方程式为4Fe+6HO+3O=4Fe(OH)
2 2 3
14.(2020·辽宁沈阳市·高三三模)锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电
池通过一种复杂的铜腐蚀“现象”产生电能,其中放电过程为2Li+CuO+HO=2Cu+2Li++2OH-,下列说法错误
2 2
的是
A.该电池的负极为Li
B.通空气时,铜被腐蚀,表面产生CuO
2
C.放电时,正极的电极反应式为O+2HO+4e-=4OH-
2 2
D.若有1 mol Li+透过固体电解质时,标准状况下参与反应的O 体积为5.6 L
2
15.(2021·临沂第七中学高三期末)第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆。
汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态,其电路
工作原理如图所示。下列说法中正确的是( )A.放电时乙为正极,充电时乙为阴极
B.汽车上坡时发生图中虚线所示的过程
C.放电时负极的电极反应式为:MH-ne-=M+nH+
n
D.电池充电时,OH-由甲侧向乙侧移动
16.(2020·江西赣州市·高三一模)最近我国科学家研制出一种高分子大规模储能二次电池,其示意图
如下所示。这种电池具有寿命长、安全可靠等优点,下列说法错误的是
A.硫酸水溶液主要作用是增强导电性
B.充电时,电极b接正极
C.d膜是质子交换膜
D.充放电时,a极有
二、主观题(共5小题,共52分)
17.(2020·林芝市第二高级中学高三月考)(10分)Eyring和Pelzer在碰撞理论的基础上提出化学反
应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个
高能量过渡态。分析图中信息,回答下列问题:
(1)如图是NO 和CO反应生成CO 和NO过程中能量变化示意图,请写出NO 和CO反应的热化学方程式:
2 2 2
_______。
(2)在反应体系中加入催化剂,对反应热_______影响(填“有”或“没有”),原因是_______。
(3)根据下列要求写出热化学方程式。
已知:①Fe(s)+ O(g)=FeO(s) ΔH=-272.0 kJ·mol-1
2 1②2Al(s)+ O(g)=AlO(s) ΔH=-1 675.7 kJ·mol-1
2 2 3 2
Al和FeO发生反应的热化学方程式是:_______。
(4)已知:
①C(s)+O(g)=CO(g) ΔH
2 2 1
②2CO(g)+O(g)=2CO(g) ΔH
2 2 2
③TiO(s)+2Cl(g)=TiCl(s)+O(g) ΔH
2 2 4 2 3
则反应TiO(s)+2Cl(g)+2C(s)=TiCl(s)+2CO(g)的ΔH=_______。(用含ΔHΔHΔH 的代数式表示)
2 2 4 1 2 3
(5)已知:
化学键 Si—O Si—Cl H—H H—Cl Si—Si Si—C
键能
460 360 436 431 176 347
(kJ·mol-1)
则:SiCl(g)+2H(g) Si(s)+4HCl(g)的反应热ΔH=_______kJ·mol-1。(已知1molSi中含有
4 2
2molSi-Si)
18.(2021·湖南高三期末)(10分)目前,我们日常生活中使用的电能主要还是来自火力发电,火力发
电是利用化石燃料燃烧,通过蒸汽机将产生的能量转化为电能,能量利用率低;燃料电池可以将燃料的化
学能直接转化为电能,能量利用率高。
(1)火力发电厂利用燃煤发电,其能量转化形式为化学能→_______→_______→电能。
(2)磷酸盐燃料电池(PAFC)是当前商业化发展最快的一种燃料电池,以浓磷酸为电解质,以贵金属催化的
气体扩散电极为正、负电极。其优点为构造简单,稳定,电解质挥发度低。磷酸盐燃料电池正极的电极反
应式为_______。
(3)碱性燃料电池(AFC)是最早进入实用阶段的燃料电池之一,也是最早用于车辆的燃料电池,以KOH、
NaOH溶液之类的强碱性溶液为电解质溶液。其优点为性能可靠,具有较高的效率。甲烷碱性燃料电池正极
的电极反应式为_______。
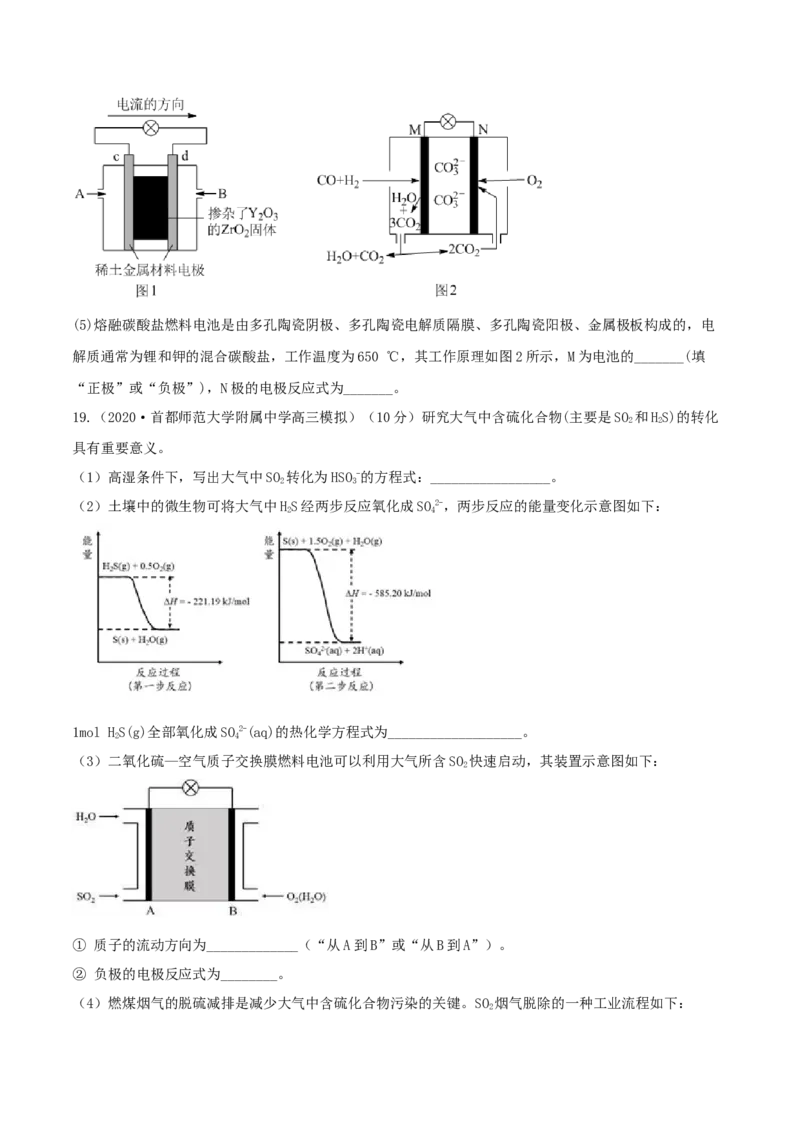
(4)固体氧化物型燃料电池(SOFC),其效率更高,可用于航空航天。如图1所示的装置中,以稀土金属材料
作惰性电极,在电极上分别通入甲烷和空气,其中固体电解质是掺杂了YO 和ZrO 的固体,它在高温下能
2 3 2
穿到O2-;A通入的气体为_______,d电极上的电极反应式为_______。(5)熔融碳酸盐燃料电池是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔陶瓷阳极、金属极板构成的,电
解质通常为锂和钾的混合碳酸盐,工作温度为650 ℃,其工作原理如图2所示,M为电池的_______(填
“正极”或“负极”),N极的电极反应式为_______。
19.(2020·首都师范大学附属中学高三模拟)(10分)研究大气中含硫化合物(主要是SO 和HS)的转化
2 2
具有重要意义。
(1)高湿条件下,写出大气中SO 转化为HSO-的方程式:_________________。
2 3
(2)土壤中的微生物可将大气中HS经两步反应氧化成SO2-,两步反应的能量变化示意图如下:
2 4
1mol HS(g)全部氧化成SO2-(aq)的热化学方程式为___________________。
2 4
(3)二氧化硫—空气质子交换膜燃料电池可以利用大气所含SO 快速启动,其装置示意图如下:
2
① 质子的流动方向为_____________(“从A到B”或“从B到A”)。
② 负极的电极反应式为________。
(4)燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。SO 烟气脱除的一种工业流程如下:
2① 用纯碱溶液吸收SO 将其转化为HSO-,反应的离子方程式是__________________。
2 3
② 若石灰乳过量,将其产物再排回吸收池,其中可用于吸收SO 的物质的化学式是______________。
2
20.(10分)(1)已知C(s,石墨)===C(s,金刚石) ΔH>0,则稳定性:金刚石 (填“>”
“<”)石墨。
(2)已知:2C(s)+2O(g)===2CO(g) ΔH
2 2 1
2C(s)+O(g)===2CO(g) ΔH
2 2
则ΔH (填“>”或“<”)ΔH。
1 2
(3)火箭的第一、二级发动机中,所用的燃料为偏二甲肼和四氧化二氮,偏二甲肼可用肼来制备。用肼
(NH)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
2 4
①N(g)+2O(g)===NO(g)
2 2 2 4
ΔH=+10.7 kJ·mol-1
②NH(g)+O(g)===N(g)+2HO(g)
2 4 2 2 2
ΔH=-543 kJ·mol-1
写出气态肼和NO 反应的热化学方程式:_____________________________
2 4
_________________________________________________________。
(4)25 ℃、101 kPa时,14 g CO在足量的O 中充分燃烧,放出141.3 kJ热量,则CO的燃烧热为ΔH=
2
。
(5)0.50 L 2.00 mol·L-1 HSO 溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,
2 4
该反应的中和热ΔH= 。
(6)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946
kJ,则N 与H 反应生成NH 的热化学方程式是___________________________________________。
2 2 3
21.(2020·山西省晋城市二中模拟)(12分)钒(V)及其化合物广泛应用于工业催化、新材料和新能源
等领域。
(1)① VO 可用于汽车催化剂,汽车尾气中含有 CO 与 NO 气体,用化学方程式解释产生 NO 的原因:
2 5
_______________________________________________________________。
②汽车排气管内安装了钒(V)及其化合物的催化转化器,可使汽车尾气中的主要污染物转化为无毒的气体
排出。已知:
N(g)+O(g)===2NO(g) ΔH=+180.5 kJ/mol
2 22C(s)+O(g)===2CO(g) ΔH=-221.0 kJ/mol
2
C(s)+O(g)===CO(g) ΔH=-393.5 kJ/mol
2 2
尾气转化的反应之一:2NO(g)+2CO(g)===N(g)+2CO(g) ΔH=__________________。
2 2
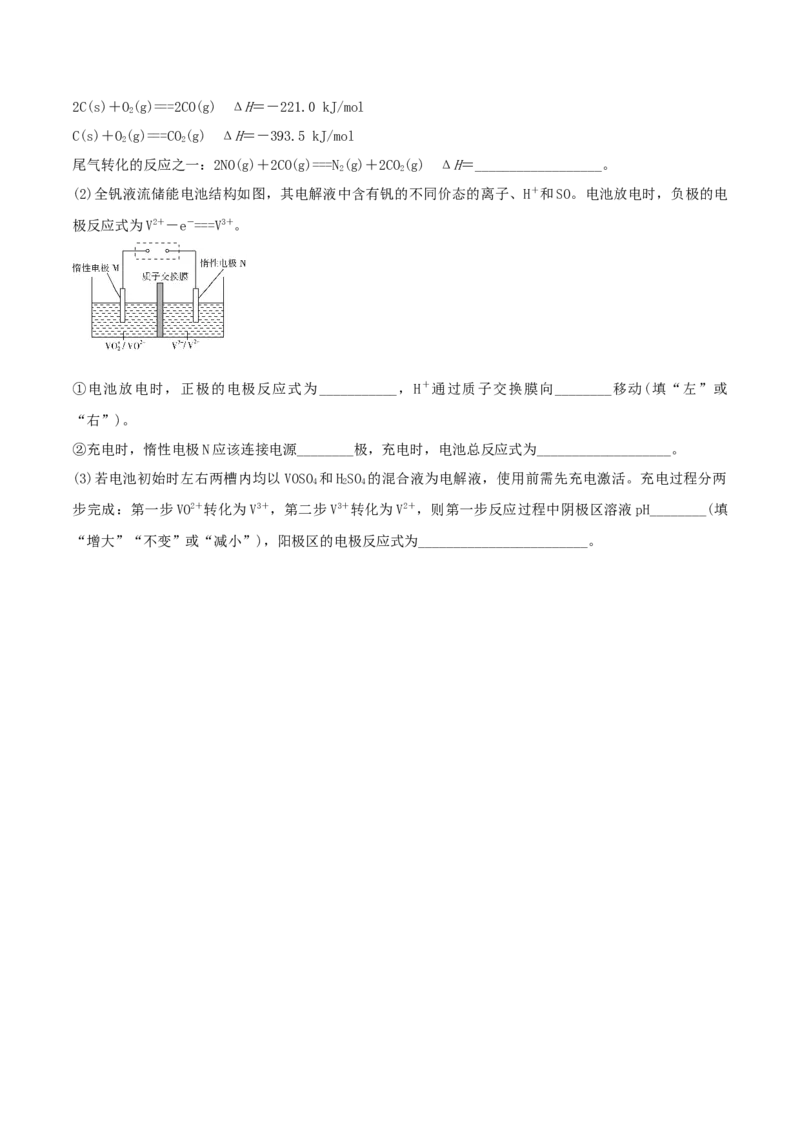
(2)全钒液流储能电池结构如图,其电解液中含有钒的不同价态的离子、H+和SO。电池放电时,负极的电
极反应式为V2+-e-===V3+。
①电池放电时,正极的电极反应式为___________,H+通过质子交换膜向________移动(填“左”或
“右”)。
②充电时,惰性电极N应该连接电源________极,充电时,电池总反应式为___________________。
(3)若电池初始时左右两槽内均以VOSO 和HSO 的混合液为电解液,使用前需先充电激活。充电过程分两
4 2 4
步完成:第一步VO2+转化为V3+,第二步V3+转化为V2+,则第一步反应过程中阴极区溶液pH________(填
“增大”“不变”或“减小”),阳极区的电极反应式为________________________。