文档内容
2025-2026 学年度高一第一学期期初试卷
化 学
注意事项:
1.答题前,考生先将自己的姓名、准考证号码填写清楚,将条形码准确粘贴在条形码区域内。
2.选择题必须使用2B铅笔填涂;非选择题必须使用0.5毫米黑色字迹的签字笔书写,字体工整,笔记清楚。
3.请按照题号顺序在答题卡各题目的答题区域内作答,超出答题区域书写的答案无效:在草稿纸、试卷上
答题无效。
4.作图可先使用铅笔画出,确定后必须用黑色字迹的签字笔描黑。
5.保持卡面清洁,不要折叠、不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。
第I卷(选择题)
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.下列叙述中,正确的是
A.“错把陈醋当成墨,写尽半生纸上酸”,陈醋是电解质
B.牙膏中摩擦剂碳酸钙固体不导电,所以碳酸钙不是电解质
C.碳量子点是一类具有荧光性能的碳纳米材料,属于胶体
D.“朝坛雾卷,曙岭烟沉”中的雾是一种气溶胶,能产生丁达尔效应
2.下列叙述中,正确的是
A.熔融的MgCl 能导电,所以MgCl 是电解质
2 2
B.铜丝、石墨均能导电,所以它们都是电解质
C.KNO 固体不导电,所以KNO 不是电解质
3 3
D.NaCl溶于水,在通电条件下才能发生电离
3.下列物质放置在空气中,因发生氧化还原反应而变质的是
A.NaOH B.Na C.Na CO D.NaHCO
2 3 3
4.某同学查阅资料得知:Cu与稀硫酸不反应,但Cu可与浓硫酸在加热的条件下反应,化学方程式为:
Δ
Cu+2H 2 SO 4 (浓) CuSO 4 +SO 2 ↑+2R,下列说法中不 . 正 . 确 . 的是
A.该反应中涉及了3种类型的化合物
B.R为相对分子质量最小的氧化物
C.反应前后,H SO 中硫的化合价全部发生了改变
2 4
D.该反应不属于四种基本反应类型中的任何一种
试卷第1页,共6页
{#{QQABBQSUgggAAoBAAAgCAQ1ACEAYkBAACAgGgEAQoAIBgBFABAA=}#}5.下列判断正确的是
A.可用水来确定某Na O粉末中是否含有Na O
2 2 2
B.可用CO 来确定Na O粉末中是否含有Na O
2 2 2 2
C.无法利用在空气中加热的方法除去Na O 中的Na O
2 2 2
D.将足量的Na O 和Na O分别加到酚酞溶液中,最终溶液均为红色
2 2 2
6.下列转化中,需要加入氧化剂才能实现的是
A.I I B.HCO CO C. Fe2 Fe3 D.MnO MnO
2 3 2 4 2
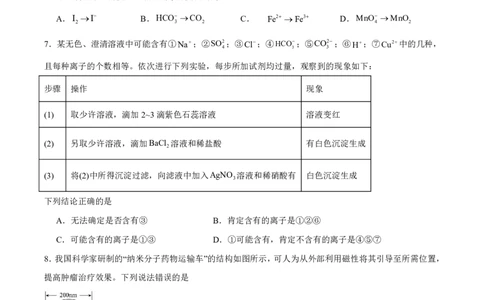
7.某无色、澄清溶液中可能含有①Na;②SO2;③Cl;④HCO;⑤CO2;⑥H;⑦Cu2中的几种,
4 3 3
且每种离子的个数相等。依次进行下列实验,每步所加试剂均过量,观察到的现象如下:
步骤 操作 现象
(1) 取少许溶液,滴加2~3滴紫色石蕊溶液 溶液变红
(2) 另取少许溶液,滴加BaCl 溶液和稀盐酸 有白色沉淀生成
2
(3) 将(2)中所得沉淀过滤,向滤液中加入AgNO 溶液和稀硝酸有 白色沉淀生成
3
下列结论正确的是
A.无法确定是否含有③ B.肯定含有的离子是①②⑥
C.可能含有的离子是①③ D.①可能含有,肯定不含有的离子是④⑤⑦
8.我国科学家研制的“纳米分子药物运输车”的结构如图所示,可人为从外部利用磁性将其引导至所需位置,
提高肿瘤治疗效果。下列说法错误的是
A.该运输车的外壳含有碳元素
B.Fe O 溶于盐酸生成2种可溶性盐
3 4
C.“纳米分子药物运输车”属于混合物
D.该物质分散到水中得到的分散系,具有丁达尔效应
试卷第2页,共6页
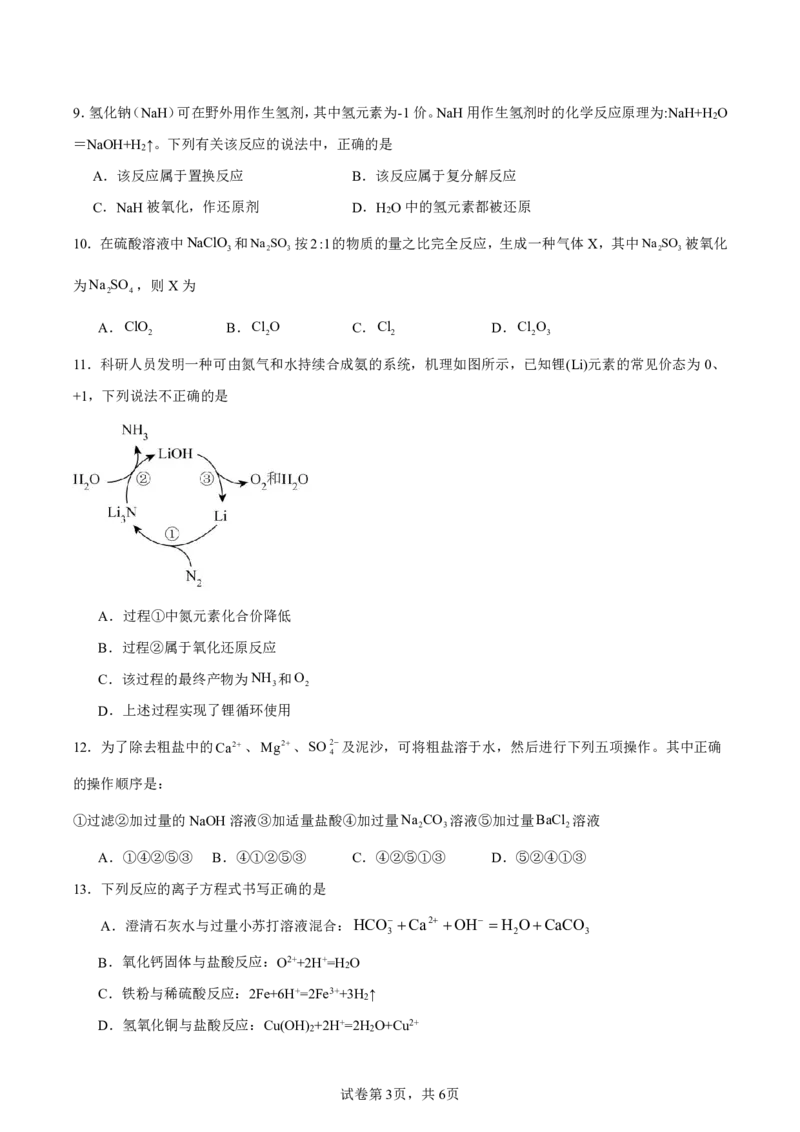
{#{QQABBQSUgggAAoBAAAgCAQ1ACEAYkBAACAgGgEAQoAIBgBFABAA=}#}9.氢化钠(NaH)可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢剂时的化学反应原理为:NaH+H O
2
=NaOH+H ↑。下列有关该反应的说法中,正确的是
2
A.该反应属于置换反应 B.该反应属于复分解反应
C.NaH被氧化,作还原剂 D.H O中的氢元素都被还原
2
10.在硫酸溶液中NaClO 和Na SO 按2:1的物质的量之比完全反应,生成一种气体X,其中Na SO 被氧化
3 2 3 2 3
为Na SO ,则X为
2 4
A.ClO B.Cl O C.Cl D.Cl O
2 2 2 2 3
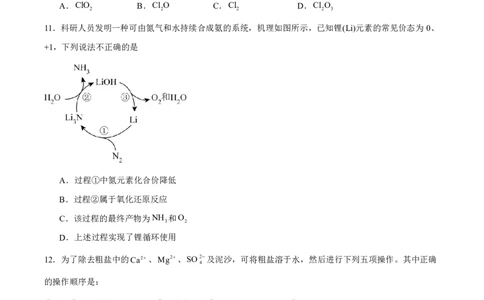
11.科研人员发明一种可由氮气和水持续合成氨的系统,机理如图所示,已知锂(Li)元素的常见价态为0、
+1,下列说法不正确的是
A.过程①中氮元素化合价降低
B.过程②属于氧化还原反应
C.该过程的最终产物为NH 和O
3 2
D.上述过程实现了锂循环使用
12.为了除去粗盐中的Ca2、Mg2、SO2及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确
4
的操作顺序是:
①过滤②加过量的NaOH溶液③加适量盐酸④加过量Na CO 溶液⑤加过量BaCl 溶液
2 3 2
A.①④②⑤③ B.④①②⑤③ C.④②⑤①③ D.⑤②④①③
13.下列反应的离子方程式书写正确的是
A.澄清石灰水与过量小苏打溶液混合:HCO Ca2 OH H OCaCO
3 2 3
B.氧化钙固体与盐酸反应:O2++2H+=H O
2
C.铁粉与稀硫酸反应:2Fe+6H+=2Fe3++3H ↑
2
D.氢氧化铜与盐酸反应:Cu(OH) +2H+=2H O+Cu2+
2 2
试卷第3页,共6页
{#{QQABBQSUgggAAoBAAAgCAQ1ACEAYkBAACAgGgEAQoAIBgBFABAA=}#}14.下列各组离子能在溶液中大量共存的是
A.K+、HCO -、SO2、OH-
3 4
B.Na+、H+、CO2、Cl-
3
C.Na+、Ca2+、NO、CO2
3 3
D.Na+、K+、Cl-、SO2
4
15.分别能实现下列转化的单质是
酸或酸性
金属单质O2碱性氧化物H2O 碱 氧化物 盐
碱或碱性
非金属单质O2酸性氧化物 H2O酸 氧化物 盐
A.Ca和C B.Ca和H C.Cu和C D.Cu和P
2
第II 卷(非选择题)
二、非选择题:本题共4小题,共55分。
16.Ⅰ、现有下列 9种物质:①铝,②纯醋酸,③CO ,④H SO ,⑤NaOH,⑥FeCl 溶液,⑦FeSO 溶液,
2 2 4 3 4
⑧乙醇,⑨碳酸钙。
(1)上述物质中属于非电解质的有 ,能导电的是 。(填序号)
(2)向⑤的溶液中通入少量③,发生反应的化学方程式为 。
(3)④在水中的电离方程式为 。
(4)⑥与⑤的溶液混合,会产生 (填写颜色)沉淀。
Ⅱ、NaHSO 通常为晶体,易溶于水,它溶于水时电离出三种不同的离子,溶液显酸性。NaHSO 受热熔化
4 4
时只能电离出两种不同离子。试回答下列问题:
(5)NaHSO 在熔融状态下电离方程式为: 。
4
(6)NaHSO 在物质分类中属于(酸、碱、盐)中哪一类物质? 。
4
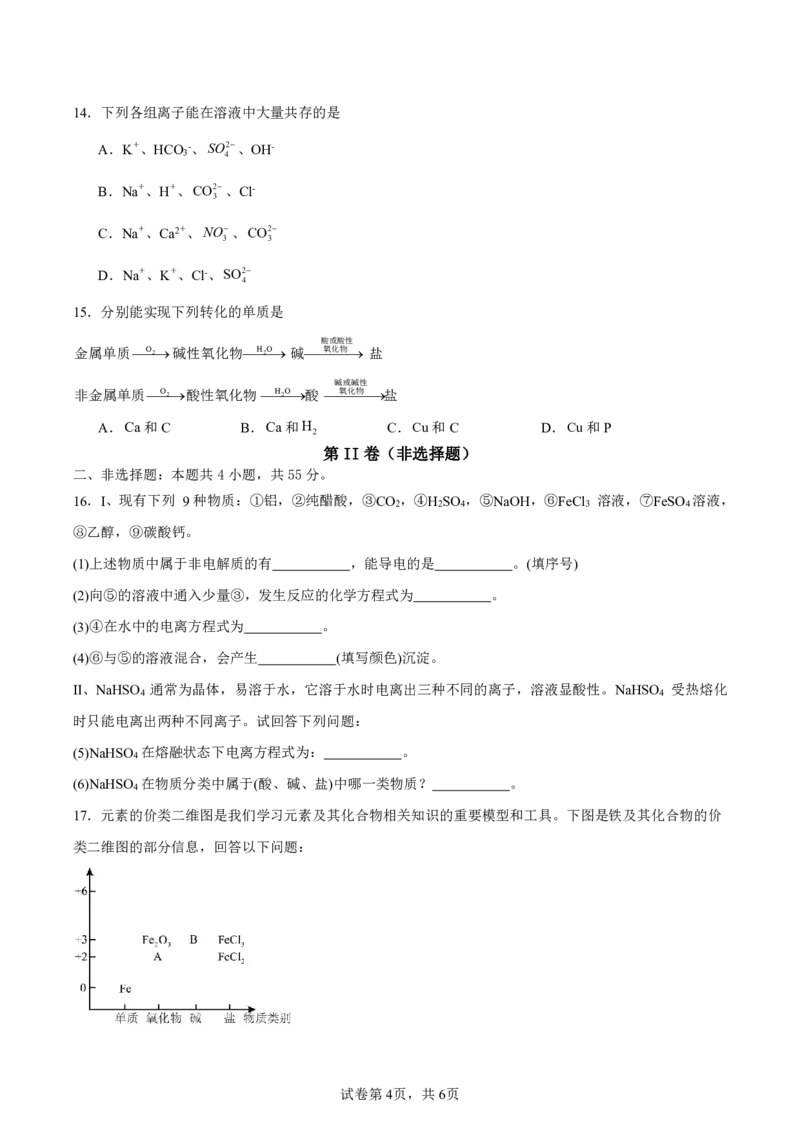
17.元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具。下图是铁及其化合物的价
类二维图的部分信息,回答以下问题:
试卷第4页,共6页
{#{QQABBQSUgggAAoBAAAgCAQ1ACEAYkBAACAgGgEAQoAIBgBFABAA=}#}(1)分别写出A、B的化学式 、 。
(2)写出Fe O 与稀硫酸反应的离子方程式 。
2 3
(3)某同学利用以下试剂研究FeCl 的性质,进行了如下预测:
3
①从化合价角度看,Fe3+具有氧化性,可能与 (填序号)发生反应。从物质类别角度看,FeCl 属
3
于盐,可能与 (填序号)发生复分解反应
A、Cl B、Fe C、NaOH D、H SO E、AgNO
2 2 4 3
②向FeCl 溶液中滴加KSCN溶液(含K+和SCN-),会生成血红色溶液,该反应可用来检验FeCl 溶液中的Fe3+,
3 3
反应方程式为FeCl +3KSCN=Fe(SCN) +3KCl。向该血红色溶液中继续滴加NaOH溶液,则会生成红褐色沉
3 3
淀,写出该反应的离子方程式
(4)高铁酸盐(如Na FeO )是一种新型绿色消毒剂,主要用于饮用水处理。
2 4
①由Na FeO 在上图的位置(未画出)可预测:Na FeO 具有 (填“氧化性”或“还原性”)
2 4 2 4
②工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
3NaClO2FeCl 10NaOH 2Na FeO 9NaCl5H O ,请用双线桥分析上面的化学方程式(从得失电子数
3 2 4 2
目、被氧化还原两个方面进行)。
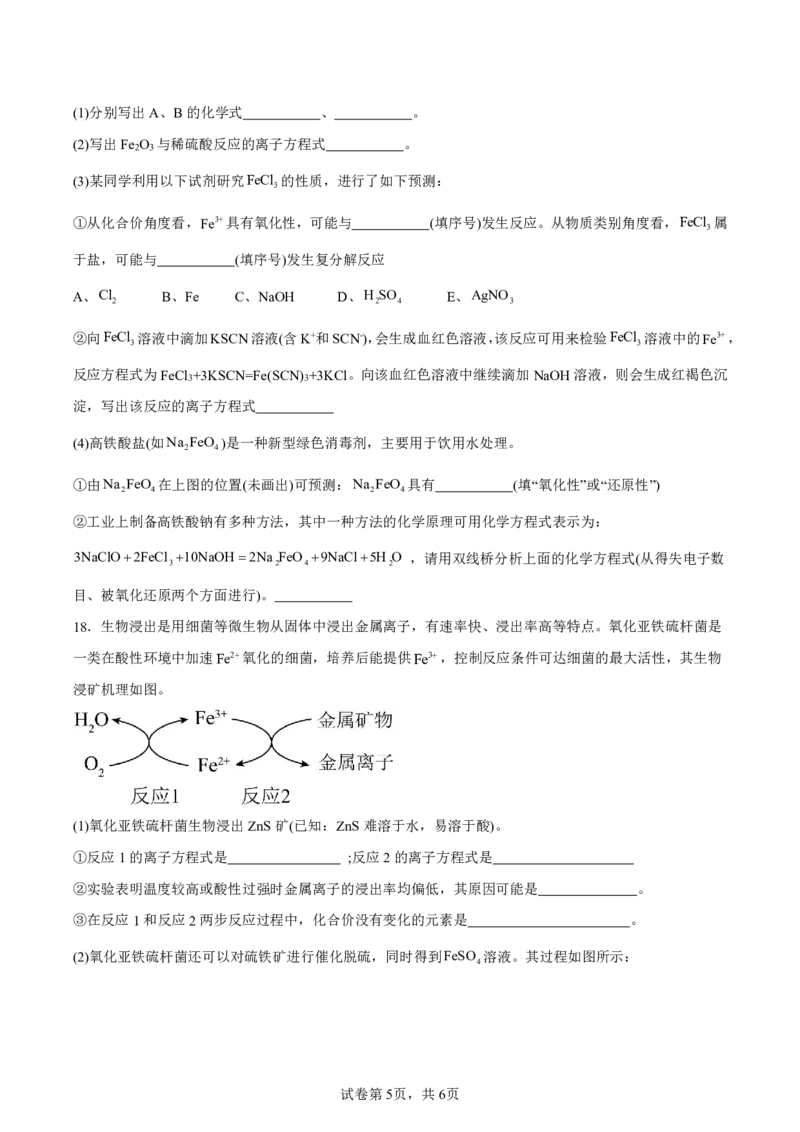
18.生物浸出是用细菌等微生物从固体中浸出金属离子,有速率快、浸出率高等特点。氧化亚铁硫杆菌是
一类在酸性环境中加速Fe2氧化的细菌,培养后能提供Fe3,控制反应条件可达细菌的最大活性,其生物
浸矿机理如图。
(1)氧化亚铁硫杆菌生物浸出ZnS矿(已知:ZnS难溶于水,易溶于酸)。
①反应1的离子方程式是 ;反应2的离子方程式是
②实验表明温度较高或酸性过强时金属离子的浸出率均偏低,其原因可能是 。
③在反应1和反应2两步反应过程中,化合价没有变化的元素是 。
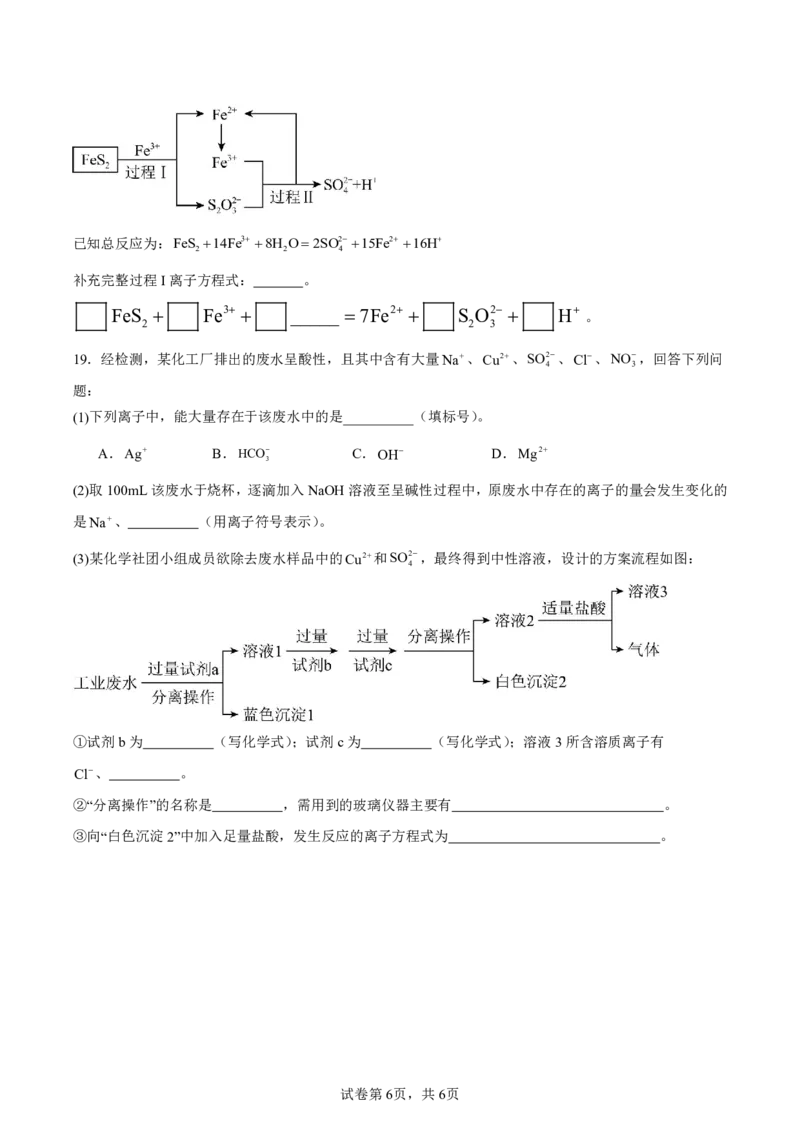
(2)氧化亚铁硫杆菌还可以对硫铁矿进行催化脱硫,同时得到FeSO 溶液。其过程如图所示:
4
试卷第5页,共6页
{#{QQABBQSUgggAAoBAAAgCAQ1ACEAYkBAACAgGgEAQoAIBgBFABAA=}#}已知总反应为:FeS 14Fe3 8H O2SO2 15Fe2 16H
2 2 4
补充完整过程I离子方程式: 。
FeS Fe3 _____ 7Fe2 S O2 H 。
2 2 3
19.经检测,某化工厂排出的废水呈酸性,且其中含有大量Na、Cu2、SO2、Cl、NO,回答下列问
4 3
题:
(1)下列离子中,能大量存在于该废水中的是__________(填标号)。
A.Ag B.HCO C.OH D.Mg2
3
(2)取100mL该废水于烧杯,逐滴加入NaOH溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的
是Na、 (用离子符号表示)。
(3)某化学社团小组成员欲除去废水样品中的Cu2和SO2,最终得到中性溶液,设计的方案流程如图:
4
①试剂b为 (写化学式);试剂c为 (写化学式);溶液3所含溶质离子有
Cl、 。
②“分离操作”的名称是 ,需用到的玻璃仪器主要有 。
③向“白色沉淀2”中加入足量盐酸,发生反应的离子方程式为 。
试卷第6页,共6页
{#{QQABBQSUgggAAoBAAAgCAQ1ACEAYkBAACAgGgEAQoAIBgBFABAA=}#}题号 1 2 3 4 5 6 7 8 9 10
答案 D A B C A C B D C A
题号 11 12 13 14 15
答案 B D D D A
16.(共14分,每空2分)
(1) ③⑧ ①⑥⑦ (2) CO +2NaOH=Na CO +H O
2 2 3 2
(3) H SO =2H++SO2 (4) 红褐色
2 4 4
(5) NaHSO (熔融)=Na++HSO (6) 盐
4 4
17.(共16分,每空2分)
(1) FeO Fe(OH) (2)Fe O +6H+=2Fe3++3H O
3 2 3 2
(3) B C、E Fe(SCN) +3OH-=Fe(OH) +3SCN-
3 3
(4) 氧化性
18.(共10分,每空2分)
细菌 细菌
(1) ① O 4Fe24H 4Fe32H O ZnS2Fe3 Zn2 S2Fe2 ② 温度较高或酸
2 2
性过强时,会导致细菌的活性降低或者失去活性 ③H、Zn
(2) FeS 6Fe3 3H O7Fe2 S O2 6H
2 2 2 3
19.(共15分,除特殊标注外,每空2分)
(1) D
(2) H+、Cu2+
(3) BaCl Na CO Na+和NO- 过滤(1分) 漏斗、烧杯、玻璃棒BaCO +2H+=Ba2++CO ↑+H O
2 2 3 3 3 2 2