文档内容
第2讲 原电池 化学电源
【2020·备考】
最新考纲:1.理解原电池的构成、工作原理及应用。2.能书写电极反应和总反应方
程式。3.了解常见化学电源的种类及其工作原理。
核心素养:1.变化观念与平衡思想:认识原电池的本质是氧化还原反应,能从多角
度、动态地分析原电池中物质的变化及能量的转化。2.科学精神与社会责任:通过
原电池装置的应用,能对与化学有关的热点问题作出正确的价值判断,能参与有
关化学问题的社会实践。
考点一 原电池的工作原理及其应用
(频数:★★☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 电
化学是化学能与热能知识的延伸,是氧化还原反应知识的应用,是高考热点,对于
本考点的主要考查知识点有:(1)电池的正负极的判断;(2)原电池的原理应用;
(3)电极方程式的书写,特别是电极方程式的书写是高考重点,应给予关注。
1.原电池的工作原理
(1)概念和反应本质
原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应。
(2)原电池的构成条件
一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与
电解质溶液反应)。
二看两电极:一般是活泼性不同的两电极。
三看是否形成闭合回路,形成闭合回路需三个条件:①电解质溶液;②两电极直接或间接接触;③两电极插入电解质溶液中。
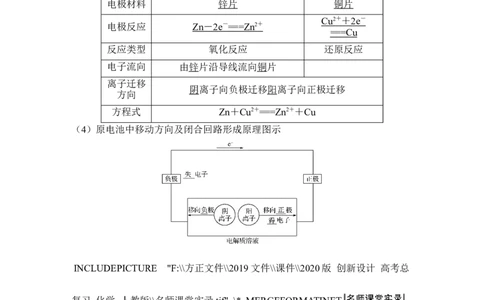
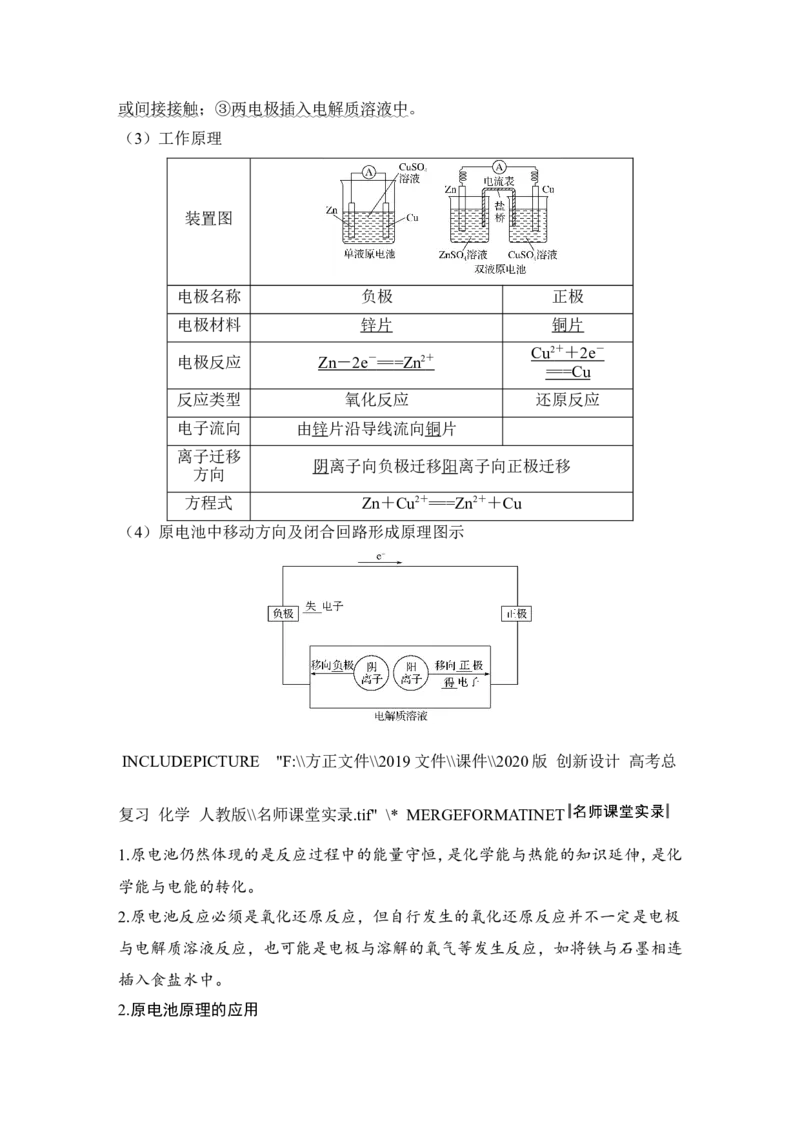
(3)工作原理
装置图
电极名称 负极 正极
电极材料 锌片 铜片
Cu 2 + + 2e -
电极反应 Zn - 2e - == =Zn 2 +
== =Cu
反应类型 氧化反应 还原反应
电子流向 由锌片沿导线流向铜片
离子迁移
阴离子向负极迁移阳离子向正极迁移
方向
方程式 Zn+Cu2+===Zn2++Cu
(4)原电池中移动方向及闭合回路形成原理图示
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.原电池仍然体现的是反应过程中的能量守恒,是化学能与热能的知识延伸,是化
学能与电能的转化。
2.原电池反应必须是氧化还原反应,但自行发生的氧化还原反应并不一定是电极
与电解质溶液反应,也可能是电极与溶解的氧气等发生反应,如将铁与石墨相连
插入食盐水中。
2.原电池原理的应用(1)加快氧化还原反应的速率
一个自发进行的氧化还原反应,设计成原电池时反应速率增大。例如,在Zn与稀
H SO 反应时加入少量CuSO 溶液能使产生H 的反应速率加快。
2 4 4 2
(2)比较金属活动性强弱
两种金属分别作原电池的两极时,一般作负极的金属比作正极的金属活泼。
(3)设计制作化学电源
①首先将氧化还原反应分成两个半反应。
②根据原电池的反应特点,结合两个半反应找出正、负极材料和电解质溶液。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.在理解形成原电池可加快反应速率时,要注意对产物量的理解,Zn与稀H SO
2 4
反应时加入少量CuSO 溶液,锌足量时,不影响产生H 的物质的量,但稀H SO 足
4 2 2 4
量时,产生H 的物质的量要减少。
2
2.把一个氧化还原反应拆写成两个电极反应时,首先要写成离子反应,要注意通过
电荷守恒与原子守恒把H+、OH-、H O分解到两个电极反应中。
2
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)在原电池中,发生氧化反应的一极一定是负极(√)
(2)在原电池中,负极材料的活泼性一定比正极材料强(×)
(3)在原电池中,正极本身一定不参与电极反应,负极本身一定要发生氧化反应
(×)
(4)在锌铜原电池中,因为有电子通过电解质溶液形成闭合回路,所以有电流产生
(×)
(5)两种活泼性不同的金属组成原电池的两极,活泼金属一定作负极(×)
2.(教材改编题)下列装置不能形成原电池的是( )解析 A、B、D项都具有①活泼性不同的电极;②电解质溶液;③闭合回路;④自
发进行的氧化还原反应,均能构成原电池;C项中酒精为非电解质,不能构成原电
池。
答案 C
3.(动手能力培养)某学校研究性学习小组欲以镁条、铝片为电极,以稀NaOH溶
液为电解质溶液设计原电池。给你一只电流表,请你画出该原电池的示意图,并标
出正负极,写出电极反应式。
答案 如图所示
负极 Al+4OH--3e-===AlO+2H O
2
正极 2H O+2e-===H ↑+2OH-
2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
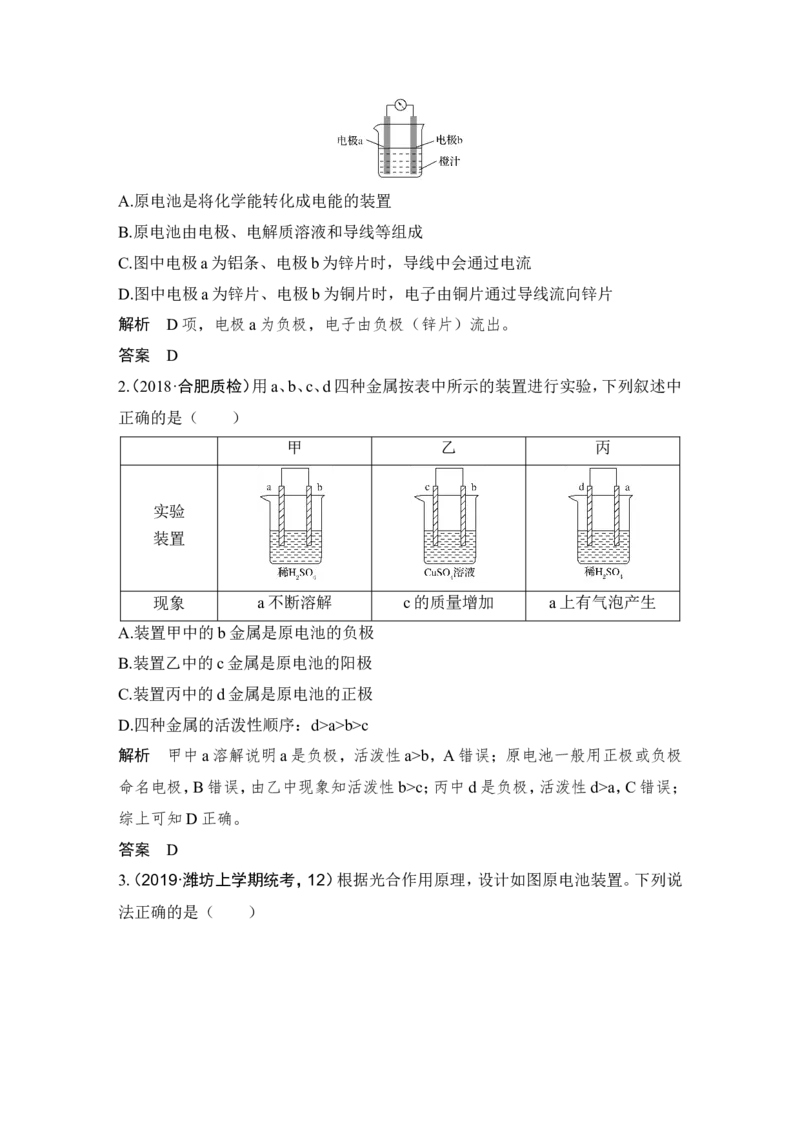
1(. 2019·聊城三中月考)课堂学习中,同学们利用铝条、锌片、铜片、导线、电流计、
橙汁、烧杯等用品探究原电池的组成。下列结论错误的是( )A.原电池是将化学能转化成电能的装置
B.原电池由电极、电解质溶液和导线等组成
C.图中电极a为铝条、电极b为锌片时,导线中会通过电流
D.图中电极a为锌片、电极b为铜片时,电子由铜片通过导线流向锌片
解析 D项,电极a为负极,电子由负极(锌片)流出。
答案 D
2(. 2018·合肥质检)用a、b、c、d四种金属按表中所示的装置进行实验,下列叙述中
正确的是( )
甲 乙 丙
实验
装置
现象 a不断溶解 c的质量增加 a上有气泡产生
A.装置甲中的b金属是原电池的负极
B.装置乙中的c金属是原电池的阳极
C.装置丙中的d金属是原电池的正极
D.四种金属的活泼性顺序:d>a>b>c
解析 甲中a溶解说明a是负极,活泼性a>b,A错误;原电池一般用正极或负极
命名电极,B错误,由乙中现象知活泼性b>c;丙中d是负极,活泼性d>a,C错误;
综上可知D正确。
答案 D
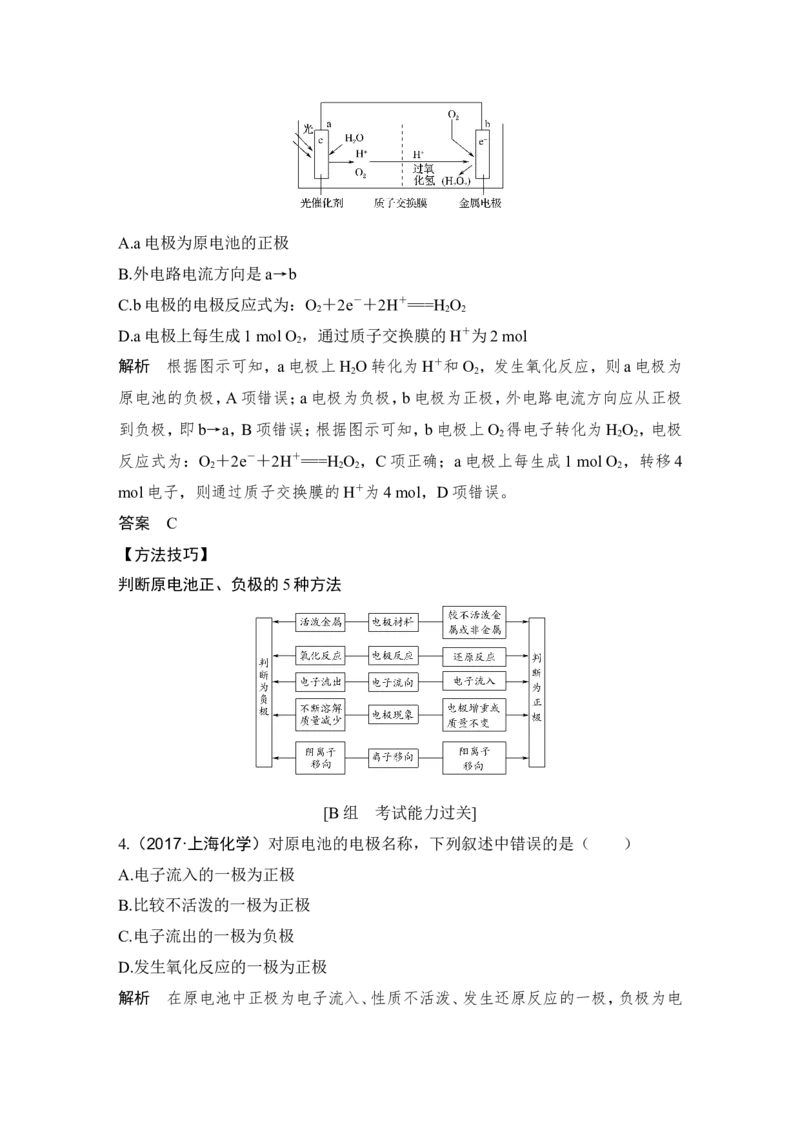
3(. 2019·潍坊上学期统考,12)根据光合作用原理,设计如图原电池装置。下列说
法正确的是( )A.a电极为原电池的正极
B.外电路电流方向是a→b
C.b电极的电极反应式为:O +2e-+2H+===H O
2 2 2
D.a电极上每生成1 mol O ,通过质子交换膜的H+为2 mol
2
解析 根据图示可知,a电极上H O转化为H+和O ,发生氧化反应,则a电极为
2 2
原电池的负极,A项错误;a电极为负极,b电极为正极,外电路电流方向应从正极
到负极,即b→a,B项错误;根据图示可知,b电极上O 得电子转化为H O ,电极
2 2 2
反应式为:O +2e-+2H+===H O ,C项正确;a电极上每生成1 mol O ,转移4
2 2 2 2
mol电子,则通过质子交换膜的H+为4 mol,D项错误。
答案 C
【方法技巧】
判断原电池正、负极的5种方法
[B组 考试能力过关]
4.(2017·上海化学)对原电池的电极名称,下列叙述中错误的是( )
A.电子流入的一极为正极
B.比较不活泼的一极为正极
C.电子流出的一极为负极
D.发生氧化反应的一极为正极
解析 在原电池中正极为电子流入、性质不活泼、发生还原反应的一极,负极为电子流出、性质较活泼、发生氧化反应的一极,故D错误。
答案 D
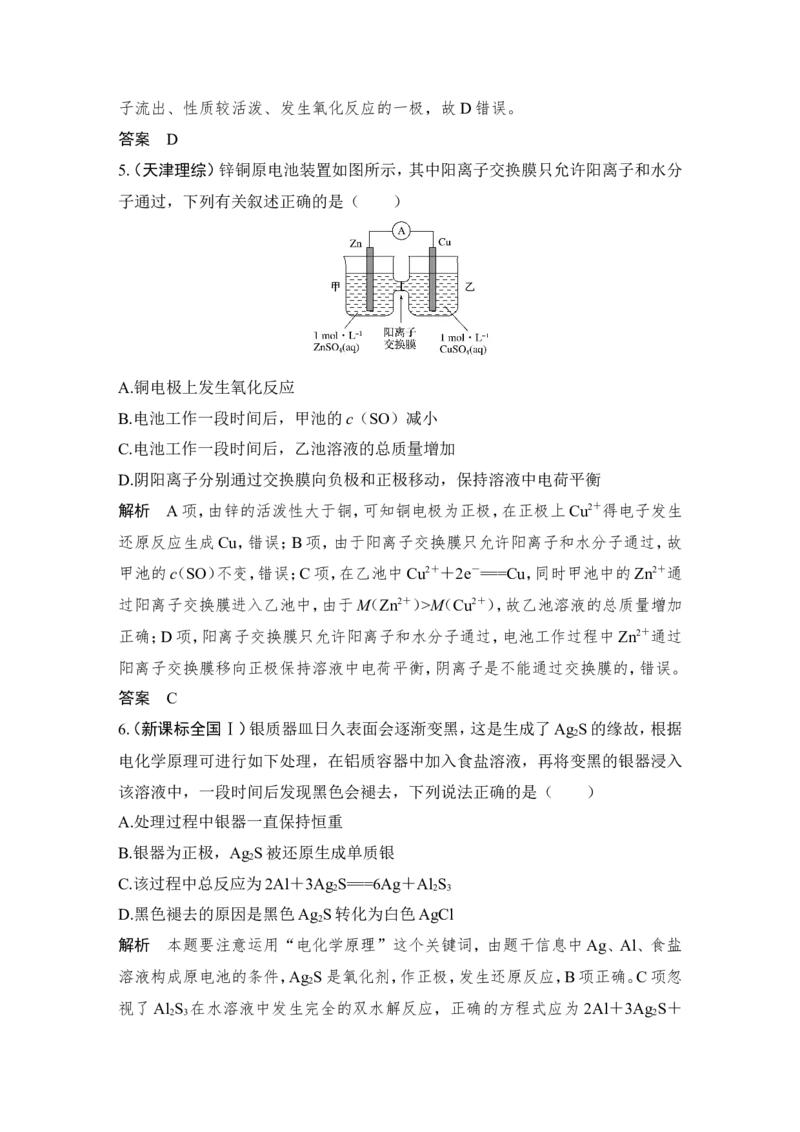
5.(天津理综)锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分
子通过,下列有关叙述正确的是( )
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
解析 A项,由锌的活泼性大于铜,可知铜电极为正极,在正极上Cu2+得电子发生
还原反应生成Cu,错误;B项,由于阳离子交换膜只允许阳离子和水分子通过,故
甲池的c(SO)不变,错误;C项,在乙池中Cu2++2e-===Cu,同时甲池中的Zn2+通
过阳离子交换膜进入乙池中,由于M(Zn2+)>M(Cu2+),故乙池溶液的总质量增加
正确;D项,阳离子交换膜只允许阳离子和水分子通过,电池工作过程中Zn2+通过
阳离子交换膜移向正极保持溶液中电荷平衡,阴离子是不能通过交换膜的,错误。
答案 C
6(. 新课标全国Ⅰ)银质器皿日久表面会逐渐变黑,这是生成了Ag S的缘故,根据
2
电化学原理可进行如下处理,在铝质容器中加入食盐溶液,再将变黑的银器浸入
该溶液中,一段时间后发现黑色会褪去,下列说法正确的是( )
A.处理过程中银器一直保持恒重
B.银器为正极,Ag S被还原生成单质银
2
C.该过程中总反应为2Al+3Ag S===6Ag+Al S
2 2 3
D.黑色褪去的原因是黑色Ag S转化为白色AgCl
2
解析 本题要注意运用“电化学原理”这个关键词,由题干信息中Ag、Al、食盐
溶液构成原电池的条件,Ag S 是氧化剂,作正极,发生还原反应,B项正确。C项忽
2
视了Al S 在水溶液中发生完全的双水解反应,正确的方程式应为 2Al+3Ag S+
2 3 26H O===6Ag+2A(l OH)↓+3H S↑。D项中黑色褪去的原因是Ag S被还原成了
2 3 2 2
Ag。
答案 B
考点二 化学电源
(频数:★★★ 难度:★★★)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 化
学电源知识是电化学中的难点,是我们高考热点题型新型化学电源的知识源头,
特别是燃料电池与充电电池更是重中之重,要熟练掌握介质对半反应的影响及充
电电池四个电极的关系。
1.一次电池
(1)碱性锌锰干电池(图一)
负极材料:Zn
电极反应: Zn + 2OH - - 2e - == =Zn ( OH )
2
正极材料:碳棒
电极反应:2MnO + 2H O + 2e - == =2MnOOH + 2OH -
2 2
总反应:Zn+2MnO +2H O===2MnOOH+Zn(OH)
2 2 2
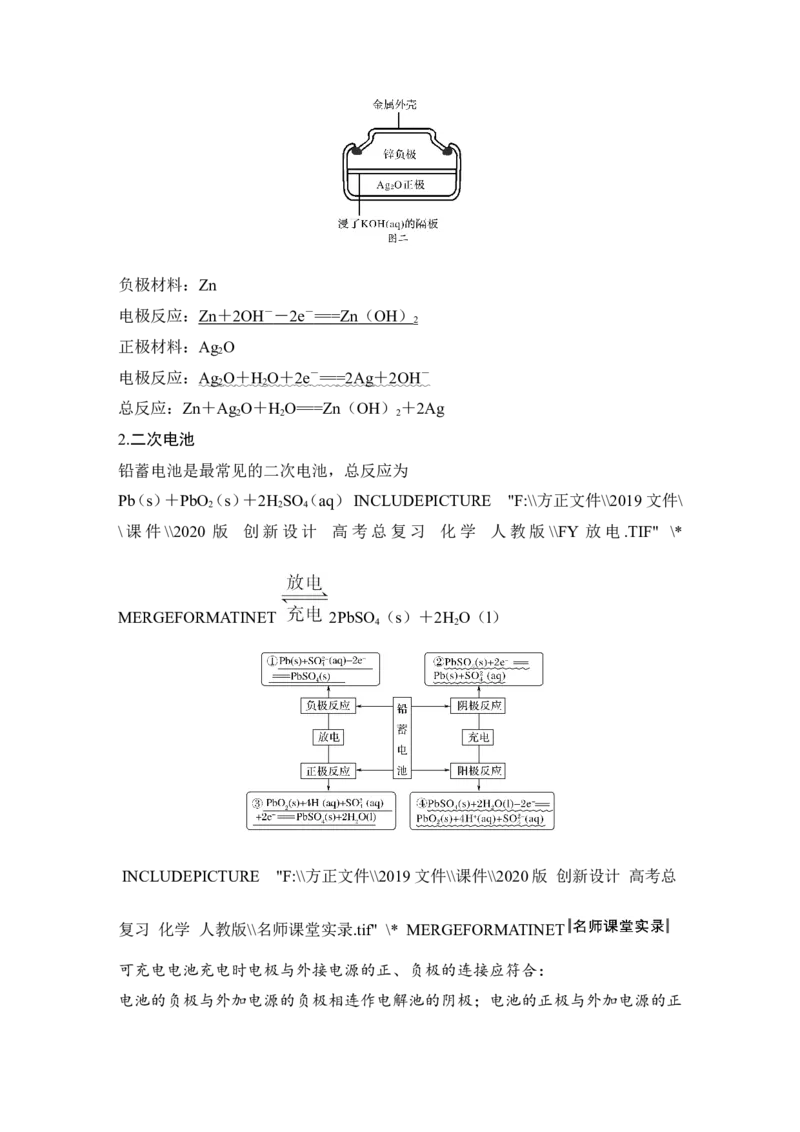
(2)锌银电池(图二)负极材料:Zn
电极反应: Zn + 2OH - - 2e - == =Zn ( OH )
2
正极材料:Ag O
2
电极反应:Ag O + H O + 2e - == =2Ag + 2OH -
2 2
总反应:Zn+Ag O+H O===Zn(OH) +2Ag
2 2 2
2.二次电池
铅蓄电池是最常见的二次电池,总反应为
Pb(s)+PbO(s)+2H SO(aq) INCLUDEPICTURE "F:\\方正文件\\2019文件\
2 2 4
\课件\\2020 版 创新设计 高考总复习 化学 人教版\\FY 放电.TIF" \*
MERGEFORMATINET 2PbSO (s)+2H O(l)
4 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
可充电电池充电时电极与外接电源的正、负极的连接应符合:
电池的负极与外加电源的负极相连作电解池的阴极;电池的正极与外加电源的正极相连作电解池的阳极。如下图(板书)
3.燃料电池
氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种:
种类 酸性 碱性
负极反应式 2H - 4 e - == =4H + 2H + 4OH - - 4 e - == =4H O
2 2 2
正极反应式 O + 4H + + 4 e - = =2H O O + 2H O + 4e - == =4OH -
2 2 2 2
电池反应式 2H +O ===2H O
2 2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.在书写燃料电池的电极反应时,要注意溶液的酸碱性,介质的酸碱性对半反应及
总反应书写的影响。
2.书写电极反应时应注意:“-ne-”相当正电荷,“+ne-”相当负电荷,依据电
荷守恒配平其他物质的系数。
3.根据移动方向, 阳离子趋向正极,在正极上参与反应,在负极上生成(如H+);
阴离子趋向负极,在负极上参与反应,在正极上生成(如OH-、O2-、CO)。
[速查速测]
1.(教材基础知识填空)(1)氢氧燃料电池以KOH溶液作电解质溶液时,工作一
段时间后,电解质溶液的浓度将 (填“减小”、“增大”或“不变”,下同)
溶液的pH 。
(2)氢氧燃料电池以H SO 溶液作电解质溶液时,工作一段时间后,电解质溶液的
2 4
浓度将 (填“减小”、“增大”或“不变”,下同),溶液的pH 。
答案 (1)减小 减小 (2)减小 增大
2.(课后习题改编)某蓄电池反应式为Fe+Ni O +3H O Fe(OH) +2Ni
2 3 2 2(OH) 。下列推断中正确的是( )
2
①放电时,Fe为正极,Ni O 为负极
2 3
②充电时,阴极上的电极反应式是Fe(OH) +2e-===Fe+2OH-
2
③充电时,Ni(OH) 为阳极
2
④蓄电池的电极必须是浸在某碱性溶液中
A.①②③ B.①②④
C.①③④ D.②③④
答案 D
3.(思维探究题)微型燃料电池是采用甲醇(质子交换膜)取代氢作燃料设计而成
的,性能良好,有望取代传统电池,说出此微型燃料电池的优点,并写出电池的负
极反应。__________________________________________________________
_____________________________________________________________________
答案 优点:①电池设计简单;
②和传统充电电池比电池的能量密度高。
负极反应:CH OH-6e-+H O===CO +6H+
3 2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.下面是几种常见的化学电源示意图,有关说法不正确的是( )
干电池示意图 铅蓄电池示意图 氢氧燃料电池示意图
A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒被破坏C.氢氧燃料电池是一种具有应用前景的绿色电源
D.铅蓄电池工作过程中,每通过2 mol电子,负极质量减轻207 g
解析 干电池是一次电池,铅蓄电池是可充电电池,属于二次电池,氢氧燃料电池
属于燃料电池,故A正确;在干电池中,Zn作负极,被氧化,故B正确;氢氧燃料电
池不需要将还原剂和氧化剂全部储藏在电池内,且工作的最终产物是水,故氢氧
燃料电池是一种具有应用前景的绿色电源,故C正确;铅蓄电池工作过程中,硫酸
铅是在负极上析出,该极质量应该增加而非减小,故D错误。
答案 D
2.(2019·烟台模拟)铅蓄电池的工作原理为:Pb+PbO +2H SO ===2PbSO +
2 2 4 4
2H O,研读下图,下列判断正确的是( )
2
A.K闭合时,d电极的电极反应式:PbSO +2e-===Pb+SO
4
B.当电路中通过0.2 mol电子时,Ⅰ中消耗的H SO 为0.2 mol
2 4
C.K闭合时,Ⅱ中SO向c电极迁移
D.K闭合一段时间后,Ⅱ可单独作为原电池,d电极为负极
解析 根据图示,K闭合时,Ⅰ为原电池,a为正极,b为负极,Ⅱ为电解池,c为阴
极,d为阳极。d为阳极,发生氧化反应:PbSO -2e-+2H O===PbO +4H++SO,
4 2 2
A项错误;根据铅蓄电池的总反应知,电路中转移0.2 mol电子时,Ⅰ中消耗0.2
mol H SO ,B项正确;K闭合时,Ⅱ中SO向阳极(d极)迁移,C项错误;K闭合一
2 4
段时间后,c电极析出Pb,d电极析出PbO ,电解质溶液为H SO 溶液,此时可以
2 2 4
形成铅蓄电池,d电极作正极,D项错误。
答案 B
3(. 传统锌锰干电池的改进)(2018·北京大联盟联考)由我国科学家研发成功的铝
锰电池是一种比能量很高的新型干电池,以氯化钠和稀氨水混合溶液为电解质,
铝和二氧化锰—石墨为两极,其电池反应为Al+3MnO +3H O===3MnO(OH)+
2 2Al(OH) 。下列有关该电池放电时的说法不正确的是( )
3
A.二氧化锰—石墨为电池正极
B.负极反应式为Al-3e-+3NH ·H O===Al(OH) +3NH
3 2 3
C.OH-不断由负极向正极移动
D.每生成1 mol MnO(OH)转移1 mol电子
解析 由电池反应方程式知,铝为电池负极,铝失去电子转化为Al(OH),A、B
3
正确;阴离子移向负极,C错误;由反应中锰元素价态变化知D正确。
答案 C
【归纳反思】
书写电极反应式时的三个原则
1.共存原则:因为物质得失电子后在不同介质中的存在形式不同,所以电极反应式
的书写必须考虑介质环境。碱性溶液中CO 不可能存在,也不可能有H+参加反应
2
当电解质溶液呈酸性时,不可能有OH-参加反应。
2.得氧失氧原则:得氧时,在反应物中加H O(电解质为酸性时)或OH-(电解质为
2
碱性或中性时);失氧时,在反应物中加H O(电解质为碱性或中性时)或H+(电解
2
质为酸性时)。
3.中性吸氧反应成碱原则:在中性电解质溶液中,通过金属吸氧所建立起来的原电
池反应,其反应的最后产物是碱。
[B组 考试能力过关]
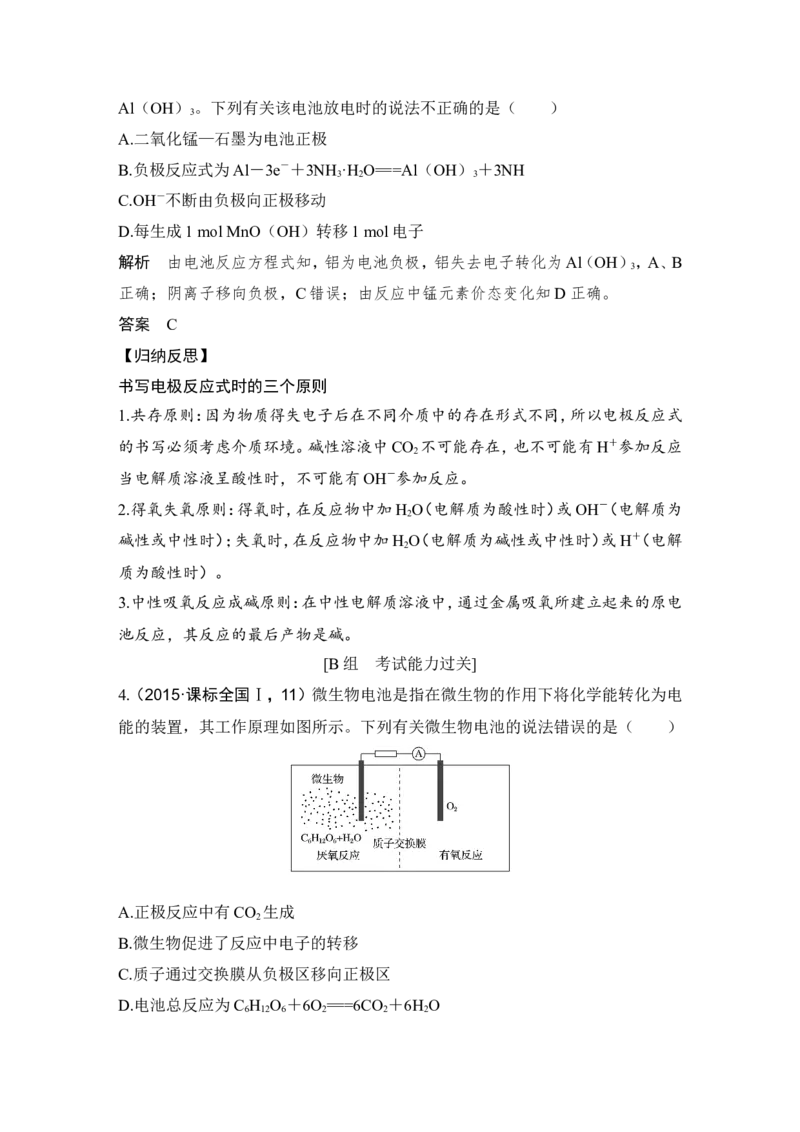
4.(2015·课标全国Ⅰ,11)微生物电池是指在微生物的作用下将化学能转化为电
能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是( )
A.正极反应中有CO 生成
2
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C H O +6O ===6CO +6H O
6 12 6 2 2 2解析 由题意可知,微生物电池的原理是在微生物的作用下,O 与C H O 发生氧
2 6 12 6
化还原反应,将化学能转化为电能,B项正确;氧气在正极反应,由于质子交换膜
只允许H+通过,则正极反应为:O +4e-+4H+===2H O,没有CO 生成,A项错误
2 2 2
负极发生反应:C H O -24e-+6H O===6CO +24H+,H+在负极区生成,移向正
6 12 6 2 2
极区,在正极被消耗,C项正确;总反应为:C H O +6O ===6CO +6H O,D项正
6 12 6 2 2 2
确。
答案 A
5.(2018·课标全国Ⅱ,12)我国科学家研发了一种室温下“可呼吸”的NaCO 二
2
次电池。将NaClO 溶于有机溶剂作为电解液,钠和负载碳钠米管的镍网分别作为
4
电极材料,电池的总反应为:3CO +4Na 2Na CO +C。下列说法错误的是(
2 2 3
)
A.放电时,ClO向负极移动
B.充电时释放CO ,放电时吸收CO
2 2
C.放电时,正极反应为:3CO +4e-===2CO+C
2
D.充电时,正极反应为:Na++e-===Na
解析 电池放电时,ClO向负极移动,A项正确;结合总反应可知放电时需吸收
CO ,而充电时释放出CO ,B项正确;放电时,正极CO 得电子被还原生成单质
2 2 2
C,即电极反应式为3CO +4e-===2CO+C,C项正确;充电时阳极发生氧化反应,
2
即C被氧化生成CO ,D项错误。
2
答案 D
6(. 2015·全国卷Ⅱ,26节选)酸性锌锰干电池是一种一次性电池,外壳为金属锌,
中间是碳棒,其周围是由碳粉、MnO 、ZnCl 和NH Cl等组成的糊状填充物。该电
2 2 4
池放电过程产生MnOOH。
该电池的正极反应式为______________________________________________,
电池反应的离子方程式为______________________________________________。维持电流强度为0.5 A,电池工作5分钟,理论上消耗锌 g。(已知F=
96 500 C·mol-1)
解析 酸性锌锰干电池中正极上发生还原反应,该电池放电过程中产生MnOOH,
则正极反应式为MnO +H++e-===MnOOH。金属锌作负极,发生氧化反应生成
2
Zn2+,则负极反应式为Zn-2e-===Zn2+,结合得失电子守恒可得电池反应式为
2MnO +2H++Zn===2MnOOH+Zn2+。电流强度为I=0.5 A,时间为t=5 min=
2
300 s,则通过电极的电量为Q=It=0.5 A×300 s=150 C,又知F=96 500 C·mol-
1,故通过电子的物质的量为≈0.001 6 mol,则理论上消耗Zn的质量为65 g·mol-
1×0.001 6 mol×1/2≈0.05 g。
答案 MnO +H++e-===MnOOH 2MnO +Zn+2H+===2MnOOH+Zn2+
2 2
0.05
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET
[A级 全员必做题]
1.下列关于原电池的叙述中正确的是( )
A.正极和负极必须是金属
B.原电池是把化学能转化成电能的装置
C.原电池工作时,正极和负极上发生的都是氧化还原反应
D.锌、铜和盐酸构成的原电池工作时,锌片上有6.5 g锌溶解,正极上就有0.1 g氢
气生成
解析 一般普通原电池中负极必须是金属,正极可以是金属或非金属导体,A错
误;原电池是把化学能转化成电能的装置,B正确;原电池工作时,正极上发生还
原反应,负极上发生氧化反应,C错误;锌、铜和盐酸构成的原电池工作时,锌片上
有6.5 g锌溶解,正极上有0.2 g氢气生成,D错误。
答案 B
2.各式各样电池的迅速发展是化学对人类的一项重大贡献。下列有关电池的叙述
正确的是( )
A.手机上用的锂离子电池可以用KOH溶液作电解液B.锌锰干电池中,锌电极是负极
C.氢氧燃料电池工作时氢气在负极上被还原
D.太阳能电池的主要材料是高纯度的二氧化硅
解析 锂能与水反应,不能用水溶液作电解液,A错误;锌锰干电池中锌失去电子
生成Zn2+为负极,B正确;氢氧燃料电池工作时氢气在负极被氧化,C错误;太阳
能电池的主要材料为硅,D错误。
答案 B
3(. 2019·深圳模拟)如图是课外活动小组设计的用化学电源使LED灯发光的装置
下列说法错误的是( )
A.铜片表面有气泡生成
B.装置中存在“化学能→电能→光能”的转换
C.如果将硫酸换成柠檬汁,导线中不会有电子流动
D.如果将锌片换成铁片,电路中的电流方向不变
解析 铜锌原电池中,Cu作正极,溶液中的氢离子在正极上得电子生成氢气,所
以Cu上有气泡生成,故A正确;原电池中化学能转化为电能,LED灯发光时,电
能转化为光能,故B正确;柠檬汁显酸性也能作电解质溶液,所以将硫酸换成柠檬
汁,仍然构成原电池,所以导线中有电子流动,故C错误;金属性Cu比Zn、Fe弱,
Cu作正极,所以电路中的电流方向不变,故D正确。
答案 C
4.(2019·山东滨州月考)下列有关说法中错误的是( )
A.某燃料电池用熔融碳酸盐作电解质,两极分别通入CO和O ,则通入CO的一极
2
为负极,电极反应式为CO-2e-+CO===2CO
2
B.Zn 粒与稀硫酸反应制氢气时,为加快反应速率,可在反应过程中滴加几滴
CuSO 溶液
4
C.根据自发氧化还原反应Cu+2NO+4H+===Cu2++2NO ↑+2H O设计原电池,
2 2
可在常温下用铜和铁作电极,使用浓硝酸作电解质溶液D.原电池中电子从负极出发,经外电路流向正极,再从正极经电解液回到负极构
成闭合回路
答案 D
5.(2019·福建厦门第一次质量检测)铁碳微电解技术是利用原电池原理处理酸性
污水的一种工艺,装置如图。若上端开口关闭,可得到强还原性的H(· 氢原子);若
上端开口打开,并鼓入空气,可得到强氧化性的·OH(羟基自由基)。下列说法错误
的是( )
A.无论是否鼓入空气,负极的电极反应式均为Fe-2e-===Fe2+
B.不鼓入空气时,正极的电极反应式为H++e-===H·
C.鼓入空气时,每生成1 mol·OH有2 mol电子发生转移
D.处理含有草酸(H C O )的污水时,上端开口应打开并鼓入空气
2 2 4
解析 根据铁碳微电解装置示意图可知,Fe为原电池负极,发生氧化反应:Fe-2e
-===Fe2+,故A正确;由题意可知上端开口关闭,可得到强还原性的H·,则不鼓入
空气时,正极的电极反应式为H++e-===H·,故B正确;鼓入空气时,正极的电极
反应式为O +2H++2e-===2·OH,每生成1 mol·OH有1 mol电子发生转移,故C
2
错误;处理含有草酸(H C O )的污水时,因C O具有很强的还原性,与氧化剂作用
2 2 4 2
易被氧化为CO 和H O,则上端开口应打开并鼓入空气生成强氧化性的·OH,以氧
2 2
化H C O 处理污水,故D正确。
2 2 4
答案 C
6.(2018·安徽“江南十校”第一次联考)某种熔融碳酸盐燃料电池以Li CO 、
2 3
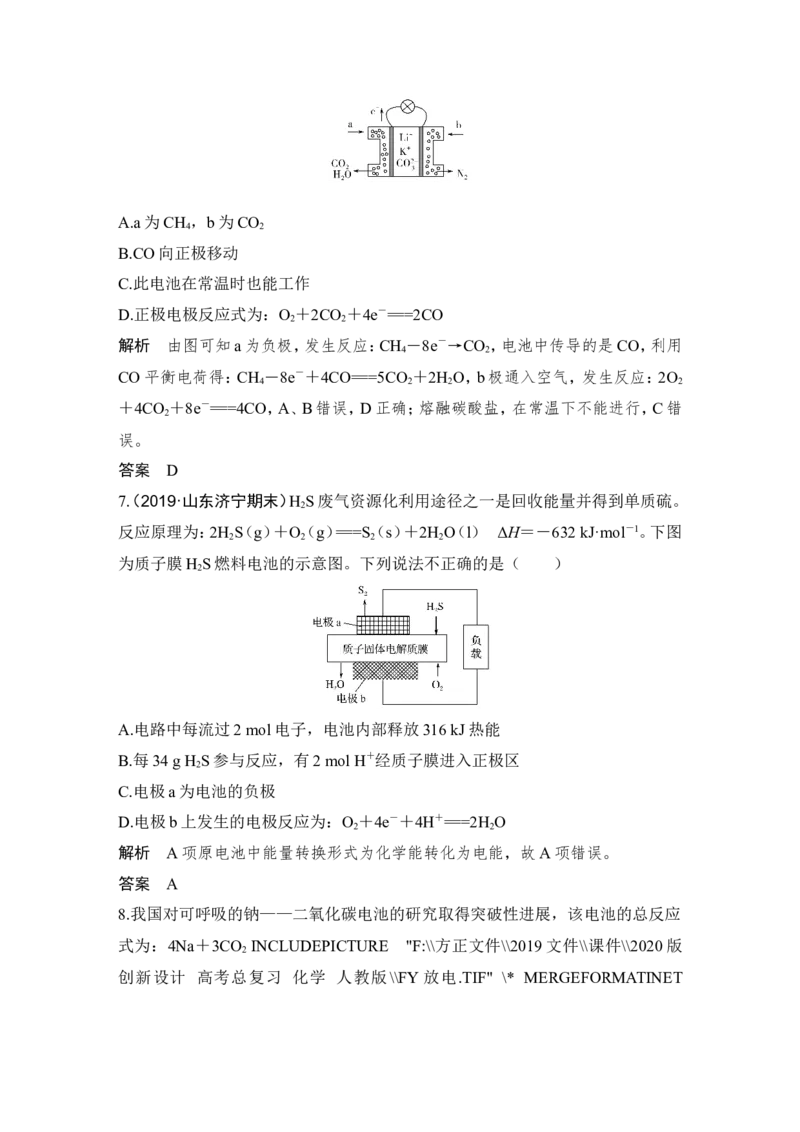
K CO 为电解质、以CH 为燃料时,该电池工作原理见图。下列说法正确的是(
2 3 4
)A.a为CH ,b为CO
4 2
B.CO向正极移动
C.此电池在常温时也能工作
D.正极电极反应式为:O +2CO +4e-===2CO
2 2
解析 由图可知a为负极,发生反应:CH -8e-→CO ,电池中传导的是CO,利用
4 2
CO平衡电荷得:CH -8e-+4CO===5CO +2H O,b极通入空气,发生反应:2O
4 2 2 2
+4CO +8e-===4CO,A、B错误,D正确;熔融碳酸盐,在常温下不能进行,C错
2
误。
答案 D
7(. 2019·山东济宁期末)H S废气资源化利用途径之一是回收能量并得到单质硫。
2
反应原理为:2H S(g)+O(g)===S(s)+2H O(l) ΔH=-632 kJ·mol-1。下图
2 2 2 2
为质子膜H S燃料电池的示意图。下列说法不正确的是( )
2
A.电路中每流过2 mol电子,电池内部释放316 kJ热能
B.每34 g H S参与反应,有2 mol H+经质子膜进入正极区
2
C.电极a为电池的负极
D.电极b上发生的电极反应为:O +4e-+4H+===2H O
2 2
解析 A项原电池中能量转换形式为化学能转化为电能,故A项错误。
答案 A
8.我国对可呼吸的钠——二氧化碳电池的研究取得突破性进展,该电池的总反应
式为:4Na+3CO INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版
2
创新设计 高考总复习 化学 人教版\\FY 放电.TIF" \* MERGEFORMATINET2Na CO +C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳
2 3
米管中)。关于该电池,下列说法错误的是( )
A.充电时,Na+从阳极向阴极移动
B.可以用乙醇代替TEGDME作有机溶剂
C.放电时,当转移1 mol电子时负极质量减轻23 g
D.放电时,正极反应式为3CO +4Na++4e-===2Na CO +C
2 2 3
解析 已知 4Na+3CO INCLUDEPICTURE "F:\\方正文件\\2019 文件\\课件\
2
\2020 版 创 新 设 计 高 考 总 复 习 化 学 人 教 版 \\FY 放 电 .TIF" \*
MERGEFORMATINET 2Na CO +C,放电时Na为负极,充电时Na金属片
2 3
连接电源的负极为阴极;A.充电时是电解池,Na+从阳极向阴极移动,故A正确;
B.Na能与乙醇反应,不可代替TEGDME做有机溶剂,故B错误;C.放电时,当转
移1 mol电子时,负极氧化的钠为1 mol,即质量减轻23 g,故C正确;D.放电时,
正极上 CO 发生还原反应生成 C,发生的电极反应为 3CO +4Na++4e-
2 2
===2Na CO +C,故D正确。
2 3
答案 B
9.(2018·安徽皖北协作区联考)一种三室微生物燃料电池可用于污水净化、海水
淡化,其工作原理如图所示,图中有机废水中有机物可用C H O 表示。下列有关
6 10 5
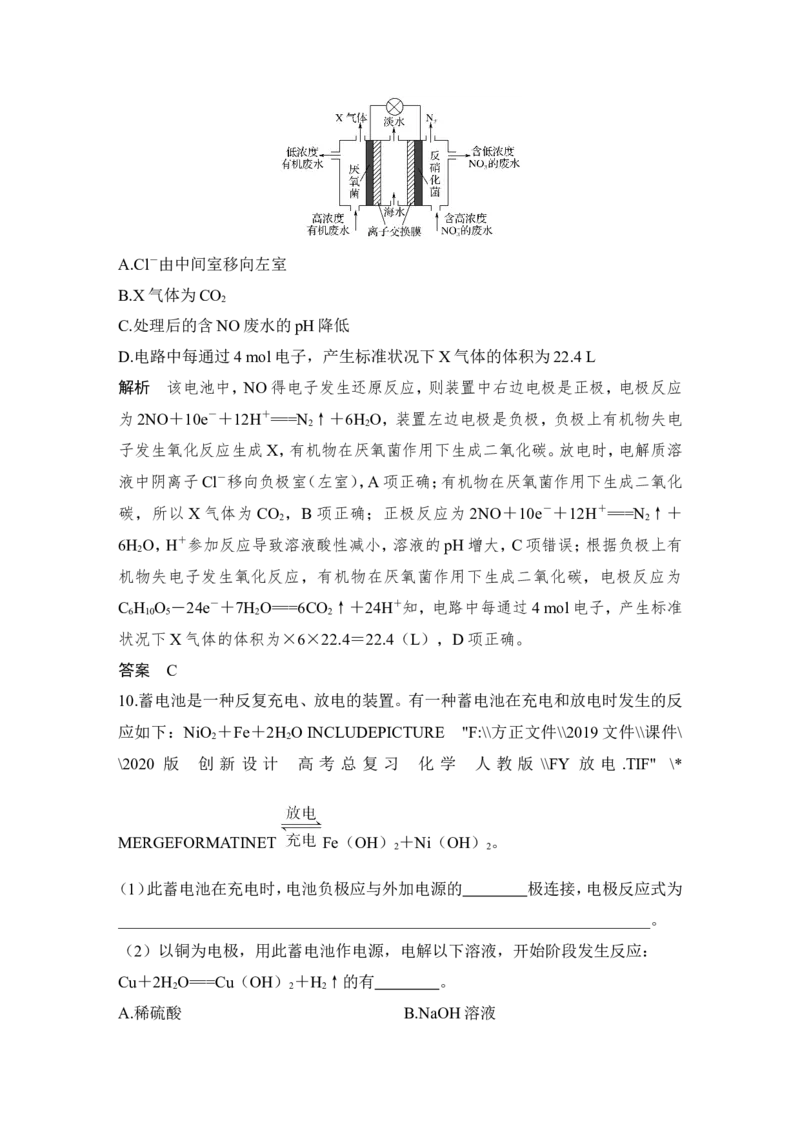
说法不正确的是( )A.Cl-由中间室移向左室
B.X气体为CO
2
C.处理后的含NO废水的pH降低
D.电路中每通过4 mol电子,产生标准状况下X气体的体积为22.4 L
解析 该电池中,NO得电子发生还原反应,则装置中右边电极是正极,电极反应
为2NO+10e-+12H+===N ↑+6H O,装置左边电极是负极,负极上有机物失电
2 2
子发生氧化反应生成X,有机物在厌氧菌作用下生成二氧化碳。放电时,电解质溶
液中阴离子Cl-移向负极室(左室),A项正确;有机物在厌氧菌作用下生成二氧化
碳,所以X气体为CO ,B项正确;正极反应为2NO+10e-+12H+===N ↑+
2 2
6H O,H+参加反应导致溶液酸性减小,溶液的pH增大,C项错误;根据负极上有
2
机物失电子发生氧化反应,有机物在厌氧菌作用下生成二氧化碳,电极反应为
C H O -24e-+7H O===6CO ↑+24H+知,电路中每通过4 mol电子,产生标准
6 10 5 2 2
状况下X气体的体积为×6×22.4=22.4(L),D项正确。
答案 C
10.蓄电池是一种反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反
应如下:NiO +Fe+2H O INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\
2 2
\2020 版 创 新 设 计 高 考 总 复 习 化 学 人 教 版 \\FY 放 电 .TIF" \*
MERGEFORMATINET Fe(OH) +Ni(OH) 。
2 2
(1)此蓄电池在充电时,电池负极应与外加电源的 极连接,电极反应式为
__________________________________________________________________。
(2)以铜为电极,用此蓄电池作电源,电解以下溶液,开始阶段发生反应:
Cu+2H O===Cu(OH) +H ↑的有 。
2 2 2
A.稀硫酸 B.NaOH溶液C.Na SO 溶液 D.CuSO 溶液
2 4 4
E.NaCl溶液
(3)假如用此蓄电池电解以下溶液(电解池两极均为惰性电极),工作一段时间后,
蓄电池内部消耗了0.36 g水,则:电解足量N(NO )溶液时某一电极析出了a g金
3 x
属N,则金属N的相对原子质量R的计算公式为R= (用含a、x的代数
式表示)。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质、CH 为燃料、空气为氧化剂、稀土
4
金属材料为电极的新型电池。已知该熔融盐电池的负极的电极反应是CH -
4
8e - + 4CO===5CO + 2H O , 则 正 极 的 电 极 反 应 式 为
2 2
_____________________________________________________________________
_____________________________________________________________________
。
解析 (1)此蓄电池在充电时,电池阴极应与外加电源的负极连接,发生氢氧化亚
铁得电子的还原反应,其电极反应式为Fe(OH) +2e-===Fe+2OH-。
2
(2)以铜为电极,用此蓄电池作电源,则阳极铜失去电子,根据总电极方程式可知
阴极是氢离子得到电子,铜离子与氢氧根结合生成氢氧化铜沉淀,稀硫酸溶液显
酸性,不能生成氢氧化铜,A错误;氢氧化钠溶液显碱性,阴极氢离子放电,可以产
生氢氧化铜,B正确;铜电极电解硫酸钠溶液,阴极氢离子放电,破坏水的电离平
衡,产生氢氧化铜,C正确;铜电极电解硫酸铜溶液,开始阴极铜离子放电,D错误;
铜电极电解氯化钠溶液,阴极氢离子放电,破坏水的电离平衡,产生氢氧化铜,E
正确。
(3)假如用此蓄电池电解以下溶液(电解池两极均为惰性电极),工作一段时间后,
蓄电池内部消耗了0.36 g水,即0.02 mol水,根据方程式可知反应中转移0.02 mol
电子。电解足量N(NO )溶液时某一电极析出了a g金属N,则根据电子得失守恒
3 x
可知,金属N的相对原子质量R的计算公式为R==50ax。
(4)已知该熔融盐电池的负极的电极反应是CH -8e-+4CO===5CO +2H O,则
4 2 2
正极是氧气得到电子,根据负极反应式可知,正极电极反应式为2O +4CO +8e-
2 2
===4CO。
答案 (1)负 Fe(OH) +2e-===Fe+2OH-
2
(2)B、C、E (3)50ax (4)O +2CO +4e-===2CO(或2O +4CO +8e-
2 2 2 2===4CO)
11.(2018·天津静海一中等五校期末联考)某兴趣小组做如下探究实验:
(1)图Ⅰ为依据氧化还原反应设计的原电池装置,该反应的离子方程式为
_____________________________________________________________________。
反应前,两电极质量相等,一段时间后,两电极质量相差12 g,则导线中通过
mol电子。
(2)如图Ⅰ,其他条件不变,若将CuCl 溶液换为NH Cl溶液,石墨电极的反应式
2 4
为_____________________________________________________________,
这是由于NH Cl溶液显 (填“酸性”“碱性”或“中性”),用离子方程
4
式 表 示 溶 液 显 此 性 的 原 因 :
______________________________________________________________________
_____________________________________________________________________
。
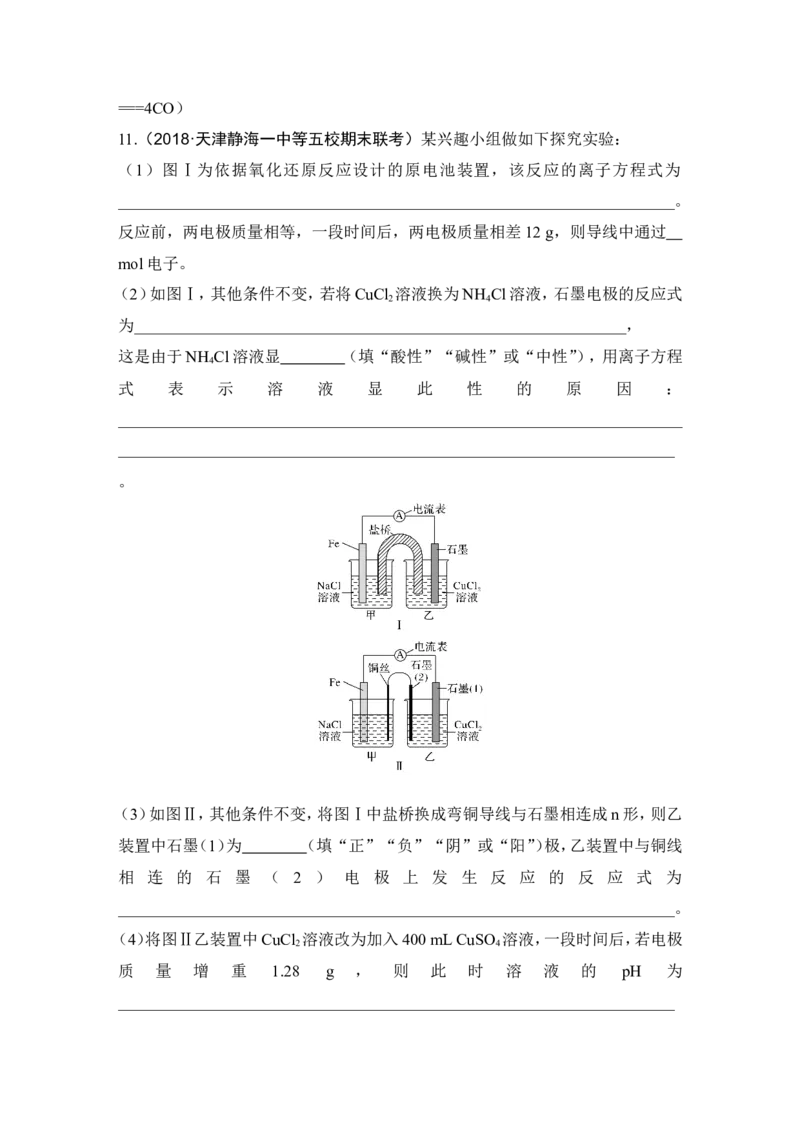
(3)如图Ⅱ,其他条件不变,将图Ⅰ中盐桥换成弯铜导线与石墨相连成n形,则乙
装置中石墨(1)为 (填“正”“负”“阴”或“阳”)极,乙装置中与铜线
相 连 的 石 墨 ( 2 ) 电 极 上 发 生 反 应 的 反 应 式 为
_____________________________________________________________________。
(4)将图Ⅱ乙装置中CuCl 溶液改为加入400 mL CuSO 溶液,一段时间后,若电极
2 4
质 量 增 重 1.28 g , 则 此 时 溶 液 的 pH 为
_____________________________________________________________________(不考虑反应中溶液体积的变化)。
解析 (1)Fe是活泼电极,失电子被氧化生成Fe2+,石墨是惰性电极,溶液中Cu2+
在石墨电极得电子被还原生成Cu,故该原电池的反应为Fe+Cu2+===Fe2++Cu。
工作过程中,Fe作负极,电极反应式为Fe-2e-===Fe2+,铁电极质量减少;石墨作
正极,电极反应式为Cu2++2e-===Cu,石墨电极质量增加;设两电极质量相差12
g时电路中转移电子为x mol,则有x mol××56 g·mol-1+x mol××64 g·mol-1=
12 g,解得x=0.2。
(2)NH Cl溶液中NH发生水解反应:NH+H O NH ·H O+H+,使溶液呈
4 2 3 2
酸性,故石墨电极(即正极)上发生的反应为2H++2e-===H ↑。
2
(3)其他条件不变,若将盐桥换成弯铜导线与石墨相连成n形,则甲装置为原电池,
Fe作负极,Cu作正极;乙装置为电解池,则石墨(1)为阴极,石墨(2)为阳极,溶液
中Cl-在阳极放电生成Cl ,电极反应式为2Cl--2e-===Cl ↑。
2 2
(4)若将乙装置中电解质溶液改为加入400 mL CuSO 溶液,则阴极反应式为Cu2+
4
+2e-===Cu,当电极质量增重1.28 g(即析出0.02 mol Cu)时,电路中转移0.04
mol电子。电解CuSO 溶液的总反应方程式为2CuSO +2H O INCLUDEPICTURE
4 4 2
"F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\反
应通电.TIF" \* MERGEFORMATINET 2H SO +2Cu+O ↑,则转移
2 4 2
0.04 mol电子时生成0.02 mol H SO ,则有c(H+)==0.1 mol·L-1,pH=-lg 0.1=
2 4
1,故此时溶液的pH为1。
答案 (1)Fe+Cu2+===Fe2++Cu 0.2
(2)2H++2e-===H ↑ 酸性 NH+H O NH ·H O+H+
2 2 3 2
(3)阴 2Cl--2e-===Cl ↑ (4)1
2
[B级 拔高选做题]
12.某原电池装置如图所示,电池总反应为2Ag+Cl ===2AgCl。下列说法正确的是
2
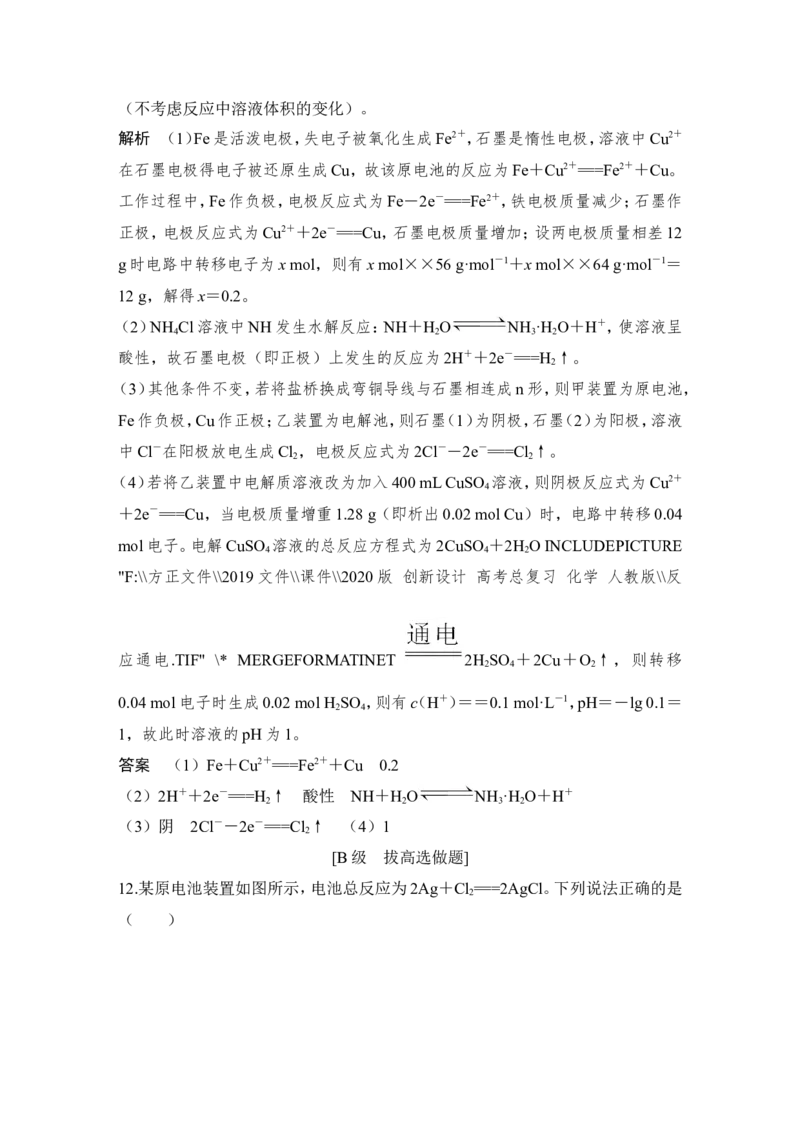
( )A.正极反应为AgCl+e-===Ag+Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
解析 根据电池总反应为2Ag+Cl ===2AgCl可知,Ag失电子作负极,氯气在正
2
极上得电子生成氯离子。正极上氯气得电子生成氯离子,其电极反应为:Cl +2e-
2
===2Cl-,故A错误;放电时,交换膜左侧银为负极失电子形成银离子与溶液中的
氯离子结合成AgCl沉淀,所以左侧溶液中有大量白色沉淀氯化银生成,故B错误
根据电池总反应为2Ag+Cl ===2AgCl可知,用NaCl溶液代替盐酸,电池的总反
2
应不变,故C错误;放电时,当电路中转移0.01 mol e-时,交换膜在左侧会有0.01
mol氢离子通过阳离子交换膜向正极移动,同时会有0.01 mol Ag失去0.01 mol电
子生成银离子,银离子会与氯离子反应生成氯化银沉淀,所以氯离子会减少0.01
mol,则交换膜左侧溶液中共约减少0.02 mol离子,故D正确;故选D。
答案 D
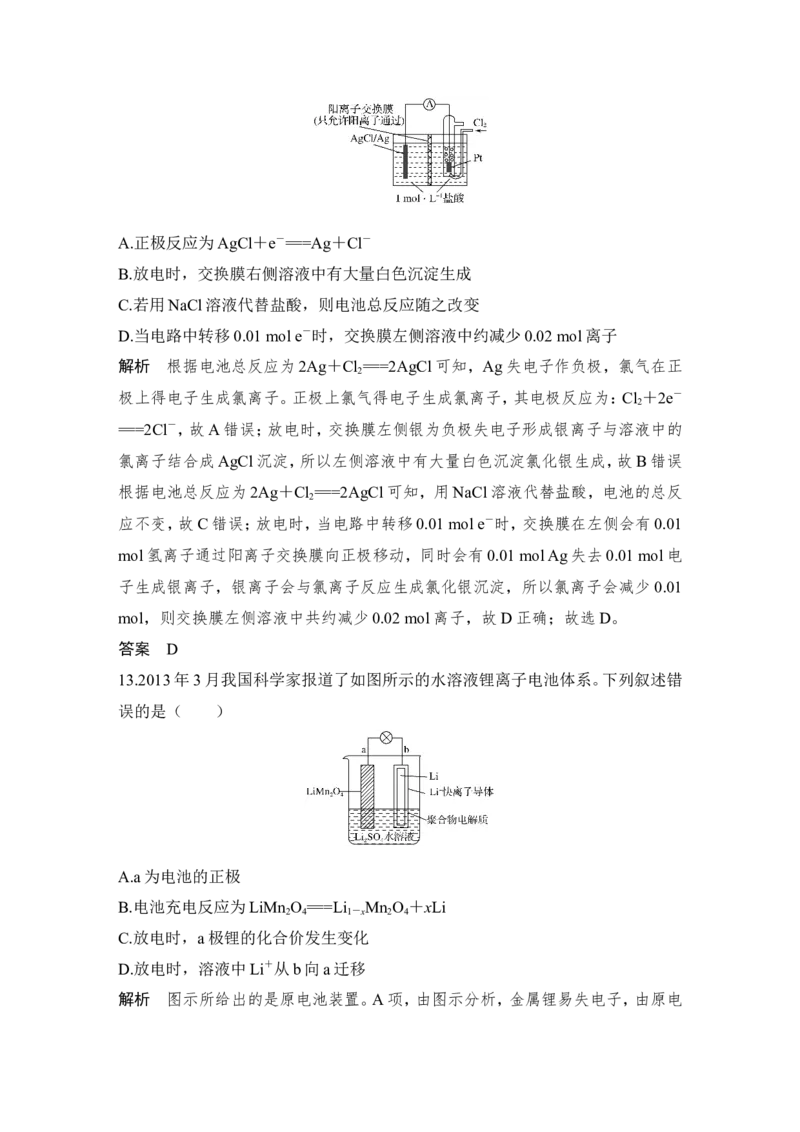
13.2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。下列叙述错
误的是( )
A.a为电池的正极
B.电池充电反应为LiMn O ===Li Mn O +xLi
2 4 1-x 2 4
C.放电时,a极锂的化合价发生变化
D.放电时,溶液中Li+从b向a迁移
解析 图示所给出的是原电池装置。A项,由图示分析,金属锂易失电子,由原电池原理可知,含有锂的一端为原电池的负极,即b为负极,a为正极,正确;B项,电
池充电时为电解池,反应式为原电池反应的逆反应,正确;C项,放电时,a极为原
电池的正极,发生还原反应的是Mn元素,锂元素的化合价没有变化,不正确;D
项,放电时为原电池,锂离子应向正极(a极)迁移,正确。
答案 C
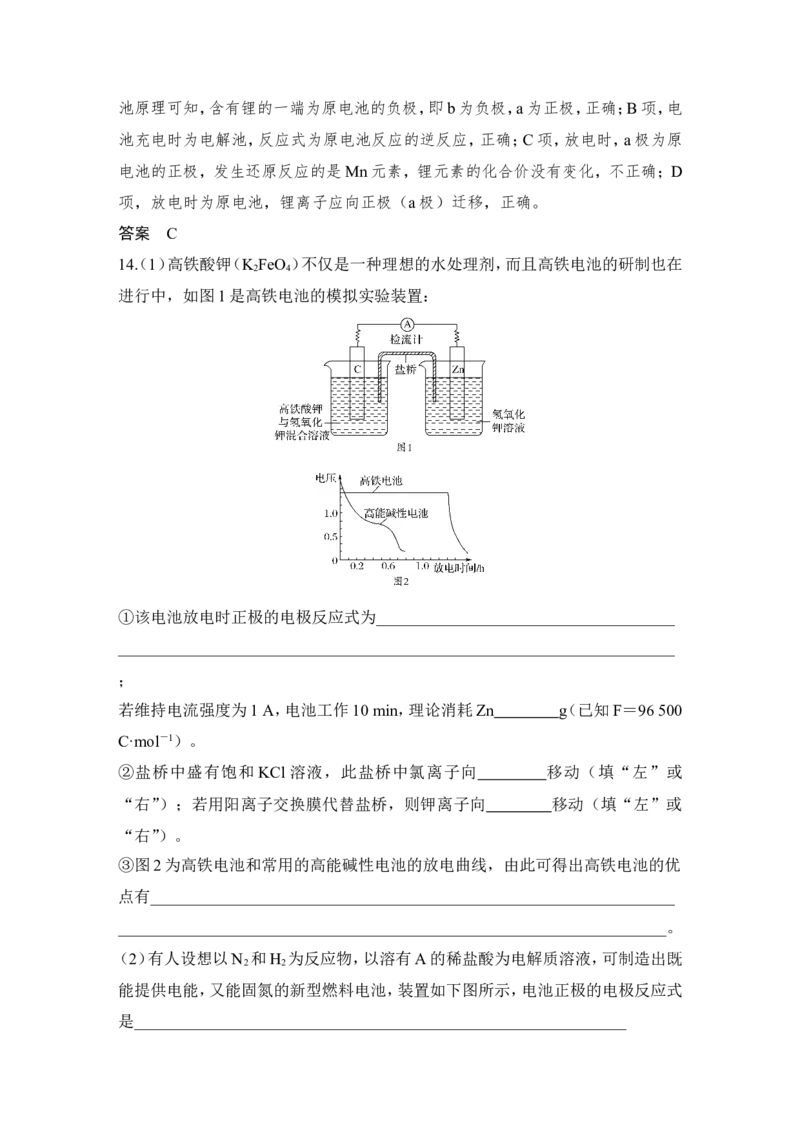
14(. 1)高铁酸钾(K FeO )不仅是一种理想的水处理剂,而且高铁电池的研制也在
2 4
进行中,如图1是高铁电池的模拟实验装置:
①该电池放电时正极的电极反应式为_____________________________________
_____________________________________________________________________
;
若维持电流强度为1 A,电池工作10 min,理论消耗Zn g(已知F=96 500
C·mol-1)。
②盐桥中盛有饱和 KCl 溶液,此盐桥中氯离子向 移动(填“左”或
“右”);若用阳离子交换膜代替盐桥,则钾离子向 移动(填“左”或
“右”)。
③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优
点有_________________________________________________________________
____________________________________________________________________。
(2)有人设想以N 和H 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既
2 2
能提供电能,又能固氮的新型燃料电池,装置如下图所示,电池正极的电极反应式
是_________________________________________________________________________________________________________________________________,
A是 。
(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如下图所示。该电池
中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向
( 填 “ 从 a 到 b” 或 “ 从 b 到 a” ) , 负 极 发 生 的 电 极 反 应 式 为
____________________________________________________________________。
解析 (1)①放电时高铁酸钾为正极,正极发生还原反应,电极反应式为FeO+
4H O+3e-===Fe(OH)↓+5OH-;若维持电流强度为1 A,电池工作十分钟,转
2 3
移电子的物质的量为1×10×60÷96 500=0.006 217 6(mol)。理论消耗Zn的质量
0.006 217 6 mol÷2×65 g·mol-1≈0.2 g(已知F=96 500 C·mol-1)。
②电池工作时,阴离子移向负极,阳离子移向正极,所以盐桥中氯离子向右移动;
若用阳离子交换膜代替盐桥,则钾离子向左移动。
③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优
点有使用时间长、工作电压稳定。
(2)该电池的本质反应是合成氨反应,电池中氢气失去电子,在负极发生氧化反应,
氮气得电子在正极发生还原反应,则正极反应式为N +8H++6e-===2NH,氨气
2
与HCl反应生成氯化铵,则电解质溶液为氯化铵溶液。
(3)工作时电极b作正极,O2-由电极b移向电极a;该装置是原电池,通入一氧化
碳的电极a是负极,负极上一氧化碳失去电子发生氧化反应,电极反应式为CO+
O2--2e-===CO 。
2
答案 (1)①FeO+4H O+3e-===Fe(OH) ↓+5OH- 0.2
2 3
②右 左③使用时间长、工作电压稳定
(2)N +8H++6e-===2NH 氯化铵
2
(3)从b到a CO+O2--2e-===CO
2