文档内容
1.下列有关溶液的酸碱性与pH的说法错误的是( )
A.溶液pH越小,酸性越强,反之,碱性越强
B.pH<7的溶液可能呈碱性
C.当溶液中的c(H+)或c(OH-)较小时,用pH表示其酸碱性更为方便
D.把pH试纸直接插入待测溶液中,测其pH
2.工农业生产和科学实验中常常涉及溶液的酸碱性,生活和健康也与溶液的酸碱性有密切
关系。pH是表示溶液酸碱度的一种方法。下列说法不正确的是( )
A.可以用pH试纸测量溶液的pH,也可以用pH计来测量
B.测量和调控溶液的pH对工农业生产、科学研究都具有重要意义
C.pH试纸可测量任何溶液的pH
D.酸碱指示剂是一些有机弱酸或弱碱,在溶液中存在电离平衡,指示剂的颜色变化在一定
pH范围内发生
3.某温度下,向c(H+)=1.0×10-6 mol·L-1的蒸馏水中加入NaHSO 晶体,保持温度不变,
4
测得溶液的c(H+)=1.0×10-2 mol·L-1。下列对该溶液的叙述不正确的是( )
A.该温度高于25 ℃
B.由水电离出来的H+的浓度为1.0×10-10 mol·L-1
C.加入NaHSO 晶体抑制水的电离
4
D.取该溶液加水稀释100倍,溶液中的c(OH-)减小
4.某温度下,测得0.01 mol·L-1 NaOH溶液的pH=10,则下列说法正确的是( )
A.该溶液温度为25 ℃
B.与等体积的pH=4的盐酸刚好中和
C.该温度下蒸馏水pH=6
D.该溶液中c(H+)=10-12 mol·L-1
5.25 ℃时,在等体积的①pH=0的HSO 溶液、②0.05 mol·L-1的Ba(OH) 溶液、③pH=
2 4 2
10的NaS溶液、④pH=5的NH NO 溶液中,发生电离的水的物质的量之比是( )
2 4 3
A.1∶10∶1010∶109
B.1∶5∶(5×109)∶(5×108)
C.1∶20∶1010∶109
D.1∶10∶104∶109
6.已知液氨的性质与水相似。T ℃时,NH +NH NH+NH,NH的平衡浓度为1×
3 3
10-15 mol·L-1,则下列说法正确的是( )
A.在此温度下液氨的离子积为1×10-17
B.在液氨中放入金属钠,可生成NaNH
2C.恒温下,在液氨中加入NH Cl,可使液氨的离子积减小
4
D.降温,可使液氨电离平衡逆向移动,且c(NH)<c(NH)
7.溶液混合后体积变化忽略不计,则下列叙述正确的是( )
A.95 ℃纯水的pH<7,说明加热可导致水呈酸性
B.室温下,pH=3的醋酸溶液,稀释10倍后pH=4
C.室温下,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
D.0.2 mol·L-1的盐酸与等体积水混合后pH=1
8.已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的一元酸HA与b
w
mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)= mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
9.如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )
A.两条曲线间任意点均有c(H+)·c(OH-)=K
w
B.M区域内(边界除外)任意点均有c(H+)<c(OH-)
C.温度:T<T
1 2
D.XZ线段上任意点均有pH=7
10.25 ℃时,体积为V、pH=a的某一元强酸溶液与体积为V 、pH=b的某一元强碱溶液
a b
均匀混合后,溶液的pH=7,已知b=6a,V<V,下列有关a的说法正确的是( )
a b
A.a可能等于1 B.a一定大于2
C.a一定小于2 D.a一定等于2
11.(2023·成都市石室中学模拟)T ℃时,水的离子积常数K =10-13,该温度下,V mL pH
w 1
=12的Ba(OH) 稀溶液与V mL pH=2的稀硫酸充分反应(混合后的体积变化忽略不计),恢
2 2
复到T ℃,测得混合溶液的pH=3,则V∶V 的值为( )
1 2
A.9∶101 B.99∶101
C.1∶100 D.1∶10
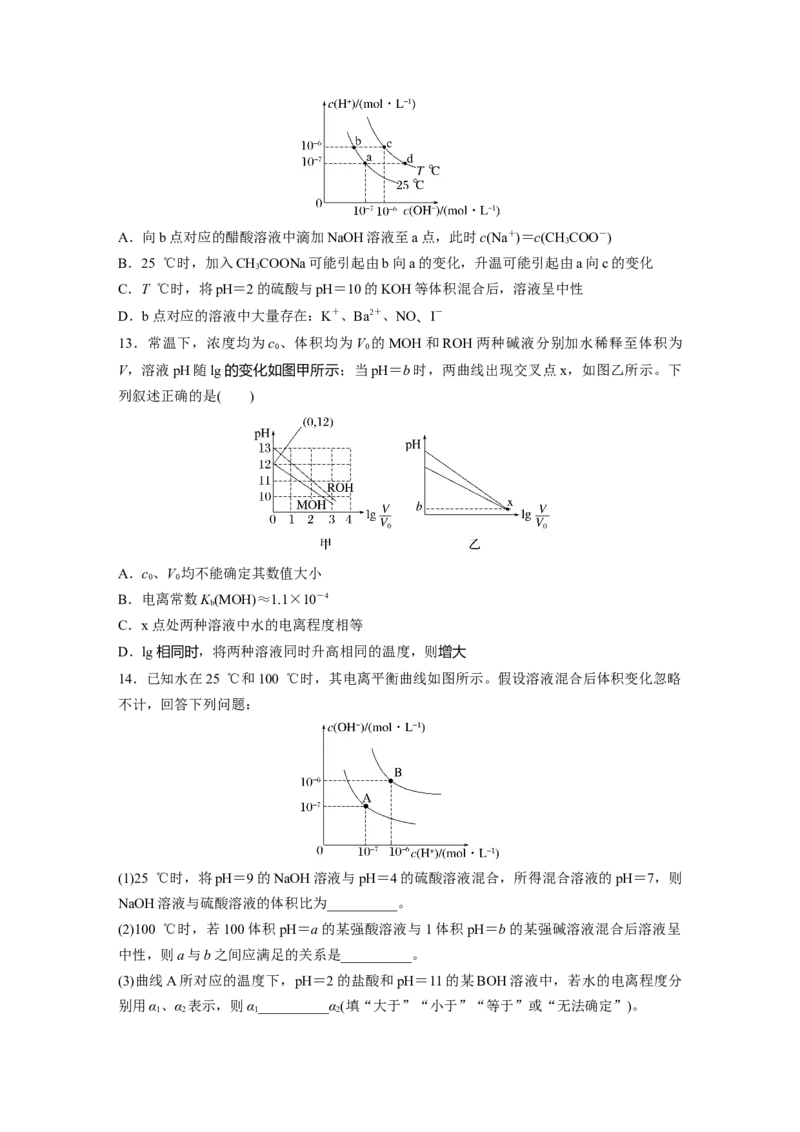
12.在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是( )A.向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CHCOO-)
3
B.25 ℃时,加入CHCOONa可能引起由b向a的变化,升温可能引起由a向c的变化
3
C.T ℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液呈中性
D.b点对应的溶液中大量存在:K+、Ba2+、NO、I-
13.常温下,浓度均为c 、体积均为V 的MOH和ROH两种碱液分别加水稀释至体积为
0 0
V,溶液pH随lg的变化如图甲所示;当pH=b时,两曲线出现交叉点x,如图乙所示。下
列叙述正确的是( )
A.c、V 均不能确定其数值大小
0 0
B.电离常数K (MOH)≈1.1×10-4
b
C.x点处两种溶液中水的电离程度相等
D.lg相同时,将两种溶液同时升高相同的温度,则增大
14.已知水在25 ℃和100 ℃时,其电离平衡曲线如图所示。假设溶液混合后体积变化忽略
不计,回答下列问题:
(1)25 ℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则
NaOH溶液与硫酸溶液的体积比为__________。
(2)100 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈
中性,则a与b之间应满足的关系是__________。
(3)曲线A所对应的温度下,pH=2的盐酸和pH=11的某BOH溶液中,若水的电离程度分
别用α、α 表示,则α__________α(填“大于”“小于”“等于”或“无法确定”)。
1 2 1 2(4)曲线B对应的温度下,将0.02 mol·L-1 Ba(OH) 溶液与等物质的量浓度的NaHSO 溶液等
2 4
体积混合后,混合溶液的pH=________。
15.(1)水在高温高压状态下呈现许多特殊的性质。当温度、压强分别超过临界温度(374.2
℃)、临界压强(22.1 MPa)时的水称为超临界水。
①与常温常压下的水相比,高温高压液态水的离子积会显著增大。解释其原因:
______________________________________________________________________________
______________________________________________________________________________。
②如果水的离子积K 从1.0×10-14增大到1.0×10-10,则相应的电离度是原来的______倍。
w
(2)已知HO 是一种二元弱酸,常温下,K =1.0×10-12、K =1.05×10-25,则HO 的电离
2 2 a1 a2 2 2
方程式为______________________________________________________________________,
则该温度下1 mol·L-1的HO 溶液的pH近似为____________(不考虑HO 的第二步电离和
2 2 2 2
水的电离)。