文档内容
1.氢氰酸(HCN)是一种弱酸,在水溶液中存在电离平衡:HCNH++CN-,常温下电离
常数为K。下列说法正确的是( )
a
A.0.1 mol·L-1 HCN溶液的pH<1
B.增大HCN溶液浓度,其电离程度减小
C.升高HCN溶液温度,平衡逆向移动
D.加入少量NaOH溶液,会使K 增大
a
2.饱和氨水中存在化学平衡和电离平衡:NH +HONH ·H ONH+OH-。下列有关
3 2 3 2
说法正确的是( )
A.常温下饱和氨水的pH<7
B.向氨水中滴加过量硫酸,上述平衡均正向移动,pH增大
C.电离是吸热过程,升高温度,上述平衡均正向移动
D.向氨水中加入少量NaOH固体,上述平衡均逆向移动,有NH 放出
3
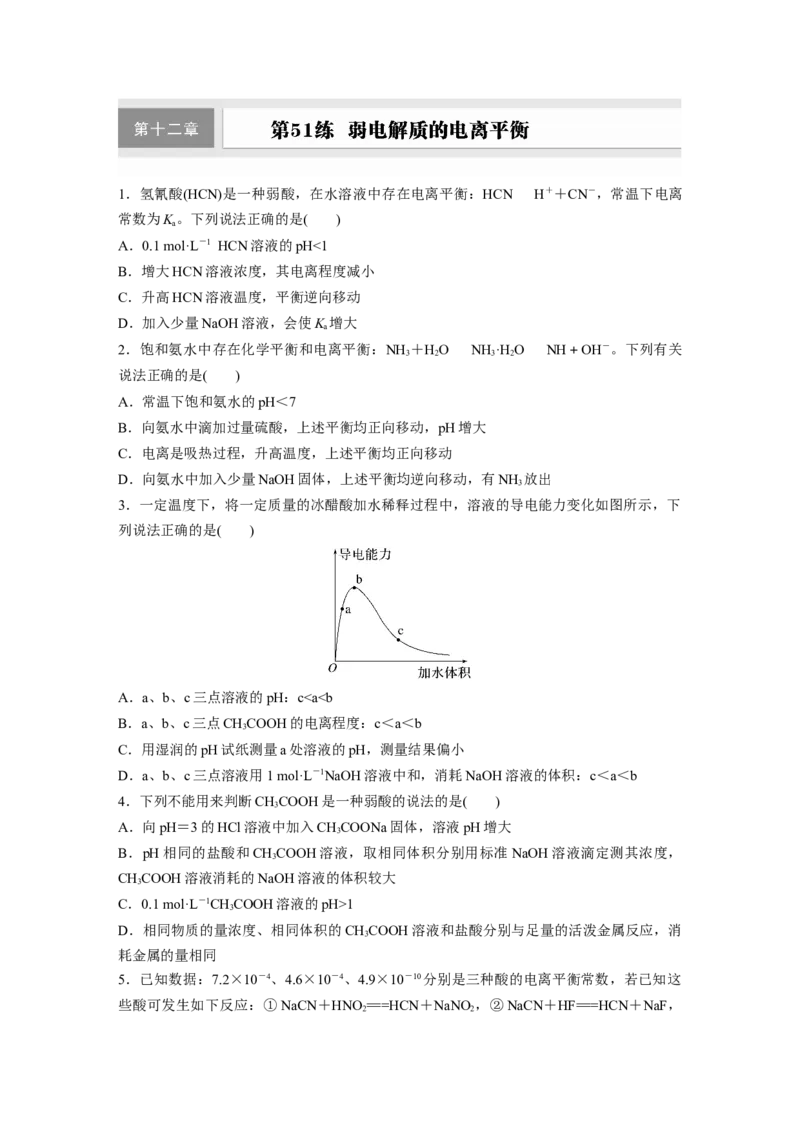
3.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下
列说法正确的是( )
A.a、b、c三点溶液的pH:c1
3
D.相同物质的量浓度、相同体积的CHCOOH溶液和盐酸分别与足量的活泼金属反应,消
3
耗金属的量相同
5.已知数据:7.2×10-4、4.6×10-4、4.9×10-10分别是三种酸的电离平衡常数,若已知这
些酸可发生如下反应:①NaCN+HNO===HCN+NaNO ,②NaCN+HF===HCN+NaF,
2 2③NaNO +HF===HNO+NaF,由此可判断下列叙述中不正确的是( )
2 2
A.HF的电离平衡常数为7.2×10-4
B.HNO 的电离平衡常数为4.9×10-10
2
C.根据①③两个反应即可知三种酸的相对强弱
D.HNO 的电离平衡常数比HCN大,比HF小
2
6.硼酸(H BO)的电离方程式为 HBO +HOB(OH)+H+。已知常温下,K(H BO)=
3 3 3 3 2 a 3 3
5.4×10-10、K(CHCOOH)=1.75×10-5。下列说法错误的是( )
a 3
A.HBO 为一元酸
3 3
B.0.01 mol·L-1 HBO 溶液的pH≈6
3 3
C.常温下,等浓度溶液的pH:CHCOONa>NaB(OH)
3 4
D.NaOH溶液溅到皮肤时,可用大量水冲洗,再涂上硼酸溶液
7.电导率可用于衡量电解质溶液导电能力的强弱。室温下,用0.100 mol·L-1氨水滴定10 mL
浓度均为0.100 mol·L-1的HCl和CHCOOH的混合液,滴定过程中溶液电导率曲线如图所
3
示。下列说法正确的是( )
A.①溶液中c(H+)为0.200 mol·L-1
B.溶液温度高低为①>③>②
C.③点溶液有c(Cl-)>c(CHCOO-)
3
D.③点后因离子数目减少使电导率略减小
8.(2023·南京模拟)常温下,次氯酸电离平衡体系中各成分的组成分数δ[δ(X)=,X为HClO
或ClO-]与pH的关系如图所示。下列有关说法正确的是( )
A.次氯酸的电离方程式为HClO===H++ClO-
B.曲线a、b依次表示δ(ClO-)、δ(HClO)的变化
C.次氯酸电离常数K 的数量级为10-7
a
D.向次氯酸溶液中加NaOH溶液,将减小
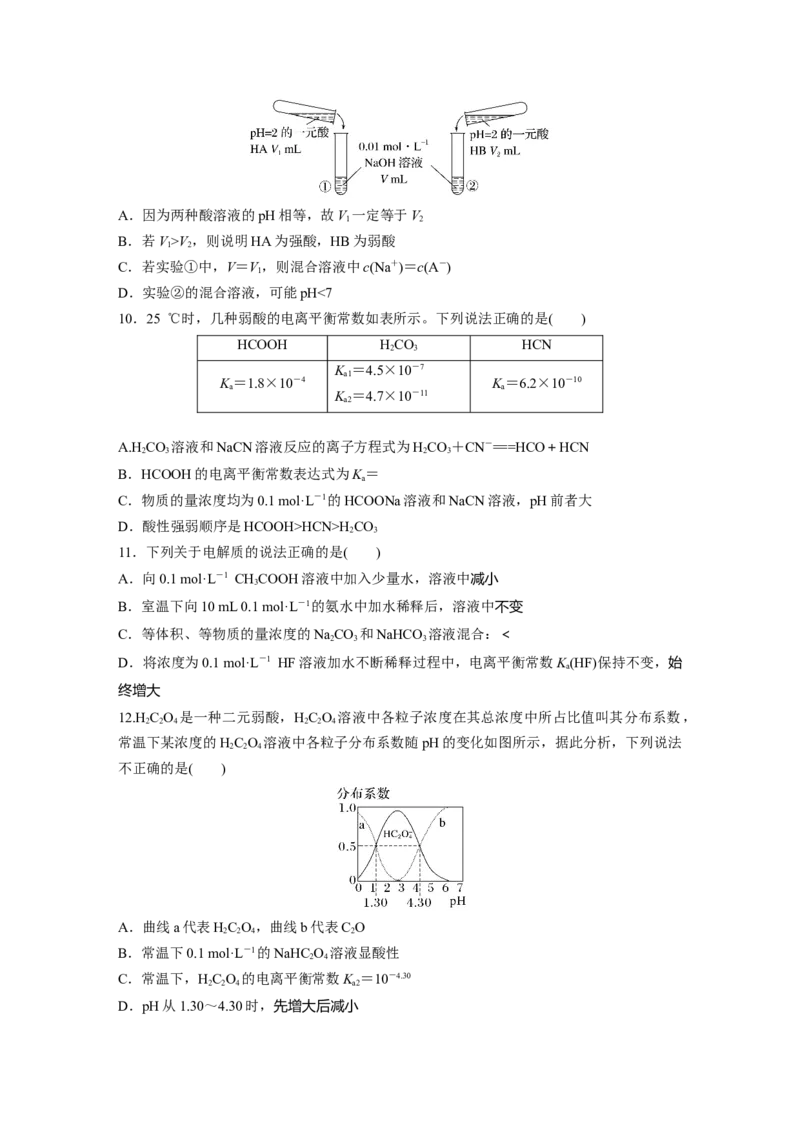
9.下列酸碱溶液恰好完全中和,如图所示,则下列叙述正确的是( )A.因为两种酸溶液的pH相等,故V 一定等于V
1 2
B.若V>V,则说明HA为强酸,HB为弱酸
1 2
C.若实验①中,V=V,则混合溶液中c(Na+)=c(A-)
1
D.实验②的混合溶液,可能pH<7
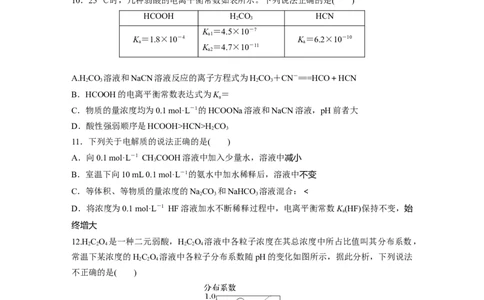
10.25 ℃时,几种弱酸的电离平衡常数如表所示。下列说法正确的是( )
HCOOH HCO HCN
2 3
K =4.5×10-7
a1
K=1.8×10-4 K=6.2×10-10
a a
K =4.7×10-11
a2
A.HCO 溶液和NaCN溶液反应的离子方程式为HCO+CN-===HCO+HCN
2 3 2 3
B.HCOOH的电离平衡常数表达式为K=
a
C.物质的量浓度均为0.1 mol·L-1的HCOONa溶液和NaCN溶液,pH前者大
D.酸性强弱顺序是HCOOH>HCN>H CO
2 3
11.下列关于电解质的说法正确的是( )
A.向0.1 mol·L-1 CHCOOH溶液中加入少量水,溶液中减小
3
B.室温下向10 mL 0.1 mol·L-1的氨水中加水稀释后,溶液中不变
C.等体积、等物质的量浓度的NaCO 和NaHCO 溶液混合:<
2 3 3
D.将浓度为0.1 mol·L-1 HF溶液加水不断稀释过程中,电离平衡常数K(HF)保持不变,始
a
终增大
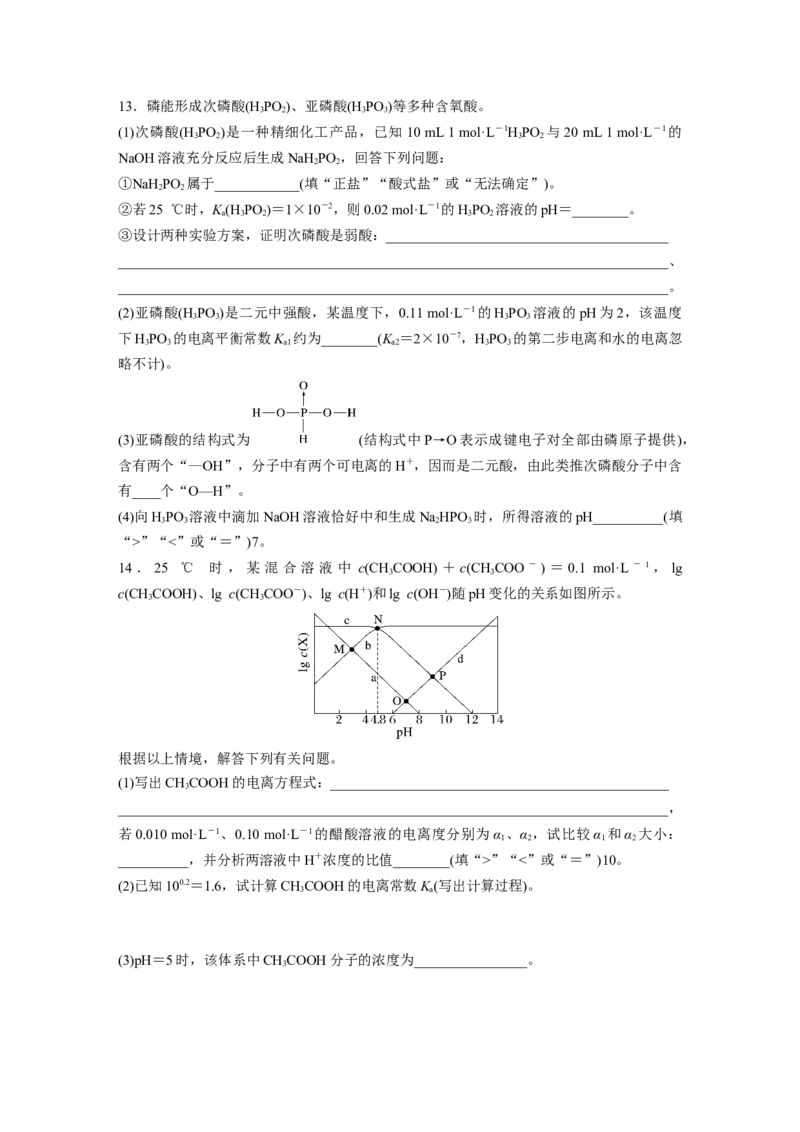
12.H C O 是一种二元弱酸,HC O 溶液中各粒子浓度在其总浓度中所占比值叫其分布系数,
2 2 4 2 2 4
常温下某浓度的HC O 溶液中各粒子分布系数随pH的变化如图所示,据此分析,下列说法
2 2 4
不正确的是( )
A.曲线a代表HC O,曲线b代表C O
2 2 4 2
B.常温下0.1 mol·L-1的NaHC O 溶液显酸性
2 4
C.常温下,HC O 的电离平衡常数K =10-4.30
2 2 4 a2
D.pH从1.30~4.30时,先增大后减小13.磷能形成次磷酸(H PO )、亚磷酸(H PO )等多种含氧酸。
3 2 3 3
(1)次磷酸(H PO )是一种精细化工产品,已知10 mL 1 mol·L-1HPO 与20 mL 1 mol·L-1的
3 2 3 2
NaOH溶液充分反应后生成NaH PO ,回答下列问题:
2 2
①NaH PO 属于____________(填“正盐”“酸式盐”或“无法确定”)。
2 2
②若25 ℃时,K(H PO )=1×10-2,则0.02 mol·L-1的HPO 溶液的pH=________。
a 3 2 3 2
③设计两种实验方案,证明次磷酸是弱酸:________________________________________
______________________________________________________________________________、
______________________________________________________________________________。
(2)亚磷酸(H PO )是二元中强酸,某温度下,0.11 mol·L-1的HPO 溶液的pH为2,该温度
3 3 3 3
下HPO 的电离平衡常数K 约为________(K =2×10-7,HPO 的第二步电离和水的电离忽
3 3 a1 a2 3 3
略不计)。
(3)亚磷酸的结构式为 (结构式中P→O表示成键电子对全部由磷原子提供),
含有两个“—OH”,分子中有两个可电离的H+,因而是二元酸,由此类推次磷酸分子中含
有____个“O—H”。
(4)向HPO 溶液中滴加NaOH溶液恰好中和生成NaHPO 时,所得溶液的pH__________(填
3 3 2 3
“>”“<”或“=”)7。
14 . 25 ℃ 时 , 某 混 合 溶 液 中 c(CHCOOH) + c(CHCOO - ) = 0.1 mol·L - 1 , lg
3 3
c(CHCOOH)、lg c(CHCOO-)、lg c(H+)和lg c(OH-)随pH变化的关系如图所示。
3 3
根据以上情境,解答下列有关问题。
(1)写出CHCOOH的电离方程式:________________________________________________
3
______________________________________________________________________________,
若0.010 mol·L-1、0.10 mol·L-1的醋酸溶液的电离度分别为 α 、α ,试比较α 和α 大小:
1 2 1 2
__________,并分析两溶液中H+浓度的比值________(填“>”“<”或“=”)10。
(2)已知100.2=1.6,试计算CHCOOH的电离常数K(写出计算过程)。
3 a
(3)pH=5时,该体系中CHCOOH分子的浓度为________________。
3