文档内容
优秀领先 飞翔梦
想
2018年江西中考模拟卷(一)
说明:1.本卷共五大题,24小题,全卷满分100分。考试时间为70分钟。
2.本卷可能用到的相对原子质量:H—1 N—14 O—16 Na—23
Al—27 Si—28 S—32 Fe—56 Cu—64 Ba—137
题号 一 二 三 四 五 总分
得分
一、单项选择题(本大题包括10小题,每小题2分,共20分。每小题有四个选项,其中只有一
个选项符合题意)
1.“东方之星”沉船事故救援时,潜水员钢瓶中携带的气体是( )
A.水蒸气 B.氮气 C.二氧化碳 D.氧气
2.通常情况下,下列溶液的溶质为液体的是( )
A.蔗糖溶液 B.酒精溶液 C.食盐溶液 D.澄清石灰水
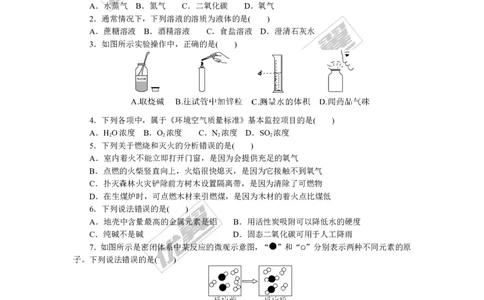
3.如图所示实验操作中,正确的是( )
4.下列各项中,属于《环境空气质量标准》基本监控项目的是( )
A.HO浓度 B.O 浓度 C.N 浓度 D.SO 浓度
2 2 2 2
5.下列关于燃烧和灭火的分析错误的是( )
A.室内着火不能立即打开门窗,是因为会提供充足的氧气
B.点燃的火柴竖直向上,火焰很快熄灭,是因为它接触不到氧气
C.扑灭森林火灾铲除前方树木设置隔离带,是因为清除了可燃物
D.在生煤炉时,可点燃木材来引燃煤,是因为木材的着火点比煤低
6.下列说法错误的是( )
A.地壳中含量最高的金属元素是铝 B.用活性炭吸附可以降低水的硬度
C.纯碱不是碱 D.固态二氧化碳可用于人工降雨
7.如图所示是密闭体系中某反应的微观示意图,“ ”和“ ”分别表示两种不同元素的原
子。下列说法错误的是( )
A.参加反应的“ ”和“ ”个数比为1∶2 B.反应前后原子种类没有改变
C.反应后该密闭体系中没有单质存在 D.该反应是化合反应
8.如图是A、B、C三种物质的溶解度随温度的变化趋势。则下列说法正确的是( )
A.t℃时A、B、C三种物质的溶解度由大到小的顺序是A、C、B
1
www.youyi100.com
第 1 页 共 8 页优秀领先 飞翔梦
想
B.t℃时30g A物质加入50g水中不断搅拌,形成的溶液质量是80g
1
C.A、B两种物质的混合溶液可通过蒸发结晶的方式提纯A
D.将t℃时A、B、C三种物质饱和溶液的温度升高到t℃时,三种溶液的溶质质量分数的大
1 2
小关系是B>C>A
9.归纳总结是化学学习中常用的方法,下列归纳总结正确的是( )
A.复分解反应中可能同时生成两种沉淀
B.同种元素组成的物质一定是单质
C.能使无色酚酞变为红色的物质一定是碱的溶液
D.有单质和化合物生成的反应一定是置换反应
10.某同学利用初中科学物质间相互转化的知识,设计了如图所示的3条铜的“旅行路线”,
每条路线中的每次转化都是通过一步化学反应来实现的,那么,每条路线中可能都有的化学反应
类型是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
二、选择填充题(本大题包括5小题,每小题3分,共15分。先在A、B、C中选择一个正确选项,
然后在D处补充一个符合题意的答案。每小题的选择2分,填充1分)
11.下列物质属于混合物的是( )
A.氯酸钾 B.石油 C.干冰 D.________
12.下列物质中,不能给人体活动提供所需能量的是( )
A.水 B.油脂 C.葡萄糖 D.________
13.南昌汉代海昏侯墓出土的文物中,保存完好的玉器非常罕见。对玉石主要成分
(NaAlSiO)的描述正确的是( )
2 6
A.含有3个氧分子 B.相对分子质量为94
C.钠元素与铝元素的质量比为23∶27 D.钠元素的质量分数为________
14.下列各项实验能达到实验目的的是( )
A.除去CO 中的少量CO——点燃
2
B.验证硫酸铵溶液——加氢氧化钠溶液
C.鉴别氢氧化钠和碳酸钠——滴加酚酞试液
D.检验CaO中混有的CaCO——__________________
3
15.下列图像能正确反应对应变化的是( )
A 向一定质量的盐酸中加入镁粉至过量
B 向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液
www.youyi100.com
第 2 页 共 8 页优秀领先 飞翔梦
想
C 加热一定量的高锰酸钾固体
D 向氢氧化钠溶液中加入X,X可能是________
三、填空与说明题(本大题包括5小题,共30分)
16.(3分)将下列短文中带点的部分,用恰当的化学用语填空:
大约46亿年前地球形成时,温度很高,大气主要含氢元素____________和氮元素,随着地球
的冷却,大气中的水蒸气冷凝并以雨水的形式降落到地表,氯化钠(氯化钠中氯元素的化合价显-
1价____________)、铵盐(铵根离子____________)等盐溶于雨水,雨水充满了地表,海洋由此形成。
17.(6分)化学,在有些人的心目中,就是中毒、腐蚀、污染等,其实这是对化学的一种误解。许
多化学研究成果的推广使用,极大地提高了我们的生活水平,可以概括为吃、穿、住、行四个方面。
请回答下列问题。
(1)吃:化肥与农药的生产和合理使用,提高了粮食产量,解决了吃饭问题。硫酸铵属于
________肥,不能与____________混合施用。
(2)穿:化学纤维的发展,使人们穿上了漂亮的衣服。鉴别合成纤维与天然纤维的方法:
______________________________。
(3)住:钢铁、水泥等建筑材料的使用,建了许多高楼大厦。钢筋混凝土属于________材料。
(4)行:利用化石能源提供动力的现代化交通工具为人们的出行带来了极大的便利,缩短了人
与人之间的距离。化石能源包括煤、石油、________。
18.(6分)乐平灯笼辣椒是景德镇十大特产之一,乐平灯笼辣椒种子曾带入神舟一号进行试验,
有果面光滑,味微辣带甜,脆爽,果肉厚等特色;具有开胃消食、暖胃驱寒、促进血液循环、美容肌
肤、止痛散热等特殊的保健功能;辣椒中维生素C含量居蔬菜之首,维生素B、胡萝卜素以及钙、
铁等矿物质含量亦较丰富。
(1)炒辣椒,闻到刺鼻的气味,说明
________________________________________________________________________;
(2)辣椒中含有人体所需的营养素有
________________________________________________________________________;
(3)辣椒放久了,会腐烂变质,此过程主要发生的是________(选填“物理”或“化学”)变化;
(4)钙是人体所需的常量元素,老年人人体缺钙通常会患____________________;
(5)辣椒中铁元素是人体所需的微量元素,人体缺铁会患贫血,铁元素的部分信息如图,则下
列说法中正确的是________(填字母)。
A.铁原子中的核外电子数为26
B.铁离子中的核外电子数为26
C.铁原子核外电子层数为四
D.铁的相对原子质量约为56g
www.youyi100.com
第 3 页 共 8 页优秀领先 飞翔梦
想
19.(7分)硅是一种重要的半导体材料,应用范围广。三氯硅烷(SiHCl)还原法是当前制备高纯
3
硅的主要方法,生产过程如图所示:
(1)写出上述流程中一种氧化物的化学式:______________;
(2)上述流程中最后一步反应的化学方程式为____________________________,该反应属于
________(填基本反应类型)反应;
(3)如果还原SiHCl 过程中混入O,可能引起的后果是________;
3 2
(4)该流程中可以循环利用的物质的化学式是__________。
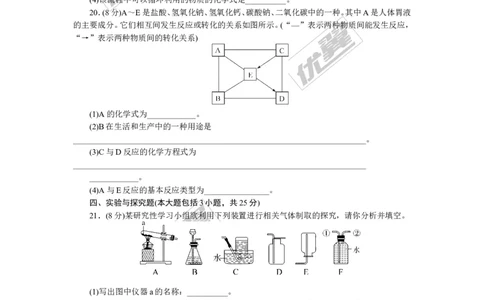
20.(8分)A~E是盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的一种。其中A是人体胃液
的主要成分。它们相互间发生反应或转化的关系如图所示。(“—”表示两种物质间能发生反应,
“→”表示两种物质间的转化关系)
(1)A的化学式为____________。
(2)B在生活和生产中的一种用途是
________________________________________________________________________。
(3)C与D反应的化学方程式为
________________________________________________________________________
____________。
(4)A与E反应的基本反应类型为________________。
四、实验与探究题(本大题包括3小题,共25分)
21.(8分)某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空。
(1)写出图中仪器a的名称:__________。
(2)实验室制取二氧化碳应选择的气体发生装置是________(填序号,下同),气体收集装置是
________。
(3)实验室加热氯酸钾和二氧化锰制取氧气的化学方程式是
________________________________。若用盛满水的F装置收集氧气,应从导管________(选填
“①”或“②”)通入。
(4)甲烷是一种无色、无味、难溶于水、密度小于空气的气体,实验室用加热无水醋酸钠和碱石
灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的组合装置是____________。
22.(9分)在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验
报告补充完整。
www.youyi100.com
第 4 页 共 8 页优秀领先 飞翔梦
想
【实验目的】铁生锈条件的探究。
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下
列实验,实验要保证有足够长的时间来观察现象。
【实验现象】实验①②无明显现象;实验③中铁丝生锈,且试管内空气体积减小。
【实验结论】铁生锈实际上是铁与空气中的________、________(填名称)发生反应的结果。
【实验思考】(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的
________。
(2)该实验创新之处在于:可根据铁丝表面的铁锈和__________________________两种现象
来判断铁丝反应进行的情况。
(3)用完的菜刀要擦干存放,理由是
________________________________________________________________________。
(4)铝比铁活泼,但铝难腐蚀,原因是
________________________________________________________________________
________________________________________________________________________。
23.(8分)在学习碳酸钠的性质的课堂上,老师在碳酸钠溶液中加入一定量的澄清石灰水产生
白色沉淀,再滤出沉淀,引导同学们对滤液中溶质的成分进行探究。同学们通过讨论认为溶质是
NaOH、NaCO、Ca(OH) 中的一种或两种,其可能情况有三种:①NaOH;②NaOH和NaCO;
2 3 2 2 3
③__________________。
小伟同学设计了下列实验方案,请你帮助完成。
小强根据小伟设计的实验方案,在滤液中加入足量稀盐酸,观察到有大量气泡产生,产生该现象
的化学方程式为____________________________________。因此他得出的结论是只有假设
________成立,该假设成立说明老师做的实验是__________________________________[选填
“恰好完全反应”“Ca(OH) 过量”或“NaCO 过量”]。
2 2 3
五、计算题(本大题包括1小题,共10分)
24.(10分)为测定某氮肥中硫酸铵的纯度(即质量分数)是否与下图标签相符合,小林取一定
量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如下表:
www.youyi100.com
第 5 页 共 8 页优秀领先 飞翔梦
想
eq \a\vs4\al(\x( )
[反应的化学方程式为(NH)SO+BaCl ===BaSO↓+2NHCl,其他成分能溶于水但不参
4 2 4 2 4 4
加反应]
(1)反应共生成BaSO 的质量为 g;
4
(2)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中硫酸铵的纯度是否与标签相符;
(请写出计算过程)
(3)反应前后,溶液中硫元素的质量 (选填“不变”“增大”或“减小”)。
www.youyi100.com
第 6 页 共 8 页优秀领先 飞翔梦
想
答案:
1.D 2.B 3.C 4.D 5.B 6.B 7.C
8.D 点拨:t℃时A、B、C三种物质的溶解度由大到小的顺序为B、C、A,A错误;t℃时A
1 1
物质的溶解度为30g,30gA物质加入50g水中不断搅拌只能溶解15g,形成的溶液质量是65g,B
错误;A物质的溶解度受温度影响变化较大,B物质的溶解度受温度影响变化较小,所以要从A、
B两种物质的混合溶液中提纯A可用降温结晶的方法,C错误;t℃时A、B、C三种物质饱和溶液
1
的溶质质量分数由大到小的顺序为B、C、A,当温度升高到t℃时,B变成不饱和溶液,C变成该
2
温度下的饱和溶液,A变成该温度下的不饱和溶液,通过看三种物质的溶解度所在的位置可知三
种溶液的溶质质量分数的大小关系为B>C>A,D正确。故选D。
9.A
10.C 点拨:第一条路线:铁与硫酸铜发生置换反应得到铜;第二条路线:氢气与氧化铜在
加热条件下发生置换反应得到铜;第三条路线:铁与硝酸铜发生置换反应得到铜。
11.B 空气(或NaOH溶液等,合理即可)
12.A 维生素(或无机盐等,合理即可)
13.C 11.4% 点拨:NaAlSiO 是由NaAlSiO 分子构成的,不含氧分子;NaAlSiO 的相对
2 6 2 6 2 6
分子质量为23+27+28×2+16×6=202;钠元素与铝元素的质量比为23∶27;钠元素的质量分
数为×100%=11.4%。
14.B 滴加稀盐酸(或稀硫酸) 点拨:混在CO 中的少量CO不能被点燃;硫酸铵溶液与氢
2
氧化钠溶液反应会生成有刺激性气味的气体;碳酸钠和氢氧化钠溶液都显碱性,用酚酞试液无法
区分;CaCO 与稀盐酸(或稀硫酸)反应有气体生成,CaO则没有。
3
15.C 水(或氯化钠溶液等,合理即可) 点拨:向一定质量的盐酸中加入镁粉,开始时氯化
镁的质量应该为零;消耗的铁的质量要小于生成的铜的质量,故可判断,随着硫酸铜溶液的加入,
金属的质量应该是增加;锰元素在反应前后质量保持不变;氢氧化钠溶液中加入X后,溶液pH减
小至接近7,但并没有等于或小于7,故X可能是水。
16.H NaCl NH
17.(1)氮 碱性物质(其他答案合理均可)
(2)燃烧,闻气味
(3)复合
(4)天然气
18.(1)分子在不断运动
(2)维生素、无机盐
(3)化学
(4)骨质疏松症
(5)AC
19.(1)SiO(其他答案合理均可)
2
(2)SiHCl+H=====Si+3HCl 置换
3 2
(3)爆炸 (4)HCl
20.(1)HCl (2)改良酸性土壤
(3)2NaOH+CO===NaCO+HO
2 2 3 2
(4)复分解反应
21.(1)试管
(2)B D
(3)2KClO=====2KCl+3O↑ ②
3 2
www.youyi100.com
第 7 页 共 8 页优秀领先 飞翔梦
想
(4)AC(或AE、AF)
22.【实验结论】氧气 水蒸气
【实验思考】(1) (2)试管内液面高度上升
(3)除去水,防止生锈
(4)铝易生成致密的氧化物薄膜,阻止铝进一步被氧化
23.NaOH和Ca(OH) (1)白色沉淀 (2)② (3)①
2
NaCO+2HCl===2NaCl+CO↑+HO ②
2 3 2 2
NaCO 过量
2 3
24.(1)23.3
(2)解:设15g氮肥样品中(NH)SO 的质量为x。
4 2 4
(NH)SO+BaCl===BaSO↓+2NHCl
4 2 4 2 4 4
132 233
x 23.3g
=
x==13.2g
氮肥中(NH)SO 的纯度:×100%=88%<96%,故与标签不相符。
4 2 4
答:该氮肥中硫酸铵的纯度与标签不相符。
(3)减小
www.youyi100.com
第 8 页 共 8 页