文档内容
2002年全国初中学生化学素质和实验能力竞赛(第十二届天原杯)复赛试题
试题说明:
⒈本试卷共7页,满分100分。
⒉可能用到的相对原子质量:
H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27
S:32 Cl:35.5 Ca:40 Cu:63.5 Zn:65
⒊考试时间:2小时
一、选择题(本题包括12小题,每小题2分,共24分。每小题有1个或2个选项符合题意。若
正确答案包括两个选项,错1个不得分,漏选1个扣1分。请将答案填在下表相应题号的空格
内。)
⒈“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅、铝质易拉罐、铜导线等
可以归为一类加以回收,它们属于
A.有机物 B.金属或合金 C.氧化物 D.盐
⒉来自海洋深处的可燃冰的主要成分是
A.CH B.H C.CO D.CO
4 2 2
⒊一辆客车夜晚行驶在公路上,发现油箱漏油,车箱里充满
了汽油的气味,这时应该采取的应急措施是
A.洒水降温并溶解汽油蒸气
B.开灯查找漏油部位,及时修理。
C.打开所有车窗,严禁一切烟火,疏散乘客离开车箱。
D.让车内人员坐好,不要随意走动。
⒋现代医学证明,人类牙齿由一层称为碱式磷酸钙的坚硬物质保护着。碱式磷酸钙的化学式
中除钙离子外,还含有一个氢氧根离子和三个磷酸根离子,则其化学式正确的是
A.Ca (PO )(OH) B.Ca (PO )(OH) C.Ca (PO )(OH) D.Ca (PO )(OH)
2 4 3 3 4 3 4 4 3 5 4 3
⒌1999年度诺贝尔化学奖授予了开创“飞秒(10-15)化学”新领域的科学家,使运用激光光谱
技术观测化学反应时分子中原子运动成为可能。你认为该技术不能观察到的是
A.原子中原子核的内部结构 B.化学反应中原子的运动
C.化学反应中生成物分子的形成 D.化学反应中反应物分子的分解
⒍常温下,取下列固体各10g,分别与90g水充分混合,所得溶液中溶质质量分数最小的是
A.Na O B.CaO C.SO D.CuSO ·5H O
2 3 4 2
⒎向一定量的饱和NaOH溶液中加入少量Na2O固体,恢复到原来温度时,下列说法中正确
的是
A.溶液中Na+总数不变 B.单位体积内的OH-数目不变
C.溶质的质量分数不变 D.溶液的质量不变
⒏配制一定溶质质量分数的NaOH溶液时,造成所配制溶液中的溶质质量分数偏高的原因
可能是
A. 所用的NaOH 已潮解。
B.用带游码的托盘天平称量NaOH固体质量时,误将砝码放在左盘,被称量物放在右盘。
C.托盘天平的左右盘上各放一张纸,调整天平至平衡后,将NaOH固体放在低上称量。
D.用量筒最取水时,俯视水面刻度线来读取体积读数。
⒐天然气、液化石油气燃烧的化学方程式分别为:CH+2O =CO +2H O;C H+5O =3CO +4H O。
4 2 2 2 3 8 2 2 2
现有一套以天然气为燃料的灶具,要改为以液化石油气为燃料的灶具,应采取的措施是
A.燃料气和空气的进入量都减少 B.燃料气和空气的进入量都增大
C.减少燃料气进入量或增大空气进入量 D.增大燃料气进入量或减少空气进入量
⒑将Mg、Al、Zn分别放入相同溶质质量分数的盐酸中,反应完成后,放出的氢气质量相同,
其可能的原因是
A.放入的三种金属质量相同,盐酸足量。
B.放入的Mg、Al、Zn的质量比为12:9:32.5,盐酸足量。
C.盐酸的质量相同,放入足量的三种金属
D.放入的盐酸质量比为3:2:1,反应后无盐酸剩余。
⒒由NaHS、MgSO 、NaHSO 组成的混合物中,已知S元素的质量分数w(S)=a%,则O元素的
4 3
质量分数w(O)为
A.1.75a% B.1-1.75a% C.1.25a% D.无法计算
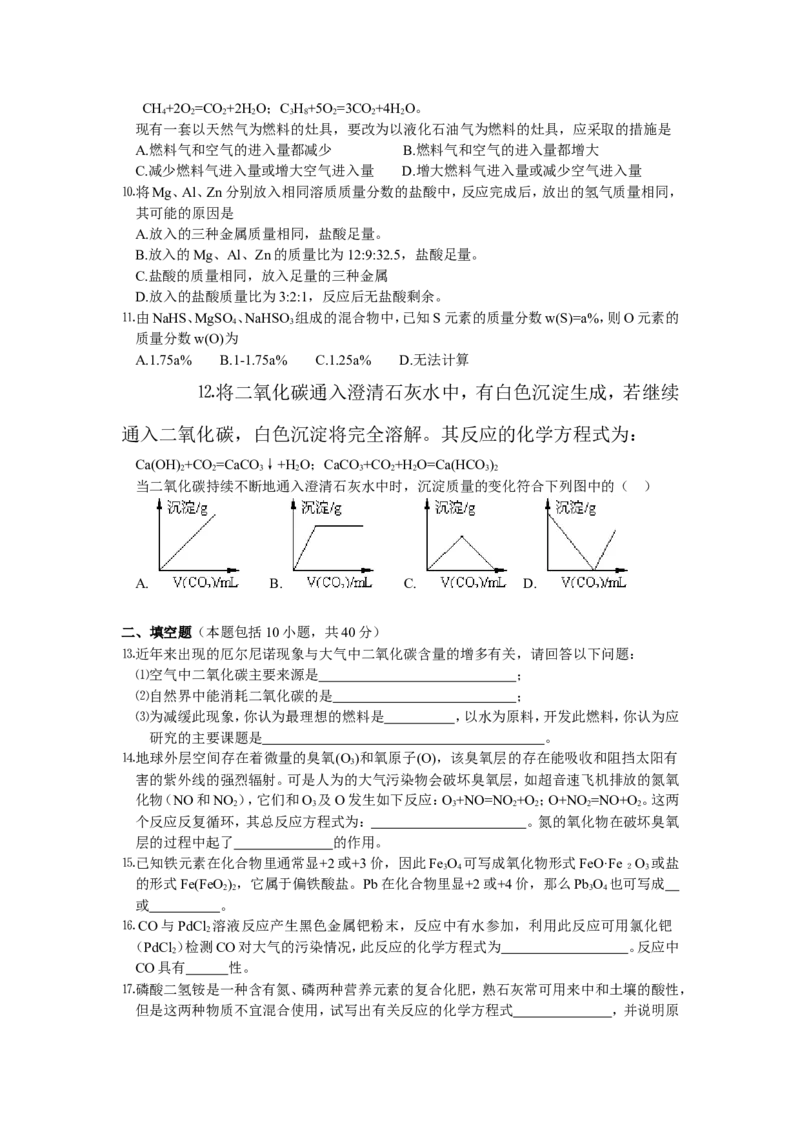
⒓将二氧化碳通入澄清石灰水中,有白色沉淀生成,若继续
通入二氧化碳,白色沉淀将完全溶解。其反应的化学方程式为:
Ca(OH) +CO =CaCO ↓+H O;CaCO +CO +H O=Ca(HCO )
2 2 3 2 3 2 2 3 2
当二氧化碳持续不断地通入澄清石灰水中时,沉淀质量的变化符合下列图中的( )
A. B. C. D.
二、填空题(本题包括10小题,共40分)
⒔近年来出现的厄尔尼诺现象与大气中二氧化碳含量的增多有关,请回答以下问题:
⑴空气中二氧化碳主要来源是 ;
⑵自然界中能消耗二氧化碳的是 ;
⑶为减缓此现象,你认为最理想的燃料是 ,以水为原料,开发此燃料,你认为应
研究的主要课题是 。
⒕地球外层空间存在着微量的臭氧(O )和氧原子(O),该臭氧层的存在能吸收和阻挡太阳有
3
害的紫外线的强烈辐射。可是人为的大气污染物会破坏臭氧层,如超音速飞机排放的氮氧
化物(NO和NO ),它们和O 及O发生如下反应:O+NO=NO +O ;O+NO =NO+O。这两
2 3 3 2 2 2 2
个反应反复循环,其总反应方程式为: 。氮的氧化物在破坏臭氧
层的过程中起了 的作用。
⒖已知铁元素在化合物里通常显+2或+3价,因此Fe O 可写成氧化物形式FeO·Fe O 或盐
3 4 2 3
的形式Fe(FeO ),它属于偏铁酸盐。Pb在化合物里显+2或+4价,那么Pb O 也可写成
2 2 3 4
或 。
⒗CO与PdCl 溶液反应产生黑色金属钯粉末,反应中有水参加,利用此反应可用氯化钯
2
(PdCl )检测CO对大气的污染情况,此反应的化学方程式为 。反应中
2
CO具有 性。
⒘磷酸二氢铵是一种含有氮、磷两种营养元素的复合化肥,熟石灰常可用来中和土壤的酸性,
但是这两种物质不宜混合使用,试写出有关反应的化学方程式 ,并说明原因 。
⒙将雕刻成球型的冰糖(其化学成分为蔗糖)置于蔗糖的饱和溶液中,保持温度和溶剂质量
都不变,几天后,小球的质量和形状有无变化? 。
⒚已知在相同温度下,气体分子的运动速度与分子的相对分子质量有关,
分子的相对分子质量越大,则其运动速度越小。图中容器 A是一种特
制的有底的素烧瓷筒,它的壁可以通过氢气分子。实验开始时,A中和
烧杯中都充满空气。当向烧杯中持续通入氢气时,导管B处发生的现
象是 ,产生这种现象的原因是 。
⒛2001年11月,美军为打击躲藏在阿富汗山洞中的恐怖分子,使用了
一种名为BLU-82的高效能燃料空气炸弹。这种炸弹爆炸时,除产生高
温外,还可使山洞内的氧气耗尽,使其中所有生物窒息死亡而山洞不致完全崩塌,以便后续
军队进入山洞鉴别死者身份。燃料空气弹的主装药之一是环氧乙烷( ),其化
学式可写作 。爆炸时,环氧乙烷先成雾状分散在空气中,然后燃爆,反应的生成
物为: 、 、 。
21.下表是某地市场销售的一种“加碘食盐”包装上的部分文字说明:
配 料 氯化钠、碘酸钾
含 碘 量 (29mg~40mg)/kg
保 质 期 18个月
食用方法 勿长时间炖炒
贮藏指南 避热、避光、密封、防潮
⑴已知碘在碘酸钾中的化合价为+5,碘酸钾的化学式为 。
⑵由食用方法和贮藏指南可推测碘酸钾的化学性质之一是 。
⑶用单质碘与氯酸钾发生置换反应可制得碘酸钾,该反应的化学方程式为 。
22.下表是我国部分城市空气质量周报,阅读并回答下列问题:
污染指 首要污 空气质 污染指 首要污 空气质
城市 城市
数 染物 量级别 数 染物 量级别
北京 92 TSP Ⅱ 济南 76 TSP Ⅱ
天津 82 TSP Ⅱ 武汉 83 NOx Ⅱ
哈尔滨 96 TSP Ⅱ 重庆 98 SOx Ⅱ
上海 74 NOx Ⅱ 贵阳 69 TSP Ⅱ
注:TSP—空气中的飘尘;NOx—氮的氧化物;SOx—硫的氧化物。
⑴最容易出现酸雨的城市是 。为减少城市酸雨的产生,可采取的措施是 。
①少用煤作燃料;②采用燃料脱硫技术;③向已酸化的土壤中加石灰;④开发新能源。
⑵汽车尾气(含有CO、SO 、NO等)是城市空气的污染物,治理的方法之一是在汽车的排气
2
管上装一个催化转换器,其特点是使CO与NO反应,生成可参与大气生态环境循环的无
毒气体,写出CO与NO反应的化学方程式 。控制城
市汽车尾气对空气造成污染的方法是 ①开发氢能源;②使用电动车;③
植树造林;④戴呼吸面具。
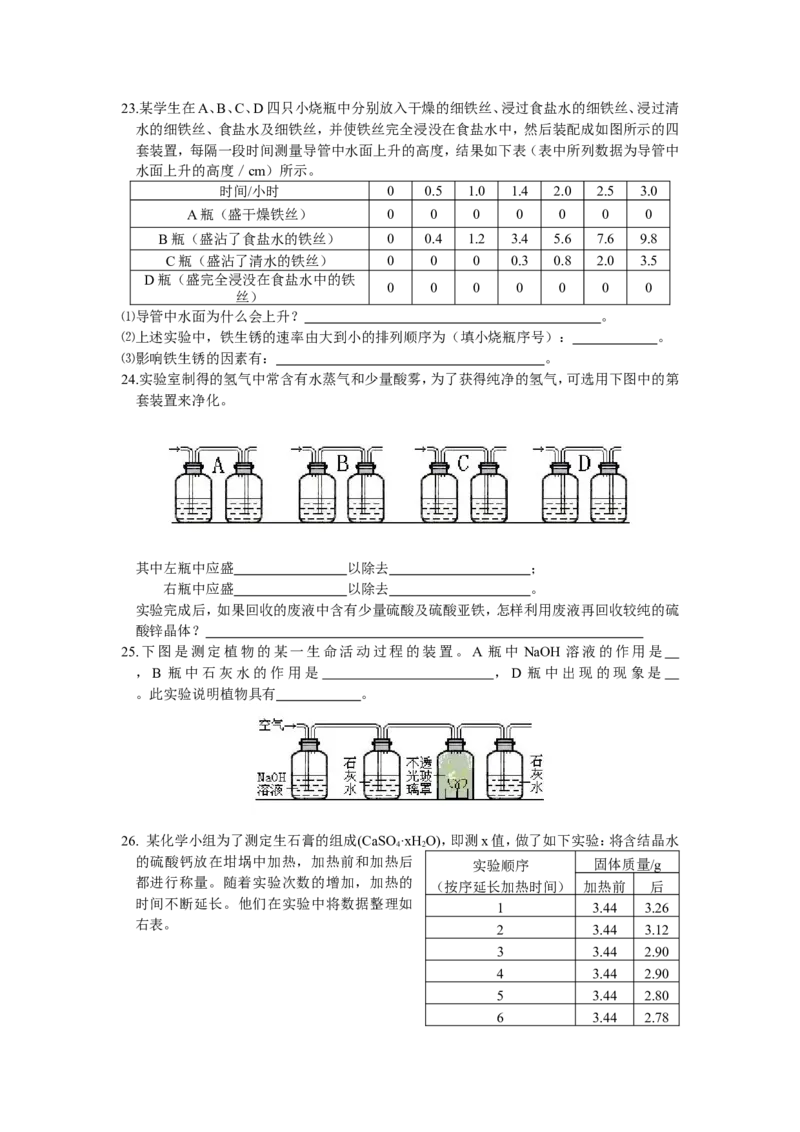
三、实验题(本题包括4小题,共24分)23.某学生在A、B、C、D四只小烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清
水的细铁丝、食盐水及细铁丝,并使铁丝完全浸没在食盐水中,然后装配成如图所示的四
套装置,每隔一段时间测量导管中水面上升的高度,结果如下表(表中所列数据为导管中
水面上升的高度/cm)所示。
时间/小时 0 0.5 1.0 1.4 2.0 2.5 3.0
A瓶(盛干燥铁丝) 0 0 0 0 0 0 0
B瓶(盛沾了食盐水的铁丝) 0 0.4 1.2 3.4 5.6 7.6 9.8
C瓶(盛沾了清水的铁丝) 0 0 0 0.3 0.8 2.0 3.5
D瓶(盛完全浸没在食盐水中的铁
0 0 0 0 0 0 0
丝)
⑴导管中水面为什么会上升? 。
⑵上述实验中,铁生锈的速率由大到小的排列顺序为(填小烧瓶序号): 。
⑶影响铁生锈的因素有: 。
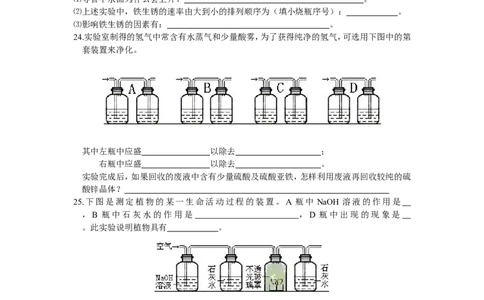
24.实验室制得的氢气中常含有水蒸气和少量酸雾,为了获得纯净的氢气,可选用下图中的第
套装置来净化。
其中左瓶中应盛 以除去 ;
右瓶中应盛 以除去 。
实验完成后,如果回收的废液中含有少量硫酸及硫酸亚铁,怎样利用废液再回收较纯的硫
酸锌晶体?
25.下图是测定植物的某一生命活动过程的装置。A 瓶中 NaOH 溶液的作用是
,B 瓶中石灰水的作用是 ,D 瓶中出现的现象是
。此实验说明植物具有 。
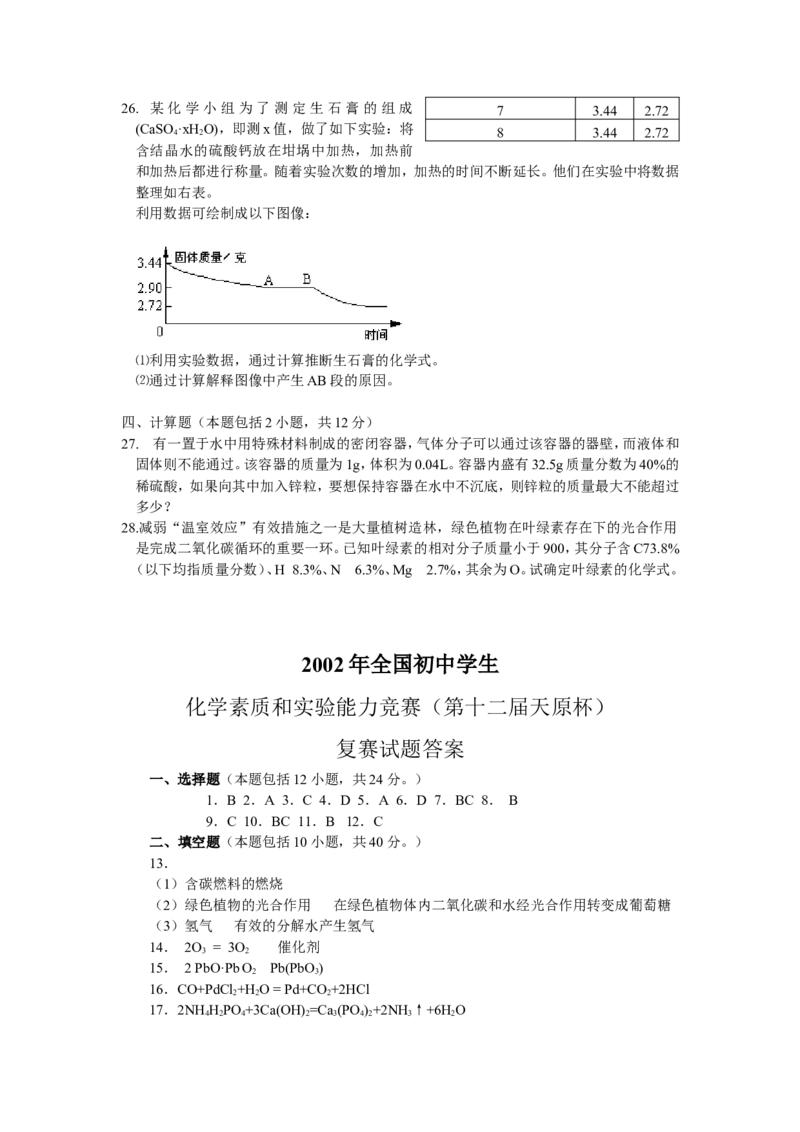
26. 某化学小组为了测定生石膏的组成(CaSO·xH O),即测x值,做了如下实验:将含结晶水
4 2
的硫酸钙放在坩埚中加热,加热前和加热后 实验顺序 固体质量/g
都进行称量。随着实验次数的增加,加热的 (按序延长加热时间) 加热前 后
时间不断延长。他们在实验中将数据整理如
1 3.44 3.26
右表。
2 3.44 3.12
3 3.44 2.90
4 3.44 2.90
5 3.44 2.80
6 3.44 2.7826. 某化学小组为了测定生石膏的组成 7 3.44 2.72
(CaSO 4 ·xH 2 O),即测x值,做了如下实验:将 8 3.44 2.72
含结晶水的硫酸钙放在坩埚中加热,加热前
和加热后都进行称量。随着实验次数的增加,加热的时间不断延长。他们在实验中将数据
整理如右表。
利用数据可绘制成以下图像:
⑴利用实验数据,通过计算推断生石膏的化学式。
⑵通过计算解释图像中产生AB段的原因。
四、计算题(本题包括2小题,共12分)
27. 有一置于水中用特殊材料制成的密闭容器,气体分子可以通过该容器的器壁,而液体和
固体则不能通过。该容器的质量为1g,体积为0.04L。容器内盛有32.5g质量分数为40%的
稀硫酸,如果向其中加入锌粒,要想保持容器在水中不沉底,则锌粒的质量最大不能超过
多少?
28.减弱“温室效应”有效措施之一是大量植树造林,绿色植物在叶绿素存在下的光合作用
是完成二氧化碳循环的重要一环。已知叶绿素的相对分子质量小于900,其分子含C73.8%
(以下均指质量分数)、H 8.3%、N 6.3%、Mg 2.7%,其余为O。试确定叶绿素的化学式。
2002 年全国初中学生
化学素质和实验能力竞赛(第十二届天原杯)
复赛试题答案
一、选择题(本题包括12小题,共24分。)
1.B 2.A 3.C 4.D 5.A 6.D 7.BC 8. B
9.C 10.BC 11.B 12.C
二、填空题(本题包括10小题,共40分。)
13.
(1)含碳燃料的燃烧
(2)绿色植物的光合作用 在绿色植物体内二氧化碳和水经光合作用转变成葡萄糖
(3)氢气 有效的分解水产生氢气
14. 2O = 3O 催化剂
3 2
15. 2 PbO·PbO Pb(PbO )
2 3
16.CO+PdCl +HO = Pd+CO +2HCl
2 2 2
17.2NH HPO +3Ca(OH) =Ca (PO )+2NH↑+6HO
4 2 4 2 3 4 2 3 2磷酸二氢铵是酸式盐显酸性,而熟石灰是碱显碱性,它们会发生反应生成难溶性的
Ca (PO ) 和易挥发性的NH 而使肥效降低。
3 4 2 3
18.小球的质量不变,形状有改变
19.
20.C HO CO、CO、HO
2 4 2 2
21.(1)KIO (2)易分解 (3)I+KClO= Cl+KIO
3 2 3 2 3
22.(1)重庆 ②④ (2)2CO+NO = N+ CO ②③
2 2
三、实验题(本题包括4小题,共24分。)
23.
(1)铁丝在生绣时会消耗烧瓶内的氧气
(2)B>C>A=D
(3)空气、水、电解质
24.C NaOH溶液 CO 浓HSO HO
2 2 4 2
向回收的废液中加入过量的锌,过滤,蒸发滤液结晶得到较纯的硫酸锌晶体
25.吸收空气中的CO ,检验空气中的CO 是否被吸收完全,
2 2
澄清溶液变浊。呼吸作用。
26.(1)解:石膏加热分解减少的质量就是水的质量,由实验数据知3.44g CaSO •xHO
4 2
完全分解得到无水CaSO2.72g,
4
CaSO•xHO==CaSO + xHO
4 2 4 2
136 18x
2.72 0.72
即136:2.72 =18x:0.72 解得x=2 所以石膏的化学式为CaSO•2HO。
4 2
(2)由实验数据知在A—B段时石膏的质量为2.90g,其中CaSO2.72g,HO0.18g。此时
4 2
其化学式可表示为2CaSO•HO。
4 2
四、计算题(本题包括2小题,共12分。)
27.解:设最多加入锌粒的质量为mg。要想保持容器在水中不沉底,密闭容器和锌粒的
质量应不大于密闭容器所受的浮力。
即ρ gV≥(1+32.5+m-2m/65)g m≤6.5×65/63 =6.7g
水
答:(略)。
28.解:由题意知叶绿素中各元素原子的个数比:
碳﹕氢﹕氮﹕镁﹕氧= ﹕ ﹕ ﹕ ﹕
=6.15﹕8.3﹕0.45﹕0.1125﹕0.55625= 55﹕73﹕4﹕1﹕5
因为叶绿素的相对分子质量小于900。所以叶绿素的分子式为C H ONMg。
55 73 5 4