文档内容
第 17 讲 物质的量浓度
知识导航
知识精讲
一、物质的量浓度的基本概念
1. 定义:单位体积溶液里所含溶质B的物质的量,叫做B的物质的量浓度
2. 符号:_______________;
3. 单位:_______________;
4. 表达式:_____________。
二、公式的简单计算
n n
c = B → n = c ×V → V = B
B V B B c
B
c n V
B
1 mol/L 0.5 mol
3 mol/L 0.2 L
1 mol 500 mL
三、物质的量浓度与溶质的质量分数
物理量 物质的量浓度 溶质的质量分数定义 表示单位体积溶液里所含溶质B的物质的量 溶液里溶质质量与溶液质量的比值
n
表达式 c = B ω(B)= ×100%
B
V
单位 mol·L-1 1
1000ρw
转化关系 c = mol·L-1
B M
四、溶液的稀释公式
溶液稀释时溶质的物质的量不变,即cV = c V 。
1 1 2 2
(c、c 为稀释前后溶液的物质的量浓度,V、V 为稀释前后溶液的体积)
1 2 1 2
举个例子
将5 mol·L-1 的盐酸10 mL稀释到200 mL,其物质的量浓度为多少?
5mol/L ×10mL= c ×200mL
2
c = 0.25 mol·L-1
2
对点训练
题型一:物质的量浓度的概念与基础计算
【例1】(2021·沭阳县修远中学高一月考)下列溶液中溶质的物质的量浓度为1 mol·L—1的是
A.将40 g NaOH溶解于1 L水中配成NaOH溶液
B.常温常压下,将22.4 L HCl气体溶于水配成1 L的盐酸
C.将1 L 0.5 mol·L-1的盐酸加热浓缩为0.5 L
D.从1 000 mL 1 mol·L-1的NaCl溶液中取出100 mL的溶液
【变2-1】(2021·浙江高一月考)下列溶液中的c(Cl-)与550mL 1mol·L-1FeCl ,溶液中的c(Cl-)相等的是
3
A.150mL 1mol·L-1NaCl溶液 B .50mL 1mol·L-1NH Cl溶液
4
C.150mL 3mol·L-1KCl溶液 D.100mL 1mol·L-1BaCl 溶液
2
题型二:溶液呈电中性的计算
【例3】(2021·普宁市大长陇中学高三月考)已知某溶液中c(Na+)=0.2mol/L,c(Mg2+)=0.25 mol/L,c(Cl-)=0.4mol/L,如果溶液中还有SO ,那么c(SO )应为
A.0.1 mol/L B.0.15molL C.0.3 mol/L D.0.5mol/L
题型三:溶液的稀释/混合计算
【变4-1】(2021·邓州市第一高级中学校高一月考)将5 的 溶液a mL稀释至b mL,稀
释后溶液中 的物质的量浓度为
A.5a/b B.b/5a C.10a/b D.a/b
题型四:物质的量浓度与质量分数的换算
【例5】(2021·黑龙江齐齐哈尔·高二期末)实验室需要 的硫酸溶液,现用市售98%浓硫酸
(密度为 )配制,用量筒取用的浓硫酸体积最适宜的是
A. B. C. D.
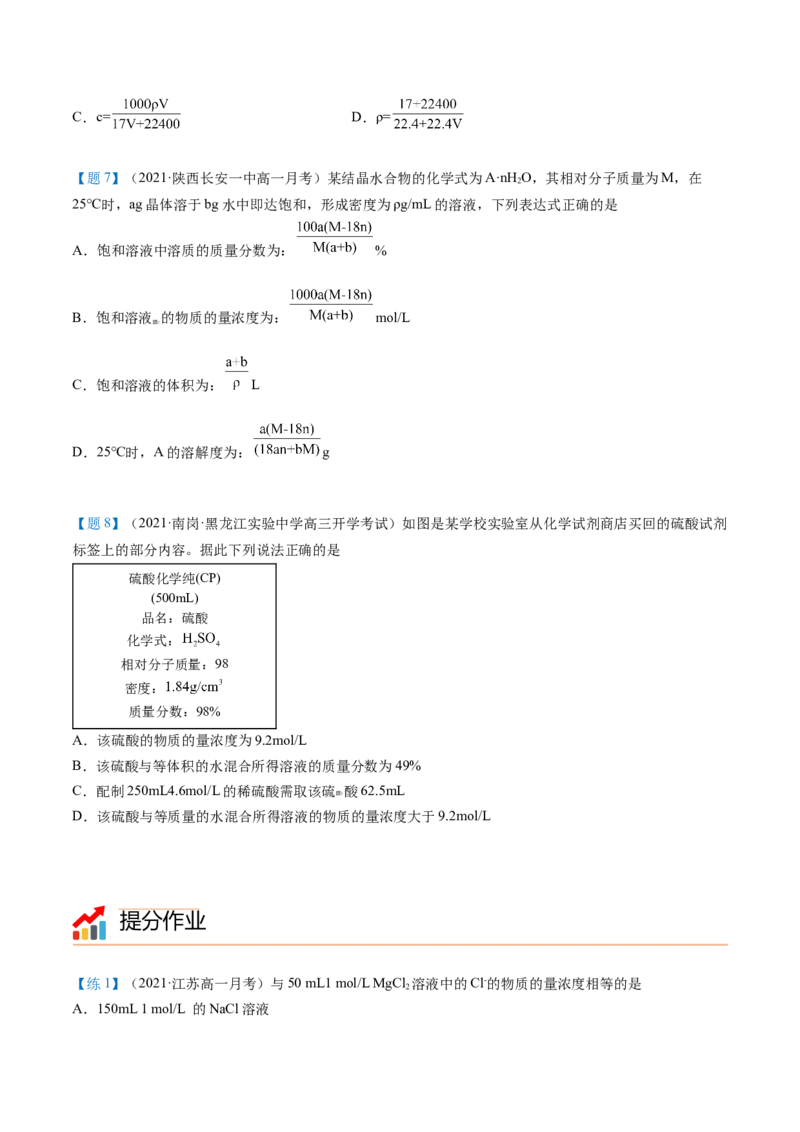
【例7】(2020·浙江绍兴·高一月考)NaCO 和NaOH的混合液100mL, 先向其中滴加Ba(OH) 溶液至不
2 3 2
产生沉淀为止,再向其中滴加稀盐酸至沉淀消失,产生的沉淀的质量与消耗盐酸的体积如图所示:
(1)原混合液中NaCO 的物质的量浓度为______。
2 3
(2)原混合液中NaCO 与NaOH的物质的量比为______。
2 3提分特训
【题1】(2021·全国高一课时练习)下列溶液中的 与200mL 1 mol·L-1硝酸钡溶液中的相同的是
A.200mL 1 mol·L-1的硝酸钠溶液 B.100mL 1.5 mol·L-1的硝酸镁溶液
C.200mL 0.5 mol·L-1的硝酸铝溶液 D.100mL 2 mol·L-1的硝酸钾溶液
【题2】(2021·宁夏沙坡头·中卫一中高一月考)下列叙述正确的是
A.1L水中溶解了40gNaOH后,所得溶液浓度为1mol·L-1
B.从1L2mol·L-1的NaCl溶液中取出0.5L,该溶液的浓度为1mol·L-1
C.配制1L0.1mol·L-1的CuSO 溶液,需用16g胆矾
4
D.将2.24L(标准状况)HCl气体溶于水制成100mL溶液,其物质的量浓度为1mol·L-1
【题3】(2021·临朐县实验中学高一月考)下列说法中正确的是
A.将322gNaSO ·10H O溶于1L水中,所得溶液的物质的量浓度为1mol·L-1
2 4 2
B.将1L2mol·L-1硫酸溶液加水稀释到2L,所得溶液的物质的量浓度为1mol·L-1
C.将1L18.4mol·L-1硫酸溶液加入到1L水中, 所得溶液物质的量浓度为9.2mol·L-1
D.将336mL氯化氢溶于水,配成300mL溶液,所得溶液物质的量浓度为0.05mol·L-1
【题4】(2020·浙江高一期中)已知稀溶液有依数性,即单位体积的稀溶液中,非挥发性溶质的分子或离
子数越多,该溶液的沸点越高。则下列溶液沸点最高的是
A.0.2mol·L-1NaCl溶液 B.0.2mol·L-1NH ·H O溶液
3 2
C.0.1mol·L-1BaCl 溶液 D.0.1mol·L-1蔗糖溶液
2
【题5】(2020·南昌市新建区第二中学高二期末)下列关于物质的量浓度表述正确的是
A.0.3 mol·L-1的NaSO 溶液中含有Na+和SO 的总物质的量为0.9 mol
2 4
B.50mL 1mol·L-1的KCl溶液和100mL 0.25 mol·L-1MgCl 溶液中,Cl-物质的量浓度相等
2
C.将10 mL 1 mol·L-1的HSO 稀释成0.1 mol·L-1的HSO ,可向其中加入100 mL水
2 4 2 4
D.含N 个Na+的NaO溶于水配成1 L溶液,Na+的物质的量浓度为1 mol·L-1
A 2
【题6】(2021·吉林延吉·延边二中高二月考)标准状况下,VL NH 溶解在1L水中(水的密度近似为
3
1g∙mL−1),所得溶液密度为ρg∙mL−1,溶质质量分数为ω,物质的量浓度为c mol∙L−1,则下列关系中不正确
的是
A.ω= B.ω=C.c= D.ρ=
【题7】(2021·陕西长安一中高一月考)某结晶水合物的化学式为A·nH O,其相对分子质量为M,在
2
25℃时,ag晶体溶于bg水中即达饱和,形成密度为ρg/mL的溶液,下列表达式正确的是
A.饱和溶液中溶质的质量分数为: %
B.饱和溶液 的物质的量浓度为: mol/L
C.饱和溶液的体积为: L
D.25℃时,A的溶解度为: g
【题8】(2021·南岗·黑龙江实验中学高三开学考试)如图是某学校实验室从化学试剂商店买回的硫酸试剂
标签上的部分内容。据此下列说法正确的是
硫酸化学纯(CP)
(500mL)
品名:硫酸
化学式:
相对分子质量:98
密度:
质量分数:98%
A.该硫酸的物质的量浓度为9.2mol/L
B.该硫酸与等体积的水混合所得溶液的质量分数为49%
C.配制250mL4.6mol/L的稀硫酸需取该硫 酸62.5mL
D.该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2mol/L
提分作业
【练1】(2021·江苏高一月考)与50 mL1 mol/L MgCl 溶液中的Cl-的物质的量浓度相等的是
2
A.150mL 1 mol/L 的NaCl溶液B.75mL 0.5 mol/L 的CaCl 溶液
2
C.50mL2 mol/L 的KCl溶液
D.75mL1 mol/L 的FeCl 溶液
3
【练2】(2020·福建省漳平第一中学高一期中)下列操作所得溶液的物质的量浓度为1mol/L的是
A.100mL水中溶解0.1molHCl气体 B.100g水中溶解4gNaOH
C.将5.85gNaCl溶于水中得到100mL溶液 D.从500mL10mol/L稀盐酸中,取出50mL
【练3】(2021·江苏高一月考)下列 关于物质的量浓度表述正确的是
A.0.2 mol/L Na SO 溶液中含有Na+和SO 总物质的量为0.6 mol
2 4
B.将62g Na O溶于水中,配成1L溶液,所得溶质的物质的量浓度为1 mol/L
2
C.用1 L水吸收22.4L氯化氢(标况下)所得盐酸的浓度是1 mol/L
D.10g 98%的硫酸(密度为1.84g cm-3)与10ml 18.4 mol/L的硫酸浓度相等
【练4】(2021·江苏苏州·高一月考)某溶液中仅含有Na+、Mg2+、SO 、Cl-四种离子其物质的量浓度之
比为c(Na+):c(Mg2+):c(Cl-)=3:5:5,若Na+浓度为3mol·L-1。则SO 的浓度为
A.2mol·L-1 B.3mol·L-1 C.4mol·L-1 D.8mol·L-1
【练5】(2021·江苏昆山·周市高级中学高一月考)向等体积等浓度的AgNO 溶液中,分别滴加NaCl、
3
MgCl 、AlCl 溶液,均恰好完全生成沉淀。则NaCl、MgCl 、AlCl 的物质的量之比为
2 3 2 3
A.1:2:3 B.3:2:1
C.6:3:2 D.9:3:1
【练6】(2019·罗平县第二中学高一期末)500m L的KAl(SO ) 溶液中含有3.9g的K+,则该溶液中
4 2
c(Al3+)为
A.1mol/L B.0.4mol/L C.0.2mol/L D.0.1mol/L
【练7】(2021·全国高一课时练习)浓度均为0.1mol•L-1的KCl、CaCl 溶液等体积混合,下列说法错误的
2
是
A.混合前CaCl 溶液中c(Cl-)=0.2mol•L-1
2
B.混合前KCl、CaCl 溶液中c(Cl-)之比为1∶2
2
C.混合前后K+、Ca2+的物质的量不变
D.混合溶液中c(Cl-)=0.3mol•L-1【练8】(2020·浙江高一期末)对1L1mol•L-1氯化镁溶液的理解,不正确的是
A.95g无水氯化镁溶于1L水中即可得到上述溶液
B.该溶液中含有95g溶质
C.该溶液中氯离子的 物质的量浓度为2mol•L-1
D.从该溶液中取出100mL,其物质的量浓度为1mol•L-1关注更新免费领取,淘宝唯一每月更新店铺:知二教育