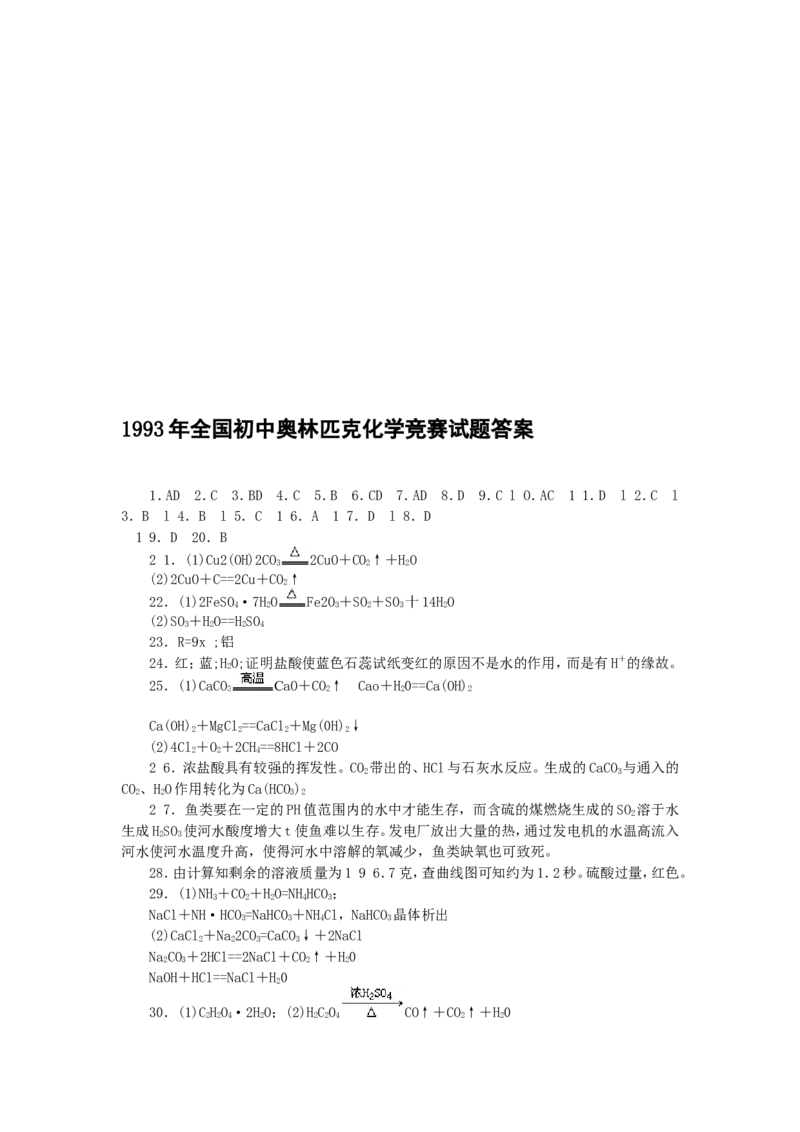文档内容
1993 年全国初中奥林匹克化学竞赛试题
可能用到原子量:
H-1 Li-7 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
Cl-35.5 K-39 Ca-40 Fe-56
一、选择题
下列各小题分别有1个或2个正确答案。本题1-15题每题2分,16-20题每题3分,
共45分。
1.由我国已故著名化工实业家吴蕴初先生创办的上海天原化工厂,目前生产的液氯含氯
99.6%,含水份小于0.05%,在化工生产中这种液氯可看做( )。
A.纯净化 B.混合物 C.化合物 D.单质
2.下列反应不属于化合、分解、置换、复合解任一反应类型的是( )。
A. 氧化钠跟三氧化硫反应
B. 晶碱(NaCO·10H O)的风化
2 3 2
C. 氧化铁与一氧化碳高温下反应
D. 苛性钠与氯化铜溶液反应
3.在下列各组物质中,具有不同原子团的是( )。
A. FeSO 与Fe(SO)
4 2 3
B. NaSO 与NaSO
2 4 2 3
C. NH Cl与NH Rr
4 4
D. KMnO 与KMnO
4 2 4
4.氢气是一种很有前途的能源。以水为原料大量制取氢气的最理想的途径是( )。
A. 由热电站提供电力电解水
B. 改进以焦炭和水制煤气的方法
C. 利用太阳能分解水
D. 使赤热的铁与水反应生产氢气
5.下列过程不会增加空气中CO 含量的是( )。
2
A. 呼吸作用 B.光合作用
C.汽油燃烧 D.煅烧石灰石
6.下列化学肥料属于复合肥料的是( )。
A.NH Cl B.NH NO C.KH PO D.KNO
4 4 3 2 4 3
7.1985年科学家发现了一种组成为C 的物质,下列说法正确的是( )。
60
A. 它的1个分子中含有60个原子
B. 它是一种新型化合物
C. 它是一种共价化合物
D. 它是一种单质
8.有甲、乙、丙、丁四种金属。仅甲在自然界主要以游离态存在,丙盐的水溶液不能用丁
制的容器盛放,丁与乙盐的水溶液不反应。这四种金属的活动性由强到弱的顺序是( )。
A.甲乙丙丁 B.丁乙甲丙 C.丙乙丁甲 D.乙丁丙甲
9.将60℃浓度为80%的硝酸铵溶液500克恒温蒸发掉5克水,析出10.5克晶体,则60℃
时硝酸铵的溶解度是( )。
A.105克 B.210克 C.400克 D.以上都不对10.向下列各对物质中加水后,难溶物不发生变化的是( )。
A.FeO、CO B.BaCO、SO
2 3 2 3 3
C.Cu(OH) 、MgO D.SiO 、KO
2 2 2
11.下列干燥剂不适宜用来干燥二氧化碳气体的是( )。
A.浓硫酸 B.无水CaCl C.P 0 D.CaO
2 2 5
12.人的胃液正常 H值在1.2—0.3之间,酸度再高就患胃酸过多症,下列物质不适宜用
P
做治疗胃酸过多症药剂成分的是( )。
A.氧化镁粉 B.氢氧化镁粉 C.氧化钙粉 D.纯碳酸钙粉
13.含有相等原子个数的钠、镁、铁、铝四种金属分别跟足量稀硫酸反应,所生成的氢气
的质量比是( )。
A.23:24:56:27 B.1:2:2:3 C.2:3:3:6 D.2:1:1:2/3
14.镁在空气中燃烧不仅生成氧化镁,还有部分镁与氮气化合(生成物中N呈-3价)。由
此可以推知12克镁在空气中燃烧后所得产物的质量为( )。
A.等于20克 B.小于20克 C.大于20克 D.以上情况都可能
15.R、X两种元素间形成多种化合物,已知其中一种化合物RX中R元素的百分含量为
46.7%,则下列化合物中R元素含量大于46.7%的是( )。
A.PX B.R X C.R X D.R X
2 2 3 2 2 5
16.在天平的两个托盘里,分别放上等重的两烧杯并分别加入等质量的稀硫酸,往左杯里
放入0.44克氧化钙,要使天平重新达到平衡,可以往右杯里加入的适宜物质是( )。
A.0.48克镁粉 B.1.00克碳酸钙
C.0.924克碳酸镁 D.0.44克铜铝合金
17.在通风良好燃烧正旺的煤炉中,下列反应最不容易发生的是( )。
A. B.
C.CO +C △ CO D.2C+O 点燃 2CO
2 2 2
18.Rn+离子有两个电子层且已达稳定结构。与Rn+的电子数相等的微粒(分子、原子和离
子,但不包括Rn+本身)可有( )。
A.6种 B.7种 C.8种 D.9种
19.某元素(R)的化合价是奇数(不变价),已知其氧化物的分子量为m,其氯化物的分子
量为n,则R的化合价为( )。
A. B. C. D.
20.测得某溶液中仅含有Na+ 、Mg2+、SO 2-、Cl四种离子,某中离子个数比为Na+:Mg2+:Cl
4
-=4:5:8,若没Na+为4n个,则SO 2-离子个数可能是( )。
4
A.2n B.3n C.6n D.8n
二、填空题(30分)
21.人类很早就发现,孔雀石在熊熊燃烧的树木中灼烧后,余烬里有一种红色光亮的金属
显露出来。试用化学方程式表示孔雀石[主要成分是Cu(OH)CO]变化的两个主要反应:
2 2 3
(1) 。
(2) 。
22.硫酸最古老的生产方法是:把绿矾(FeSO·7H O)装入反应器中加强热,会流出油状
4 2
液体,并放出有刺激性气味的气体(SO ),反应器中的固体变为红色。这个变化的过程可用两
2
个化学方式表示。
(1) 。
(2) 。23.取某金属0.45克与量稀硫酸反应,测得生成气体0.05克。已知该金属的原子量小于
40,且核内中子数比质子数多1个,可推知该金属的原子量(R)与其化合价(X)的关系式是
,最终确定该金属元素是 。
24.某同学欲证明盐酸与氯化氢气体性质不同,他向A、B、C、三支洁净试管里各放一片
干燥的蓝色石蕊试纸,然后向A试管里加入盐酸,试纸显 色;往B试管中通入
干燥的氯化氢气体,试纸显 色。这时他认为由此还不能得出满意的结论,于
是向C试管中加入一种分子式为 的物质,他之所以加入这种物质的理由
是 。
25.金属镁主要由电解熔融MgCl 的方法制得的。海水中溶有少量氯化镁,海边又盛产
2
贝壳(主要成分是CaCO)以它们为主要原料生产镁的大致程序是:
3
海水→Mg(OH) MgCl 溶液—→无水MgCl Mg+Cl
2 2 2 2
(1)写出以海水和贝壳为原料制取Mg(OH) 所涉及到的化学方程式: 。
2
(2)电解MgCl 产物之一的Cl 可与空气、甲烷起反应(产物为HCl、CO)再制得盐酸,循
2 2
环使用。写出该反应的化学方程式 。
26.某同学用下图所示的装置,使用较浓盐酸跟足量碳酸钠固
体反应,并将所生成的气体通入石灰水中。他在较长一般时间内
未发现石灰水变浑,原因是 ;然后石灰水
变浑,但很快又变澄清,浑浊现象消失很快的原因是:
。
三、简答题(15分)
27.某热电厂地处多雨地带,所使用的燃料煤中含少量硫,燃烧的气体未经处理即排往空
中,又有部分发电用水未经冷却排入河流。观察其下游几十公里的河水中鱼类几乎绝迹,试
解释出现这种现象的原因(必要时写出有关反应的化学方程式)。
28.向敞口烧瓶中加入12.6克碳酸氢钠,再加入浓度为14.7%的硫酸溶液100克,烧瓶连
同药品的起始质量为200克,用自动计时和称装置每秒钟测量一次烧怀连同药品的质量,所
得质量与时间的关系如曲线所示。试通过计算并对照曲线回答:碳酸氢钠反应到一半时所用
的时间约是多少秒?往反应停止后的溶液中滴入石蕊试液,试液呈什么颜色?
29.(1)下表列出了NaCl等四种盐在不同温度下的溶解度数据(克)。
0℃ 10℃ 20℃ 30℃ 40℃
NaCl 35.7 35.8 36 36.3 36.6
NH HCO 11.9 15.8 21.0 27.0 -
4 3
NaHCO 6.9 8.2 9.6 11.1 12.7
3
NH Cl 29.4 33.3 37.2 41.4 45.8
4
(1) 往NaCl浓溶液中通入氨气达到饱和,再通入二氧化碳,即有晶粒析出。试判
断这种晶粒是哪一种物质?写出有关反应的化学方程式。(2) 上面实验中所用食盐需要预先提纯,除去其中的CaCl、MgCl 杂质。请写出除
2 2
去CaCl 杂质的反应的化学方程式。
2
四、(10分)
30.某晶体的分子量为126,它的分子式可用HC O·nHO表示,取6.3克该晶体,在
x y z 2
100℃完全失水后称得固体质量为4.5克。又测得C、H、O在无水HC O 的质量百分比分别
x y z
为2.2%、26.7%、71.1%。
(1) 通过计算确定该晶体的分子式。
(2)上述无水物加入少量浓硫酸共热后生成CO、CO、HO,试写出这个反应的化学方程
2 2
式: 。
(3)实验室可以用上面的反应制取CO。为了得到较多量的干燥而纯净的CO,应将混合
气体先通过 溶液除去 ,再通过 除去
,最后就剩下纯净的CO。1993 年全国初中奥林匹克化学竞赛试题答案
1.AD 2.C 3.BD 4.C 5.B 6.CD 7.AD 8.D 9.C l O.AC 1 1.D l 2.C l
3.B l 4.B l 5.C 1 6.A 1 7.D l 8.D
1 9.D 20.B
2 1.(1)Cu2(OH)2CO 2CuO+CO↑+HO
3 2 2
(2)2CuO+C==2Cu+CO↑
2
22.(1)2FeSO·7HO Fe2O+SO+SO 十14HO
4 2 3 2 3 2
(2)SO+HO==HSO
3 2 2 4
23.R=9x ;铝
24.红;蓝;HO;证明盐酸使蓝色石蕊试纸变红的原因不是水的作用,而是有H+的缘故。
2
25.(1)CaCO CaO+CO↑ Cao+H0==Ca(OH)
3 2 2 2
Ca(OH)+MgCl==CaCl+Mg(0H)↓
2 2 2 2
(2)4Cl+O+2CH==8HCl+2CO
2 2 4
2 6.浓盐酸具有较强的挥发性。CO 带出的、HCl与石灰水反应。生成的CaCO 与通入的
2 3
CO、HO作用转化为Ca(HCO)
2 2 3 2
2 7.鱼类要在一定的PH值范围内的水中才能生存,而含硫的煤燃烧生成的SO 溶于水
2
生成HSO 使河水酸度增大t使鱼难以生存。发电厂放出大量的热,通过发电机的水温高流入
2 3
河水使河水温度升高,使得河水中溶解的氧减少,鱼类缺氧也可致死。
28.由计算知剩余的溶液质量为1 9 6.7克,查曲线图可知约为1.2秒。硫酸过量,红色。
29.(1)NH+CO+HO=NHHCO;
3 2 2 4 3
NaCl+NH·HCO=NaHCO+NHCl,NaHCO 晶体析出
3 3 4 3
(2)CaCl+Na2CO=CaCO↓+2NaCl
2 2 3 3
NaCO+2HCl==2NaCl+CO↑+H0
2 3 2 2
NaOH+HCl==NaCl+H0
2
30.(1)CHO·2HO;(2)HCO CO↑+CO↑+H0
2 2 4 2 2 2 4 2 2(3)Na0H;CO;浓HSO;水蒸气
2 2 4