文档内容
1999年全国初中学生化学素质和实验能力竞赛(第九届天原杯)复赛试题
H:1 C:12 N:14 O:16 S:32 Cl:35.5 Mg:24 Al:27 K:39 Mn:55
一、选择题(本题15小题,每小题2分,共30分、每小题有1个或2个选项符合题意,若
有两个答案的错1个不得分,漏选1个扣1分。)
⒈某矿泉水标签上印有主要的矿物质成分如下(单位为mg/L):Ca 20,K 39,Mg
3,Zn 0.06,F 0.02等,这里的Ca,K,Mg,Zn,F是指( )
A.单质 B.元素 C.金属离子 D.分子
⒉飘尘是物质燃烧时产生的粒状飘浮物,颗粒很小,不易沉降、它与空气中的SO ,O,接
2 2
触时,SO 会部分转化为SO ,使空气的酸度增加、飘尘所起的作用可能是( )
2 3
A.氧化剂 B.还原剂 C.催化剂 D.吸附剂
⒊打雷放电时,空气中有少量氧气会转化成臭氧(3O=2O ),下列有关说法中正确的是(
2 3
)
A.该变化是物理变化 B.O 与O 都是单质
2 3
C.O 与O 是不同的物质 D.O 与O 的性质完全相同
2 3 2 3
⒋在大气层中,因CO 的含量不断增加而引起“温室效应”,造成大气中CO 含量增加
2 2
的主要原因是( )
A.由于动植物呼吸作用增加
B.由实验室逸出的CO 增加
2
C.由于森林绿化面积迅速递减,使得自然界吸收CO 的能力降低
2
D、由于大量燃烧矿物燃料
⒌有CuO、Fe、H、Ba(OH) 溶液,KCO 溶液,NaOH溶液,稀硫酸等七种物质,在常温下
2 2 2 3
两种物质间能发生的化学反应最多有( )
A.4个 B.5个 C.6个 D.7个
⒍在氯化亚铁和氯化铜的混合溶液中加入锌粉,下列说法中不正确的是( )
A.若反应完成后锌有剩余,则溶液中有Zn2+无Cu2+,可能有Fe2+
B.若反应完成后锌有剩余,则溶液中有Zn2+,没有Cu2+和Fe2+
C.若反应完成后锌无剩余,溶液中若有Cu2+,则一定有Fe2+
D.若反应完成后锌无剩余,溶液中若无Cu2+,则可能有Zn2+和Fe2+
⒎两种化合物AB和DB ,若A元素的化合价与HO中O的化合价绝对值相同,则D的
2 2
化合价为( )
A.+4 B.+2 C.-2 D.-3
⒏测得某溶液中含Cu2+,K+,SO 2-,Cl-四种离子,且阳离子的个数比为Cu2+:K+=3:4,则
4
SO 2-与Cl-的个数比可能是( )
4
A.3:2 B.1:3 C.1:8 D.2:5
⒐由C,H两种元素组成的化合物叫烃,碳原子数在4及以下的烃在常温常压下通常为气
体,常温常压时烃C H 和另一种烃组成的混合气体中碳元素的质量分数为87%,则混入的
2 4
烃可能是( )
A.CH B.C H C.C H D.C H
4 2 2 2 8 8 8
10.在室温时,将硝酸钠和氯化钾两种饱和溶液混合后无晶体析出,在加热蒸发时,开始析
出的晶体是( )
A.KNO B.KCI C.NaNO D.NaCl
3 3
11.在toC时,100g水中加入mgNaCO 或加ngNaCO·10H O,均可使溶液达到饱和,
2 3 2 3 2
则m和n的关系式正确的是( )A. B.
C. D.
12.某学生的实验报告中有以下实验数据,其中正确的是( )
A.用托盘天平称取11.709食盐 B.用量筒量取5.29 mL盐酸
C.用pH试纸测得溶液的pH是5.4 D.用托盘天平称取2.5g锌
13.某学生用量筒量取液体,将量筒平放且面对刻度平视测量、初次视线与量筒内凹液面
的最低处保持水平,读数为20 mL,倒出部分液体后,俯视凹液面的最低处,读数为5mL则
该学生实际倒出液体的体积( ) 、
A.大于15 mL B.小于15 m1 C.等于15 m1 D.无法确定
14.对于化学反应A+B=C+D,下列说法中错误的是( ).
A.若生成物C和D分别是盐和水,则反应物一定是酸和碱
B.若A和C是单质,B和D是化合物,则该反应一定是置换反应
C.若A是可溶性碱,B是可溶性盐,则C、D可能是两种沉淀
D.若A,B各取10g混合,使其充分反应,则C,D质量的总和一定等于20 g
15.1.6g某物质在氧气中完全燃烧生成4.4g二氧化碳和3.6g水,关于该物质的组成有下
列论断:①一定含C、H;②一定不含O;③可能含O;④一定含O;⑤分子中C、H的原子个数
比为1:2;⑥分子中C、H的原子个数比为1:4、其中正确的是( )、
A.①②⑥ B.①②⑤ C.①③⑥ D.①④⑤
二、填空题(本题包括9小题,共34分)
16.汽车尾气中含有CO和NO等有毒气体,其净化过程如下:(1)在催化剂催化作用下,
CO将NO还原成N;(2)再通人过量空气,使剩余的CO完全氧化、试写出有关反应的化学
2
方程式:
(1) (2)
17.为鉴定氯酸钾中含有氯元素,给定的试剂和实验操作有:①滴加AgNO 溶液;②冷
3
却后,加水溶解;③加热;④滴加稀硝酸;⑤过滤后取滤液;⑥加催化剂二氧化锰。按实验操作
的先后,其顺序正确的是(填号)
18.有些牙膏中添加有少量的氟化物如氟化钠(NaF)等,写出氟化钠溶于水的电离方程
。刷牙时氟化钠跟牙齿矿物质——羟磷石[Ca (PO )(OH) ]反应生成氟磷灰石[Ca (PO )F],
10 4 6 2 10 4 6 2
氟磷灰石具有更能抗酸(牙缝中食物残渣发酵生成的有机酸)的作用,从而达到防治龋齿的
目的。写出生成氟磷灰石反应的化学方程式
。
19.欲防止煤燃烧产生的SO 污染大气,有多种化学方法,例如:
2
(1)在煤中掺消石灰:煤燃烧时,SO 与消石灰反应生成CaSO ,CaSO 再被氧化成
2 3 3
CaSO,写出反应的化学方程式 。
4
(2)回收利用:将工厂燃煤废气中的SO 通人石灰乳中,可生成Ca(HSO ),它可用于造
2 3 2
纸浆等、写出反应的化学方程式 。
20.证明“光合作用需要二氧化碳的实验”可利用图1所示的甲(玻璃缸中盛NaOH溶
液)、乙(玻璃缸中盛清水)两个装置,将这两个装置同时放在黑暗处一昼夜,然后一起放到阳
光下,几小时后,检验甲装置中植物的叶片没有新的淀粉生成,而乙装置中植物的叶片却有
新的淀粉生成,其原因是甲装置里的CO ,反应的化学方程
2
式是 。21.有X、Y、Z三种元素,它们的原子核内质子数均不超过18,它们能相互形成XZ和
YZ型化合物,X2+和氖原子的核外电子排布相同;Y原子和X2+的电子层数相同,但比Z原子
少2个电子,Y原子的最外层电子数是次外层的2倍。试求:
(1)X、Y、Z原子核内的质子数 、 、 。
(2)若X、Y、Z的原子核内的质子数与中子数均相等,则化合物XYZ 的式量是
3
。
22.许多在水溶液中的反应
(如复分解反应),往往有易溶物
转化为难溶物或难溶物转
化为更难溶物的现象。表 1为相
同温度下某些物质的溶解度。
(1)若在有氯化银固体的水
中加人硫化钠溶液,可能发生的
现象是 。
(2)生成硫酸铵化肥的方法之一是:把石膏粉(CaSO)悬浮于水中,不断通人氨气并再
4
通人二氧化碳,充分反应后,立即过滤,滤液经蒸发而得到硫酸铵晶体。写出该反应的化学方
程式 。
23.已知海水中含有氯化镁,但因其含量低而不能用于生产镁。某工厂利用海水和海边
丰富的贝壳(主要成分是CaCO )资源来制取氢氧化镁,然后制取较纯净的氯化镁,并再用于
3
生产镁。写出制取氯化镁的有关反应的化学方程式 。
24.河水里的微生物使有机物(以C H O 表示)转化为CO 和HO的过程中所需的O
6 10 5 2 2 2
量叫生化需氧量(BOD),BOD是衡量水体质量的一个指标。
(1)C H O 和O,反应生成CO 和HO的化学方程式为
6 10 5 2 2 2
(2)20oC时,1.0L某水体(假使该水的密度为1g/mL)中含有机物(C H O)的质量分数
6 10 5
为0.0010%。则该水体的BOD为 g/L
(3)20oC时,1.0L水中溶O0.0092g。上述水体适合于鱼类生存吗? 。
2
原因是 。
三、实验题(共24分。)
25.欲确定某碳酸钠样品(含有少量硫酸钠)中其碳酸钠的质量分数,可进行如下实验:
称取样品ag,加水溶解,在该溶液中加入过量的盐酸使溶液呈酸性,再加入过量氯化
钡溶液,过滤、洗涤沉淀,并将沉淀烘干,称量沉淀为bg。请回答:
⑴溶液用盐酸酸化的原因是 。
⑵需要加入过量氯化钡溶液的原因是 。
⑶检验氯化钡是否加入过量的方法是 。
⑷计算样品中含NaCO 质量分数的表达式是 。
2 3
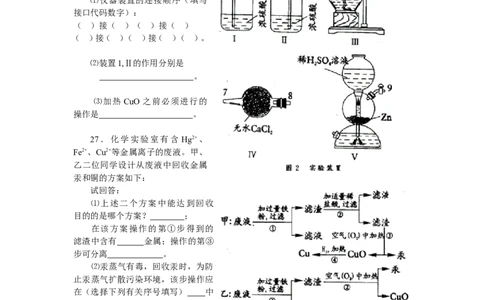
26.利用图2示连接装置,进
行氢气还原氧化铜的实验,并测定
铜的相对原子质量(已知H,O的相
对原子质量)。
试回答:
⑴仪器装置的连接顺序(填写
接口代码数字):
( )接( )( )接( )
( )接( )( )接( )( )。
⑵装置1,Ⅱ的作用分别是
。
⑶加热 CuO 之前必须进行的
操作是 。
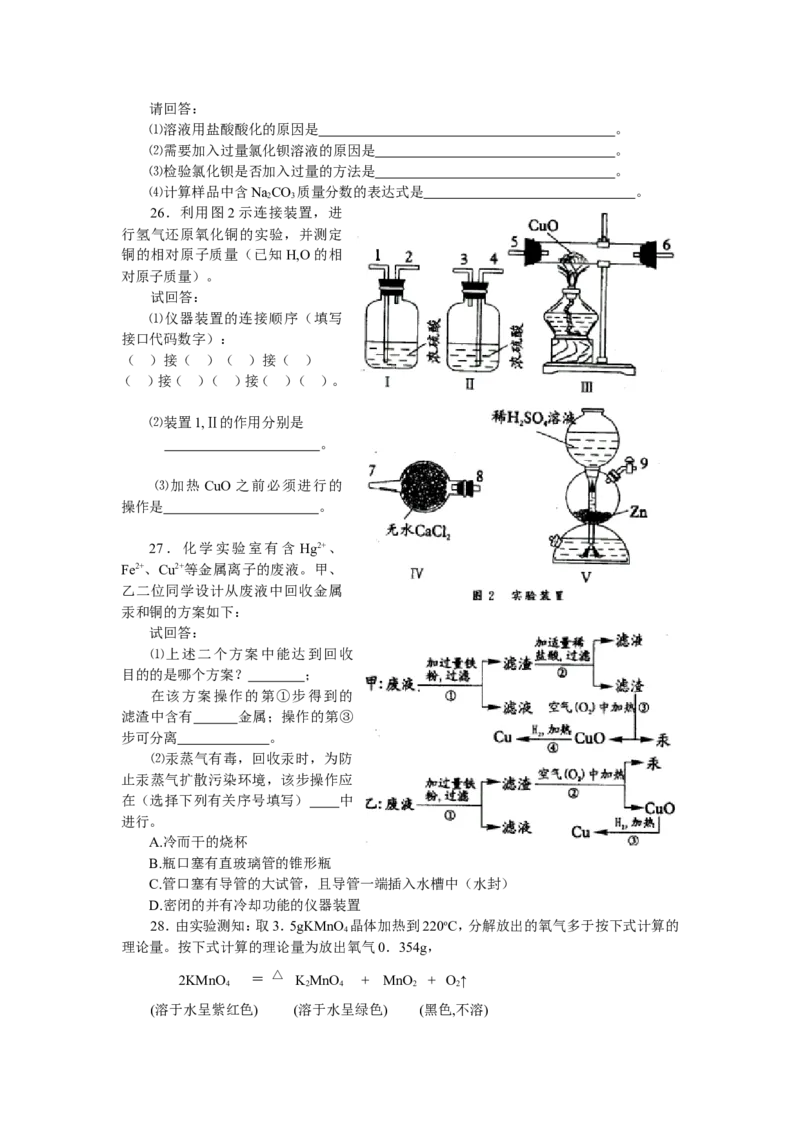
27.化学实验室有含 Hg2+、
Fe2+、Cu2+等金属离子的废液。甲、
乙二位同学设计从废液中回收金属
汞和铜的方案如下:
试回答:
⑴上述二个方案中能达到回收
目的的是哪个方案? ;
在该方案操作的第①步得到的
滤渣中含有 金属;操作的第③
步可分离 。
⑵汞蒸气有毒,回收汞时,为防
止汞蒸气扩散污染环境,该步操作应
在(选择下列有关序号填写) 中
进行。
A.冷而干的烧杯
B.瓶口塞有直玻璃管的锥形瓶
C.管口塞有导管的大试管,且导管一端插入水槽中(水封)
D.密闭的并有冷却功能的仪器装置
28.由实验测知:取3.5gKMnO 晶体加热到220oC,分解放出的氧气多于按下式计算的
4
理论量。按下式计算的理论量为放出氧气0.354g,
2KMnO = △ KMnO + MnO + O ↑
4 2 4 2 2
(溶于水呈紫红色) (溶于水呈绿色) (黑色,不溶)换算成标准状况下的体积为248mL,而实际测得的氧气为308 mL(标准状况),超过理论量
为:(308-248)m1,=60 mL。试回答:
⑴怎样用实验证明:超理论量的
氧气不是来自MnO ?
2
⑵怎样用实验证明超理论量的氧
气是由 KMnO 分解产生的?(要求
2 4
用 KMnO 制取氧气后的残渣实验,
4
如图3所示。)
⑶怎样从“最后残渣”中分离
出MnO ?
2
四、计算题(共12分。)
29.白色粉未X是NaCO 与NaHCO 的混合物。取甲、乙、丙三份质量不同的X样品分
2 3 3
别跟50 g相同的稀盐酸充分反应,得到气体的质量与X的质量关系如表2。
表2得到气体的质量与X的质量关系
实验组别 甲 乙 丙
稀盐酸质量/g 50 50 50
X的质量/g 3.80 6.20 7.20
气体的质量/g 1.76 2.62 2.62
试计算X中NaCO 与NaHCO 的质量分数各是多少?
2 3 3
30.出土木制文物常处于水饱和状态,出土后若任其自然干燥将收缩、变形。一种保持文
物原状的方法是:将95份(质量)KSO ·A1(SO )·24H O(明矾)和5份HO混合加热到
2 4 2 4 3 2 2
90℃制成饱和溶液,并继续加热到92oC~95oC,将木制文物浸渍其中。待明矾充分渗人,使明
矾溶液取代木材中的水分后,趁热将文物从明矾溶液中取出,冷却至室
温。明矾在文物中结晶,再在文物外部涂一层亚麻油。求90℃时明矾的溶解度(回答大于某值
即可,但要写出计算过程。已知明矾溶解度随着温度升高显著变化)。
1999年全国初中学生化学素质和实验能力竞赛试题
参考答案及评分标准
一、选择题(本题15小题,每小题2分,共30分。每小题有1个或2个选项符合题意。若有
两个答案的错1个不得分, 漏选1个扣1分。)
1 2 3 4 5 6 7 8
B C B、C C、D C A A B、C
9 10 11 12 13 14 15
B D B D A D A
二、填空题(共34分)
16.(1) 2NO+2CO N+2CO (2分)
2 2(2) 2CO+O 2CO (写催化剂也对) (2分)
2 2
17.⑥③②⑤①④或⑥③②⑤④① (2分)
18.NaF = Na+ + F- (1)
Ca (PO )(OH) + 2NaF = Ca (PO )F + 2NaOH (2分)
10 4 6 2 10 4 6 2
19.(1) SO + Ca(OH) = CaSO + H O (1分)
2 2 3 2
2CaSO + O = 2CaSO (1分)
3 2 4
(2) Ca(OH) + 2SO = Ca(HSO ) (2分)
2 2 3 2
20.被NaOH溶液吸收掉了 (2分)
2NaOH + CO = Na CO + H O (2分)
2 2 3 2
21.(1) 12、6、8 (3分) (2) 84 (1分)
22.(1) AgCl白色固体表面变黑 (2分)
(2) CaSO + 2NH + CO + H O = CaCO ↓+( NH ) SO (2分)
4 3 2 2 3 4 2 4
23 . CaCO CaO + CO ↑(1分) CaO + H O = Ca(OH) (1分)
3 2 2 2
Ca(OH) + MgCl = Mg(OH) ↓+ CaCl (1分)
2 2 2 2
Mg(OH) + 2HCl = MgCl + 2H O (1分)
2 2 2
24.(1) C H O + 6O = 6CO + 5 H O (1分) (2) 0.012 (2分)
6 10 5 2 2 2
(3)不适于鱼类生存, 因为0.012 克/升(BOD) > 0.0092克/升 (2分)
三、实验题(共24分)
25.(1) 除去CO2-,防止BaCO 沉淀生成 (2分)
3 3
(2) 将SO 2-完全转化为BaSO 沉淀 (2分)
4 4
(3) 将生成的沉淀静置,在上层清液中滴加BaCl 溶液,
2
若没有白色沉淀产生,证明BaCl 已滴加过量 (2分)
2
(4) a 142 b (2分)
233
100%
a
26.(1) (9)接(1)(2)接(5)(6)接(8)(7)接(4)(3) (2分,错1个无分)
(2)吸收H 中的水蒸气、防止空气中的水蒸气进入装置Ⅳ (2分)
2
(3) ①检验H 的纯度,并先通入已经验纯的H 至装置 内的空气赶净 (2分)
2 2
27.(1) 甲 (1分) Hg、Cu、Fe (1分,缺答1个不给分)
Hg、Cu (1分,缺答或错答1个都不给分)
(2) C或D (1分)
28.(1)另取少量MnO ,在酒精灯火焰上加热,插入带火星的木条,木条不复燃 (2分)
2
(2)用酒精灯火焰集中加热“残渣”,又收集到一定体积 的氧气(2分)(3)将“最后残渣”加入适量的水溶解,过滤,即可分离出MnO (2分)
2
四、计算题(共12分)
29.由题意所给的质量关系表可知,乙、丙实验组由于X过量,
故不能据此计算。
设甲组样品中NaCO 的质量为x,NaHCO 的质量为y
2 3 3
NaCO + 2HCl = 2NaCl + H O + CO ↑
2 3 2 2
106 44
x 44x
106
NaHCO + HCl = NaCl + H O + CO ↑ (2分)
3 2 2
84 44
y 44y
84
即得 x + y = 3.80 克 44x +44y = 1.76 克
106 84
解得 x = 2.12克 y =1.68克 (3分)
故样品X中: w(Na CO) =2.12 克 =55.8%
2 3 100%
3.80 克
w(NaHCO ) = =44.2% (2分)
3
答(略)
30.95克明矾和5克水混合的溶液中含水的质量为:
95克×432+ 5.0克 = 48.3克
948
含KSO ·Al (SO ) 的质量为:100克-48.3克= 51.7克 (2分)
2 4 2 4 3
设95份明矾和5份水混合的溶液中每100克水中含KSO ·Al (SO ) 的质量为x
2 4 2 4 3
48.3克∶51.7克=100克∶x x = 107克 (2分)
即90 ℃时明矾的溶解度>107克 (2分)
答(略)