文档内容
1995 年全国初中奥林匹克化学竞赛
原子量:H-1 C-12 N-14 O-16 Na-23
Mg-24 Al-27 S-32 Cl-35.5 K-39 Ca-40
Fe-56 Cu-64 Zn-65 Ag-108 Ba-137
一、(本题共40分)下列小题分别有1个或2个正确答案,把正确答案的编号填在括号里。
1.天原化工厂是氯碱工业的现代化工厂,原料食盐用水溶解制得饱和食盐水,在电解前
要除去杂质(如氯化钙、硫酸钙、氯化镁),通常要加入的试剂是( )
①AgNO ②BaCl ③NaOH ④NaCO ⑤Ca(OH)
3 2 2 3 2
(A) ①②③ (B)②③④ (C)①④⑤ (D)②③⑤
2.下列各组物质中,前者属纯净物,后者属混合物的是( )
(A)汽油 丁烷 (B)钢 生铁
(C)水 水煤气 (D)乙烯 聚氯乙烯
3.下列叙述中正确的是( )
(A)混合物中元素一定呈化合态。
(B)某物质中只含有一种元素,该物质一定是纯净物。
(C)同素异形体之间的转变一定是化学变化。
(D)某纯净物质不是化合物就是单质。
2
+1 - +4 +2
4.有 H、 O、C、Ca四种元素,按指定化合价最多可以组成化合物的种数
是( )
(A)5 (B)6 (C)7 (D)8
5.X、Y两种元素的化合价分别是+1、-2,它们跟硫元素共同形成化合物的分子式
是( )
(A)XSY (B)XSY (C)XSY (D)XSY
2 4 2 3 2 4
6.下列溶液通入气体后与下图中的曲线变化相符的 是 (
) pH
(A)氯化钠溶液中不断通入氯化氢气体 值
(B)澄清石灰水中不断通入二氧化碳气体
(C)盐酸中不断通入氨气 7
(D)碳酸钠溶液中不断通入氯化氢气体
7. 碳元素与某非金属元素R可形成化合物CR ,已 知 在
X
一个分子中各原子的电子数之和为74,则R的原子序数 0 和 X
的值分别是( ) 通往气体的量
(A)16,2 (B)35,4 (C)17,4 (D)26,3
8.将NaNO 和KC1两种饱和溶液混合后无晶体析出,在加热蒸发时开始有晶体析出,此
3
晶体是( )
(A)NaCl (B)KNO (C)KCl (D)NaNO
3 3
9.在实验室里用硝酸钠、盐酸、纯碱、石灰石和蒸馏水五种试剂,无法制取的物质是(
)(A)二氧化碳 (B)氢气 (C)烧碱 (D)浓硝酸
10.下列各组物质的溶液,不加任何试剂就能将其一一区别出来的是( )
(A)BaCl 、CuSO 、NaOH、NaCl
2 4
(B)NaSO 、BaCl 、KCO、KNO
2 4 2 2 3 3
(C)FeCl 、NaOH、HSO 、Ba(NO )
3 2 4 3 2
(D)NaCl、NaCO、Zn(NO )、HSO
2 3 3 2 2 4
11.某一饱和硫酸铜溶液中,加入含18O的带标记的无水硫酸铜粉末a克,则如果保持温
度不变,其结果是( )
(A)无水硫酸铜不再溶解,a克粉末不变
(B)溶液中可找到带标记的SO 2-,而且白色粗末变为蓝色晶体,其质量大于a克
4
(C)溶液中可找到带标记的SO 2-,而且白色粗末变为蓝色晶体,其质量小于a克
4
(D)溶液中溶解与结晶体达到平衡状态,有部分带标记的SO 2-进入溶液,但固体粉末
4
仍是a克。
12.X、Y两元素的原子量之比为2:1,由两元素形成的化合物中X、Y元素的质量比为
2:3,其中X元素的化合物价为+a,则化合物中Y元素的化合价为( )
(A)- (B)- (C)— (D)—
13.某元素氧化物的分子量为a,价态相同的硫酸盐的分子量为b,则此元素的化合价可
能是( )
(A) (B) (C) (D)
14.将某物质的溶液蒸发60克水后,温度降到20℃,析出无水晶体5克,再蒸发60克水,
温度仍降到20℃,又析出无水晶体6克,下列叙述中正确的是( )
(A)将原溶液变成饱和溶液,需补充溶质1克
(B)将原溶液变成饱和溶液,需补充溶质6克
(C)20℃时该溶质的溶解度为10克
(D)20℃时该溶质的溶解度为8.3克
15.已知某盐在不同温度下的溶解度如下表。若把质量百分比浓度为32%的该盐溶液,由
50℃逐渐冷却,则开始有晶体析出的温度范围是( )
温度(℃) 0 10 20 30 40
溶解度(克) 13.3 20.9 31.6 45.8 63.9
(A)0℃~10℃ (B)10℃~20℃
(C)20℃~30℃ (D)30℃~40℃
16.室温时,将质量各为5克的下列物质分别放入100克水里,充分搅拌后所得溶液的质
量百分比浓度最小的是( )
(A)氧化钠 (B)氧化钙 (C)氧化钾) (D)氢氧化钠
17.在空气中加热4.8克铜粉,使其全部变成氧化铜。然后把它放入足量的稀硫酸中,待
反应完毕后,再加蒸发溶剂,那么可制得硫酸铜晶体的质量是( )
(A)9.38克 (B)18.75克 (C)12克 (D)24克
18.粉末状金属混合物12克,加入足量的稀硫酸后产生1克氢气,这种金属混合物可能
是( )
(A)Al和Fe (B)Zn和Fe (C)Mg和Cu (D)Mg和Zn
19.现有5.85克NaCl样品(其中混有少量下列某种盐类),当它跟足量硝酸银充分反应
后,得到AgCl沉淀14.4克,则可能混入的盐是( )
(A)KCl (B)CaCl (C)BaCl (D)MgCl
2 2 2
20.已知在相同的温度和压强下,任何气体的体积和分子数成正比。在1体积空气中混入1体积二氧化碳,在高温下跟足量的焦炭反应,假设氧气和二氧化碳都转化为一氧化碳,则反
应后气体中一氧化碳的体积百分含量约是( )
(A)33.3% (B)50% (C)67% (D)75%
二、(本题共24分)
21.上海天原化工厂以食盐、水为主要原料生产多种化工产品。
(1)以食盐和水为反应物,经过电解获得氯气、氢气和氢氧化钠。该反应的化学方程式是
。
(1) 将氯气溶于水时,有一部分氯气跟水发生以下反应:
Cl+H O HClO+HCl
2 2
(次氯酸)
写出氯气通入消石灰水溶液中发生反应的化学方程式:
。
22.硅酸盐是构成地壳岩石的主要成分,化学上常用二氧化硅和氧化物的形成表示其组
成。例如,镁橄榄石(MgSiO)常以2MgO·SiO 表示。依照上法表示下列硅酸盐的组成:
2 4 2
高岭石Al(Si O)(OH)
2 2 5 4
钙沸石Ca(Al Si O ) ·3HO
2 3 10 2
滑石Mg(Si O )(OH)
3 4 10 2
23.当前发展较快、高效低毒的灭火剂叫“1211”灭火剂,其他学式是CFlB,命名方法
2 r
是按碳、氟、氯、溴的顺序分别以阿拉伯数字表示相应的原子数(末尾的“0”可略去)。按此
命名原则,写出下列几种新型灭火剂的化学式:
1301 , 122 , 2402 。
24.砷化氢AsH 是一种很强的还原剂,在室温下它能在空气中自然,其氧化产物是砒霜
3
(AsO),写出该反应的化学方程式 。
2 3
25.我国古代将炉甘石(ZnCO)、赤铜(CuO)和木炭混合后加热到800℃左右,得到一种
3 2
外观似金子的合金名为“金钅俞 石”。写出有关反应的公学方程式:
。
三、(本题共20分)
26.有一种工业废水,已知其中含有大量硫酸亚铁,少量的银离子和钠离子等,以及部分
污泥。试设计一个既经济又合理的方法回收金属银和硫酸亚铁。分别列出实验步骤并说明每
一实验步骤的目的。
27.物质溶于水时,有的放热会使溶液温度升高;有的吸热会使溶液温度降低。
现用广口瓶、试管、弯曲成如图形状的玻璃管,合适的橡皮塞和水为材料,设计一
个装置,使它能对物质溶于水时的吸热或放热现象进行研究。画出装置图,并简述
原理。
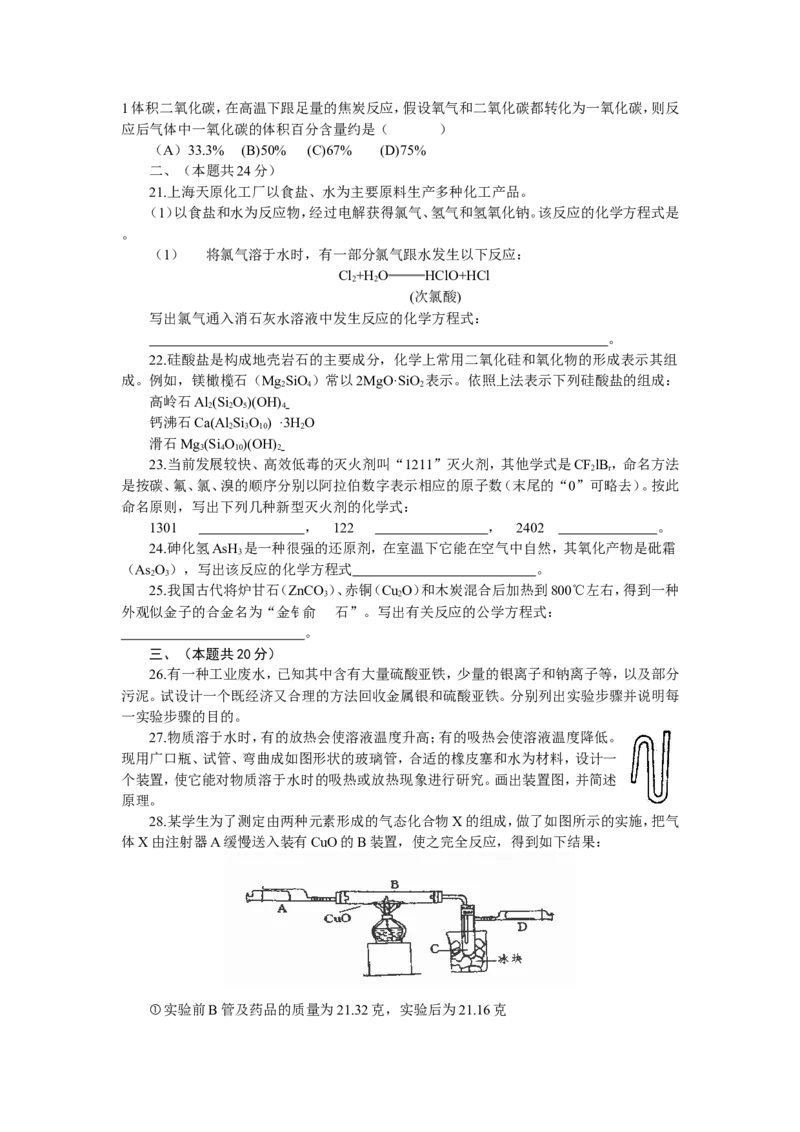
28.某学生为了测定由两种元素形成的气态化合物X的组成,做了如图所示的实施,把气
体X由注射器A缓慢送入装有CuO的B装置,使之完全反应,得到如下结果:
①实验前B管及药品的质量为21.32克,实验后为21.16克②C管中收集到的物质电解后可得到H 和O,在D中收集到的是N。
2 2 2
③X中两元素的质量比是14:3。问:
(1)C中收集到的液体,质量是 克。
(2)在实验中看到的现象是 。
(3)B中反应的化学方程式是 。
29.今有一混有NaSO 、NH HCO 和NaCl的固体,在实验室中以此混合物为原料要得到
2 4 4 3
少量纯净的NaCl溶液。写出选用的试剂和实验步骤。
30.从含CuS的铜矿石中冶炼铜有多种方法。其中一种是:
2
①先将矿石通空气高温焙烧,生成两种氧化物。
②将焙烧过的矿石加上比它质量少一半的未经焙烧过的矿
石,混合均匀后隔绝空气再行高温煅烧,结果得到金属铜和一种刺激
性气体。写出上述反应的化学方程式:
、 。
31.现有硫酸、氯化钡、硫酸钠和碳酸钠四瓶溶液,为鉴别它们先把四瓶溶液标上A、B、
C、D,然后进行以下实验。
①A跟B混合有气体产生;A跟C混合有白色沉淀生成;A跟D混合时无明显的反应现
象。
②A跟C反应所生成的白色沉淀能溶于B跟C反应后的溶液中。
由此可知:A是 ,B是 ,C是 ,D是 。
四、(本题共10分)
32.将一定量碳酸氢钠和铜的混合粉末放在容器里,在空气中用酒精灯加热至质量不再
改变,此时发现加热前后固体总质量相等,写出有关的化学方程式,并计算原混合粉末中含
铜的质量百分率。(碳酸氢钠加热会发生分解,生成碳酸钠、二氧化碳和水,计算结果精确到
0.1%。)
33.80℃时硫酸铜溶解度为55克(克/100)克水。现有50克14.8%的硫酸铜溶液和5克
38.7%的硫酸铜溶液,把这两种溶液混合,并要使混合后的溶液在80℃时成为饱和溶液。问
(1)可采用哪些措施?(2)如果试剂只有CuSO ·5H O,请按所采取的措施分别进行计算得出
4 2
结论。(计算结果精确到0.1克)
1995年全国初中奥林匹克化学竞赛试题答案
1.B 2.CD 3.CD 4.C 5.CD 6.D 7.C 8.A 9.D1 O.AD 1 1.B l 2.B 1 3.
AD 1 4.AC 1 5.D 1 6.B 1 7·B1 8.A 1 9.BD 20.D
21.(1)2NaCl+2HO 2NaOH+H↑+Cl↑
2 2 2
(2)2Cl+2Ca(OH)=CaCl 2+Ca(ClO)+2HO
2 2 2 2
22.AlO·2SiO·2HO,CaO·3SiO·A12O·3HO,
2 3 2 2 2 3 2
3MgO·4SiO·H0
2 2
23.CFBr;CFCl;CFBr
3 2 2 4 2
24.2AsH+3O=AsO+3HO
3 2 2 3 2
25.①ZnCO ZnO+CO↑
3 2
②2ZnO+C 2Zn+CO↑
2③2CuO+C 4Cu+CO↑
2 2
26.①过滤除去污泥。②向滤液中加入过量的铁粉,使Ag还原为Ag。⑧过滤,将Ag和过
量的铁粉从溶液中分离出来。④将混有Fe粉的Ag用稀HSO 处理,使Fe溶解。⑤过滤,分离
2 4
出银。⑥将③、⑤两步的滤液合并,蒸发浓缩,冷却结晶。⑦过滤,得硫酸亚铁晶体。加热晶体
使其失去结晶水得到FeSO
4
27.如右图,在玻璃管中加水,在试管中加水,照图连接好装置后,向试管中加入NHNO
4 3
晶体,可观察到弯曲玻璃管左边液面上升,右边液面下降,说明物质溶于水时有吸热现象发
生。产生上述现象的原因是NHNO 溶于水时扩散(物理)过程吸收的热量大于水合(化学)过程
4 3
放出的热量,敌表现为溶液温度降低,广口瓶内气压减小,故左边液面上升,右边液面下降.
28.(1)O.1 8;(2)黑色固体逐渐变为红色;C管中有无色液体出现;D的内管向外推动。
(3)2NH+3CuO 3Cu十N↑+3H0
3 2 2
29.(1)在试管中加入固体混合物,并加热。(2)加热的固体残渣冷却后加水溶解。(3)向溶
液中加入足量的BaCl 溶液。(4)向试管溶液中再加入足量NaCO 溶液。(5)过滤。(6)向滤液
2 2 3
中加入盐酸至不再产生气泡为止。(7)将溶液加热煮沸即得到NaCl溶液
30.2CuS+3O 2Cu0+2SO;
2 2 2 2
2Cu0+CuS 6Cu+SO↑
2 2 2
3 1.NaCO,HSO.BaCl,NaSO;
2 3 2 4 2 2 4
3 2.5 9.6%
3 3.(1)①加入CuSO;或CuSO·5HO;②加热蒸发一部分水,再降温至80℃。(2)用蒸
4 4 2
发溶剂的方法需蒸发28.7克水;用增加溶质的方法需增加35.7克CuSO·5HO。
4 2