文档内容
1997年全国初中学生化学素质和实验能力竞赛复赛试题
可能用到的相对原子质量:
C—12, H—1, Na—23, O—16, Ca—40, CI—35.5
一、选择题(每题有1个或2个选项符合题意,每小题2分,共40分)
1.下列叙述正确的是( )
(A)某物质中含有一种元素,则该物质一定是纯净物
(B)金刚石和石墨之间的转变一定是化学变化
(C)不同物质其相对分子质量一定不同
(D)不同的原子可相互组合成复杂的原子
2.初三课本有一幅彩图,其内容是一只漂亮的金丝雀和水中的金鱼生活“在一起”,
制作这个鸟笼的高分子薄膜必须具备的性质是( )
(A)绝热 (B)透气 (C)导电 (D)隔水
3.我国城市环境中,空气污染物主要是( )
(A)CO、CI 、N (B)SO 、NO 、CO
2 2 2 2 2
(C)NH 、CO、NO (D)HCI、SO 、N
3 2 2 2
4.按照核外电子排布规律:各电子层最多容纳电子数为2n(2 n为电子层数);最外层电
子数不超过8个;次外层电子数不超过18个,预测核电荷数为118的元素的原子核外电
子层排布是( )
(A)2,8,18,32,32,18,8 (B)2,8,18,32,50,8
(C)2,8,18,32,18,8 (D)2,8,18,32,50,18,8
5.科学实验证明:空气中微量臭氧(O)可抵抗阳光中紫外线对人体损害,作空调和冰箱
3
的致冷剂“氟里昂”是一种氯氟烃(以 代替其化学式),它可破坏臭氧层,其反应过程
可表示为: +O → O+O, O+O→ +O ,根据所学知识可知氯氟烃在反应中的作用
3 2 2
是( )
(A)氧化剂 (B)还原剂 (C)催化剂 (D)稳定剂
6.下列各组中的物质,只用水就能鉴别的是( )
(A)固体:氯化钾、硫酸钠、硫酸钡 (B)气体:氢气、氧气、二氧化碳
(C)固体:碳酸钙、氯化钠、氢氧化钠(D)液体:汽油、水、浓硫酸
7.如果一个碳12原子的相对原子质量为24,则不会改变的是( )
(A)氧原子的相对质量 (B)一个碳-12原子的质量
(C)硫酸的式量 (D)10克二氧化碳所含的分子个数
8.下列广告语中,你认为符合科学道理的是( )
(A)“超纯水”、“超纯蒸馏水”绝对卫生,对人体有益,
(B)本饮料由纯天然物质配制而成,绝对不含化学物质,对人体无害
(C)含氟牙膏可以预防龋齿
(D)含碘食盐可以防治甲状腺肿大9.用锌、氧化铜、稀硫酸作原料制取铜,有下列两种途径:
⑴
若用这两种方法制得的铜的质量相等时,下列叙述符合实际实验结果的是
(A)消耗相同质量的氧化铜 (B)消耗相同质量的锌
(C)消耗相同质量的硫酸 (D)生成硫酸锌的质量可能不同
10.某同学欲配制溶质质量分数为8%的食盐水80克,在用托盘天平称量食盐时,他把
食盐和砝码的位置放颠倒了(1克以下用游码),那么实际上他所配制的食盐水的溶质质
量分数为( )
(A)8.5% (B)7% (C)14% (D)8%
11.核电荷数为1~18的X、Y两元素,X元素原子的最外层电子数与次外层电子数差
的绝对值等于电子层数;Y元素比X元素的原子多2个最外层电子,则X与Y不可能形
成的化合物是( )
(A)XY (B)XY (C)XY (D)X Y
2 5 2
12.下列括号中的物质是除去杂质所用药品,其中错误的是( )
(A)氧化钙中有杂质碳酸钙(盐酸)(B)二氧化碳中有少量一氧化碳(氧气)
(C)氢气中有氯化氢(氢氧化钠溶液)(D)硫酸亚铁溶液中有硫酸铜(铁粉)
13.几种物质溶于水,能电离出K+、Mg2+、SO 、NO —四种离子,已知其中Mg2+、K+、
3
NO —离予个数比为4:5:3,则SO 与NO —的离子个数比为( )
3 3
(A)2:1 (B)10:3 (C)5:3 (D)3:5
14.常温下乙烷(C H )气体和酒精蒸气的混合物中,氧元素的质量分数为x%,则其混
2 6
合物中碳元素的质量分数是( )
(A) (B) (C) (D)
15.某生用含有杂质碳酸钠的烧碱样品与硫酸发生中和反应,那么,与等质量等溶质质
量分数的硫酸溶液恰好中和时,所用烧碱样品质量比用纯氢氧化钠的质量( )
(A)偏高 (B)偏低 (C)不变 (D)无法比较
16.某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、NaCO、NaCI三种溶液使
2 3
它们分别沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确
的是( )
(A)NaCO、NaCI、NaOH (B)NaOH、NaCI、NaCO
2 3 2 3
(C)NaCI 、NaOH 、 NaCO (D)NaCI 、NaCO、NaOH
2 3 2 3
17.金属M的样品中含有不跟盐酸反应的杂质,取样品20克投入适量的盐酸恰好完全
反应,生成MCI 和2克H,测知MCI 中含CI的质量分数为79.8%,则样品中M的
3 2 3
质量分数是( )(A)90% (B)10% (C)45% (D)54%
18.右图里有6个编号,每个编号代表下列物质中的一种物质,凡
用直线连接的相邻两种物质均能发生化学反应,供填写的物质有:
a.碳酸钠溶液;b.硫酸镁溶液;C.氯化钡溶液;d.稀硫酸;e.
铁;f.硝酸铜溶液,则图中③表示的物质的编号是( )
(A)e (B)f (C)a (D)d
19.t℃时,向x克KNO 不饱和溶液中,加入a克KNO 或蒸发掉 克水恢复到t℃,溶
3 3
液达到饱和,据此下列推论错误的是( )
(A)在t℃时,KNO 的溶解度为 克
3
(B)若原溶液中溶质质量分数为 ,则x=2
(C)若原不饱和溶液蒸发掉2 克水,恢复到原温度,能析出2a克KNO
3
(D)在t℃时所配得的KNO 溶液中溶质质量分数≤ 。
3
20.m克金属A(A的原子相对质量为m)与足量稀硫酸反应产生x克氢气,n克金属B
(B的原子相对质量为n)与足量稀盐酸反应产生y克氢气,且x=y,若要确定反应中A、
B两种金属的化合价,至少需要知道的数据是( )
(A)x与y的比值 (B)x或y的确切值
(C)m与n的比值 (D)酸的溶质质量分数
二、填空题(共30分)
21.(1)制作松花蛋所需配料有纯碱、氯化钠、生石灰、草木灰(内含碳酸钾)、开水,此
外还需要米糠、稻壳等,根据所学知识推断用配料制做时发生的化学反应有(用化学方
程式表) 。
(2)硫和氧的化学性质相似,在某些化合物中,硫原子可以代替氧原子,请完成下列
化学反应方程式:
①CS 和NaS水溶液混合振荡 。
2 2
②PS 溶于NaS溶液中 。
2 5 2
22.(1)某有机物中,有关元素的质量分数如下:含碳71.58%,含氢6.67%,含氮
4.91%,其余为氧,若该有机物分子中只含1个氮原子,则它的式量为 ,
化学式是 。
(2)肥皂的主要成分为硬脂酸钠(C H COONa),它是一种有机酸的钠盐,在肥皂
17 35
水中滴入盐酸会出现白色沉淀,这沉淀物是 (写名称);若在肥皂水中
加入硬水(含Ca2+、Mg2+)也会出现白色沉淀,此沉淀主要是 (写名称)
。23.(1)在分开盛放的A、B两溶液中,共含有Na+、Cu2+、Ba2+、Mg2+、NO -、OH-、SO
3
7种离子,两溶液里所含离子各不相同,已知A溶液里含3种阳离子和2种阴离子,其
余 在 B 溶 液 里 , 则 B 溶 液 里 所 含 离 子 应 该 是
。
(2)葡萄糖和蔗糖都属于糖类,大多数糖的组成可用C (H O)n表示,式中的“HO”
m 2 2
只说明糖分子中H、O的原子个数比相当于水的组成;糖类通常叫碳水化合物。(当 =
n=6时为葡萄糖,当 =12,n=11时为蔗糖)。实验室证实蔗糖是碳水化合物的实
验原理是(填文字) 。
24.(1)在CO还原CuO的反应中,Cu元素由+2价变为零价,C元素由+2价变为+4价,
在高中化学课本里把元素化合价发生变化的反应叫做氧化还原反应,上述反应中 CuO
为氧化剂,CO为还原剂,现有下列事实:衣物上沾了KMnO 溶液的污迹不易洗去,若用
4
维生素C制成的溶液擦洗,就能很快洗掉污迹,测知洗涤液中有Mn2+,可以推知擦洗过
程发生了 反应,反应中维生素C起了 作用。
(2)写出实验室以水为基本原料(如需其他试剂,根据价廉易得
的原则自己选定)制取H 的两个化学方程式(用两种反应类型):
2
。
25.(1)将30℃时含有某种溶质的溶液136克,分成两等份,其中一份加入该溶质10克,
结果只溶解2克就不再溶解了;将另一份冷却到0℃时,析出溶质5.5克,此时溶液的溶
质质量分数为20%,则该物质在30℃时的溶解度为 。
(2)四瓶贴有A、B、C、D标签的溶液,只知道它们是碳酸钾、硝酸钡、硫酸钾、硫酸氢
钾的溶液,在不用其他试剂的情况下,对这些溶液进行实验,记录如下:
(提示:KHSO=K++H++SO )①A+D→溶液+气体 ②B+C→溶液+沉淀
4
B+D→溶液+
A+B→溶液+
则A、B、C、D的化学式分别为:A 、B 、C 、D
三、实验题(共20分)
26.为了验证烧碱样品中是否含有氯化钠,正确的操作顺序是;
(1) ;(2) ;
(3) 。
27.向混有少量硝酸铜的硝酸银溶液中加入铁粉,当反应完成后过滤,得到滤液和金属。
(1)若向滤液中加入盐酸即生成氯化银沉淀,则滤出的金属是 ,(2)若
将滤出金属放入盐酸溶液有气泡产生,则滤液中一定存在的阳离子是
,不可能存在的离子是 。
28.某学生为了将氯化钠和氯化钙两种固体混合物分离,设计了下列实验方案:
试回答下列问题:
(1)B物质是 (填化学式)。
(2)若用上述实验方法分离得到的 NaCI,会含有杂质,除去杂质的方法是
。
(3)若要测定该混合物中氯化钠的质量分数,除称量B物质外,还需称量另一种物质
的质量才能计算确定,这种物质是 。
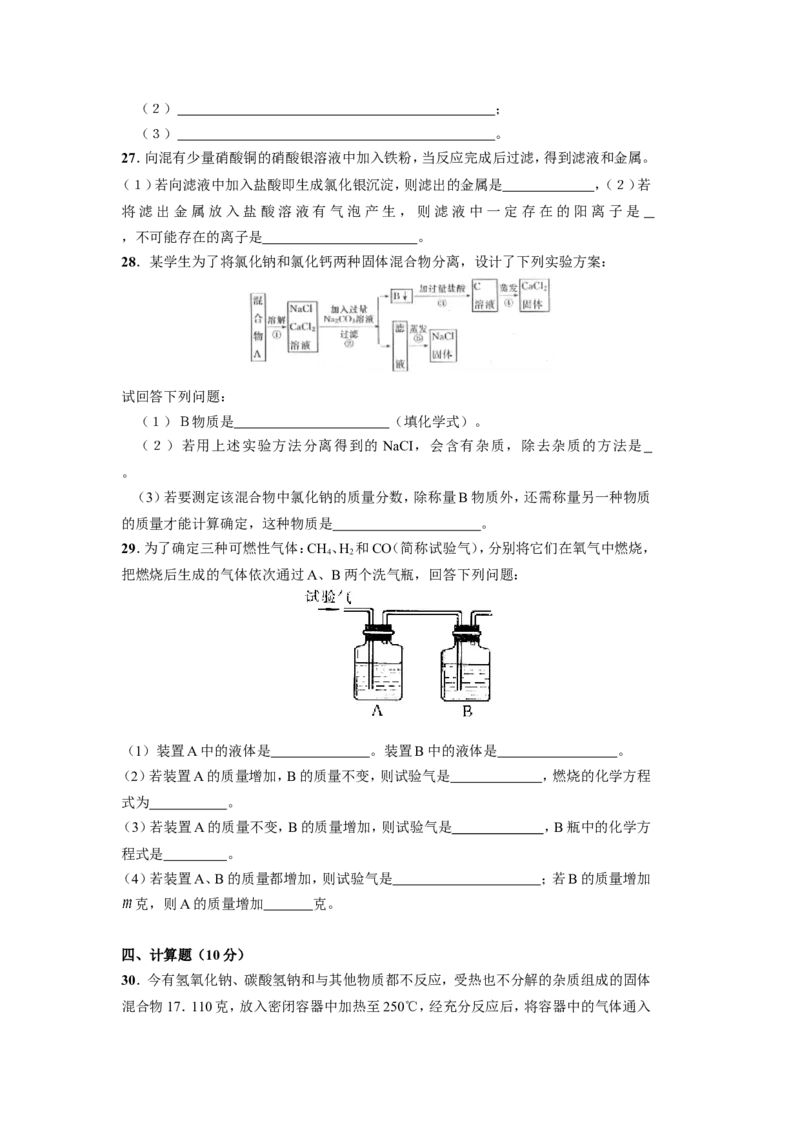
29.为了确定三种可燃性气体:CH、H 和CO(简称试验气),分别将它们在氧气中燃烧,
4 2
把燃烧后生成的气体依次通过A、B两个洗气瓶,回答下列问题:
(1)装置A中的液体是 。装置B中的液体是 。
(2)若装置A的质量增加,B的质量不变,则试验气是 ,燃烧的化学方程
式为 。
(3)若装置A的质量不变,B的质量增加,则试验气是 ,B瓶中的化学方
程式是 。
(4)若装置A、B的质量都增加,则试验气是 ;若B的质量增加
克,则A的质量增加 克。
四、计算题(10分)
30.今有氢氧化钠、碳酸氢钠和与其他物质都不反应,受热也不分解的杂质组成的固体
混合物17.110克,放入密闭容器中加热至250℃,经充分反应后,将容器中的气体通入过量的澄清石灰水中得到白色沉淀2.500克;当容器中的残留固体冷却到室温后,全部
溶于水制成50.00毫升溶液,从中取出10.00毫升,恰好可与含HCI1.825克的盐酸溶
液25.00毫升中和至中性,求原混合物中含杂质的质量分数。
1997 年全国初中奥林匹克化学竞赛试题答案
1.B 2.B、D 3.B 4.A 5.C 6.C、D 7.B、D 8.C、D9.A、D 1O.B l1.D l 2.A、B
l3.C l4.B l5.A l6.C l7.A l8.C l9.C 20.A
21.(1)CaO+HO=Ca(OH),
2 2
Ca(OH)+NaCO===CaCO↓+2NaOH
2 2 3 3
Ca(OH)+KCO=CaCO↓+2KOH
2 2 3 3
(2)CS+NaSNaCS PS+3NaS==2NaPS.
2 2 2 2 3 2 5 2 2 4
22.(1)285 C H9ON
17 1 3
(2)硬脂酸 硬脂酸钙 硬脂酸镁
23.(1)Ba2+、OH-
(2)浓硫酸与蔗糖反应,脱去蔗糖中相当于水的组成的氢、氧(即脱水),使蔗糖炭化
24.(1)发生了氧化还原还原剂
(2)2Na+2HO=2NaOH+H↑(其他活泼金属亦可)
2 2
2HO 2H↑+O↑
2 2 2
25.(1)40克 (2)KHSO Ba(NO) KSO KCO
4 3 2 2 4 2 3
26.(1)用蒸馏水将烧碱样品溶解、配成溶液
(2)加入硝酸使溶液的pH<7(用pH试纸试验)
(3)加入硝酸银溶液,若有白色沉淀生成证明有NaCl存在,反之就没有NaCl存在
27.(1)Ag (2)Fe2+、Cu2+、Ag+
28.(1)CaCO (2)在第⑤步蒸发结晶前向滤液中滴加盐酸至不再产生气泡为止
3
(3)固体混合物
29.(1)浓硫酸 NaOH溶液
(2)H 2H+O 2HO
2 2 2 2
(3)CO CO+2NaOH=NaCO+HO
2 2 3 2
(4)CH 9m/11 克
4
四 30.
解:由题意可知NaHCO 过量,NaOH与CO 反应和Na0H与 NaHCO 直接反应所生成的NaCO
3 2 3 2 3
总质量是不变的,取NaHCO 计算更简便,有关反应如下:
3
NaOH+NaHCO=NaCO+HO ①
3 2 3 2
2NaHCO=NaCO+CO↑+H0↑ ②
3 2 3 2 2
CO+Ca(OH)==CaCO++H0 ③
2 2 3 2
NaCO+2HCl=2NaCl+HO+CO↑④
2 3 2 2
(1)设反应②分解的NaHCO 质量为x,分解产生的NaCO 质量为y,由②③有:
3 2 3
2NaHCO~NaCO~CaCO
3 2 3 3
2×84 106 100
x y 2.500克
x=4.200克 y=2.650克(2)设残留物中NaCO 的总质量为z,由①
2 3
有 NaCO~2HCl
2 3
z=13.250克反应①产生的NaCO 质量为 1 3.2 50克一2.65 O克=1 O.600克 l 0.600
2 3
克NaCO 是原混合物中的NaOH(设质量为w)和除发生分解反应之外的NaHCO(设质量为x’)
2 3 3
恰好反应生成的,它们的质量关系是:
NaOH~NaHCO~NaCO
3 2 3
46 84 106
w x’ 10.600克
w=4.000克,x'=8.400克
杂质的质量分数为2.98%
答:略