文档内容
第 17 讲 溶液的酸碱性与 pH 的计算
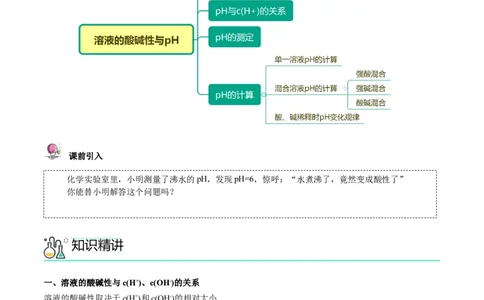
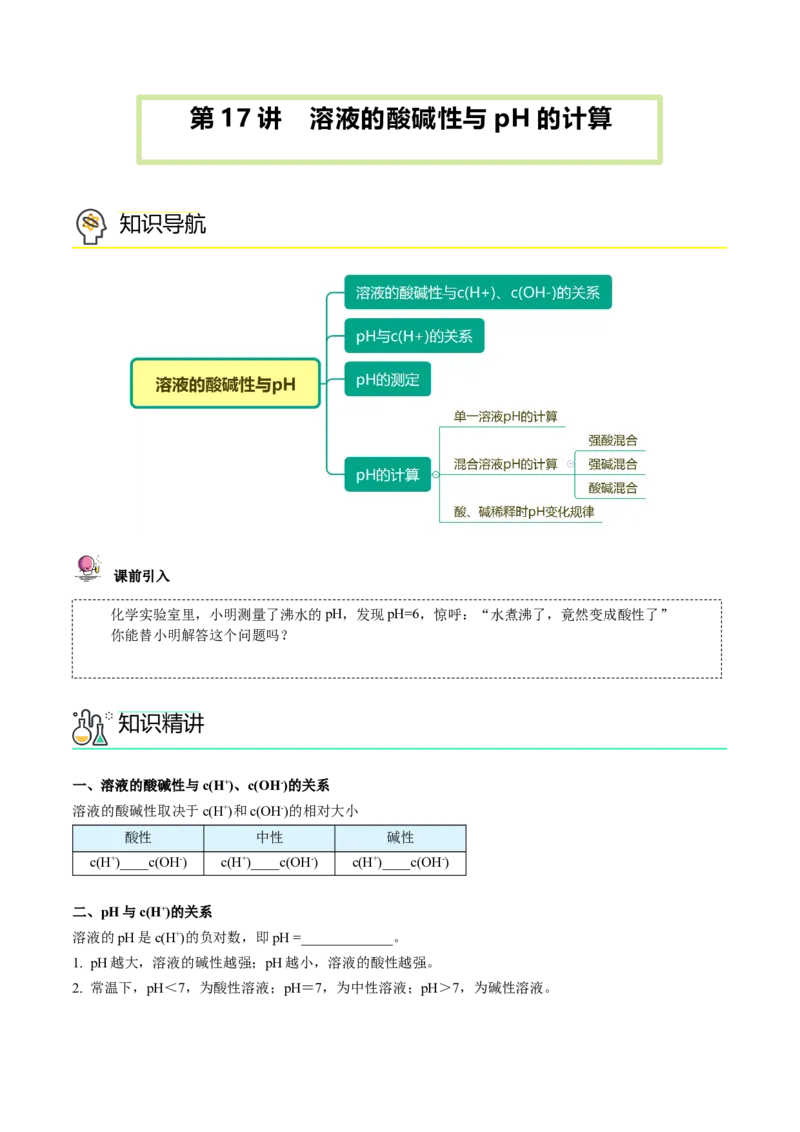
知识导航
小杨老师 15521324728 侵权必究
课前引入
化学实验室里,小明测量了沸水的pH,发现pH=6,惊呼:“水煮沸了,竟然变成酸性了”
你能替小明解答这个问题吗?
杨sir化学,侵权必究
知识精讲
小杨老师 15521324728 侵权必究
一、溶液的酸碱性与c(H+)、c(OH-)的关系
溶液的酸碱性取决于c(H+)和c(OH-)的相对大小
酸性 中性 碱性
c(H+)____c(OH-) c(H+)____c(OH-) c(H+)____c(OH-)
二、pH与c(H+)的关系
杨sir化学,侵权必究
溶液的pH是c(H+)的负对数,即pH =_____________。
1. pH越大,溶液的碱性越强;pH越小,溶液的酸性越强。
2. 常温下,pH<7,为酸性溶液;pH=7,为中性溶液;pH>7,为碱性溶液。思考与交流:求100℃下,NaCl水溶液中c(H+) 与pH。
三、pH的测定
1.pH试纸
(1)使用方法
取一小块pH试纸于干燥洁净的玻璃片或表面皿上,用干燥洁净的玻璃棒蘸取试液点在试纸上,当试纸颜
色变化稳定后迅速与标准比色卡对照,读出pH。
(2)分类
① 广泛pH试纸:其pH范围是 1~14 (最常用),可以识别的pH差约为1。
② 精密pH试纸:可判别0.2或0.3的pH差值。
杨sir化学,侵权必究
③ 专用pH试纸:用于酸性、中性或碱性溶液的专用pH试纸。
2.pH计
pH计,又叫酸度计,可精密测量溶液的pH,其量程为0~14。
注意
② pH试纸不能测定具有漂白性的溶液的pH。
② 不能用湿润的玻璃棒蘸取待测液,也不能将pH试纸先用水润湿,否则溶液被稀释,可能造成误差
(酸性溶液的pH偏大、碱性溶液的pH偏小、中性溶液的pH无影响)。
杨sir化学,侵权必究
四、pH的计算
1.单一溶液pH的计算
(1)酸性溶液中,先求c(H+),再计算pH = -lgc(H+);
K
(2)碱性溶液中,先求c(OH-),再由c(H+) = w 求 c(H+),最后计算pH = -lgc(H+)。
c(OH-) 杨sir化学,侵权必究
2.混合溶液pH的计算
(1)强酸混合,先求 ,再计算pH = -lgc(H+);
K
(2)强碱混合,先求 ,再由 c(H+) = w 求 c(H+),最后计算 pH =
c(OH-)
-lgc(H+)。
(3)强酸强碱混合
① 恰好完全反应,pH=7(25℃);
杨sir化学,侵权必究
② 酸过量,先求 ,再计算pH = -lgc(H+);K
③ 碱过量,先求 ,再由 c(H+) = w 求 c(H+),最后计算 pH =
c(OH-)
-lgc(H+)。
3.酸、碱稀释时pH变化规律
杨sir化学,侵权必究
(1)pH = a 的强酸溶液,稀释10m 倍,pH = a + m(室温下,a+ m<7)
pH = a 的弱酸溶液,稀释10m 倍,a<pH<a + n(室温下,a+ m<7)
(2)pH = b 的强碱溶液,稀释10n 倍,pH = b - n(室温下,b - n>7)
pH = b 的弱酸溶液,稀释10n 倍,b - n<pH<b(室温下,b - n>7)
(3)pH = a 的强酸溶液,稀释一倍(或与可忽略的酸/碱等体积混合),pH = a + 0.3(室温下,a+0.3
<7)
(4)pH = b 的强碱溶液,稀释一倍(或与可忽略的酸/碱等体积混合),pH = b - 0.3(室温下,b - 0.3
>7)
明辨是非
(1)如果c(H+)≠c(OH-),则溶液一定呈一定的酸碱性________;
(2)任何水溶液中都有c(H+)和c(OH-)________;
(3)c(H+)等于10-6 mol·L-1的溶液一定呈现酸性________;
(4)25 ℃时,纯水和烧碱溶液中水的离子积常数不相等________;
(5)在100 ℃时,纯水的pH>7________;
(6)如果c(H+)/ c(OH-)的值越大,则酸性越强 ________;
(7)升高温度,水的电离程度增大,酸性增强 ________;
(8)25 ℃时,0.01 mol·L-1的KOH溶液的pH=12________;
(9)pH减小,溶液的酸性一定增强________;
(10)100 ℃时,0.01 mol·L-1盐酸的pH=2,0.01 mol·L-1的NaOH溶液的pH=10________;
(11)1.0×10-3 mol·L-1盐酸的pH=3,1.0×10-8 mol·L-1盐酸的pH=8 ________;
(12)pH=a的醋酸溶液稀释一倍后,溶液的pH=b,则a>b________。
对点训练
小杨老师 15521324728 侵权必究
题型一:溶液酸碱性的判断
杨sir化学,侵权必究
【变1-1】下列溶液一定呈酸性的是
A.含有H+离子的溶液 B.c(H+)>(K )1/2
w
C.pH小于7的溶液 D.使石蕊试液显紫色的溶液题型二:pH的类似物理量
杨sir化学,侵权必究
【变2】pc类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-
3mol/L,则该溶液溶质的pc=3。下列说法正确的是
A.25°C时,0.01mol/LNa S水溶液中,pc(H+)+pc(OH-)=14
2
B.用0.01mol/L的NaOH溶液滴定某浓度的盐酸,滴定过程中pc(OH-)逐渐增大
C.某温度下,弱酸HB的K=1×10-5mol/L,则该溶液中pc(H+)+pc(B-)=l0
a
D.向0.0lmol/L的Ca(HCO ) 溶液中逐渐滴加烧碱溶液,滴加过程中pc(Ca2+)逐渐减小
3 2
题型三:单一溶液pH的相关计算
杨sir化学,侵权必究
【变3-2】常温下,pH=11的氢氧化钡溶液中,由水电离出的 为
A. B.
C. D.
【变3-5】某溶液中由水电离出的c(H+)=10-10mol·L-1,那么该溶液的pH可能为( )
A.10 B.4 C.10或4 D.11
杨sir化学,侵权必究
题型四:混合溶液pH的相关计算
杨sir化学,侵权必究
【变4-1】已知lg2=0.3,将pH=2和pH=5的稀盐酸等体积混合,混合后溶液的pH约为
A.2.3 B.3.5 C.4.7 D.3
【变5-2】100℃,水的离子积为 ,此温度下,将pH之和为13的HCl和NaOH两溶液混合后溶液
为中性,HCl和NaOH溶液的体积比为
A.1:10 B.10:1 C.100:1 D.1:100
题型五:溶液稀释与pH的相关计算
杨sir化学,侵权必究
【变6-1】常温下,将pH=a的氨水稀释到原体积的100倍,下列有关说法不合理的是
A.NH ·HO的电离平衡向右移动 B.溶液中c(OH-)增大
3 2
C.溶液中c(H+)增大 D.稀释后pH﹥a-2
【变6-3】常温下,pH=10的X、Y两种碱溶液各1mL,分别加水稀释到100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是
A.稀释前,两种碱溶液中溶质的物质的量浓度一定相等
B.稀释后,X溶液的碱性比Y溶液的碱性强
C.完全中和X、Y溶液时,消耗同浓度盐酸的体积:V >V
X Y
D.若8”、“<”或“=”),原因是_______;该温度下 的 溶液的
_______;由水电离出的 _______ 。
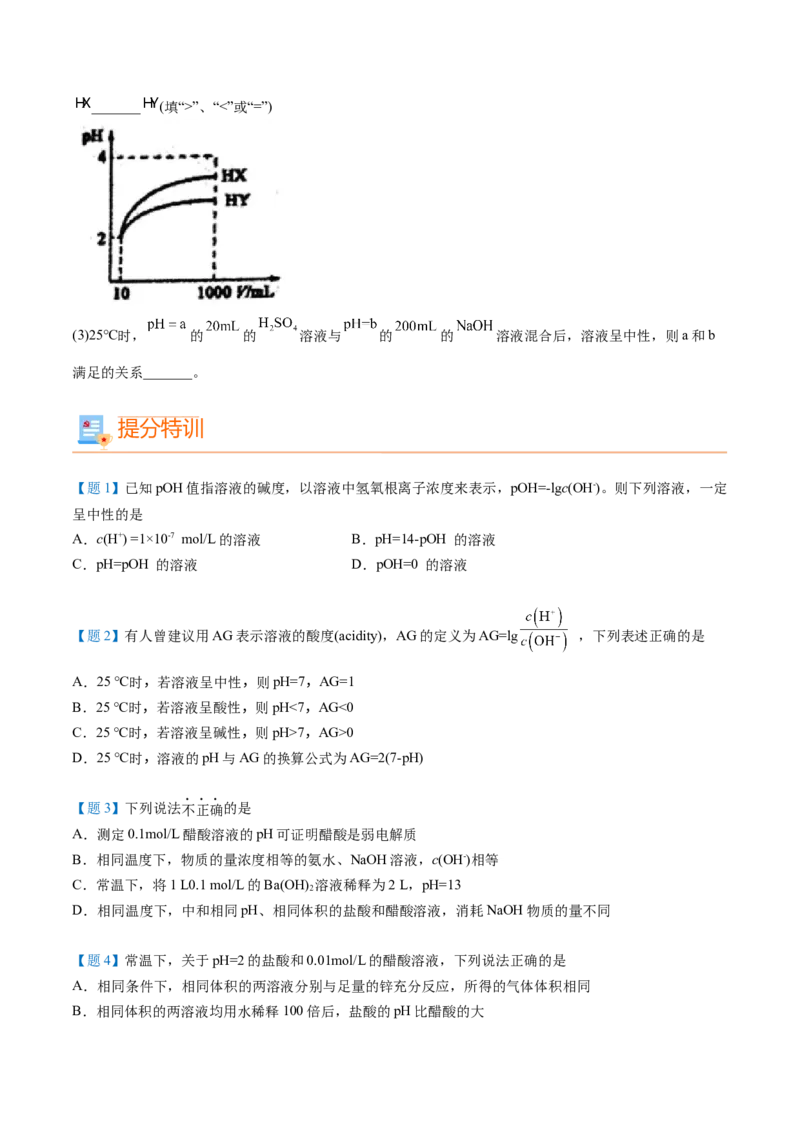
(2)体积均为 、pH均为2的一元酸 与 ,加水稀释过程中pH与溶液体积的关系如图所示,则酸性_______ (填“>”、“<”或“=”)
(3)25℃时, 的 的 溶液与 的 的 溶液混合后,溶液呈中性,则a和b
满足的关系_______。
提分特训
小杨老师 15521324728 侵权必究
【题1】已知pOH值指溶液的碱度,以溶液中氢氧根离子浓度来表示,pOH=-lgc(OH-)。则下列溶液,一定
呈中性的是
A.c(H+) =1×10-7 mol/L的溶液 B.pH=14-pOH 的溶液
C.pH=pOH 的溶液 D.pOH=0 的溶液
【题2】有人曾建议用AG表示溶液的酸度(acidity),AG的定义为AG=lg ,下列表述正确的是
A.25 ℃时,若溶液呈中性,则pH=7,AG=1
B.25 ℃时,若溶液呈酸性,则pH<7,AG<0
C.25 ℃时,若溶液呈碱性,则pH>7,AG>0
D.25 ℃时,溶液的pH与AG的换算公式为AG=2(7-pH)
【题3】下列说法不正确的是
A.测定0.1mol/L醋酸溶液的pH可证明醋酸是弱电解质
B.相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
杨sir化学,侵权必究
C.常温下,将1 L0.1 mol/L的Ba(OH) 溶液稀释为2 L,pH=13
2
D.相同温度下,中和相同pH、相同体积的盐酸和醋酸溶液,消耗NaOH物质的量不同
【题4】常温下,关于pH=2的盐酸和0.01mol/L的醋酸溶液,下列说法正确的是
A.相同条件下,相同体积的两溶液分别与足量的锌充分反应,所得的气体体积相同
B.相同体积的两溶液均用水稀释100倍后,盐酸的pH比醋酸的大C.相同条件下,取同体积两溶液进行导电性实验,灯泡的亮度相同
D.用相同浓度的氢氧化钠分别中和等体积的两溶液至中性,则c(CHCOO-)=c(Cl-)
3
【题5】常温下,下列各混合或稀释后溶液中,pH最大的是
A. 的烧碱溶液稀释1000倍
B. 的氨水稀释1000倍
C. 的醋酸和 的烧碱溶液等体积混合
D. 的盐酸稀释1000倍
杨sir化学,侵权必究
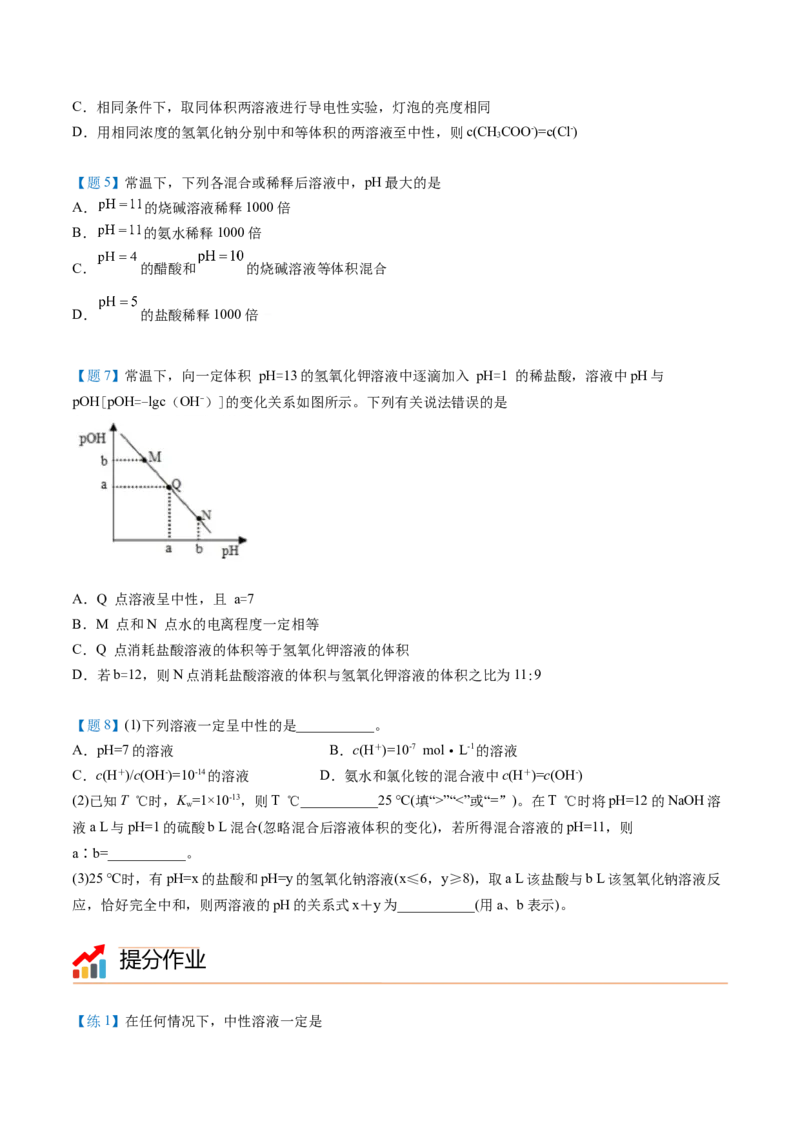
【题7】常温下,向一定体积 pH=13的氢氧化钾溶液中逐滴加入 pH=1 的稀盐酸,溶液中pH与
pOH[pOH=-lgc(OH-)]的变化关系如图所示。下列有关说法错误的是
A.Q 点溶液呈中性,且 a=7
B.M 点和N 点水的电离程度一定相等
C.Q 点消耗盐酸溶液的体积等于氢氧化钾溶液的体积
D.若b=12,则N点消耗盐酸溶液的体积与氢氧化钾溶液的体积之比为11:9
【题8】(1)下列溶液一定呈中性的是___________。
A.pH=7的溶液 B.c(H+)=10-7 mol·L-1的溶液
C.c(H+)/c(OH-)=10-14的溶液 D.氨水和氯化铵的混合液中c(H+)=c(OH-)
(2)已知T ℃时,K =1×10-13,则T ℃___________25 ℃(填“>”“<”或“=”)。在T ℃时将pH=12的NaOH溶
w
液a L与pH=1的硫酸b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=11,则
a∶b=___________。
(3)25 ℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取a L该盐酸与b L该氢氧化钠溶液反
应,恰好完全中和,则两溶液的pH的关系式x+y为___________(用a、b表示)。
杨sir化学,侵权必究
提分作业
小杨老师 15521324728 侵权必究
【练1】在任何情况下,中性溶液一定是A.pH=7 B.c(H+)=c(OH-)
C.c(H+)·c(OH-)=1×10-14 D.c(H+)=c(OH-)=1×10-7
【练2】已知人体体液中存在维持体液pH相对稳定的平衡: CO+ H O HCO H++ ,则下列说
2 2 2 3
法不合理的是
A.当人体体内的酸碱平衡失调时,血液的pH是诊断疾病的一个重要参数
B.如果CO 进入体液,会使体液的pH减小
2
C.当强酸性物质进入体液后,平衡向左移动
杨sir化学,侵权必究
D.静脉滴注生理盐水,体液的pH会有大幅改变
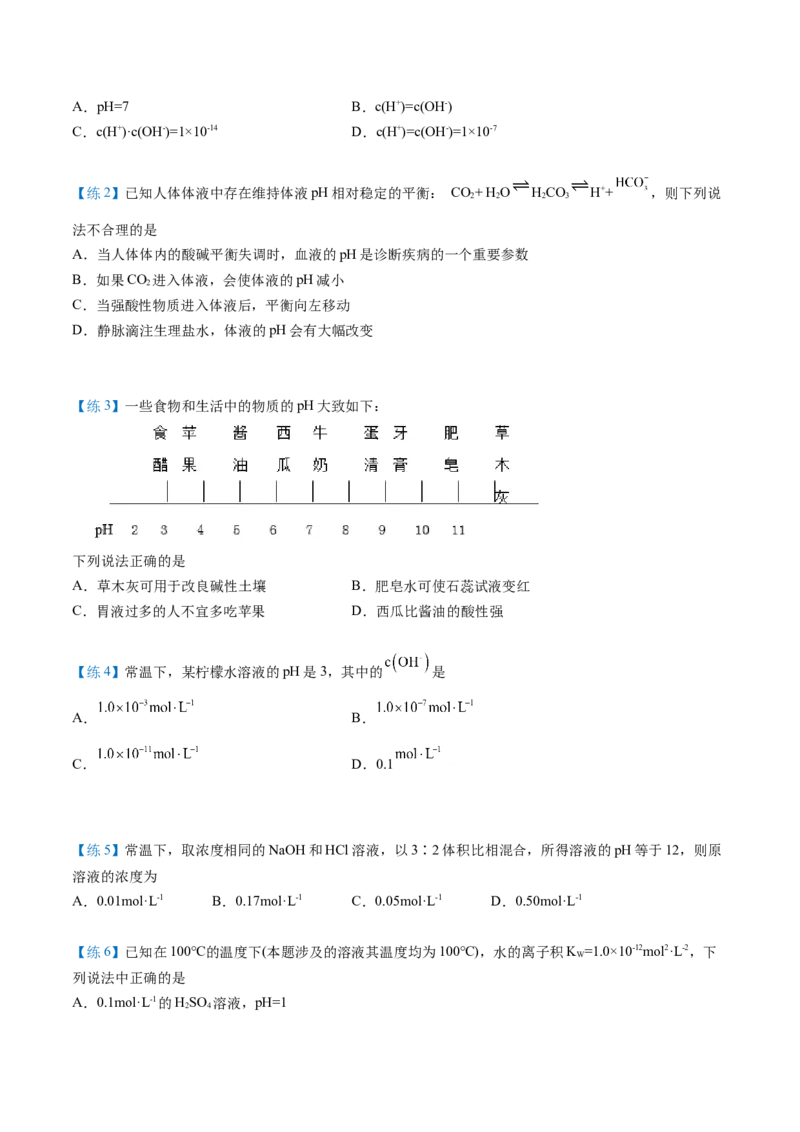
【练3】一些食物和生活中的物质的pH大致如下:
下列说法正确的是
A.草木灰可用于改良碱性土壤 B.肥皂水可使石蕊试液变红
C.胃液过多的人不宜多吃苹果 D.西瓜比酱油的酸性强
【练4】常温下,某柠檬水溶液的pH是3,其中的 是
A. B.
C. D.0.1
杨sir化学,侵权必究
【练5】常温下,取浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12,则原
溶液的浓度为
A.0.01mol·L-1 B.0.17mol·L-1 C.0.05mol·L-1 D.0.50mol·L-1
【练6】已知在100℃的温度下(本题涉及的溶液其温度均为100℃),水的离子积K =1.0×10-12mol2·L-2,下
W
列说法中正确的是
A.0.1mol·L-1的HSO 溶液,pH=1
2 4B.0.001mol·L-1的NaOH溶液,pH=11
C.0.005mol·L-1的HSO 溶液与0.01mol·L-1的NaOH溶液等体积混合,混合溶液的pH为6,溶液显酸性
2 4
D.将pH=8的Ba(OH) 溶液与pH=5的稀盐酸混合,欲使混合溶液的pH=7,则Ba(OH) 溶液与稀盐酸的体
2 2
积比为2:9
【练7】pH=6和pH=3的两种盐酸以等体积混合后,溶液的pH是________。
【练8】已知室温时,0.1 mol·L-1的氨水在水中有 1% 发生电离,回答下列各问题:
(1)溶液的pH=___________。
(2)该温度下NH ·H O的电离平衡常数K=___________ 。
3 2
(3)升高温度时,K将___________(填“增大”、“减小”或“不变”),pH将___________(填“增大”、“减小”或“不
变”)。
杨sir化学,侵权必究
(4)由0.1 mol·L-1的氨水电离出的c(OH-)约为水电离出的c(OH-)的___________倍。
(5)要使溶液中c(OH-)/c(NH·H O)值增大,可以采取的措施是___________ (填序号)。
3 2
①通入少量HCl ②升高温度 ③加少量NaOH固体 ④加水倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育