文档内容
第 15 讲 电离平衡常数
知识导航
小杨老师 15521324728 侵权必究
知识精讲
小杨老师 15521324728 侵权必究
一、电离平衡常数的概念与表达式
杨sir化学,侵权必究
1.概念
在一定条件下,当弱电解质的电离达到平衡时,溶液中弱电解质电离所生成的各种离子浓度的乘积,与溶
液中未电离分子的浓度之比是一个常数,这个常数叫做电离平衡常数,简称电离常数,用 K 表示(通常
用K、K 分别表示弱酸、弱碱的电离平衡常数)。
a b 杨sir化学,侵权必究
2.表示方法
(1)一元弱酸、弱碱
电离方程式 电离常数表达式
c(H+)·c(CH3COO-)
CHCOOH CHCOOH ⇌ CHCOO- + H+ K=
3 3 3 a c(CH3COOH)
c(NH+)·c(OH-)
NH ·H O NH ·H O ⇌ NH ++ OH- K = 4
3 2 3 2 4 b c(NH3·H2O)
(2)多元弱酸、弱碱
电离方程式 电离常数表达式c(H+)·c(HCO-)
K = 3
HCO ⇌ H+ +HCO- 1 c(H2CO3)
HCO 2 3 3
2 3
HCO - ⇌ H+
+CO2- c(H+)·c(CO2-)
3 3 K = 3
2 c(HCO-)
3
c(Cu2+ )·c2(OH-)
Cu(OH) Cu(OH) ⇌Cu2+ + 2OH- K=
2 2 c[Cu(OH)2]
二、电离平衡常数的意义
1. 意义
电离平衡常数表示弱电解质的电离能力。一定温度下,K值越大,弱电解质的电离程度越大,酸性(或碱
性)越强。
杨sir化学,侵权必究
2. 实例
下表是几种弱酸常温下的电离平衡常数,则酸性强弱顺序为:CHCOOH>HCO>HS> >HS-
3 2 3 2 HCO-
3
CHCOOH HCO HS
3 2 3 2
K =4.3×10-7 K =9.1×10-8
K=1.8×10-5 1 1
K =5.6×10-11 K =1.1×10-12
2 2
三、电离平衡常数的影响因素
1. 内因:弱电解质本身的性质。
2. 外因:电离平衡常数只跟温度有关,温度升高,电离平衡常数增大。
杨sir化学,侵权必究
四、电离度
1. 概念:弱电解质达电离平衡时,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的)的
百分数。
2. 影响因素
①内因:弱电解质本身的性质
②外因:温度及浓度
3. 意义:表示不同弱电解质在水溶液中的电离程度,在相等条件下可用电离度比较弱电解质的相对强弱。
五、电离常数的计算
1. 列出“三段式”
2. 由于弱电解质的电离程度比较小,最终计算时,一般弱电解质的平衡浓度≈起始浓度(即忽略弱电解质
电离的部分)。
杨sir化学,侵权必究
举个例子例:25 ℃ a mol·L-1的CHCOOH
3
CHCOOH ⇌CHCOO-+H+
3 3
起始浓度/mol·L-1 a 0 0
变化浓度/mol·L-1 x x x
平衡浓度/mol·L-1 a-x x x
c(H+)·c(CH3COO-)
则K= = ≈
a c(CH3COOH)
六、弱酸与盐溶液的反应规律
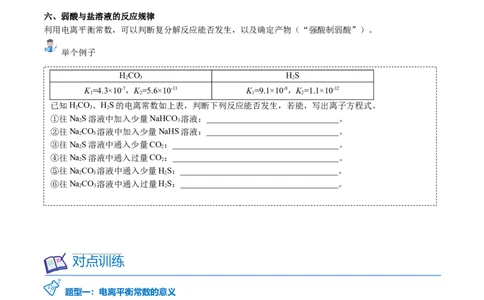
利用电离平衡常数,可以判断复分解反应能否发生,以及确定产物(“强酸制弱酸”)。
举个例子
HCO HS
2 3 2
K =4.3×10-7,K =5.6×10-11 K =9.1×10-8,K =1.1×10-12
1 2 1 2
已知HCO、HS的电离常数如上表,判断下列反应能否发生,若能,写出离子方程式。
2 3 2
①往NaS溶液中加入少量NaHCO 溶液:_______________________________。
2 3
②往NaCO 溶液中加入少量NaHS溶液:_______________________________。
2 3
③往NaS溶液中通入少量CO:_______________________________________。
2 2
④往NaS溶液中通入过量CO:_______________________________________。
2 2
⑤往NaCO 溶液中通入少量HS:_____________________________________。
2 3 2
⑥往NaCO 溶液中通入过量HS:_____________________________________。
2 3 2
对点训练
小杨老师 15521324728 侵权必究
题型一:电离平衡常数的意义
杨sir化学,侵权必究
【例1】下表是几种弱酸在常温下的电离平街常数:
CHCOOH HCO HS HPO
3 2 3 2 3 4
K =7.5×10-3
a1
K =4.3×10-7 K =9.1×10-8
a1 a1
1.8×10-5 K =6.2×10-8
a2
K =5.6×10-11 K =1.1×10-12
a2 a2
K =2.2×10-13
a3
则下列说法中不正确的是
A.碳酸的酸性强于氢硫酸B.多元弱酸的酸性主要由第一步电离决定
C.常温下,加水稀释醋酸, 增大
D.向弱酸溶液中加少量NaOH溶液,电离平衡常数不变
题型二:根据电离常数书写方程式
杨sir化学,侵权必究
【变2-2】部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HCN HCO
2 3
K =4.3×10-7
i1
电离平衡常数(25℃) K=1.77×10-4 K=4.9×10-10
i i
K =5.6×10-11
i2
下列选项错误的是
A.CN-+H O+CO=HCN+
2 2
B.2HCOOH+ =2HCOO-+H O+CO↑
2 2
C.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D.等浓度的HCOOH和HCN稀释相同的倍数后PH前者大于后者
题型三:电离平衡移动
杨sir化学,侵权必究
【变3】已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CHCOOH CHCOO-+H+,要使溶液中
3 3
增大,可以采取的措施是
①加少量烧碱固体 ②升高温度 ③加少量冰醋酸 ④加水 ⑤加少量醋酸钠固体
A.②④ B.②③⑤ C.③④⑤ D.①②
杨sir化学,侵权必究
题型四:电离平衡常数综合
杨sir化学,侵权必究【例4】已知25 ℃时,电离平衡常数:
化学式 CHCOOH HCO HClO
3 2 3
电离平衡常数 1.8×10-5 K=4.4×10-7 K=4.7×10-11 3.0×10-8
1 2
回答下列问题:
(1)下列四种物质电离出质子的能力由大到小的顺序是___________(填标号)。
a.HCO - b.HClO c.CHCOOH d.HCO
3 3 2 3
(2)下列反应不能发生的是___________。
A.
B.ClO-+CH COOH=CH COO-+HClO
3 3
C.
D.
(3)用蒸馏水稀释0.10 mol·L-1的醋酸,则下列各式表示的数值随水量的增加而增大的是___________。
A. B. C. D.
【变4-2】25℃时,部分物质的电离平衡常数如表所示:
化学式 CHCOOH HCO HClO HCN
3 2 3
K =4.3×10-7
a1
电离平衡常数(K) 1.8×10-5 3.0×10-8 5.0×10-10
a
K =5.6×10-11
a2
请回答下列问题:
(1)CH COOH、HCO、HClO、HCN的酸性由强到弱的顺序_____。
3 2 3
(2)向NaCN中通入少量的CO,发生反应的离子方程式为_____。
2
(3)取0.10molCHCOOH(冰醋酸)作导电性实验,测得其平衡时的导电率随加入的水量变化如图所示:
3
①常温下,b点醋酸溶液的浓度约为0.02molL-1,该溶液中的CHCOOH的电离度为_____,若使此溶液中
3
⋅CHCOOH的电离程度增大且c(H+)也增大的方法是_____。
3
②从图像可知,在一定浓度的醋酸溶液中加水,c(CHCOO-)_____(填“增大”,“减小”或“不确定”)。
3
③若实验测得c点处溶液中c(CHCOOH)=amol L-1,c(CHCOO-)=bmolL-1,则该条件下CHCOOH的电离
3 3 3
常数K=_____。(用含a、b的代数式表示) ⋅ ⋅
a
④H+浓度相同等体积的两份溶液A(盐酸)和B(CHCOOH)分別与不同质量的锌粉反应,若最后仅有一份溶
3
液中存在锌,放出氢气的质量相同,则下列说法正确的是_____(填写序号)。
a.反应所需要的时间:B>A b.开始反应时的速率:A>B
c.参加反应的锌物质的量:A=B d.A中有锌剩余
杨sir化学,侵权必究
提分特训
小杨老师 15521324728 侵权必究
【题1】已知25℃时有关弱酸的电离平衡常数如下表所示,则下列有关说法正确的是
弱酸化学式 CHCOOH HCN HCO
3 2 3
K =4.3×10−7
电离平衡常 1
1.8×10−5 4.9×10−10
数 K =5.6×10−11
2
A.等物质的量浓度的各溶液pH关系为:pH(CH COOH)<pH(H CO)<pH(HCN)
3 2 3
B.醋酸溶液加水稀释,其电离程度先增大后减小
杨sir化学,侵权必究
C.NaCN中通入少量CO 发生的化学反应为:NaCN+CO+H O=HCN+NaHCO
2 2 2 3
D.HCO 的电离常数表达式:
2 3
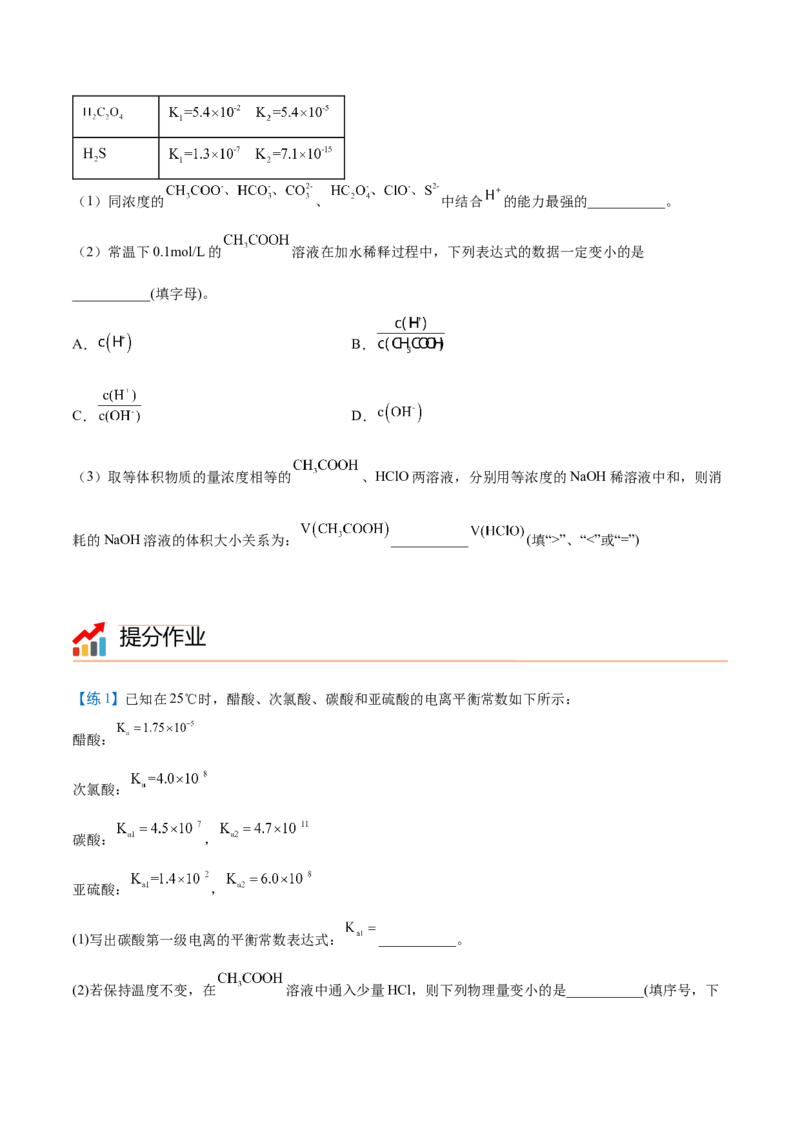
【题3】结合下表回答下列问题(均为常温下的数据):请回答下列问题:
酸 电离常数(Ka)
HClO(1)同浓度的 、 中结合 的能力最强的___________。
(2)常温下0.1mol/L的 溶液在加水稀释过程中,下列表达式的数据一定变小的是
___________(填字母)。
杨sir化学,侵权必究
A. B.
C. D.
(3)取等体积物质的量浓度相等的 、HClO两溶液,分别用等浓度的NaOH稀溶液中和,则消
耗的NaOH溶液的体积大小关系为: ___________ (填“>”、“<”或“=”)
提分作业
小杨老师 15521324728 侵权必究
【练1】已知在25℃时,醋酸、次氯酸、碳酸和亚硫酸的电离平衡常数如下所示:
醋酸:
次氯酸:
碳酸: ,
亚硫酸: ,
(1)写出碳酸第一级电离的平衡常数表达式: ___________。
(2)若保持温度不变,在 溶液中通入少量HCl,则下列物理量变小的是___________(填序号,下同)。
a. b.c(H+) c. 的电离平衡常数
(3)下列离子方程式错误的是___________。
a.少量 通入次氯酸钠溶液中:
b.少量 通入次氯酸钙溶液中:
c.过量 通入澄清石灰水中:
杨sir化学,侵权必究
【练2】已知在 时,醋酸、次氯酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸 次氯酸
碳酸 亚硫酸
(1)写出亚硫酸的第一步电离平衡常数表达式 _______。
(2)在相同条件下, 、 、 和 结合 的能力由弱到强的顺序是_______。
(3)若保持温度不变,在醋酸溶液中通入少量 气体,下列量会变小的是_______(填字母序号,下同)。
a. b. c.醋酸的电离平衡常数
(4)下列离子方程式中正确的是的是_______。
A.少量 通入次氯酸钠溶液中:
B.少量 通入次氯酸钙溶液中:
C.过量 通入氢氧化钠溶液中:
杨sir化学,侵权必究
【练3】回答下列问题:
(1)已知室温时,0.1 mol∙L-1某一元酸HA在水中有0.1%发生电离,回答下列问题:①该溶液中c(H+)=_______ mol∙L-1
②HA的电离平衡常数K=_______。
③由HA电离出的c(H+)约为水电离出的c(H+)的_______倍。
杨sir化学,侵权必究
(2)部分弱酸的电离平衡常数如表:用“>”“<”或“=”填空。
弱酸 HCOOH HCO HClO
2 3
K=4.4×10-7
电离平衡常数/25 1
K=1.77×10-4 3.0×10-8
℃ K=4.7×10-11
2
①在相同浓度的HCOOH和HClO的溶液中,溶液导电能力:HCOOH_______HClO。
② 的电离平衡常数表达式为_______
③将少量CO 气体通入NaClO溶液中,写出该反应离子方程式_______。
2倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育