文档内容
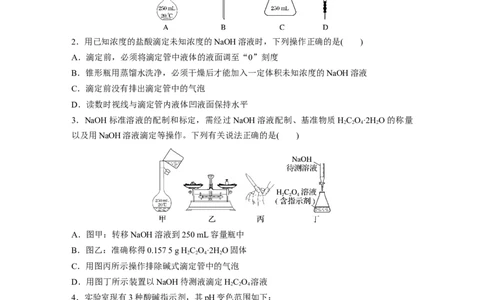
1.(2021·广东,7)测定浓硫酸试剂中HSO 含量的主要操作包括:①量取一定量的浓硫酸,
2 4
稀释;②转移定容得待测液;③移取20.00 mL待测液,用0.100 0 mol·L-1的NaOH溶液滴
定。上述操作中,不需要用到的仪器为( )
2.用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作正确的是( )
A.滴定前,必须将滴定管中液体的液面调至“0”刻度
B.锥形瓶用蒸馏水洗净,必须干燥后才能加入一定体积未知浓度的NaOH溶液
C.滴定前没有排出滴定管中的气泡
D.读数时视线与滴定管内液体凹液面保持水平
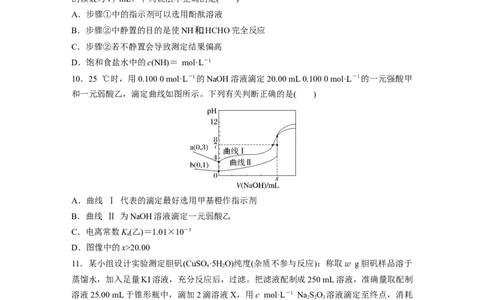
3.NaOH标准溶液的配制和标定,需经过NaOH溶液配制、基准物质HC O·2H O的称量
2 2 4 2
以及用NaOH溶液滴定等操作。下列有关说法正确的是( )
A.图甲:转移NaOH溶液到250 mL容量瓶中
B.图乙:准确称得0.157 5 g HC O·2H O固体
2 2 4 2
C.用图丙所示操作排除碱式滴定管中的气泡
D.用图丁所示装置以NaOH待测液滴定HC O 溶液
2 2 4
4.实验室现有3种酸碱指示剂,其pH变色范围如下:
甲基橙:3.1~4.4 石蕊:5.0~8.0
酚酞:8.2~10.0
用0.100 0 mol·L-1NaOH溶液滴定未知浓度的CHCOOH溶液,恰好完全反应时,下列叙述
3
正确的是( )
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂5.(2023·天津和平区统考模拟)用标准盐酸滴定未知浓度的NaOH溶液,下列各操作中,不
会引起实验误差的是( )
A.用甲基橙作指示剂,当溶液由黄色变为橙色,立即读数,停止滴定
B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗后装入一定体积的NaOH溶液
C.取10.00 mL NaOH溶液放入洗净的锥形瓶中,再加入适量蒸馏水
D.取10.00 mL NaOH溶液放入锥形瓶后,把碱式滴定管尖嘴处液滴吹去
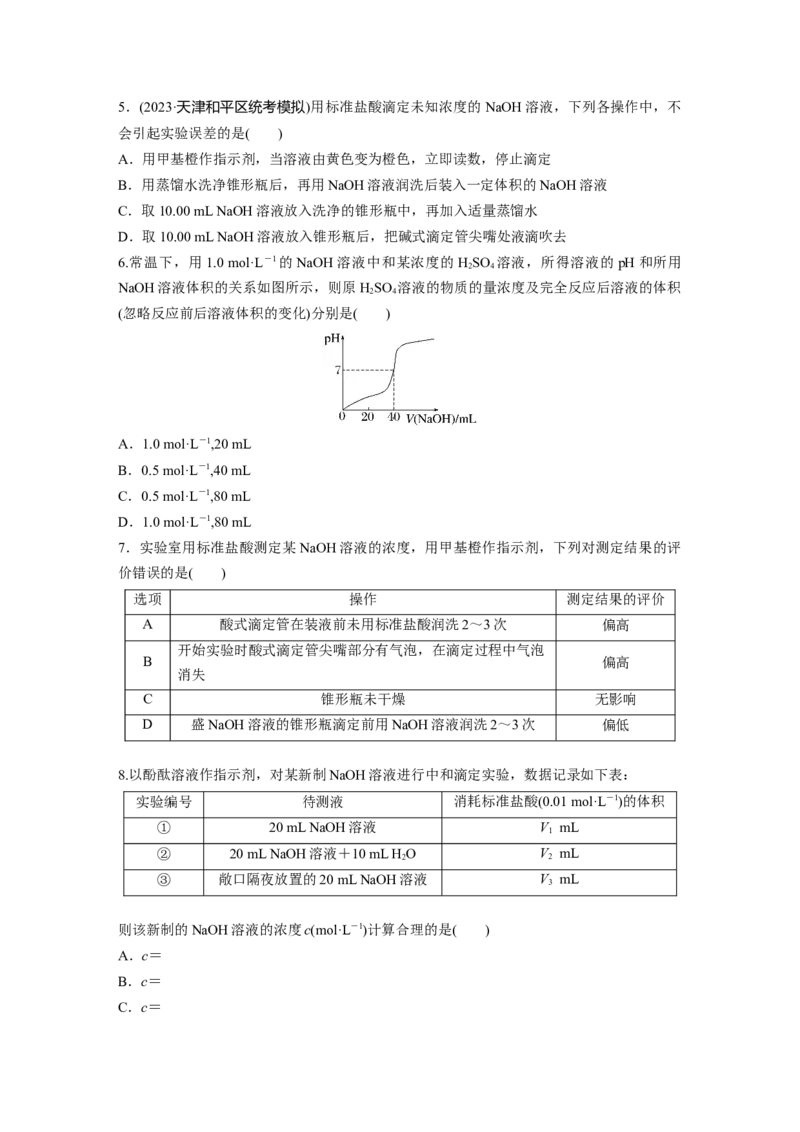
6.常温下,用1.0 mol·L-1的NaOH溶液中和某浓度的HSO 溶液,所得溶液的pH和所用
2 4
NaOH溶液体积的关系如图所示,则原HSO 溶液的物质的量浓度及完全反应后溶液的体积
2 4
(忽略反应前后溶液体积的变化)分别是( )
A.1.0 mol·L-1,20 mL
B.0.5 mol·L-1,40 mL
C.0.5 mol·L-1,80 mL
D.1.0 mol·L-1,80 mL
7.实验室用标准盐酸测定某NaOH溶液的浓度,用甲基橙作指示剂,下列对测定结果的评
价错误的是( )
选项 操作 测定结果的评价
A 酸式滴定管在装液前未用标准盐酸润洗2~3次 偏高
开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡
B 偏高
消失
C 锥形瓶未干燥 无影响
D 盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 偏低
8.以酚酞溶液作指示剂,对某新制NaOH溶液进行中和滴定实验,数据记录如下表:
实验编号 待测液 消耗标准盐酸(0.01 mol·L-1)的体积
① 20 mL NaOH溶液 V mL
1
② 20 mL NaOH溶液+10 mL H O V mL
2 2
③ 敞口隔夜放置的20 mL NaOH溶液 V mL
3
则该新制的NaOH溶液的浓度c(mol·L-1)计算合理的是( )
A.c=
B.c=
C.c=D.c=
9.生产和实验中广泛采用甲醛法测定饱和食盐水样品中的 NH含量。利用的反应原理为
4NH+6HCHO===(CH)NH+(一元酸)+3H++6HO。实验步骤如下:
2 6 4 2
①甲醛中常含有微量甲酸,应先除去。取甲醛a mL于锥形瓶中,加入1~2滴指示剂,用
浓度为b mol·L-1的NaOH溶液滴定,滴定管的初始读数为V mL,当锥形瓶内溶液呈微红
1
色时,滴定管的读数为V mL。
2
②向锥形瓶中加入饱和食盐水试样c mL,静置1分钟。
③用上述滴定管中剩余的NaOH溶液继续滴定锥形瓶内溶液,至溶液呈微红色时,滴定管
的读数为V mL。下列说法不正确的是( )
3
A.步骤①中的指示剂可以选用酚酞溶液
B.步骤②中静置的目的是使NH和HCHO完全反应
C.步骤②若不静置会导致测定结果偏高
D.饱和食盐水中的c(NH)= mol·L-1
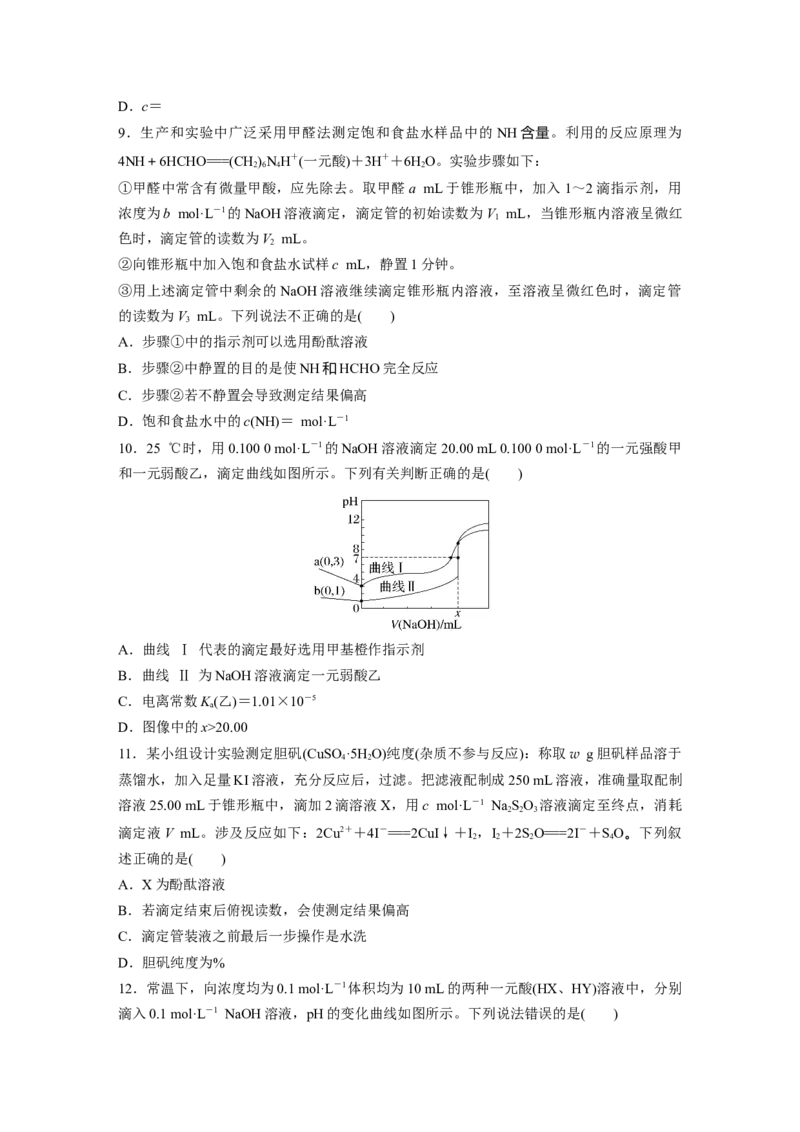
10.25 ℃时,用0.100 0 mol·L-1的NaOH溶液滴定20.00 mL 0.100 0 mol·L-1的一元强酸甲
和一元弱酸乙,滴定曲线如图所示。下列有关判断正确的是( )
A.曲线 Ⅰ 代表的滴定最好选用甲基橙作指示剂
B.曲线 Ⅱ 为NaOH溶液滴定一元弱酸乙
C.电离常数K(乙)=1.01×10-5
a
D.图像中的x>20.00
11.某小组设计实验测定胆矾(CuSO ·5H O)纯度(杂质不参与反应):称取w g胆矾样品溶于
4 2
蒸馏水,加入足量KI溶液,充分反应后,过滤。把滤液配制成250 mL溶液,准确量取配制
溶液25.00 mL于锥形瓶中,滴加2滴溶液X,用c mol·L-1 Na SO 溶液滴定至终点,消耗
2 2 3
滴定液V mL。涉及反应如下:2Cu2++4I-===2CuI↓+I ,I +2SO===2I-+SO。下列叙
2 2 2 4
述正确的是( )
A.X为酚酞溶液
B.若滴定结束后俯视读数,会使测定结果偏高
C.滴定管装液之前最后一步操作是水洗
D.胆矾纯度为%
12.常温下,向浓度均为0.1 mol·L-1体积均为10 mL的两种一元酸(HX、HY)溶液中,分别
滴入0.1 mol·L-1 NaOH溶液,pH的变化曲线如图所示。下列说法错误的是( )A.N点:c(Na+)=c(Y-)+c(HY)
B.M点:c(X-)>c(Na+)
C.滴至pH=7时,消耗NaOH溶液的体积:HX溶液>HY溶液
D.滴入10 mL NaOH溶液时,溶液中水的电离程度:HX溶液<HY溶液
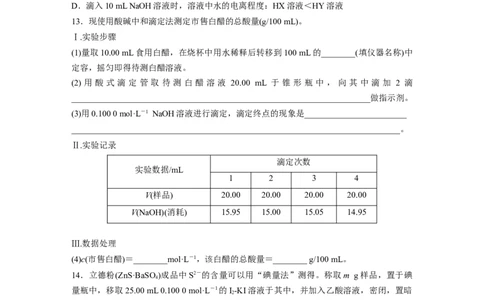
13.现使用酸碱中和滴定法测定市售白醋的总酸量(g/100 mL)。
Ⅰ.实验步骤
(1)量取10.00 mL食用白醋,在烧杯中用水稀释后转移到100 mL的________(填仪器名称)中
定容,摇匀即得待测白醋溶液。
(2) 用 酸 式 滴 定 管 取 待 测 白 醋 溶 液 20.00 mL 于 锥 形 瓶 中 , 向 其 中 滴 加 2 滴
______________________________________________________________________做指示剂。
(3)用0.100 0 mol·L-1 NaOH溶液进行滴定,滴定终点的现象是________________________
_____________________________________________________________________________。
Ⅱ.实验记录
滴定次数
实验数据/mL
1 2 3 4
V(样品) 20.00 20.00 20.00 20.00
V(NaOH)(消耗) 15.95 15.00 15.05 14.95
Ⅲ.数据处理
(4)c(市售白醋)=________mol·L-1,该白醋的总酸量=________ g/100 mL。
14.立德粉(ZnS·BaSO )成品中S2-的含量可以用“碘量法”测得。称取m g样品,置于碘
4
量瓶中,移取25.00 mL 0.100 0 mol·L-1的I-KI溶液于其中,并加入乙酸溶液,密闭,置暗
2
处反应5 min,有单质硫析出。以淀粉为指示剂,过量的I 用0.100 0 mol·L-1 Na SO 溶液
2 2 2 3
滴定,反应式为I +2SO===2I-+SO。测定时消耗NaSO 溶液的体积为V mL。终点颜色
2 2 4 2 2 3
变化为________________________,样品中S2-的含量为________________(写出表达式)。
15.中华人民共和国国家标准规定葡萄酒中SO 最大使用量为0.25 g·L-1。某兴趣小组用如
2
图装置(夹持装置略)收集某葡萄酒中SO ,并对其含量进行测定。
2(1)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO 全部逸出并与C中HO 完全反应,C
2 2 2
中反应的化学方程式为__________________________________________________________
_____________________________________________________________________________。
(2)除去C中过量的HO ,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,简述滴定前排
2 2
气泡的操作:____________________________________________________________________
_____________________________________________________________________________。
(3)①若滴定终点时溶液的pH=8.8,则选择的指示剂为____________;描述达到滴定终点
的现象:________________________________________________________________________
_____________________________________________________________________________。
②若滴定终点时溶液的pH=4.2,则选择的指示剂为__________;描述达到滴定终点的现象:
_____________________________________________________________________________
_____________________________________________________________________________。
(4)若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
________(填序号)。
①=10 mL ②=40 mL ③<10 mL ④>40 mL
(5)滴定至终点时,消耗 NaOH 溶液 25.00 mL,列式计算该葡萄酒中 SO 含量:
2
_____________________________________________________________________________
_____________________________________________________________________________
_____________________________________________________________________________。
(6)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施:_______________
_____________________________________________________________________________。