文档内容
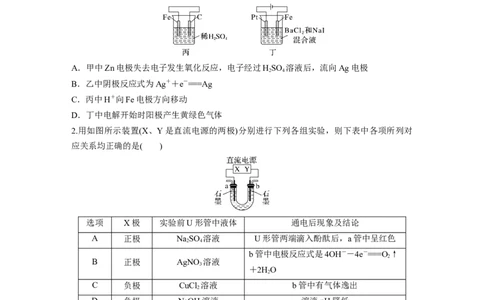
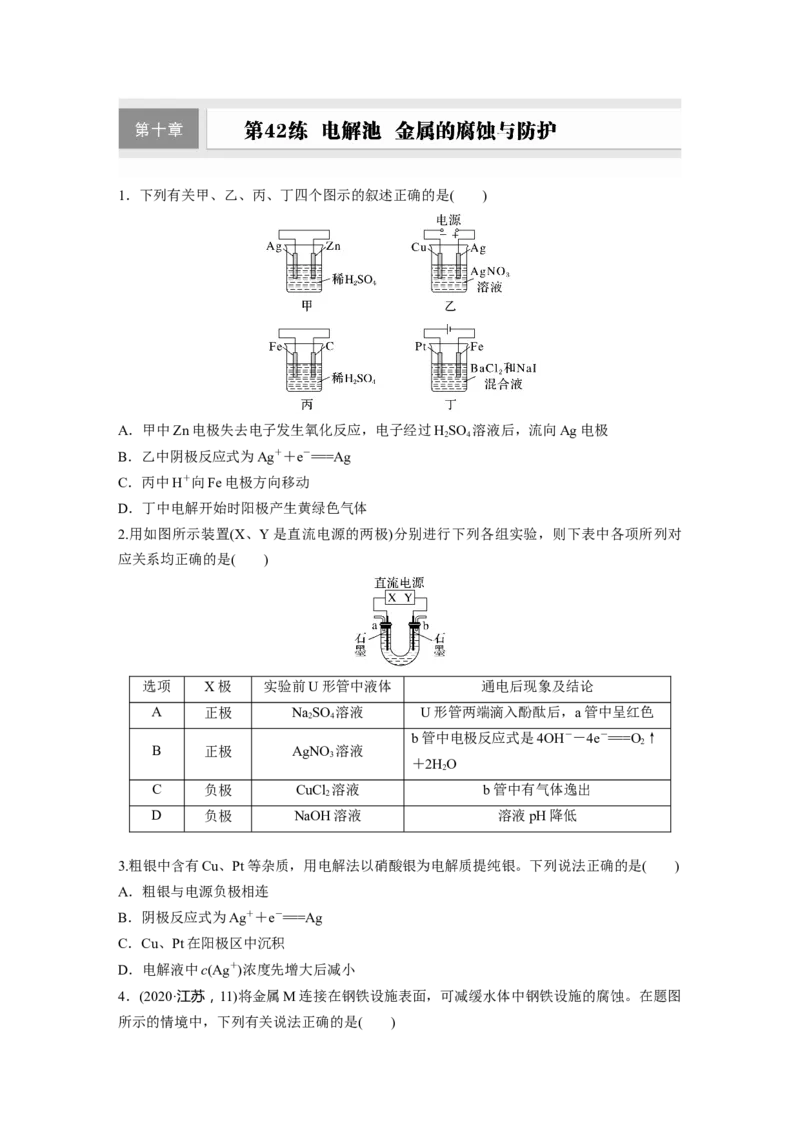
1.下列有关甲、乙、丙、丁四个图示的叙述正确的是( )
A.甲中Zn电极失去电子发生氧化反应,电子经过HSO 溶液后,流向Ag电极
2 4
B.乙中阴极反应式为Ag++e-===Ag
C.丙中H+向Fe电极方向移动
D.丁中电解开始时阳极产生黄绿色气体
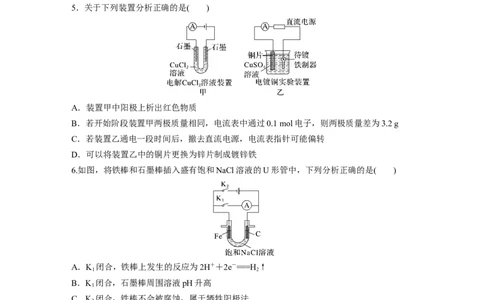
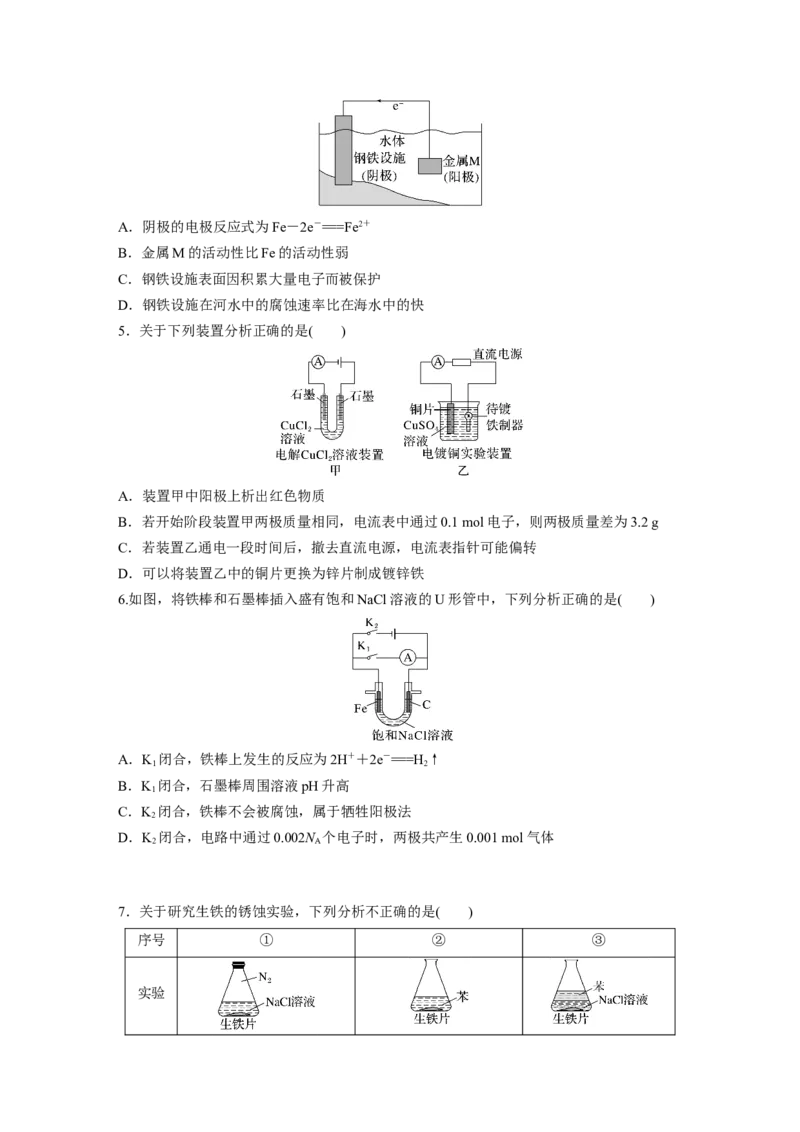
2.用如图所示装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中各项所列对
应关系均正确的是( )
选项 X极 实验前U形管中液体 通电后现象及结论
A 正极 NaSO 溶液 U形管两端滴入酚酞后,a管中呈红色
2 4
b管中电极反应式是4OH--4e-===O ↑
2
B 正极 AgNO 溶液
3
+2HO
2
C 负极 CuCl 溶液 b管中有气体逸出
2
D 负极 NaOH溶液 溶液pH降低
3.粗银中含有Cu、Pt等杂质,用电解法以硝酸银为电解质提纯银。下列说法正确的是( )
A.粗银与电源负极相连
B.阴极反应式为Ag++e-===Ag
C.Cu、Pt在阳极区中沉积
D.电解液中c(Ag+)浓度先增大后减小
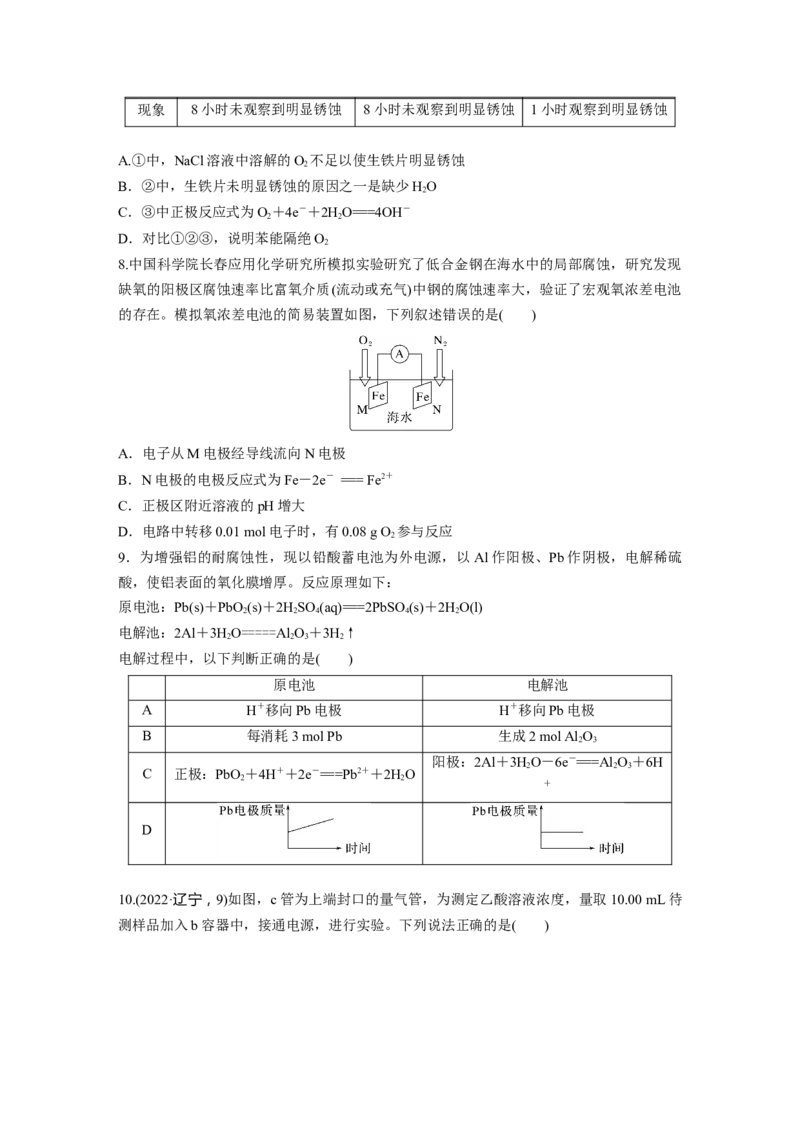
4.(2020·江苏,11)将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图
所示的情境中,下列有关说法正确的是( )A.阴极的电极反应式为Fe-2e-===Fe2+
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
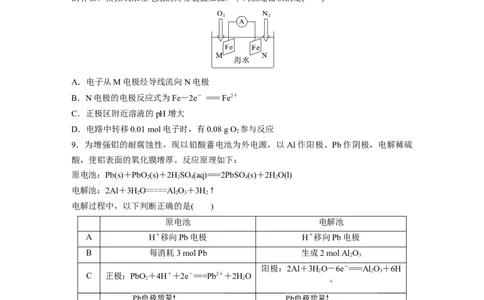
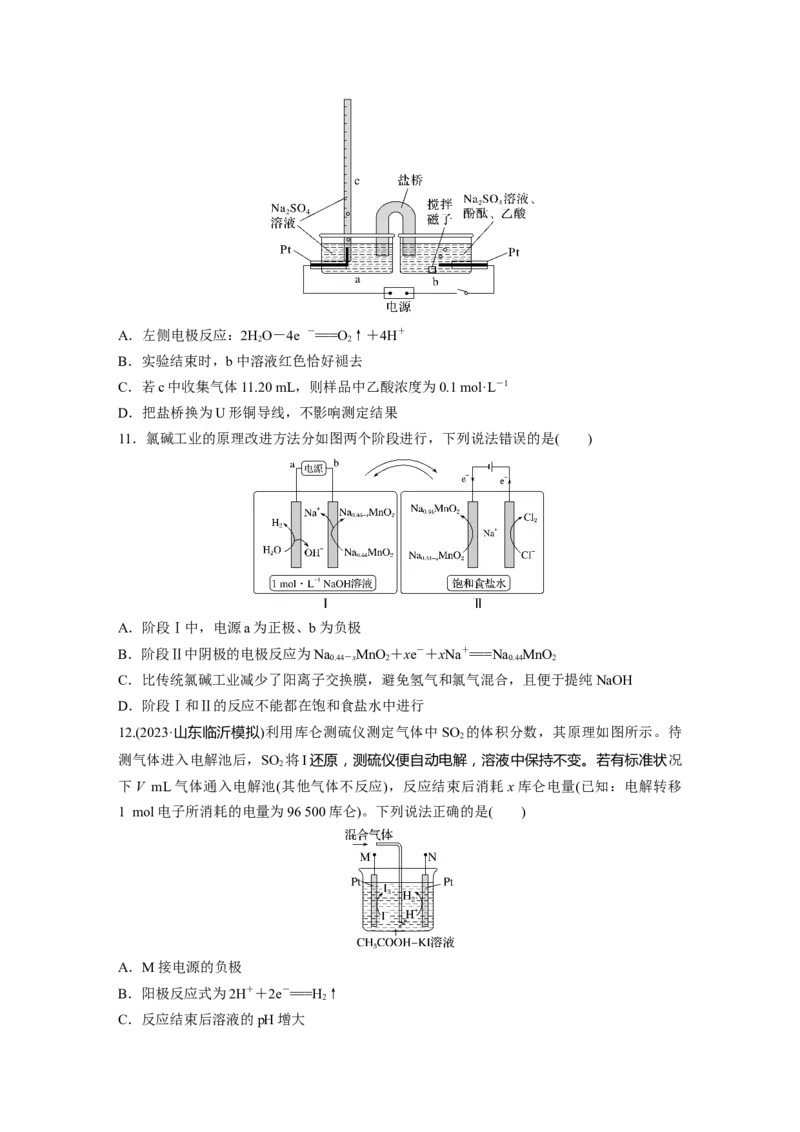
5.关于下列装置分析正确的是( )
A.装置甲中阳极上析出红色物质
B.若开始阶段装置甲两极质量相同,电流表中通过0.1 mol电子,则两极质量差为3.2 g
C.若装置乙通电一段时间后,撤去直流电源,电流表指针可能偏转
D.可以将装置乙中的铜片更换为锌片制成镀锌铁
6.如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是( )
A.K 闭合,铁棒上发生的反应为2H++2e-===H ↑
1 2
B.K 闭合,石墨棒周围溶液pH升高
1
C.K 闭合,铁棒不会被腐蚀,属于牺牲阳极法
2
D.K 闭合,电路中通过0.002N 个电子时,两极共产生0.001 mol气体
2 A
7.关于研究生铁的锈蚀实验,下列分析不正确的是( )
序号 ① ② ③
实验现象 8小时未观察到明显锈蚀 8小时未观察到明显锈蚀 1小时观察到明显锈蚀
A.①中,NaCl溶液中溶解的O 不足以使生铁片明显锈蚀
2
B.②中,生铁片未明显锈蚀的原因之一是缺少HO
2
C.③中正极反应式为O+4e-+2HO===4OH-
2 2
D.对比①②③,说明苯能隔绝O
2
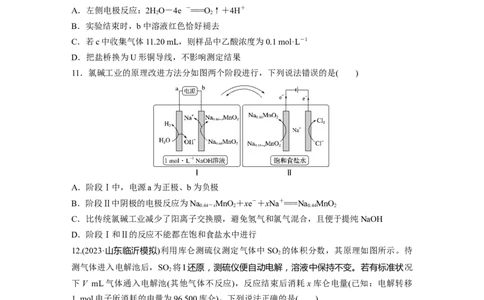
8.中国科学院长春应用化学研究所模拟实验研究了低合金钢在海水中的局部腐蚀,研究发现
缺氧的阳极区腐蚀速率比富氧介质(流动或充气)中钢的腐蚀速率大,验证了宏观氧浓差电池
的存在。模拟氧浓差电池的简易装置如图,下列叙述错误的是( )
A.电子从M电极经导线流向N电极
B.N电极的电极反应式为Fe-2e- === Fe2+
C.正极区附近溶液的pH增大
D.电路中转移0.01 mol电子时,有0.08 g O 参与反应
2
9.为增强铝的耐腐蚀性,现以铅酸蓄电池为外电源,以 Al作阳极、Pb作阴极,电解稀硫
酸,使铝表面的氧化膜增厚。反应原理如下:
原电池:Pb(s)+PbO (s)+2HSO (aq)===2PbSO(s)+2HO(l)
2 2 4 4 2
电解池:2Al+3HO=====Al O+3H↑
2 2 3 2
电解过程中,以下判断正确的是( )
原电池 电解池
A H+移向Pb电极 H+移向Pb电极
B 每消耗3 mol Pb 生成2 mol Al O
2 3
阳极:2Al+3HO-6e-===AlO+6H
2 2 3
C 正极:PbO +4H++2e-===Pb2++2HO
2 2
+
D
10.(2022·辽宁,9)如图,c管为上端封口的量气管,为测定乙酸溶液浓度,量取10.00 mL待
测样品加入b容器中,接通电源,进行实验。下列说法正确的是( )A.左侧电极反应:2HO-4e -===O ↑+4H+
2 2
B.实验结束时,b中溶液红色恰好褪去
C.若c中收集气体11.20 mL,则样品中乙酸浓度为0.1 mol·L-1
D.把盐桥换为U形铜导线,不影响测定结果
11.氯碱工业的原理改进方法分如图两个阶段进行,下列说法错误的是( )
A.阶段Ⅰ中,电源a为正极、b为负极
B.阶段Ⅱ中阴极的电极反应为Na MnO +xe-+xNa+===Na MnO
0.44-x 2 0.44 2
C.比传统氯碱工业减少了阳离子交换膜,避免氢气和氯气混合,且便于提纯NaOH
D.阶段Ⅰ和Ⅱ的反应不能都在饱和食盐水中进行
12.(2023·山东临沂模拟)利用库仑测硫仪测定气体中SO 的体积分数,其原理如图所示。待
2
测气体进入电解池后,SO 将I还原,测硫仪便自动电解,溶液中保持不变。若有标准状况
2
下V mL气体通入电解池(其他气体不反应),反应结束后消耗x库仑电量(已知:电解转移
1 mol电子所消耗的电量为96 500库仑)。下列说法正确的是( )
A.M接电源的负极
B.阳极反应式为2H++2e-===H ↑
2
C.反应结束后溶液的pH增大D.混合气体中SO 的体积分数为×100%
2
13.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过 30%,
在此工艺中,物料传输和转化关系如图,其中电极未标出,所用离子交换膜只允许阳离子通
过。
(1)分析比较图示中a%与b%的大小:a%____(填“>”“<”或“=”)b%。
(2)写出燃料电池B中的正极的电极反应:_________________________________________。
(3)图中Y是____________(填化学式),若电解产生11.2 L(标准状况)该物质,则至少转移电
子________mol;X元素的基态原子的电子排布式为__________。
14.(1)一种用铅酸蓄电池进行电絮凝净水装置如图所示,回答下列问题:
①装置Ⅰ中Y电极的电极材料是__________________________________________________
(填化学式),工作时SO向________(填“X”或“Y”)电极移动;Y电极的电极反应式为
______________________________________________________________________________
______________________________________________________________________________。
②装置Ⅱ中Al电极的电极反应式为_______________________________________________
______________________________________________________________________________
______________________________________________________________________________。
③每消耗103.5 g Pb,装置的电流效率为80%,则理论上电解池阴极上生成________mol
H。
2
(2)[2020·全国卷Ⅱ,34(3)]CH 和CO 都是比较稳定的分子,科学家利用电化学装置实现两
4 2
种分子的耦合转化,其原理如图所示:①阴极上的反应式为____________________________________________________________。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH 和CO 体积比为________。
4 2