文档内容
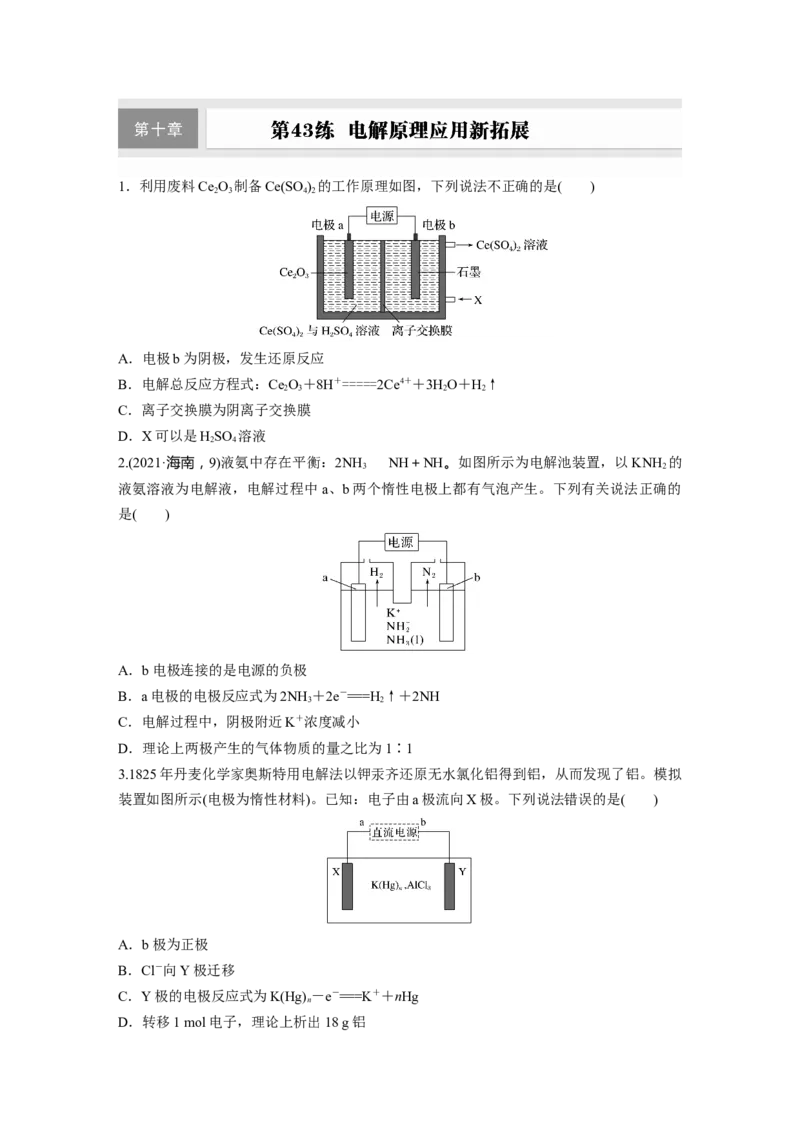
1.利用废料Ce O 制备Ce(SO) 的工作原理如图,下列说法不正确的是( )
2 3 4 2
A.电极b为阴极,发生还原反应
B.电解总反应方程式:Ce O+8H+=====2Ce4++3HO+H↑
2 3 2 2
C.离子交换膜为阴离子交换膜
D.X可以是HSO 溶液
2 4
2.(2021·海南,9)液氨中存在平衡:2NH NH+NH。如图所示为电解池装置,以KNH 的
3 2
液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的
是( )
A.b电极连接的是电源的负极
B.a电极的电极反应式为2NH +2e-===H↑+2NH
3 2
C.电解过程中,阴极附近K+浓度减小
D.理论上两极产生的气体物质的量之比为1∶1
3.1825年丹麦化学家奥斯特用电解法以钾汞齐还原无水氯化铝得到铝,从而发现了铝。模拟
装置如图所示(电极为惰性材料)。已知:电子由a极流向X极。下列说法错误的是( )
A.b极为正极
B.Cl-向Y极迁移
C.Y极的电极反应式为K(Hg) -e-===K++nHg
n
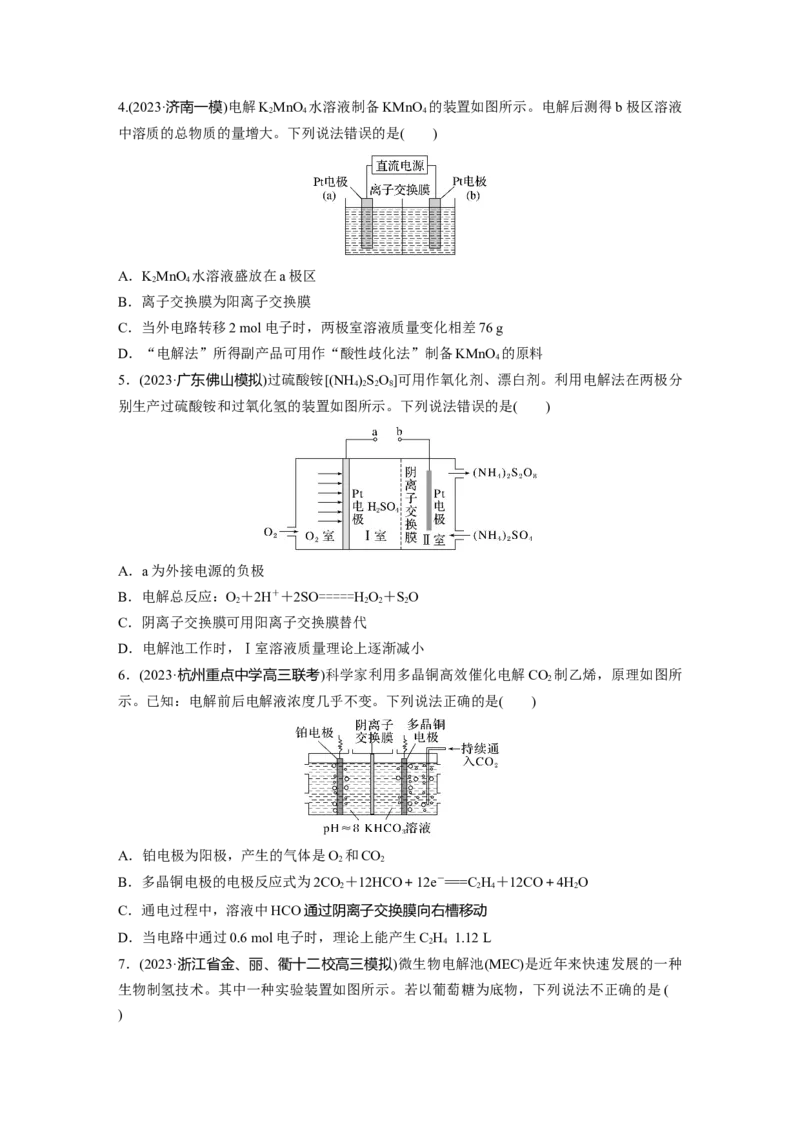
D.转移1 mol电子,理论上析出18 g铝4.(2023·济南一模)电解KMnO 水溶液制备KMnO 的装置如图所示。电解后测得b极区溶液
2 4 4
中溶质的总物质的量增大。下列说法错误的是( )
A.KMnO 水溶液盛放在a极区
2 4
B.离子交换膜为阳离子交换膜
C.当外电路转移2 mol电子时,两极室溶液质量变化相差76 g
D.“电解法”所得副产品可用作“酸性歧化法”制备KMnO 的原料
4
5.(2023·广东佛山模拟)过硫酸铵[(NH )SO]可用作氧化剂、漂白剂。利用电解法在两极分
4 2 2 8
别生产过硫酸铵和过氧化氢的装置如图所示。下列说法错误的是( )
A.a为外接电源的负极
B.电解总反应:O+2H++2SO=====HO+SO
2 2 2 2
C.阴离子交换膜可用阳离子交换膜替代
D.电解池工作时,Ⅰ室溶液质量理论上逐渐减小
6.(2023·杭州重点中学高三联考)科学家利用多晶铜高效催化电解CO 制乙烯,原理如图所
2
示。已知:电解前后电解液浓度几乎不变。下列说法正确的是( )
A.铂电极为阳极,产生的气体是O 和CO
2 2
B.多晶铜电极的电极反应式为2CO+12HCO+12e-===C H+12CO+4HO
2 2 4 2
C.通电过程中,溶液中HCO通过阴离子交换膜向右槽移动
D.当电路中通过0.6 mol电子时,理论上能产生C H 1.12 L
2 4
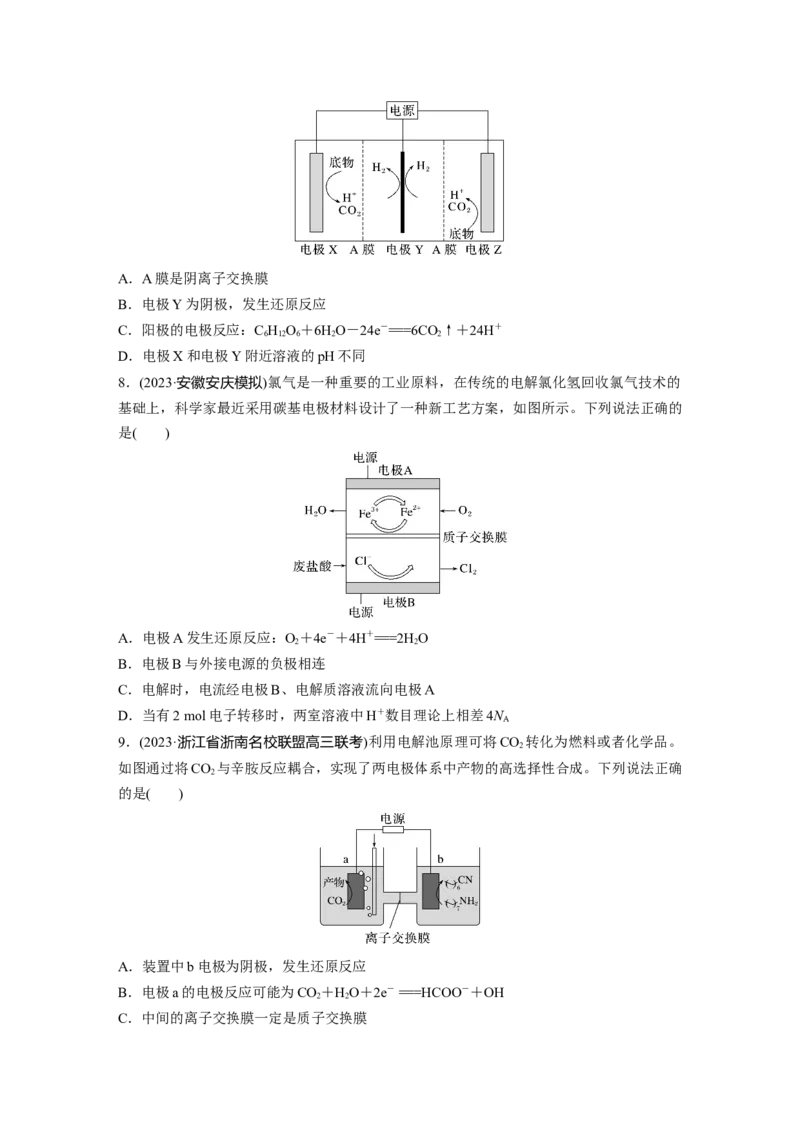
7.(2023·浙江省金、丽、衢十二校高三模拟)微生物电解池(MEC)是近年来快速发展的一种
生物制氢技术。其中一种实验装置如图所示。若以葡萄糖为底物,下列说法不正确的是(
)A.A膜是阴离子交换膜
B.电极Y为阴极,发生还原反应
C.阳极的电极反应:C H O+6HO-24e-===6CO↑+24H+
6 12 6 2 2
D.电极X和电极Y附近溶液的pH不同
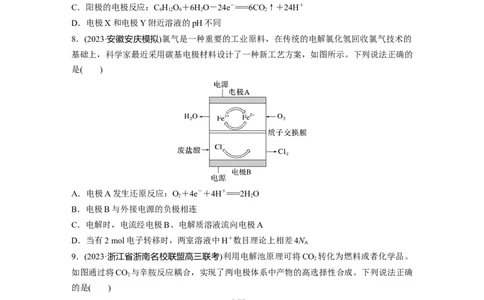
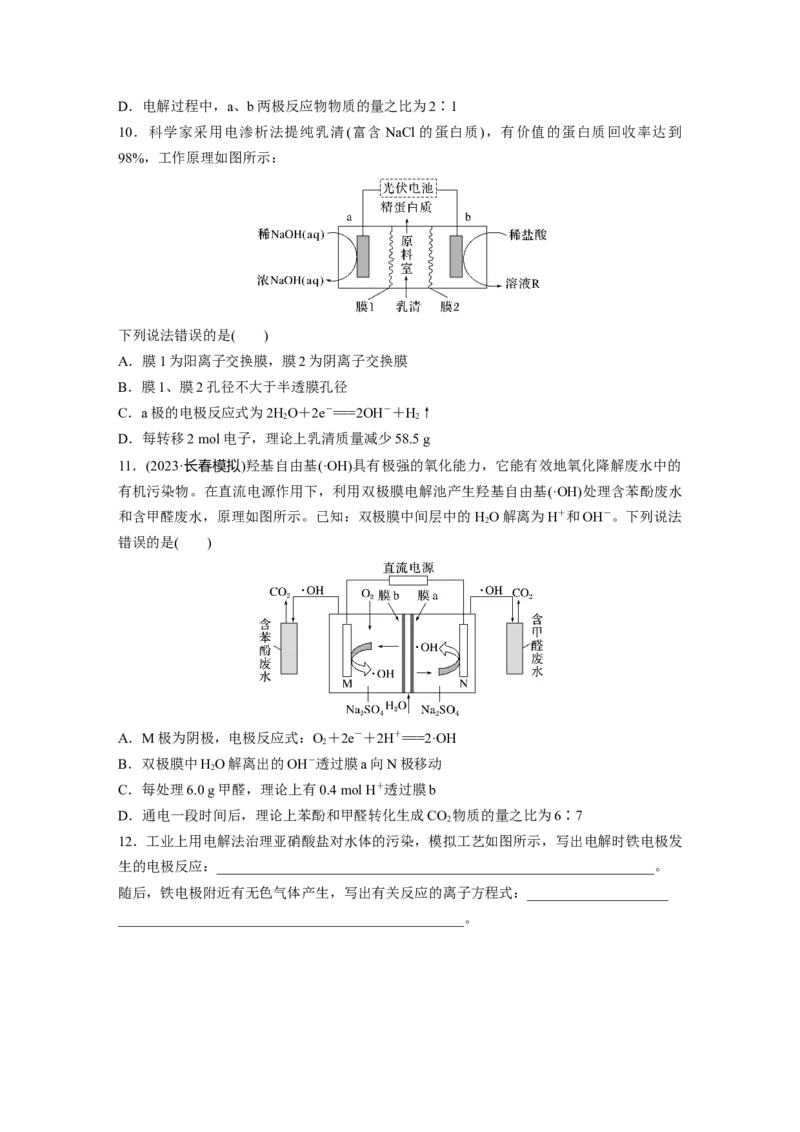
8.(2023·安徽安庆模拟)氯气是一种重要的工业原料,在传统的电解氯化氢回收氯气技术的
基础上,科学家最近采用碳基电极材料设计了一种新工艺方案,如图所示。下列说法正确的
是( )
A.电极A发生还原反应:O+4e-+4H+===2HO
2 2
B.电极B与外接电源的负极相连
C.电解时,电流经电极B、电解质溶液流向电极A
D.当有2 mol电子转移时,两室溶液中H+数目理论上相差4N
A
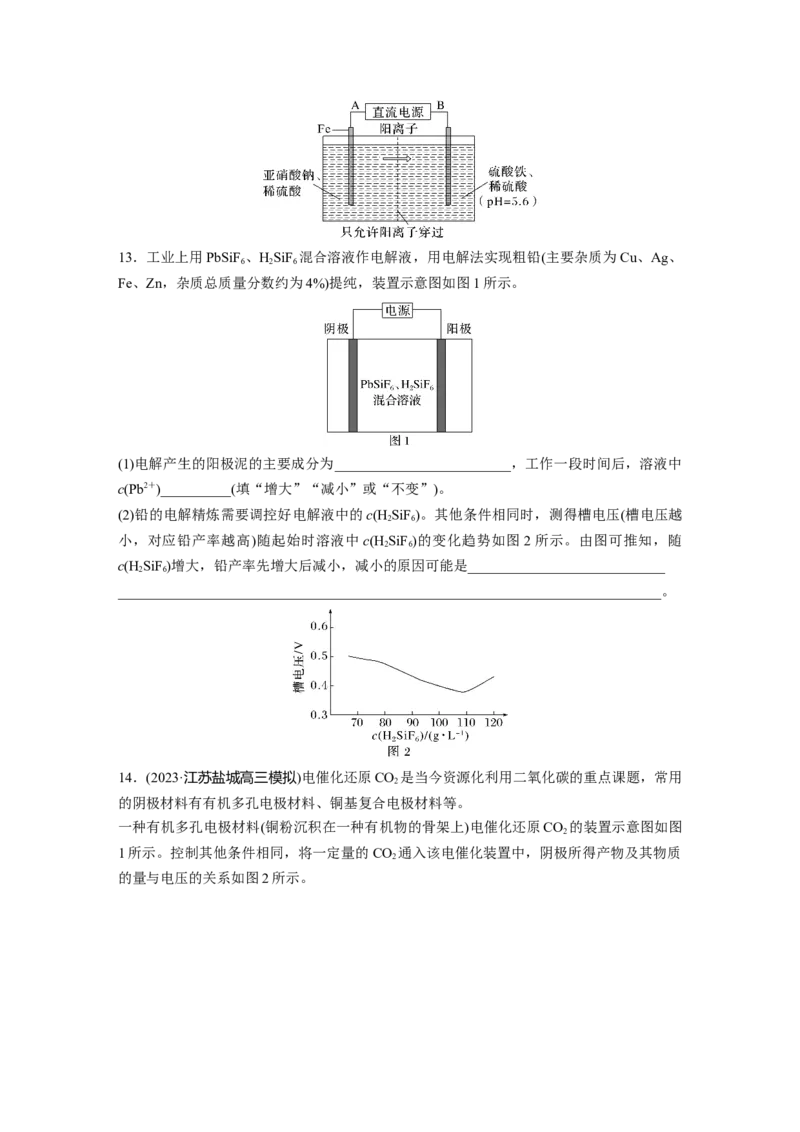
9.(2023·浙江省浙南名校联盟高三联考)利用电解池原理可将CO 转化为燃料或者化学品。
2
如图通过将CO 与辛胺反应耦合,实现了两电极体系中产物的高选择性合成。下列说法正确
2
的是( )
A.装置中b电极为阴极,发生还原反应
B.电极a的电极反应可能为CO+HO+2e- ===HCOO-+OH
2 2
C.中间的离子交换膜一定是质子交换膜D.电解过程中,a、b两极反应物物质的量之比为2∶1
10.科学家采用电渗析法提纯乳清(富含NaCl的蛋白质),有价值的蛋白质回收率达到
98%,工作原理如图所示:
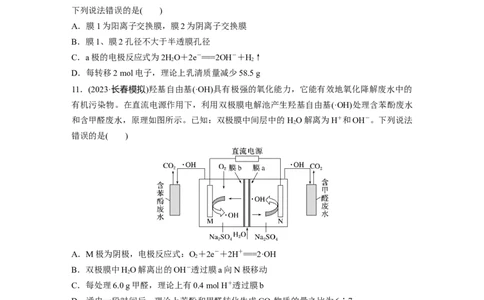
下列说法错误的是( )
A.膜1为阳离子交换膜,膜2为阴离子交换膜
B.膜1、膜2孔径不大于半透膜孔径
C.a极的电极反应式为2HO+2e-===2OH-+H↑
2 2
D.每转移2 mol电子,理论上乳清质量减少58.5 g
11.(2023·长春模拟)羟基自由基(·OH)具有极强的氧化能力,它能有效地氧化降解废水中的
有机污染物。在直流电源作用下,利用双极膜电解池产生羟基自由基(·OH)处理含苯酚废水
和含甲醛废水,原理如图所示。已知:双极膜中间层中的 HO解离为H+和OH-。下列说法
2
错误的是( )
A.M极为阴极,电极反应式:O+2e-+2H+===2·OH
2
B.双极膜中HO解离出的OH-透过膜a向N极移动
2
C.每处理6.0 g甲醛,理论上有0.4 mol H+透过膜b
D.通电一段时间后,理论上苯酚和甲醛转化生成CO 物质的量之比为6∶7
2
12.工业上用电解法治理亚硝酸盐对水体的污染,模拟工艺如图所示,写出电解时铁电极发
生的电极反应:______________________________________________________________。
随后,铁电极附近有无色气体产生,写出有关反应的离子方程式:____________________
_________________________________________________。13.工业上用PbSiF 、HSiF 混合溶液作电解液,用电解法实现粗铅(主要杂质为Cu、Ag、
6 2 6
Fe、Zn,杂质总质量分数约为4%)提纯,装置示意图如图1所示。
(1)电解产生的阳极泥的主要成分为_________________________,工作一段时间后,溶液中
c(Pb2+)__________(填“增大”“减小”或“不变”)。
(2)铅的电解精炼需要调控好电解液中的c(H SiF)。其他条件相同时,测得槽电压(槽电压越
2 6
小,对应铅产率越高)随起始时溶液中c(H SiF)的变化趋势如图2所示。由图可推知,随
2 6
c(H SiF)增大,铅产率先增大后减小,减小的原因可能是____________________________
2 6
_____________________________________________________________________________。
14.(2023·江苏盐城高三模拟)电催化还原CO 是当今资源化利用二氧化碳的重点课题,常用
2
的阴极材料有有机多孔电极材料、铜基复合电极材料等。
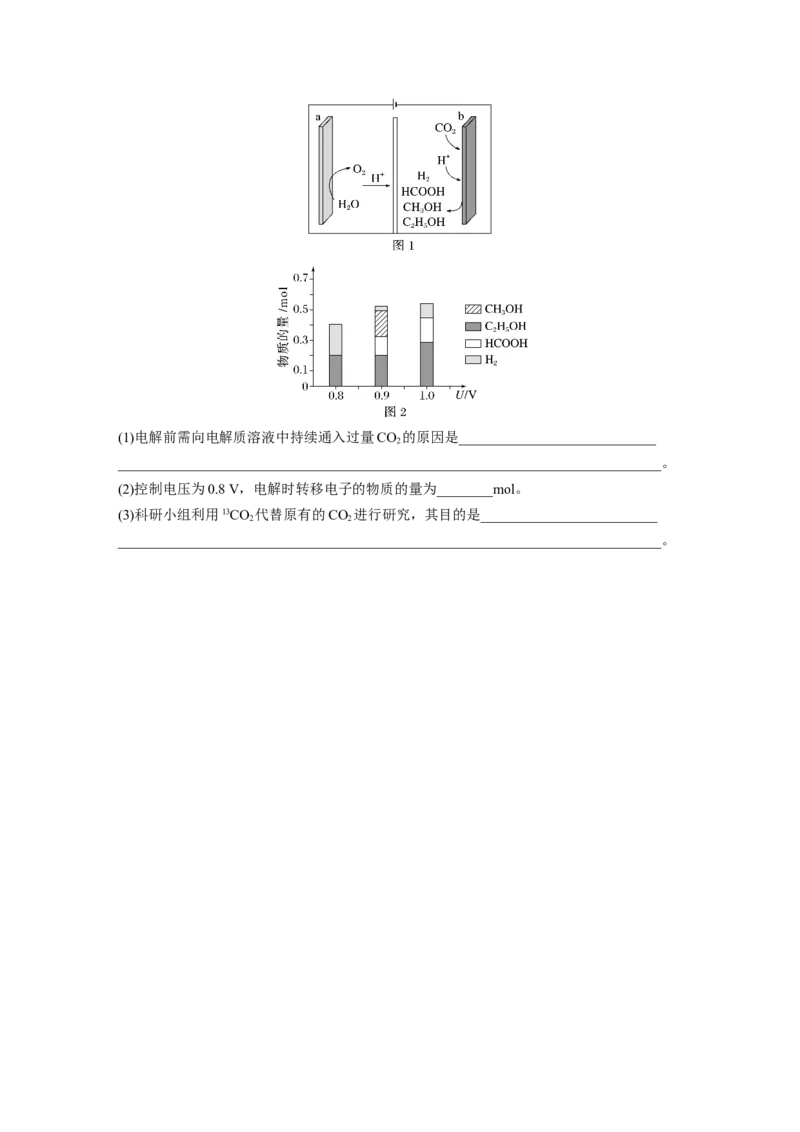
一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO 的装置示意图如图
2
1所示。控制其他条件相同,将一定量的CO 通入该电催化装置中,阴极所得产物及其物质
2
的量与电压的关系如图2所示。(1)电解前需向电解质溶液中持续通入过量CO 的原因是____________________________
2
_____________________________________________________________________________。
(2)控制电压为0.8 V,电解时转移电子的物质的量为________mol。
(3)科研小组利用13CO 代替原有的CO 进行研究,其目的是_________________________
2 2
_____________________________________________________________________________。