文档内容
第十章 化学实验基础与探究
测试卷
时间:75分钟 分值:100分
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O16 Na 23 Al 27 P 31 S 32 Cl 35.5 K 39 Ca
40 Fe 56 Cu 64 Br 80 Ag 108 Ba 137
一、选择题(每小题只有一个正确选项,共15×3分)
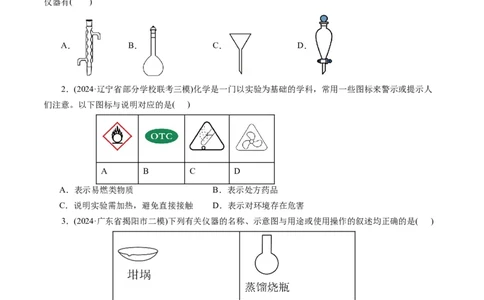
1.(2024·浙江省义乌中学高三首考模拟)实验得到的乙酸乙酯混合物中除去乙酸和乙醇,需要用到的
仪器有( )
A. B. C. D.
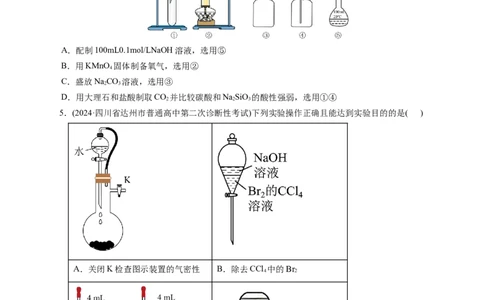
2.(2024·辽宁省部分学校联考三模)化学是一门以实验为基础的学科,常用一些图标来警示或提示人
们注意。以下图标与说明对应的是( )
A B C D
A.表示易燃类物质 B.表示处方药品
C.说明实验需加热,避免直接接触 D.表示对环境存在危害
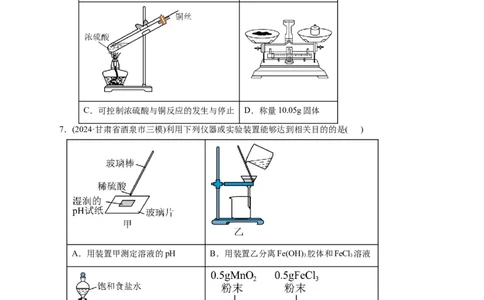
3.(2024·广东省揭阳市二模)下列有关仪器的名称、示意图与用途或使用操作的叙述均正确的是( )
A.可用于对固体进行高温加
B.可用于制备蒸馏水
热C.分液时将磨口瓶塞上的凹槽 D.洗气除杂实验中将气体
对准漏斗口颈上的小孔 从小口通入
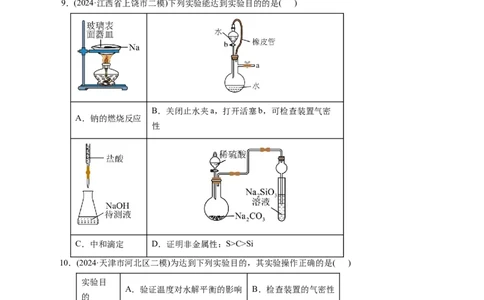
4.(2024·安徽省安庆市三模)下列实验中,所选装置(可添加试剂,可重复使用)不合理的是( )
A.配制100mL0.1mol/LNaOH溶液,选用⑤
B.用KMnO 固体制备氧气,选用②
4
C.盛放NaCO 溶液,选用③
2 3
D.用大理石和盐酸制取CO 并比较碳酸和NaSiO 的酸性强弱,选用①④
2 2 3
5.(2024·四川省达州市普通高中第二次诊断性考试)下列实验操作正确且能达到实验目的的是( )
A.关闭K检查图示装置的气密性 B.除去CCl 中的Br
4 2
C.探究浓度对化学反应速率的影响 D.配制一定物质的量浓度的溶液
6.(2024·辽宁省部分学校高三三模联考)下图所示的实验操作及描述均正确,且能达到相应目的的是()
A.用于NaOH 溶液滴定盐酸溶液 B.用于吸收尾气氨气
C.可控制浓硫酸与铜反应的发生与停止 D.称量10.05g固体
7.(2024·甘肃省酒泉市三模)利用下列仪器或实验装置能够达到相关目的的是( )
A.用装置甲测定溶液的pH B.用装置乙分离Fe(OH) 胶体和FeCl 溶液
3 3
D.用装置丁比较MnO 和FeCl 对HO 分
2 3 2 2
C.用装置丙检验乙炔具有还原性
解的催化效果
8.(2024·江苏省南京市二模)下列由废易拉罐制取 的实验原理与装置不能达到实验目的的是( )A.用装置甲溶解废易拉罐细屑 B.用装置乙过滤得到Na[Al(OH)]溶液
4
C.用装置丙制取Al(OH) 沉淀 D.用装置丁灼烧Al(OH) 制取Al O
3 3 2 3
9.(2024·江西省上饶市二模)下列实验能达到实验目的的是( )
B.关闭止水夹a,打开活塞b,可检查装置气密
A.钠的燃烧反应
性
C.中和滴定 D.证明非金属性:S>C>Si
10.(2024·天津市河北区二模)为达到下列实验目的,其实验操作正确的是( )
实验目
A.验证温度对水解平衡的影响 B.检查装置的气密性
的
实验操
作
实验目
C.混合浓硫酸和乙醇 D.检验溶液的
的实验操
作
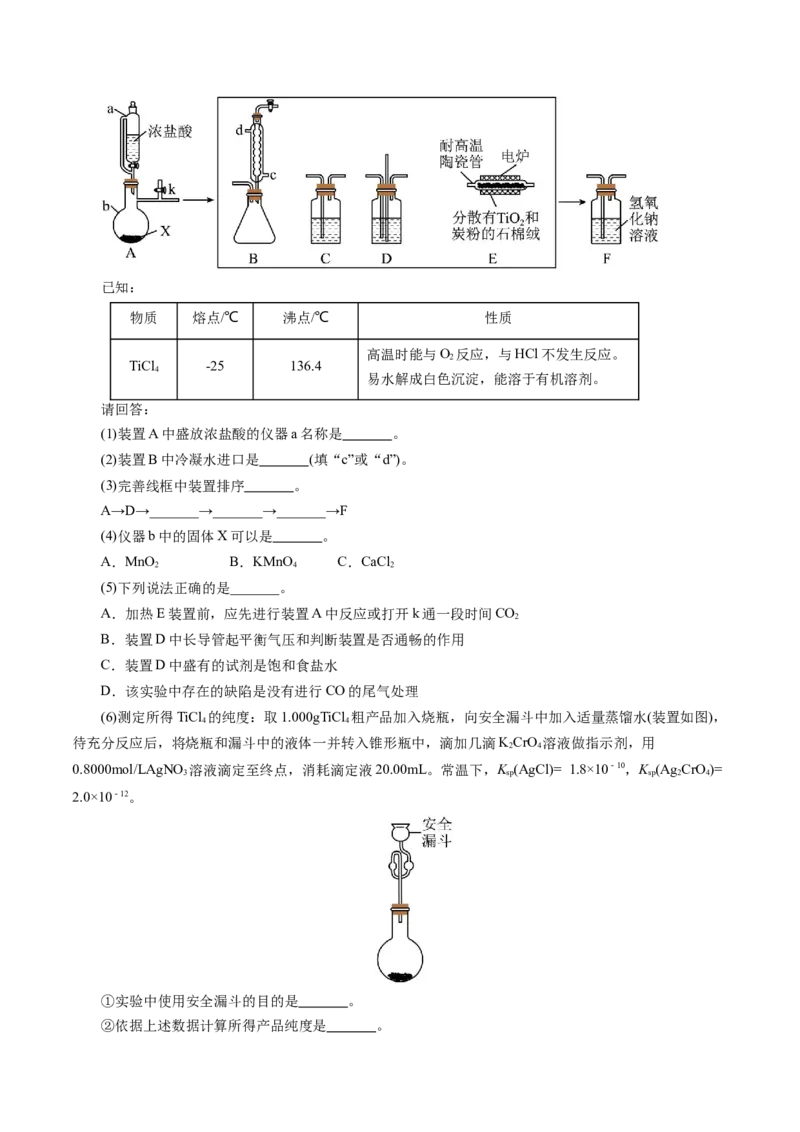
11.(2024·安徽合肥市三模)下列实验装置中能达到实验目的的是( )
A B C D
A.除去Cl 中少量HCl B.蒸干制备胆矾 C.熔融纯碱 D.制备Cl
2 2
12.(2024· 江浙高中(县中)发展共同体高三联考)某废催化剂含SiO、ZnS、CuS及少量的Fe O。某实
2 3 4
验小组以该废催化剂为原料,回收锌和铜,设计实验流程如图:
下列说法不正确的是( )
A.可用铁氰化钾检验滤液1中是否含有Fe2+
B.步骤①操作中,生成的气体需用NaOH溶液或CuSO 溶液吸收
4
C.滤渣1成分是SiO 和CuS,滤渣2成分可能为SiO 和S
2 2
D.步骤④的操作:将滤液2蒸发至有大量晶体析出,停止加热,自然冷却
13.(2024·浙江省义乌中学高三首考模拟)阿司匹林片的有效成分是乙酰水杨酸,辅助成分是淀粉。某
实验小组设计实验方案如下:下列说法不正确的是( )
A.操作Ⅰ研碎的目的为了增大接触面积,加快乙酰水杨酸的溶解
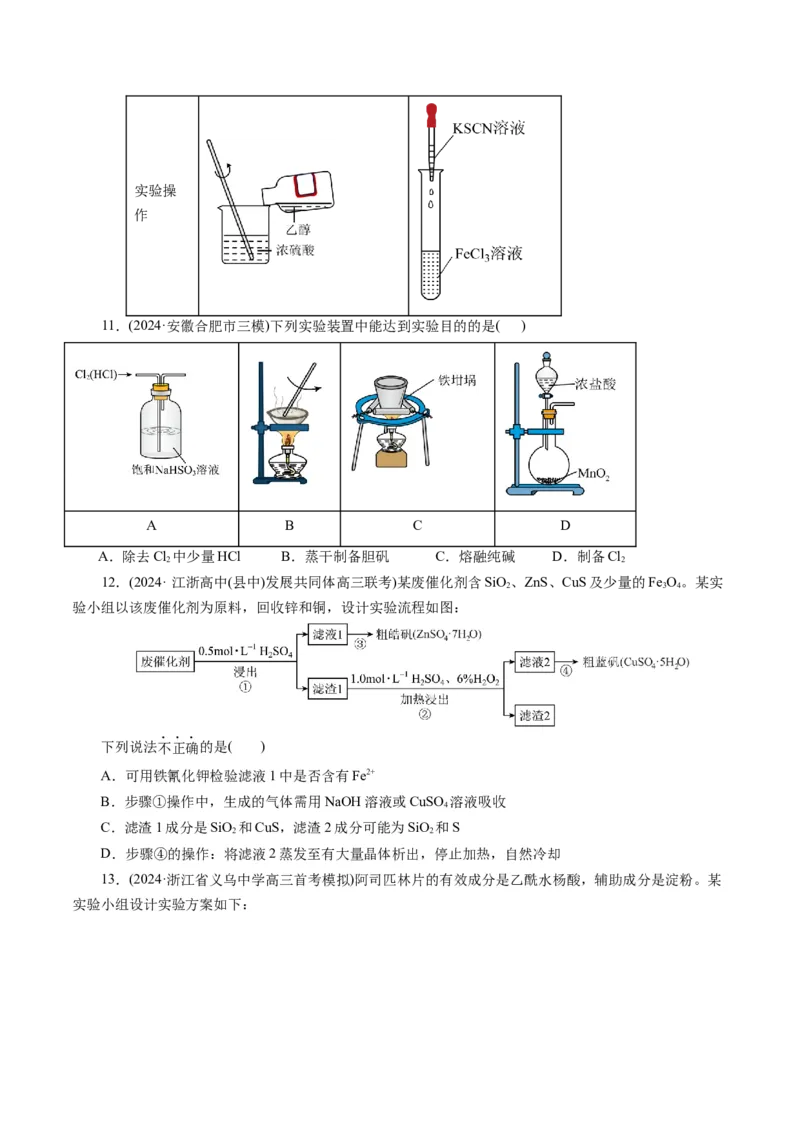
B.操作Ⅱ可观察到溶液显红色,操作Ⅴ可观察到溶液显紫色
C.操作Ⅲ目的为了加快酯基的水解,可用足量 溶液替代,仍可显色
D.操作Ⅳ为了中和过量硫酸,否则溶液酸性过强不易显色
14.(2024·浙江省稽阳联谊学校高三联考)CuCl为白色粉末状固体,难溶于水和乙醇,在潮湿环境中,
容易被空气氧化,是一种重要工业原料。工业以硫化铜精矿为原料,制备氯化亚铜的流程如下图所示:
下列说法不正确的是( )
A.步骤①会产生有毒气体,可用石灰乳吸收
B.步骤②适当增大硫酸浓度、加热可以加快浸出速率
C.步骤③应先加入NaSO 溶液,再缓慢滴加NaCl溶液
2 3
D.步骤④中X可以是无水乙醇
15.(2024·浙江省嘉兴市高三联考)一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH )] SO ·H O是一种重要
3 4 4 2
的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如
下:
下列说法不正确的是( )
A.操作I中发生的主要反应为:Fe+H O+2H+= Fe2++2H O
2 2 2
B.操作II中趁热过滤除去的是难溶性杂质和氢氧化铁
C.操作III中洗涤可用乙醇和水的混合液,干燥可采用减压干燥方式
D.设计操作IV的目的是为了提高乙醇的利用率
二、非选择题(共5小题,共55分)
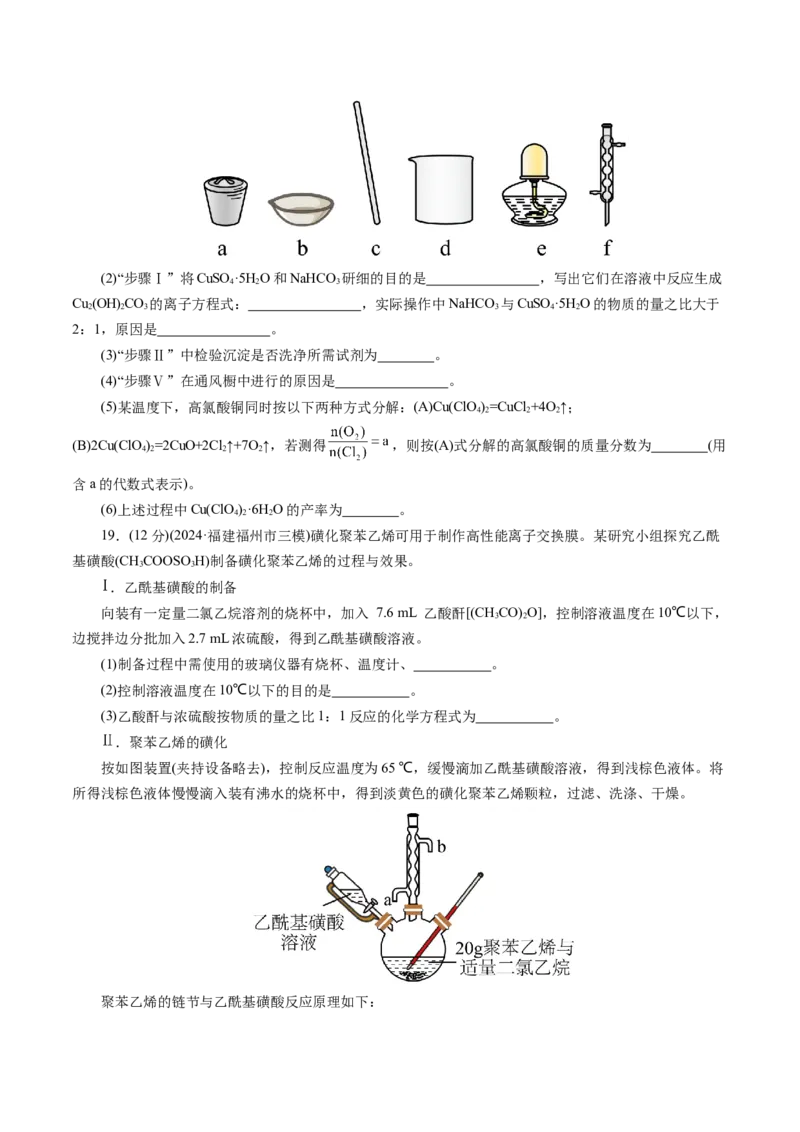
16.(10分)(2024·浙江省宁波市高三下学期二模)TiCl 是制备金属钛的重要中间体,某兴趣小组利用如
4
下装置在实验室制备TiCl (夹持装置略),反应方程式为:TiO+2C+2Cl TiCl +2CO。
4 2 2 4已知:
物质 熔点/℃ 沸点/℃ 性质
高温时能与O 反应,与HCl不发生反应。
2
TiCl -25 136.4
4
易水解成白色沉淀,能溶于有机溶剂。
请回答:
(1)装置A中盛放浓盐酸的仪器a名称是 。
(2)装置B中冷凝水进口是 (填“c”或“d”)。
(3)完善线框中装置排序 。
A→D→_______→_______→_______→F
(4)仪器b中的固体X可以是 。
A.MnO B.KMnO C.CaCl
2 4 2
(5)下列说法正确的是_______。
A.加热E装置前,应先进行装置A中反应或打开k通一段时间CO
2
B.装置D中长导管起平衡气压和判断装置是否通畅的作用
C.装置D中盛有的试剂是饱和食盐水
D.该实验中存在的缺陷是没有进行CO的尾气处理
(6)测定所得TiCl 的纯度:取1.000gTiCl 粗产品加入烧瓶,向安全漏斗中加入适量蒸馏水(装置如图),
4 4
待充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴KCrO 溶液做指示剂,用
2 4
0.8000mol/LAgNO 溶液滴定至终点,消耗滴定液20.00mL。常温下,K (AgCl)= 1.8×10-10,K (Ag CrO)=
3 sp sp 2 4
2.0×10-12。
①实验中使用安全漏斗的目的是 。
②依据上述数据计算所得产品纯度是 。17.(10分)(2024·浙江省杭州市高三下学期二模)过氧化钙(CaO)微溶于水,碱性条件下较稳定,可作
2
为医用防腐剂和消毒剂,也可作为改良剂为农业、园艺和生物技术应用提供氧气。以下是一种实验室制备
较高纯度过氧化钙的流程图:
(1)步骤I需要量取 盐酸,所用的仪器是___________。
A. 量筒 B. 量筒
C. 碱式滴定管 D. 烧杯
(2)下列说法正确的是___________。
A.步骤I中应使用过量的盐酸,以提高碳酸钙的利用率
B.步骤Ⅱ中的煮沸操作的主要目的是加快反应速率
C.步骤Ⅲ中的混合操作,应将氯化钙溶液滴入氨水-双氧水混合液中
D.步骤V中可用冰水洗涤
(3)写出步骤Ⅲ发生反应的化学方程式 ,步骤Ⅲ采用冰水浴可提高产率,其原因有(回答两
点) 。
(4)准确称取 产品配成 溶液。取 溶液,加入5mL6mol·L-1醋酸溶液和2-3滴0.1
mol·L-1MnSO 溶液,用0.02 mol·L-1KMnO 标准溶液滴定至浅红色,半分钟不褪色;平行测定3次,消耗
4 4
KMnO 标准溶液的平均值为 。
4
①MnSO 溶液的作用是 。
4
②CaO 的纯度为 。
2
18.(11分)(2024·江西省部分重点中学第二次联考)高氯酸铜晶体Cu(ClO)·6H O易溶于水,120℃开始
4 2 2
分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
Ⅰ.称取12.5g CuSO ·5H O和9.6g NaHCO ,混合研细后,投入100mL70~80℃热水,快速搅拌,静置
4 2 3
得绿色沉淀[Cu(OH) CO];
2 2 3
Ⅱ.冷却,过滤,用少量蒸馏水洗涤沉淀2~3次;
Ⅲ.在沉淀中慢慢滴加70% HClO 溶液,适度加热搅拌至不再产生气体;
4
Ⅳ.过滤,得蓝色高氯酸铜溶液;
Ⅴ.在通风橱中蒸发至不再产生白雾,继续蒸发至有晶膜出现,冷却、结晶、过滤、洗涤,得蓝色晶体;
Ⅵ.60℃下,在烘箱中干燥2h,得16.695g Cu(ClO)·6H O晶体。
4 2 2
回答下列问题:
(1)“步骤Ⅰ”中研磨用到的仪器名称是 ,“步骤Ⅴ”中蒸发需要用到下列仪器中的
(填字母序号)。(2)“步骤Ⅰ”将CuSO ·5H O和NaHCO 研细的目的是 ,写出它们在溶液中反应生成
4 2 3
Cu(OH) CO 的离子方程式: ,实际操作中NaHCO 与CuSO ·5H O的物质的量之比大于
2 2 3 3 4 2
2:1,原因是 。
(3)“步骤Ⅱ”中检验沉淀是否洗净所需试剂为 。
(4)“步骤Ⅴ”在通风橱中进行的原因是 。
(5)某温度下,高氯酸铜同时按以下两种方式分解:(A)Cu(ClO)=CuCl+4O ↑;
4 2 2 2
(B)2Cu(ClO)=2CuO+2Cl↑+7O ↑,若测得 ,则按(A)式分解的高氯酸铜的质量分数为 (用
4 2 2 2
含a的代数式表示)。
(6)上述过程中Cu(ClO)·6H O的产率为 。
4 2 2
19.(12分)(2024·福建福州市三模)磺化聚苯乙烯可用于制作高性能离子交换膜。某研究小组探究乙酰
基磺酸(CHCOOSOH)制备磺化聚苯乙烯的过程与效果。
3 3
.乙酰基磺酸的制备
向装有一定量二氯乙烷溶剂的烧杯中,加入 7.6 mL 乙酸酐[(CH CO) O],控制溶液温度在10℃以下,
3 2
边搅拌边分批加入2.7 mL浓硫酸,得到乙酰基磺酸溶液。
(1)制备过程中需使用的玻璃仪器有烧杯、温度计、 。
(2)控制溶液温度在10℃以下的目的是 。
(3)乙酸酐与浓硫酸按物质的量之比1:1反应的化学方程式为 。
.聚苯乙烯的磺化
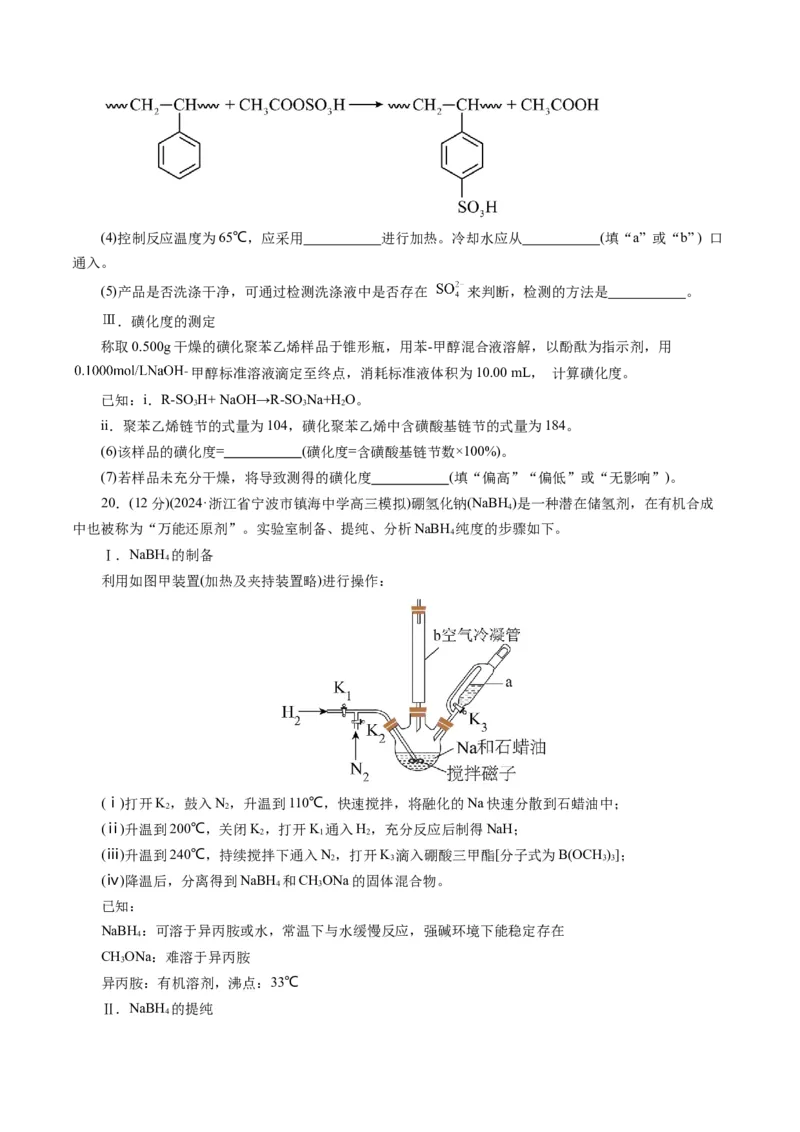
按如图装置(夹持设备略去),控制反应温度为65 ℃,缓慢滴加乙酰基磺酸溶液,得到浅棕色液体。将
所得浅棕色液体慢慢滴入装有沸水的烧杯中,得到淡黄色的磺化聚苯乙烯颗粒,过滤、洗涤、干燥。
聚苯乙烯的链节与乙酰基磺酸反应原理如下:(4)控制反应温度为65℃,应采用 进行加热。冷却水应从 (填“a” 或“b” ) 口
通入。
(5)产品是否洗涤干净,可通过检测洗涤液中是否存在 来判断,检测的方法是 。
.磺化度的测定
称取0.500g干燥的磺化聚苯乙烯样品于锥形瓶,用苯-甲醇混合液溶解,以酚酞为指示剂,用
甲醇标准溶液滴定至终点,消耗标准液体积为10.00 mL, 计算磺化度。
已知:i.R-SO H+ NaOH→R-SO Na+HO。
3 3 2
ii.聚苯乙烯链节的式量为104,磺化聚苯乙烯中含磺酸基链节的式量为184。
(6)该样品的磺化度= (磺化度=含磺酸基链节数×100%)。
(7)若样品未充分干燥,将导致测得的磺化度 (填“偏高”“偏低”或“无影响”)。
20.(12分)(2024·浙江省宁波市镇海中学高三模拟)硼氢化钠(NaBH )是一种潜在储氢剂,在有机合成
4
中也被称为“万能还原剂”。实验室制备、提纯、分析NaBH 纯度的步骤如下。
4
Ⅰ.NaBH 的制备
4
利用如图甲装置(加热及夹持装置略)进行操作:
(ⅰ)打开K,鼓入N,升温到110℃,快速搅拌,将融化的Na快速分散到石蜡油中;
2 2
(ⅱ)升温到200℃,关闭K,打开K 通入H,充分反应后制得NaH;
2 1 2
(ⅲ)升温到240℃,持续搅拌下通入N,打开K 滴入硼酸三甲酯[分子式为B(OCH )];
2 3 3 3
(ⅳ)降温后,分离得到NaBH 和CHONa的固体混合物。
4 3
已知:
NaBH :可溶于异丙胺或水,常温下与水缓慢反应,强碱环境下能稳定存在
4
CHONa:难溶于异丙胺
3
异丙胺:有机溶剂,沸点:33℃
Ⅱ.NaBH 的提纯
4NaBH 可采用索氏提取法提纯,其装置如图乙所示,实验时将NaBH 和CHONa的固体混合物放入滤
4 4 3
纸套筒1中,烧瓶中加入异丙胺。烧瓶中异丙胺受热蒸发上升,冷凝后滴入滤纸套筒1中,再经导管返回
烧瓶,从而实现连续萃取。
Ⅲ.纯度分析
步骤1:取m g产品(杂质不参加反应)溶于 溶液后配成 溶液,取 置于碘量瓶中,
加入VmL c mol·L-1的KIO 溶液充分反应。(3NaBH +4KIO=3NaBO +4KI+6H O)
1 1 3 4 3 2 2
步骤2:向步骤1反应后溶液中加入过量的KI溶液,用稀硫酸调节pH,使过量KIO 转化为I,冷却
3 2
后于暗处放数分钟。
步骤3:将步骤2所得混合液调pH约为5.0,加入几滴淀粉,用cmol·L-1NaSO 标准溶液滴定至终点,消
2 2 2 3
耗溶液VmL。(I+2 Na SO= Na SO+2 NaI)
2 2 2 2 3 2 4 6
回答下列问题:
(1)仪器a的名称是 。
(2)写出NaH与B(OCH ) 反应的化学方程式 。
3 3
(3)下列有关说法不正确的是__________。
A.NaBH 和 中氢化合价相同 B.装置甲应该处于无水、无氧的反应环境
4
C.装置乙中异丙胺蒸汽沿导管2上升 D.萃取完全后,NaBH 在圆底烧瓶中
4
(4)按照先后顺序对本实验的滴定操作排序
检查是否漏水→蒸馏水洗涤→ →a→_______→_______→________。
a.加液至“0”刻度以上 处
b.调整液面至“0”刻度或“0”刻度下方,记录读数V
1
c.倾斜转动滴定管,使标准液润湿滴定管内壁,将润洗液从下口排出
d.赶出尖嘴部分气泡
e.向碱式滴定管中加3~5 mL Na SO 标准液
2 2 3
f.向酸式滴定管中加3~5 mL Na SO 标准液
2 2 3
g.左手控制活塞(或挤压玻璃珠),右手振荡锥形瓶
h.左手振荡锥形瓶,右手控制活塞(或挤压玻璃珠)
(5)产品中NaBH 的纯度为 %。
4