文档内容
《物质结构 元素周期律》单元测试(基础巩固)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共54分)
1.(本题3分)(2021·江苏·苏州市相城区陆慕高级中学高一期中) 可以作为核聚变材料。下列关于
的叙述正确的是
A. 和 是同一种核素 B. 原子核内中子数为6
C. 原子核内质子数为13 D. 和 互为同位素
【答案】D
【详解】
A. 和 所含质子数相同,但质量数(或中子数)不同,不是同种核素,A错误;
B.中子数=质量数-质子数,所以 原子核内中子数为13-6=7,B错误;
C.左下角数字为质子数,所以 原子核内质子数为6,C错误;
D. 和 为碳元素的不同核素,互为同位素,D正确;
综上所述答案为D。
2.(本题3分)(2021·上海市徐汇中学高二期中)关于短周期元素的说法不正确的是
A.短周期中共有18种元素
B.有3种元素的原子最外电子层达到了8电子稳定结构
C.活泼的非金属元素主要集中在短周期
D.地壳中含量最多的金属元素和非金属元素都在短周期
【答案】B
【详解】
A.短周期即前三周期中共有18种元素,A正确;
B.有2种元素的原子最外电子层达到了8电子稳定结构,即Ne、Ar,B错误;
C.同周期自左向右非金属性逐渐增强,同主族从上到下非金属性逐渐减弱,因此活泼的非金属元素主要
集中在短周期,C正确;D.地壳中含量最多的金属元素和非金属元素分别是Al、O,都在短周期,D正确;
答案选B。
3.(本题3分)(2021·江苏盐城·高二学业考试)硼和氮都属于元素周期表第2周期元素,它们原子结构中
相同的是
A.电子层数 B.质子数 C.最外层电子数 D.核外电子数
【答案】A
【详解】
周期数等于原子的电子层数,硼和氮都属于第2周期,故两者原子结构中电子层数相同;
答案选A。
4.(本题3分)(2021·全国·高一课时练习)下列有关钾及钾的化合物叙述错误的是
A.钾及钾的化合物灼烧时均会发出紫色的火焰
B. 受热易分解产生
C.金属钾燃烧时生成氧化钾
D.金属钾可保存在煤油中
【答案】C
【详解】
A.焰色反应是金属元素的性质,钾元素的焰色为紫色,故钾及钾的化合物灼烧均为紫色火焰,故A正确;
B.碳酸氢钾不稳定,受热成碳酸钾和二氧化碳,故B正确;
C.由金属钠燃烧产生过氧化钠,钾比钠活泼,则钾单质燃烧时产物更复杂,可能有过氧化钾、超氧化钾
等,但不是氧化钾,故C错误;
D.钾的密度比煤油大,且与煤油不反应,可将钾保存在煤油中,故D正确;
故选:C。
5.(本题3分)(2021·全国·高一课时练习)下列说法正确的是
a.同主族元素从上至下,单质的氧化性逐渐减弱,熔点逐渐降低
b.在周期表中,同周期第IIA族和第IIIA元素质子数相差可能是1、11或25
c.卤族元素由上至下,阴离子的还原性增强,单质的颜色加深
d.碱金属单质物理通性是硬度小,密度小,熔点低
e.卤素单质越活泼,其熔沸点越低
f.可以利用非金属单质与氢气反应的难易程度来证明其元素非金属性的强弱
g.碱性:LiOH>NaOH>KOH>RbOH
h.酸性:HClOHBrO>HIO,h错误;
4 4 4
综上所述,有5个说法正确,B满足题意。
答案选B。
6.(本题3分)(2021·上海市第二中学高一阶段练习)下列关于卤素单质性质的说法错误的是
A.溴在常温下为液体,易挥发
B.碘在常温下为紫黑色固体,易挥发
C.溴可溶于水,更易溶于四氯化碳等有机溶剂中
D.碘蒸汽为紫色,碘水为棕黄色,碘的四氯化碳溶液呈紫红色
【答案】B
【详解】
A.溴单质在常温下为液体,容易挥发,A说法正确;
B.碘单质在常温下为紫黑色固体,易升华,B说法错误;
C.溴可溶于水,在四氯化碳等有机溶剂中溶解度更大,更易溶,C说法正确;D.碘蒸汽为紫色,碘水为棕黄色,碘的四氯化碳溶液呈紫红色,D说法正确;
答案选B。
7.(本题3分)(2021·全国·高一专题练习)向NaBr、NaI混合液中,通入一定量氯气后,将溶液蒸干并充
分灼烧,得到固体剩余物质的组成不可能是
A.NaCl,NaI B.NaCl,NaBr
C.NaCl,NaBr,NaI D.NaCl
【答案】A
【分析】
Br-、I-的还原性:Br-<I-,向NaBr、NaI的混合溶液中通入一定量氯气后,先发生反应
2NaI+Cl =2NaCl+I ,氯气过量时再发生反应:2NaBr+Cl =2NaCl+Br ,据此结合Br 和I 的性质分析。
2 2 2 2 2 2
【详解】
A.当加入氯气,氯气先和碘离子反应,后和溴离子反应,所以固体是中不可能是NaCl、NaI,故A符合
题意;
B.当氯气少量时,发生反应2NaI+Cl =2NaCl+I ,部分2NaBr+Cl =2NaCl+Br 反应,加热过程中,碘升华,
2 2 2 2
所以固体是NaCl、NaBr,故B不符合题意;
C.当氯气少量时,只发生部分2NaI+Cl =2NaCl+I 反应,加热过程中,碘升华,所以固体是NaCl、
2 2
NaBr、NaI,故C不符合题意;
D.当氯气过量时,发生反应2NaI+Cl =2NaCl+I 、2NaBr+Cl =2NaCl+Br ,加热过程中,Br 易挥发、I 易
2 2 2 2 2 2
升华,最后剩余固体是NaCl,故D不符合题意。
答案选A。
8.(本题3分)(2021·全国·高一课时练习)关于卤素单质(X )的下列叙述中正确的是
2
A.都能与氢气因剧烈化合而爆炸 B.都能与铁反应生成FeX
3
C.都能与钠反应生成NaX D.都能与水反应生成氢卤酸HX和次卤酸HXO
【答案】C
【详解】
A.碘单质与氢气的反应为可逆反应,不会剧烈反应,A错误;
B.Fe3+的氧化性大于I-,所以碘单质与Fe反应时生成FeI,B错误;
2
C.钠的还原性很强,卤素单质都能和钠反应生成NaX,C正确;
D.F 与水反应生成HF和氧气,D错误;
2
答案选C。
9.(本题3分)(2021·全国·高一期末)下列关于现行元素周期表的说法错误的是A.利用放射性同位素释放的射线可以杀死人体内的恶性肿瘤
B.一般在过渡元素中寻找一些化学反应新型催化剂
C.所有副族元素都是金属元素,副族包含过渡元素和Ⅷ族
D.研制农药通常考虑含有元素周期表右上角元素(氟、氯、硫、磷等)的有机物
【答案】C
【详解】
A.放射性同位素释放的某些射线贯穿性很强,可以用于杀死人体内的恶性肿瘤,A正确;
B.过渡元素中的重金属元素通常可以作为一些化学反应新型催化剂,B正确;
C.过渡元素包含ⅠB~ⅦB族元素和Ⅷ族元素,C错误;
D.通常农药中含有F、Cl、S、P、As等元素,所以研制农药通常考虑含有元素周期表右上角元素(氟、氯、
硫、磷等)的有机物,D正确;
综上所述答案为C。
10.(本题3分)(2021·全国·高一专题练习)下列有关原子核外电子的说法错误的是
A.每个电子层作为最外层时,最多可容纳8个电子
B.电子在核外是分层排布的
C.电子不停地做高速运动
D.离原子核近的电子能量低,离原子核远的电子能量高
【答案】A
【详解】
A.第一个电子层作为最外层时,最多可容纳2个电子,如氦原子,故A错误;
B.电子在原子中处于不同的能量状态,按照能量不同分层排布,故B正确;
C.原子核外的电子,在核外不停的作无规则高速移动,故C正确;
D.原子核外区域能量可能不同,距核由近到远,能量由低到高,即离原子核近的电子能量低,离核远的
电子能量高,故D正确;
故选A。
11.(本题3分)(2021·全国·高三专题练习)根据元素周期律表无法判断的是
A.稳定性:HO>HS>PH B.酸性:HClO>H SO >H SiO
2 2 3 4 2 3 2 3
C.碱性:KOH>NaOH>LiOH D.氧化性:F>O >N
2 2 2
【答案】B
【详解】
A.同一周期元素的非金属性随原子序数的增大而增强;同一主族元素的非金属性随原子序数的增大而减弱。元素的非金属性越强,其简单氢化物的稳定性就越强。元素的非金属性:O>S>P,所以氢化物的稳定
性:HO>HS>PH,A正确;
2 2 3
B.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,由于S元素最高价含氧酸是
HSO ,不是HSO ,因此不能根据元素周期律判断酸性:HClO>H SO >H SiO,B错误;
2 4 2 3 4 2 3 2 3
C.同一主族元素的金属性随原子序数的增大而增强。元素的金属性越强,其最高价氧化物对应的水化物
的碱性就越强。元素的金属性:K>Na>Li,所以碱性:KOH>NaOH>LiOH,C正确;
D.元素的非金属性越强,其相应的单质的氧化性就越强。由于元素的非金属性:F>O>N,所以单质的氧
化性:F>O >N ,D正确;
2 2 2
故选B。
12.(本题3分)(2020·甘肃·兰州一中高一期中)下列叙述能说明氯元素非金属性比硫元素强的是
①HCl的溶解度比HS大 ②HCl的酸性比HS强 ③HCl的稳定性比HS强 ④还原性:Cl-<S2-
2 2 2
⑤HClO的酸性比HSO 弱 ⑥Cl 与铁反应生成FeCl ,而S与铁反应生成FeS ⑦Cl 能与HS反应
2 4 2 3 2 2
生成S ⑧向NaSO 溶液中滴入适量盐酸可产生SO
2 3 2
A.③④⑥⑦ B.①③⑥⑦⑧ C.③④⑤⑦⑧ D.全部
【答案】A
【详解】
溶解度为物理性质,①不能说明;
比较酸性必须为最高价含氧酸,②不能说明;
氢化物的稳定性可以说明氯元素的非金属性大于硫,③正确;
离子的还原性可以说明,④正确;
不是最高价含氧酸,⑤错误;
氯气的氧化性大于硫,⑥可以说明;
氯气与硫化氢生成硫单质,氧化剂的氧化性大于氧化产物的氧化性,⑦可以说明;
比较酸性必须为最高价含氧酸及对应的盐,⑧不可以说明;
答案选A。
13.(本题3分)(2021·上海市徐汇中学高二期中)元素性质的周期性变化不包括
A.原子半径 B.主要化合价 C.原子核外电子层数D.金属性和非金属性
【答案】C
【详解】
随原子序数的递增,元素的原子半径、主要化合价、金属性和非金属性都呈现出周期性变化规律,称为元
素周期律;元素性质的周期性变化不包括原子核外电子层数的变化,故选C。14.(本题3分)(2021·浙江·诸暨中学高一期中)下列化学用语表示不正确的是
A.S2-的结构示意图 B.氯化铵的电子式:
C.N 的结构式:N≡N D.中子数为6的氮原子: N
2
【答案】B
【详解】
A.S是16号元素,S2-核外电子排布是2、8、8,所以S2-的结构示意图为: ,A正确;
B.氯化铵是离子化合物,阳离子 与阴离子Cl-之间以离子键结合,故其电子式为
,B错误;
C.N原子最外层有5个电子,其中含有3个成单电子,在N 中2个N原子通过3个共价键结合,从而使
2
分子中各原子都达到稳定结构,故N 的结构式:N≡N,C正确;
2
D.N是7号元素,原子核内有7个质子,中子数为6的氮原子的质量数是13,所以可表示为: N,D正
确;
故合理选项是B。
15.(本题3分)(2021·上海静安·高一期末)下列叙述中正确的是
A.含离子键的化合物一定是离子化合物
B.含共价键的化合物一定是共价化合物
C.全部由非金属元素形成的化合物一定是共价化合物
D.在离子化合物中也可能含有金属键
【答案】A
【详解】
A.含离子键的化合物一定是离子化合物,如NaCl、NaOH均一定含离子键,故A正确;
B.含共价键的化合物可能为离子化合物,如NaOH、NaClO等,故B错误;C.非金属元素形成的化合物可能为离子化合物,如铵盐,故C错误;
D.在离子化合物中也可能含有共价键和离子键,不可能含有金属键,故D错误;
答案:A。
16.(本题3分)(2021·浙江浙江·高一阶段练习)下列说法正确的是
A.冰的密度小于水,是因为冰中水分子的氢键导致分子间出现较大空隙
B.HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高
C.某物质在熔融态时能导电,则该物质定是离子化合物
D.NaO、NaHSO 熔融状态下,阳离子与阴离子个数比均为2:1
2 4
【答案】A
【详解】
A.冰中由于氢键的作用,水分子间形成正四面体结构,使得水分子间的空隙变大,所以水变冰后体积增
大,密度变小,A项正确;
B.非金属性越强,气态氢化物越稳定,则HF、HCl、HBr、HI的热稳定性依次减弱;而相对分子质量大
的沸点高,但HF分子之间含氢键,则沸点为:HF>HI>HBr>HCl,B项错误;
C.金属能导电,物质在熔融态时能导电,则该物质可能为金属或合金或离子化合物,C项错误;
D.NaHSO 晶体中阳离子与阴离子个数比为1:1,NaO晶体中阳离子与阴离子个数比为2:1,D项错误;
4 2
答案选A。
17.(本题3分)(2021·甘肃省徽县第二中学高一阶段练习)下列有关锂及其化合物的叙述中,不正确的是
A.LiHCO 受热能分解
3
B.Li可以与N 化合生成LiN
2 3
C.LiCO 与盐酸反应生成无色气体
2 3
D.Li在氧气中燃烧产物LiO中含有离子键
2
【答案】B
【详解】
A.锂与钠位于第IA族,性质具有相似性,均能失去最外层的一个电子,体现还原性,但由于原子核外电
子层有差异,使得原子核对核外电子引力有差异,因此化学性质上具有差异性。NaHCO 受热易分解,生
3
成碳酸钠、二氧化碳和水,则LiHCO 受热也能分解,故A正确;
3
B.Na与N 化合生成NaN(氮化钠),则Li与N 化合生成LiN(氮化锂),故B错误;
2 3 2 3
C.NaCO 与盐酸反应生成无色气体CO,则LiCO 与盐酸反应也能生成无色气体CO,故C正确;
2 3 2 2 3 2
D.Na与氧气反应,常温下生成NaO,点燃条件下产物是NaO,而Li的金属性弱于Na,Li在氧气中燃
2 2 2
烧产物是LiO,它是离子化合物,含有离子键,故D正确。
2故选B。
18.(本题3分)(2021·江苏·高二学业考试)短周期主族元素X、Y、Z的原子序数依次增大,X原子的最
外层电子数是次外层电子数的2倍,Y是地壳中含量最多的元素,Z是同周期金属性最强的元素。下列说
法正确的是
A.X元素位于第二周期VIA族
B.简单气态氢化物的热稳定性:X>Y
C.Y与Z形成的化合物只有一种
D.原子半径:r(Z)>r(X)>r(Y)
【答案】D
【分析】
短周期主族元素X、Y、Z的原子序数依次增大,X原子的最外层电子数是次外层电子数的2倍,则X核外
电子排布是2、4,所以X是C元素;Y是地壳中含量最多的元素,则Y是O元素;Z是同周期金属性最强
的元素,则Z是Na元素,然后根据元素周期律及物质的性质分析解答。
【详解】
根据上述分析可知:X是C,Y是O,Z是Na元素。
A.X是C元素,元素核外电子排布是2、4,根据元素的原子结构与元素在周期表的位置关系。可知C位
于元素周期表第二周期第IVA族,A错误;
B.元素的非金属性越强,其相应的简单氢化物的稳定性就越强。元素的非金属性:C<O,所以简单氢化
物的稳定性:CH<HO,即简单气态氢化物的热稳定性:X<Y,B错误;
4 2
C.Y是O,Z是Na元素,二者形成的化合物有NaO、NaO,因此Y与Z形成的化合物不仅只有一种,
2 2 2
C错误;
D.原子核外电子层数越多,原子半径越大;当原子核外电子层数相同时,原子序数越小,原子半径越大,
所以原子半径大小关系为:r(Z)>r(X)>r(Y),D正确;
故合理选项是D。
二、填空题(共34分)
19.(本题8分)(2021·全国·高一课时练习)已知氟、氯、溴、碘在元素周期表中位于同一纵行,都是典型
的非金属元素,都能与大多数金属化合生成盐,故统称为卤素。卤素单质都具有氧化性,其氧化性强弱顺
序是F>Cl>Br >I ,它们都能与H、HO等反应。
2 2 2 2 2 2
(1)若用X 表示卤素单质,则X 与H 化合的化学方程式是________________________,其反应条件难
2 2 2
易规律是________________________________________。(2)氧化性强的卤素单质(如Cl)能把氧化性弱的卤素从其卤化物(如NaBr或KI)中置换出来。请写出将氯
2
气通入碘化钾溶液中的化学方程式:______________________,离子方程式:
________________________________。
【答案】X+H=2HX 按F、Cl、Br 、I 顺序与H 化合由易到难 Cl+2KI=2KCl+I Cl+2I-
2 2 2 2 2 2 2 2 2 2
=2Cl-+I
2
【分析】
(1)卤素单质的氧化性强弱顺序是F>Cl>Br >I ,它们与同一种还原剂H 反应,由易到难,均生成卤化
2 2 2 2 2
氢,据此进行分析;
(2)氯气的氧化性大于碘,所以氯气能够置换碘,据此写出该反应的化学方程式和离子方程式。
【详解】
(1)由题意可知,卤素单质的氧化性强弱顺序是F>Cl>Br >I ,它们与同一种还原剂H 反应,由易到难,
2 2 2 2 2
生成物均为卤化氢,所以X 与H 化合的化学方程式是 X+H=2HX;
2 2 2 2
综上所述,本题答案是:X+H=2HX;按F、Cl、Br 、I 顺序与H 化合由易到难。
2 2 2 2 2 2 2
(2)氯气通入碘化钾溶液中生成氯化钾和单质碘,化学方程式:Cl+2KI=2KCl+I;碘化钾、氯化钾均
2 2
属于强电解质,均能溶于水,拆成离子形式,所以离子方程式:Cl+2I-=2Cl-+I ;
2 2
综上所述,本题答案是:Cl+2KI=2KCl+I ;Cl+2I-=2Cl-+I。
2 2 2 2
20.(本题12分)(2021·甘肃·永昌县第一高级中学高一期末)根据要求回答下列问题。
①CaBr ②HO ③NaCl ④HO ⑤NaO ⑥Ca(OH) ⑦HClO
2 2 2 2 2 2 2
(1)只含有离子键的是___(填序号,下同)。
(2)含有共价键的离子化合物是___,其中含有非极性共价键的物质的电子式为___。
(3)属于共价化合物的是___。
(4)熔融状态下能导电的化合物是___。
(5)用电子式表示HO的形成过程___。
2
【答案】
(1)①③
(2) ⑤⑥
(3)②④⑦
(4)①③⑤⑥
(5)
【分析】(1)
①CaBr 中只含离子键,②HO中只含共价键,③NaCl中含离子键,④HO 中含共价键,⑤NaO 中含离
2 2 2 2 2 2
子键和共价键,⑥Ca(OH) 中含离子键和共价键,⑦HClO中只含共价键,只含有离子键的是:①③;
2
(2)
含有共价键的离子化合物是⑤⑥,含有非极性共价键的物质是⑤NaO,其电子式为 ;
2 2
(3)
含有共价键的共价化合物为②④⑦;
(4)
CaBr 、NaCl、NaO、Ca(OH) 是含离子键的离子化合物,在熔融状态下能够导电,故选①③⑤⑥;
2 2 2 2
(5)
水属于共价化合物,以共用电子对形成化学键,用电子式表示HO的形成过程为
2
。
21.(本题14分)(2021·重庆·高一期末)元素周期律是自然科学的基本规律,元素周期表是元素周期律的
具体表现形式,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。 我们可以利用元素的
性质、它在周期表中的位置和它的原子结构三者之间的密切关系来指导化学学习研究。下图为元素周期表
的一部分,请回答下列问题:
A
B
C D E
(1)A、B、C、D、E五种元素中原子半径最小的是_______(填元素符号)。
(2)D在元素周期表中的位置是_______。
(3)E的最高价氧化物对应的水化物的化学式为_______。
(4)元素C与E形成的化合物电子式为_______。
(5)化合物C B 中含有的化学键类型是_______,C B 与CO 反应的化学方程式为_______。
2 2 2 2 2
(6)化合物AB、AD中热稳定性高的是_______(填化学式),原因是_______。
2 2【答案】H 第三周期VIA族 HClO 离子键、共价键
4
HO O 的非金属性更强,简单氢化物的热稳定性更高
2
【分析】
由A、B、C、D、E在周期表中的位置可知五种元素分别为H、O、Na、S、Cl,据此解答。
【详解】
(1)原子的核外电子层数越少半径越小,电子层数相同时,核电荷数越大半径越小,五种元素中H只有一个
电子层,原子半径最小,故答案为:H;
(2)D为S,原子序数为16,处于周期表中第三周期第VIA族,故答案为:第三周期VIA族;
(3)E为Cl,最外层电子数为7,最高正价为+7价,最高价氧化物的水化物为HClO,故答案为:HClO;
4 4
(4)C与E形成的化合物为NaCl,属于离子化合物,其电子式为: ,故答案为:
;
(5)化合物C B 为 ,由两个钠离子和一个过氧根离子组成,钠离子和过氧根之间存在离子键,过氧根
2 2
内部存在共价键;过氧化钠与二氧化碳反应产生碳酸钠和氧气,反应方程式为:
,故答案为:离子键、共价键; ;
(6)元素的非金属性越强形成的气态氢化物越稳定,非金属性:O>S,则氢化物的稳定性:HO>HS,故答
2 2
案为:O;O的非金属性更强,简单氢化物的热稳定性更高;
三、实验题(共12分)
22.(本题12分)(2021·广东·揭阳华侨高中高一阶段练习)已知非金属单质硫(S)是淡黄色固体粉末,难溶
于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列
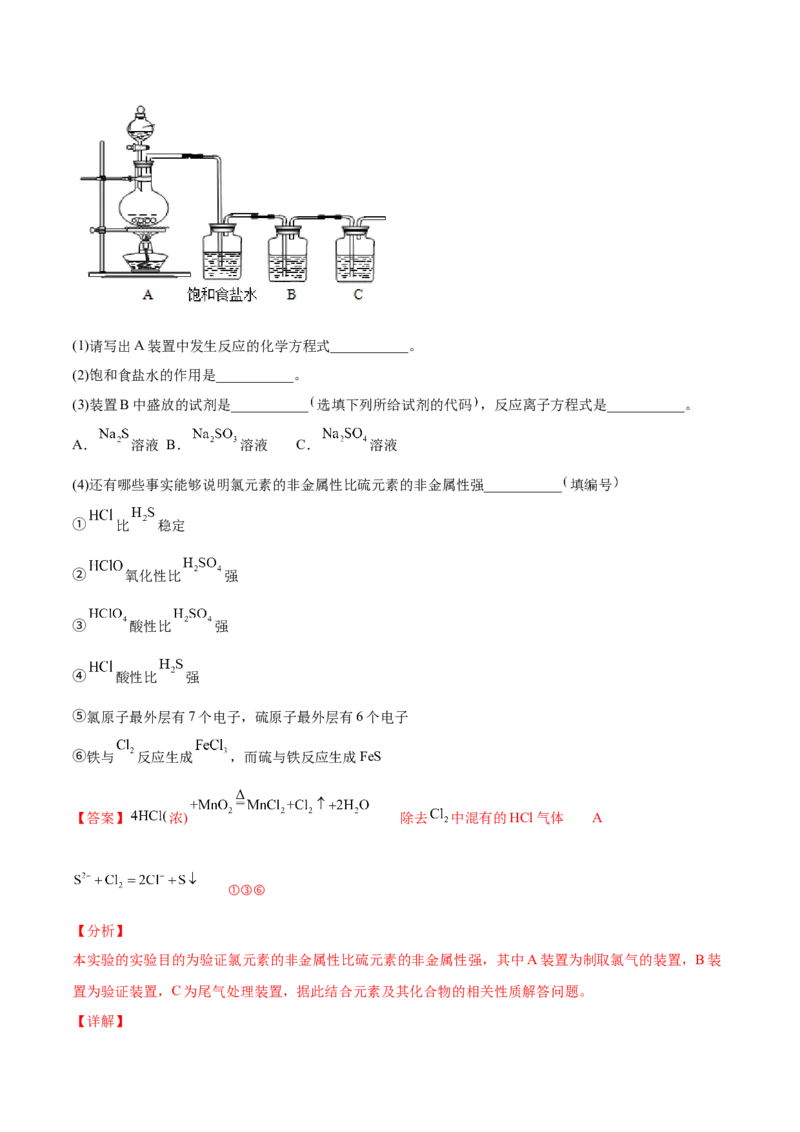
问题:(1)请写出A装置中发生反应的化学方程式___________。
(2)饱和食盐水的作用是___________。
(3)装置B中盛放的试剂是___________ 选填下列所给试剂的代码 ,反应离子方程式是___________。
A. 溶液 B. 溶液 C. 溶液
(4)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强___________ 填编号
① 比 稳定
② 氧化性比 强
③ 酸性比 强
④ 酸性比 强
⑤氯原子最外层有7个电子,硫原子最外层有6个电子
⑥铁与 反应生成 ,而硫与铁反应生成FeS
【答案】 浓) 除去 中混有的HCl气体 A
①③⑥
【分析】
本实验的实验目的为验证氯元素的非金属性比硫元素的非金属性强,其中A装置为制取氯气的装置,B装
置为验证装置,C为尾气处理装置,据此结合元素及其化合物的相关性质解答问题。
【详解】(1)A装置为制取氯气的装置,实验室常用浓盐酸与二氧化锰混合加热制取氯气,反应的化学方程式为
浓) ;
(2)浓盐酸易挥发,故制得的氯气中含有挥发的HCl气体,饱和食盐水可除去Cl 中混有的HCl气体;
2
(3)B装置为验证装置,可选用NaS溶液,由于Cl 的氧化性强于S,故可以从NaS中置换出S,发生的反
2 2 2
应为 ;
(4)①非金属性越强,氢化物越稳定, 比 稳定,说明非金属性Cl>S,①选;
② 氧化性比 强不能说明非金属性Cl>S,②不选;
③非金属性越强,最高价氧化物对应水化物的酸性越强, 酸性比 强,说明非金属性Cl>S,
③选;
④HCl和HS均不是Cl和S的最高价含氧酸,故 酸性比 强不能说明非金属性Cl>S,④不选;
2
⑤氯原子最外层有7个电子,硫原子最外层有6个电子不能说明非金属性Cl>S,⑤不选;
⑥铁与 反应生成 ,而硫与铁反应生成FeS,说明氧化性:Cl>S,则非金属性Cl>S,⑥选;
2
综上,答案选①③⑥。关注更新免费领取,淘宝唯一每月更新店铺:知二教育