文档内容
《物质结构 元素周期律》单元测试(培优提升)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共48分)
1.(本题3分)《本草纲目》中的“石碱”条目下写道:“彼人采蒿蓼之属, 开窖浸水,漉起,晒干烧灰,以
原水淋汁,每百引入粉面二、三斤,久则凝淀如石,连汁货之四方,浣衣发面,甚获利也。他处以灶灰淋
浓汁,亦去垢发面。”下列说法错误的是
A.“石碱”中含有离子键
B.“石碱”中含有极性共价键
C.“石碱”是离子化合物
D.“石碱”中含有非极性共价键
2.(本题3分)下列关于 的说法错误的是
A.核外电子数为33 B.位于元素周期表第4周期ⅣA族
C. 和 的化学性质几乎相同 D.a克 含有的中子数目为
3.(本题3分)下列关于原子结构的说法有误的是
A.原子的种类由质子数和中子数决定
B. 可发生核聚变反应是化学变化
C.在原子结构分层排布中,M层(第三层)容纳电子数最多为18
D.在化学反应过程中,原子核不发生变化,但原子外层电子可能发生变化
4.(本题3分)下列有关原子结构和元素周期律表述正确的是
①原子序数为15的元素的最高化合价为+3
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族
⑤同周期相邻主族元素的原子序数之差一定为1
⑥同一元素的各种同位素的物理性质、化学性质均相同⑦金属元素原子的最外层电子数一定≤4
A.②④ B.①②⑤ C.②⑤⑦ D.③④⑤⑥⑦
5.(本题3分)下列说法正确的是
A.某短周期元素最外层有2个电子,则其一定是第ⅡA族元素
B.主族元素的单原子阳离子一定具有稀有气体的电子层结构(H+除外)
C.元素周期表有7个主族8个副族,副族均由长周期元素组成
D.主族元素在周期表中的位置只取决于该元素的电子层数
6.(本题3分)下列关于元素周期表说法正确的是
A.元素周期表中最外层电子数为2的元素一定在第ⅡA族
B.在过渡元素中找优良催化剂和耐高温、耐腐蚀的合金材料
C.元素所在族序数等于元素原子最外层电子数
D.元素周期表有七个横行,分为七个周期,有18个纵行,分为18个族,其中8、9、10三个纵行合称第
Ⅷ族
7.(本题3分)氰[(CN) ]的化学性质与卤素(X )很相似,化学上称之为拟卤素,其氧化性介于Br 和I 之间,
2 2 2 2
下列有关说法不正确的是( )
A.常温时,(CN) 和NaOH溶液反应的产物中有NaCNO
2
B.MnO 和HCN反应的产物中有 (CN)
2 2
C.向KCN溶液中加入碘水反应的产物中一定有KI
D.在NaBr和KCN混合溶液中通入少量Cl 的产物中一定有(CN)
2 2
8.(本题3分)以下关于锂、钠、钾、铷、铯的叙述不正确的是( )
① 氢氧化物中碱性最强的是CsOH ② 单质熔点最高的是铯
③ 它们的密度依次增大 ④ 其单质的还原性依次增强
⑤ 它们对应离子的氧化性依次增强 ⑥ 单质与水反应的剧烈程度依次增加
⑦ 单质与相同浓度、相同体积的盐酸反应的剧烈程度依次增加
A.① ⑤ ⑦ B.② ⑥ C.② ③ ⑤ D.② ③ ④
9.(本题3分)下列各组物质的性质由强到弱的顺序排列正确的是
A.酸性:HClO>H PO >H SO B.氢化物稳定性:HF>H O>NH
4 3 4 2 4 2 3C.碱性:NaOH>Al(OH) >Mg(OH) D.还原性:HF>HCl>HI>HBr
3 2
10.(本题3分)下列说法中正确的是( )
A.金属只有正价,非金属只有负价
B.氟无正价,氧无最高正价
C.主族元素的最高正价等于其原子最外层电子数
D.同周期元素的最外层电子数越多,原子半径越大
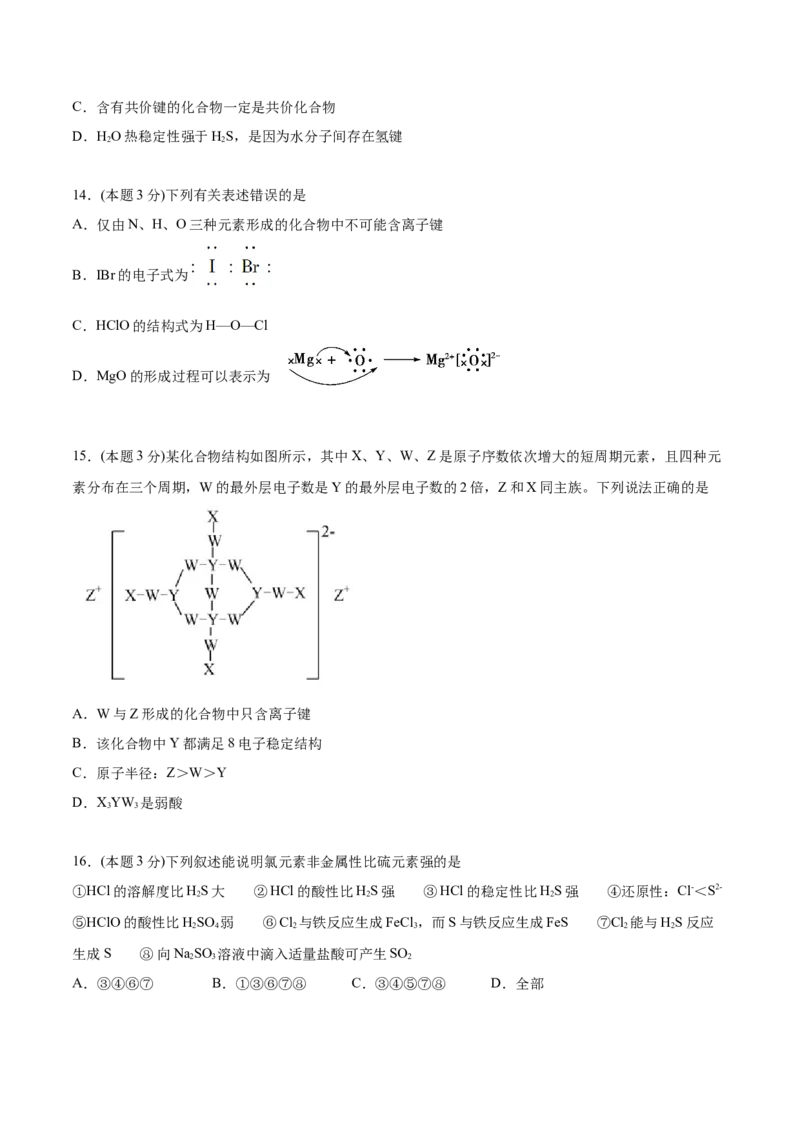
11.(本题3分)短周期元素X、Y、Z、M原子序数依次增大,Z的最简单氢化物与最高正价的氧化物的水
化物能发生反应生成盐,M的最高正价与最低负价绝对值之差为4,它们组成的一种分子结构如图。下列
说法正确的是
A.非金属性:
B.原子半径:
C.Y、Z、M的最简单氢化物的沸点:
D.Y、Z、M的最高价氧化物的水化物均为强酸
12.(本题3分)氢化钠(NaH)是一种白色的离子化合物,其中钠元素显+1价;氢化钠与水反应生成H 和
2
NaOH。下列叙述中,不正确的是
A.NaH的电子式为Na+[:H]-
B.NaH中H-的电子层排布与氦原子的电子层排布相同
C.反应中每生成1molH 时,转移的电子数为2N
2 A
D.NaH与HO反应时,HO做氧化剂
2 2
13.(本题3分)下列有关微粒间相互作用说法正确的是
A.金属元素和非金属元素之间只能形成离子键,非金属元素之间只能形成共价键
B.过氧化钠和水反应时既有离子键和共价键的断裂,又有离子键和共价键的形成C.含有共价键的化合物一定是共价化合物
D.HO热稳定性强于HS,是因为水分子间存在氢键
2 2
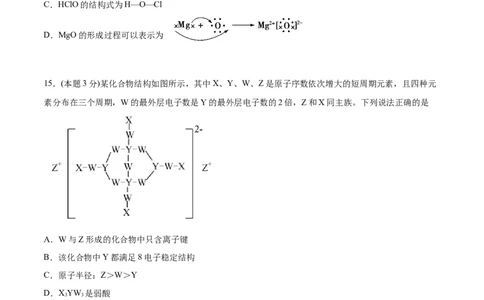
14.(本题3分)下列有关表述错误的是
A.仅由N、H、O三种元素形成的化合物中不可能含离子键
B.IBr的电子式为
C.HClO的结构式为H—O—Cl
D.MgO的形成过程可以表示为
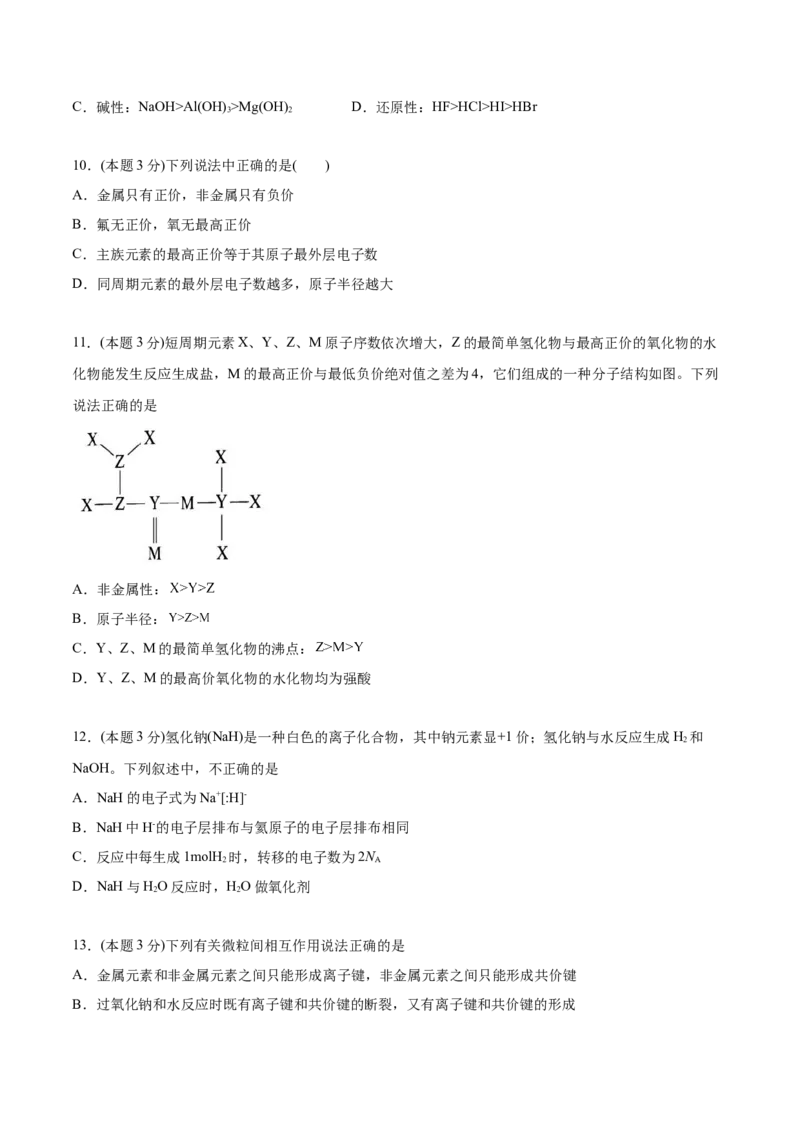
15.(本题3分)某化合物结构如图所示,其中X、Y、W、Z是原子序数依次增大的短周期元素,且四种元
素分布在三个周期,W的最外层电子数是Y的最外层电子数的2倍,Z和X同主族。下列说法正确的是
A.W与Z形成的化合物中只含离子键
B.该化合物中Y都满足8电子稳定结构
C.原子半径:Z>W>Y
D.XYW 是弱酸
3 3
16.(本题3分)下列叙述能说明氯元素非金属性比硫元素强的是
①HCl的溶解度比HS大 ②HCl的酸性比HS强 ③HCl的稳定性比HS强 ④还原性:Cl-<S2-
2 2 2
⑤HClO的酸性比HSO 弱 ⑥Cl 与铁反应生成FeCl ,而S与铁反应生成FeS ⑦Cl 能与HS反应
2 4 2 3 2 2
生成S ⑧向NaSO 溶液中滴入适量盐酸可产生SO
2 3 2
A.③④⑥⑦ B.①③⑥⑦⑧ C.③④⑤⑦⑧ D.全部二、填空题(共52分)
17.(本题12分)(1)写出下列物质的电子式:
NH Cl_______,N_______,HClO_______。
4 2
(2)用电子式表示出下列化合物形成过程:
NaO_______,CO_______。
2 2
(3)已知有下列物质:①HNO②硫单质③NaOH④液氦⑤NaO⑥HO⑦CCl ⑧NH Cl⑨KBr⑩O,分别将
3 2 2 2 2 4 4 2
正确的序号填入相应的位置。
以上物质中只含有离子键的是_______;只含有共价键的是_______;既含有离子键又含有共价键的是
_______;含有非极性共价键的化合物是_______;不含化学键的是_______。
18.(本题8分)据报道,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将给量子计
算机的研究带来重大突破。已知铷是37号元素。根据相关知识回答下列问题:
(1)铷(Rb)位于元素周期表的第________周期________族。
(2)关于铷的结构和性质判断正确的是________(填序号)。
①与水反应比钠剧烈
②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO
2
④它的阳离子最外层电子数和镁相同
⑤它是还原剂
(3)现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,这种碱
金属可能是________(填序号)。
a.Li b.Na
c.K d.Cs
19.(本题16分)元素①~⑩在周期表中的位置如表所示,试回答下列问题。
(1)上述10 种元素中,化学性质最不活泼的是___(填元素符号,下同);与水反应最激烈的金属元素是___________。
(2)元素②的气态氢化物的分子式是_____;上述10 种元素中,其最高价氧化物对应水化物的酸性最强
的物质是_______(填化学式)。
(3)元素③与④形成的常用作供氧剂的化合物的电子式_________。
(4)①②⑤元素的原子半径由小到大的顺序为______(用元素符号表示) ;
请用一个化学方程式(或离子方程式)说明元素⑦和⑩非金属性的强弱:_____。
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:____________。
20.(本题16分)A、B、C、D、E是位于短周期的主族元素。已知:①氢化物的稳定性H D>H C;
m m
②Cm-、E(m-1)-具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最
大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下
列问题:
(1)H D 的电子式为_______,含有_______(填“离子键”、“极性键”或“非极性键”)。
m m
(2)Cm-、E(m-1)-的还原性强弱顺序为_______、离子半径大小顺序为_______(均用离子符号表示),能证明
其还原性强弱的离子方程式为_______。
(3)比较两种氢化物的沸点:H D_______H C(填“>”或“<”),其中一种物质沸点高的主要原因为_______;
m m
C元素在元素周期表中的位置为_______。
(4)用于判断C和D非金属性强弱的依据是_______。
A.简单气态氢化物的稳定性 B.与氢气化合的难易程度
C.得电子数目的多少 D.最高价含氧酸的酸性关注更新免费领取,淘宝唯一每月更新店铺:知二教育