文档内容
下学期期中学业水平质量调研试题
九年级化学
说明:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。第Ⅰ卷1~3页,第Ⅱ卷4
~6页。全卷满分100分,考试时间90分钟。
2.答卷前,考生务必将自己的姓名、考号、考试科目涂写在答题卡和答题纸上。
3.第Ⅰ卷每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改
动,用橡皮擦干净后,再选涂其他答案标号,第Ⅱ卷题目的答案用黑色签字笔写在答题纸
的相应位置上,写在试卷上的答案无效。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Ca-40
第Ⅰ卷
(选择题 共36分)
一、选择题(本题包括18小题,每小题只有一个选项符合题意,每题2分,共36分)
1.下列物质的用途,主要是由其物理性质决定的是( )
A.氧气可用于医疗急救 B.澄清石灰水可用于检验二氧化碳
C.天然气可用于取暖、做饭 D.铁水可铸成铁锅
2.下列工艺制作中包含化学变化的是( )
A.粘土烧制陶瓷 B.纸剪成窗花 C.冰做成冰雕 D.糖捏成糖人
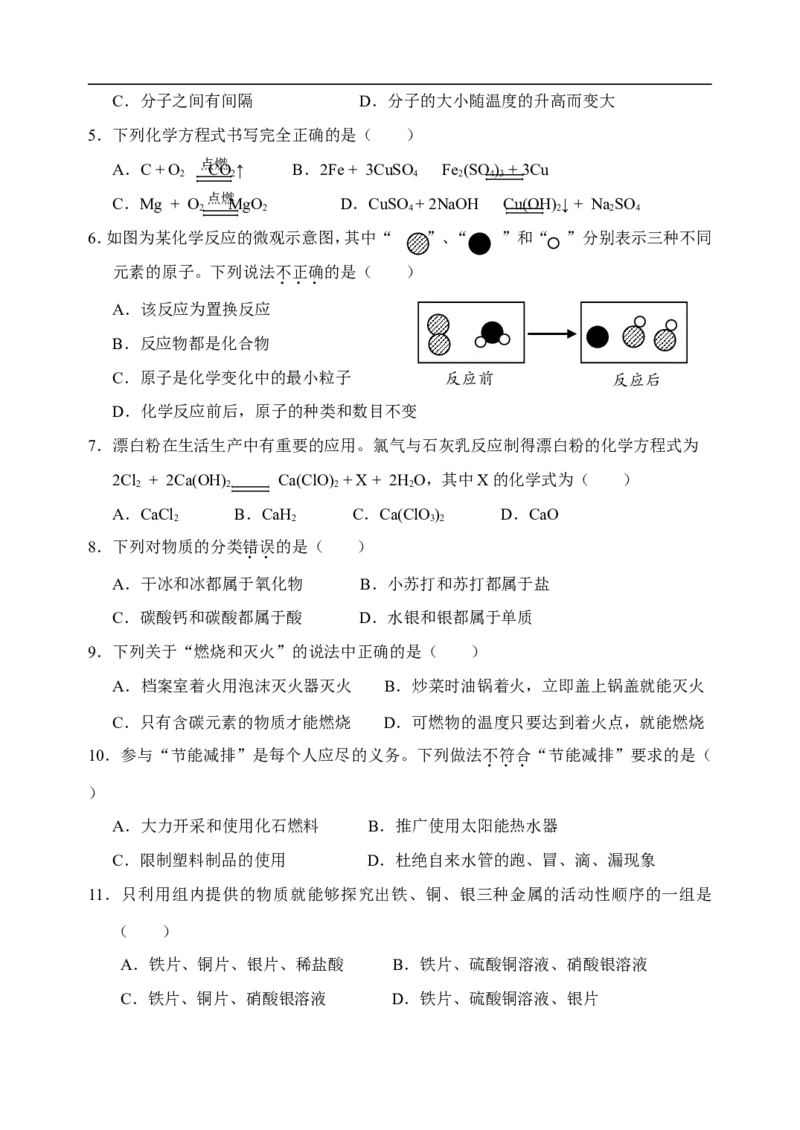
3.下列实验操作中,错误的是( )
A.熄灭酒精灯 B.检查气密性 C.滴加液体 D.加热液体
4.变瘪的乒乓球放入热水中能重新鼓起来,说明了( )
A.分子在不断运动 B.分子的质量和体积都很小C.分子之间有间隔 D.分子的大小随温度的升高而变大
5.下列化学方程式书写完全正确的是( )
A.C + O 点 C 燃 O↑ B.2Fe + 3CuSO Fe (SO ) + 3Cu
2 2 4 2 4 3
C.Mg + O 点 燃 MgO D.CuSO + 2NaOH Cu(OH) ↓ + NaSO
2 2 4 2 2 4
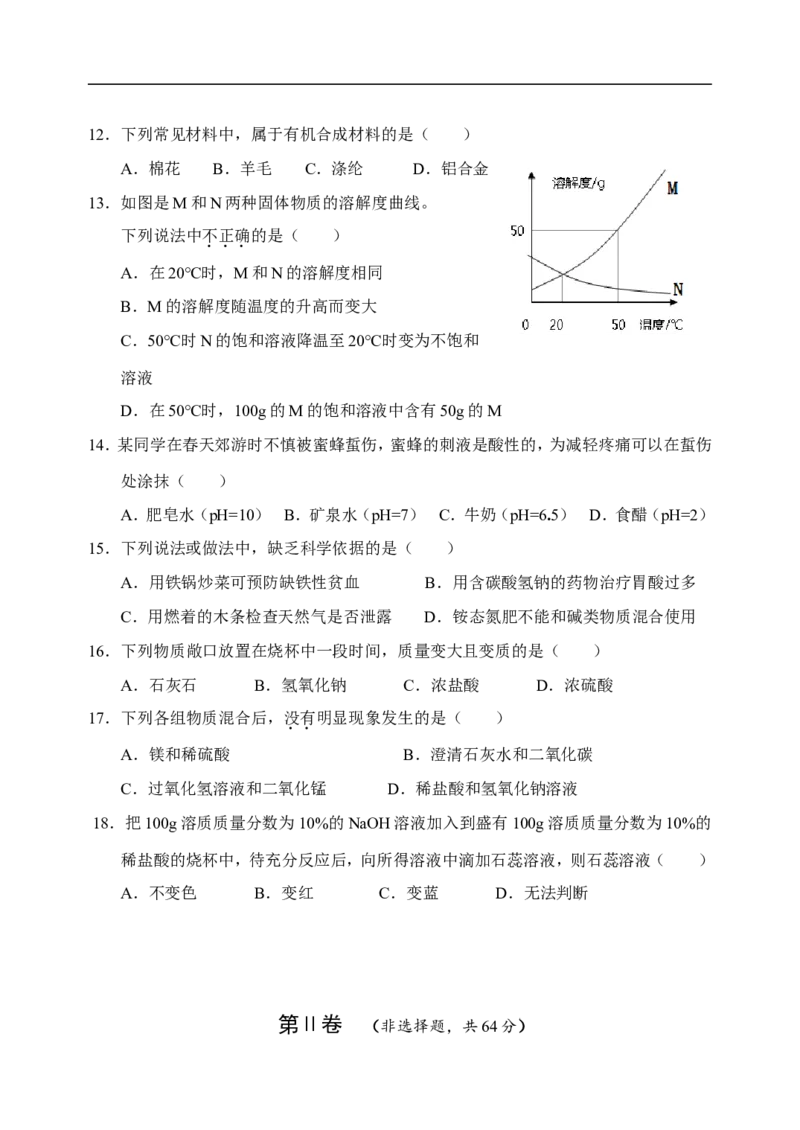
6.如图为某化学反应的微观示意图,其中“ ”、“ ”和“ ”分别表示三种不同
元素的原子。下列说法不正确的是( )
A.该反应为置换反应
B.反应物都是化合物
C.原子是化学变化中的最小粒子 反应前 反应后
D.化学反应前后,原子的种类和数目不变
7.漂白粉在生活生产中有重要的应用。氯气与石灰乳反应制得漂白粉的化学方程式为
2Cl + 2Ca(OH) Ca(ClO) + X + 2HO,其中X的化学式为( )
2 2 2 2
A.CaCl B.CaH C.Ca(ClO ) D.CaO
2 2 3 2
8.下列对物质的分类错误的是( )
A.干冰和冰都属于氧化物 B.小苏打和苏打都属于盐
C.碳酸钙和碳酸都属于酸 D.水银和银都属于单质
9.下列关于“燃烧和灭火”的说法中正确的是( )
A.档案室着火用泡沫灭火器灭火 B.炒菜时油锅着火,立即盖上锅盖就能灭火
C.只有含碳元素的物质才能燃烧 D.可燃物的温度只要达到着火点,就能燃烧
10.参与“节能减排”是每个人应尽的义务。下列做法不符合“节能减排”要求的是(
)
A.大力开采和使用化石燃料 B.推广使用太阳能热水器
C.限制塑料制品的使用 D.杜绝自来水管的跑、冒、滴、漏现象
11.只利用组内提供的物质就能够探究出铁、铜、银三种金属的活动性顺序的一组是
( )
A.铁片、铜片、银片、稀盐酸 B.铁片、硫酸铜溶液、硝酸银溶液
C.铁片、铜片、硝酸银溶液 D.铁片、硫酸铜溶液、银片12.下列常见材料中,属于有机合成材料的是( )
A.棉花 B.羊毛 C.涤纶 D.铝合金
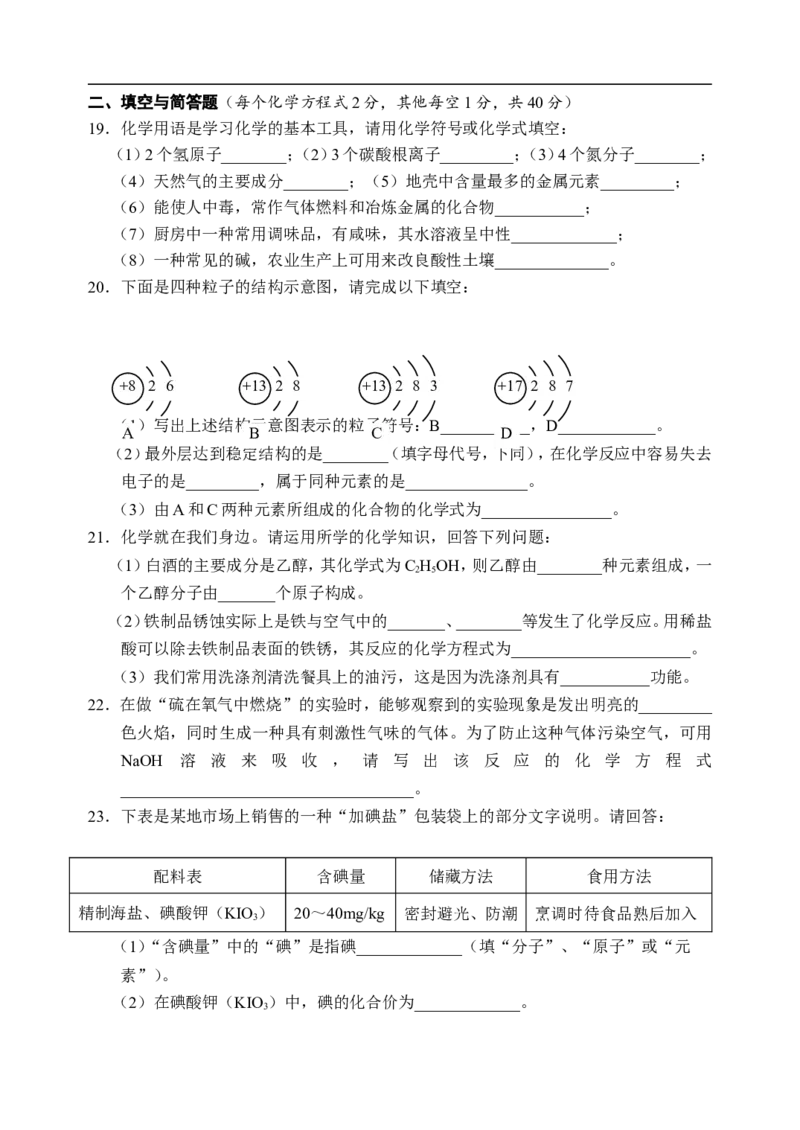
13.如图是M和N两种固体物质的溶解度曲线。
下列说法中不正确的是( )
A.在20℃时,M和N的溶解度相同
B.M的溶解度随温度的升高而变大
C.50℃时N的饱和溶液降温至20℃时变为不饱和
溶液
D.在50℃时,100g的M的饱和溶液中含有50g的M
14.某同学在春天郊游时不慎被蜜蜂蜇伤,蜜蜂的刺液是酸性的,为减轻疼痛可以在蜇伤
处涂抹( )
A.肥皂水(pH=10) B.矿泉水(pH=7) C.牛奶(pH=6.5) D.食醋(pH=2)
15.下列说法或做法中,缺乏科学依据的是( )
A.用铁锅炒菜可预防缺铁性贫血 B.用含碳酸氢钠的药物治疗胃酸过多
C.用燃着的木条检查天然气是否泄露 D.铵态氮肥不能和碱类物质混合使用
16.下列物质敞口放置在烧杯中一段时间,质量变大且变质的是( )
A.石灰石 B.氢氧化钠 C.浓盐酸 D.浓硫酸
17.下列各组物质混合后,没有明显现象发生的是( )
A.镁和稀硫酸 B.澄清石灰水和二氧化碳
C.过氧化氢溶液和二氧化锰 D.稀盐酸和氢氧化钠溶液
18.把100g溶质质量分数为10%的NaOH溶液加入到盛有100g溶质质量分数为10%的
稀盐酸的烧杯中,待充分反应后,向所得溶液中滴加石蕊溶液,则石蕊溶液( )
A.不变色 B.变红 C.变蓝 D.无法判断
第Ⅱ卷
(非选择题,共64分)二、填空与简答题(每个化学方程式2分,其他每空1分,共40分)
19.化学用语是学习化学的基本工具,请用化学符号或化学式填空:
(1)2个氢原子________;(2)3个碳酸根离子_________;(3)4个氮分子________;
(4)天然气的主要成分________;(5)地壳中含量最多的金属元素_________;
(6)能使人中毒,常作气体燃料和冶炼金属的化合物___________;
(7)厨房中一种常用调味品,有咸味,其水溶液呈中性_____________;
(8)一种常见的碱,农业生产上可用来改良酸性土壤______________。
20.下面是四种粒子的结构示意图,请完成以下填空:
+8 2 6 +13 2 8 +13 2 8 3 +17 2 8 7
(1)写出上述结构示意图表示的粒子符号:B___________,D____________。
A B C D
(2)最外层达到稳定结构的是________(填字母代号,下同),在化学反应中容易失去
电子的是_________,属于同种元素的是_______________。
(3)由A和C两种元素所组成的化合物的化学式为________________。
21.化学就在我们身边。请运用所学的化学知识,回答下列问题:
(1)白酒的主要成分是乙醇,其化学式为C HOH,则乙醇由________种元素组成,一
2 5
个乙醇分子由_______个原子构成。
(2)铁制品锈蚀实际上是铁与空气中的_______、________等发生了化学反应。用稀盐
酸可以除去铁制品表面的铁锈,其反应的化学方程式为______________________。
(3)我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有___________功能。
22.在做“硫在氧气中燃烧”的实验时,能够观察到的实验现象是发出明亮的_________
色火焰,同时生成一种具有刺激性气味的气体。为了防止这种气体污染空气,可用
NaOH 溶 液 来 吸 收 , 请 写 出 该 反 应 的 化 学 方 程 式
____________________________________。
23.下表是某地市场上销售的一种“加碘盐”包装袋上的部分文字说明。请回答:
配料表 含碘量 储藏方法 食用方法
精制海盐、碘酸钾(KIO) 20~40mg/kg 密封避光、防潮 烹调时待食品熟后加入
3
(1)“含碘量”中的“碘”是指碘_____________(填“分子”、“原子”或“元
素”)。
(2)在碘酸钾(KIO)中,碘的化合价为_____________。
3(3)碘酸钾和氯酸钾有着相似的化学性质,在加热时容易分解,其生成物之一是空气中
体积分数占21%的气体,请写出该反应的化学方程式______________________。
24.已知A、B、C、D、E是初中化学常见的物质。D物质的水溶液为蓝色,E是相对分子质
量最小的氧化物,它们的转化关系如图所示:
A
(1)写出下列物质的化学式: +O 2 +CO
A B
C___________,D____________。 △ △
C
+H SO
(2)写出A物质与O 反应的化学方程式 2 4
2
_____________________________________,
D E
该反应的基本反应类型为_______________;
(3)写出B物质与CO反应的化学方程式
________________________________________,通过这个反应说明了CO具有
__________(填“可燃性”、“还原性”或“氧化性”) 。
25.向含有AgNO、Cu(NO ) 和Mg(NO)的混合溶液中加入一定量的铁粉,待充分反应后
3 3 2 3
过滤,向得到的滤渣中加入稀盐酸,发现有气体产生,请回答:
(1)滤渣中的物质有___________________,滤液中的溶质有____________________。
(2)请写出铁粉与硝酸银溶液反应的化学方程式______________________________。
三、实验探究题(每个化学方程式2分,其他每空1分,共12分)
26.长期使用的水壶底部会结有一层水垢,其主要成分是CaCO 和Mg(OH) 。某同学把家
3 2
里烧水用的铝制水壶带到了化学实验室,想探究盐酸与水垢反应的情况。
(1)当该同学把一定量的盐酸倒入铝壶底部时,立刻产生大量气体,水垢逐渐溶解、消
失,请写出稀盐酸与Mg(OH) 反应的化学方程式____________________________。
2
(2)当水垢被除净后,该同学发现水壶底部仍有气体产生,该气体是___________。
(3)实验反思:在用盐酸除铝制水壶内的水垢时,应注意________________________。
27.小亮同学想通过实验探究某企业采用氨碱法制得纯碱样品的成分。
【提出问题】该纯碱样品中含有哪些物质?
【猜想与假设】猜想一:只含有NaCO; 猜想二:含有NaCO 和NaHCO 。
2 3 2 3 3
【查阅资料】
NaHCO 溶液 NaCO 溶液
3 2 3
加入稀盐酸 现象Ⅰ 产生气泡
加入饱和澄清石灰水 溶液变浑浊 现象Ⅱ
加入CaCl 溶液 无明显变化 溶液变浑浊
2
(1)表中的现象Ⅰ为______________________。
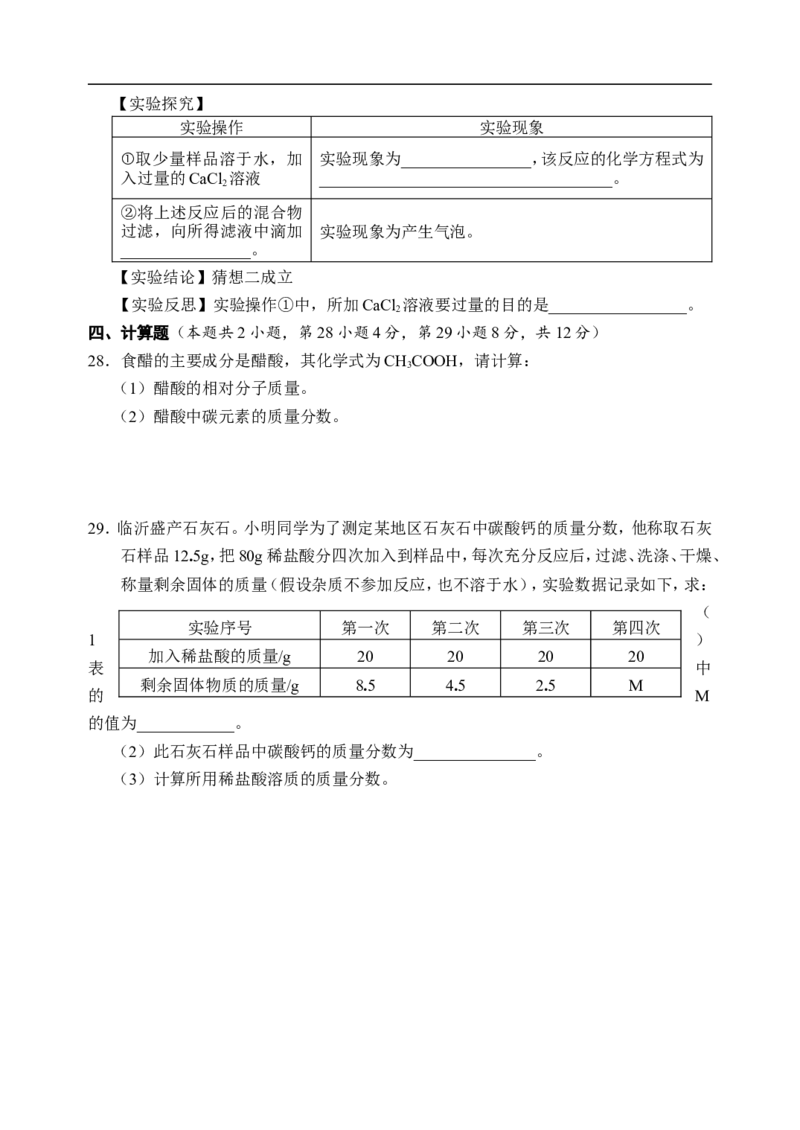
(2)现象Ⅱ对应的化学方程式为____________________________________________。【实验探究】
实验操作 实验现象
①取少量样品溶于水,加 实验现象为________________,该反应的化学方程式为
入过量的CaCl 溶液 ____________________________________。
2
②将上述反应后的混合物
过滤,向所得滤液中滴加 实验现象为产生气泡。
________________。
【实验结论】猜想二成立
【实验反思】实验操作①中,所加CaCl 溶液要过量的目的是_________________。
2
四、计算题(本题共2小题,第28小题4分,第29小题8分,共12分)
28.食醋的主要成分是醋酸,其化学式为CHCOOH,请计算:
3
(1)醋酸的相对分子质量。
(2)醋酸中碳元素的质量分数。
29.临沂盛产石灰石。小明同学为了测定某地区石灰石中碳酸钙的质量分数,他称取石灰
石样品12.5g,把80g稀盐酸分四次加入到样品中,每次充分反应后,过滤、洗涤、干燥、
称量剩余固体的质量(假设杂质不参加反应,也不溶于水),实验数据记录如下,求:
(
实验序号 第一次 第二次 第三次 第四次
1 )
加入稀盐酸的质量/g 20 20 20 20
表 中
剩余固体物质的质量/g 8.5 4.5 2.5 M
的 M
的值为____________。
(2)此石灰石样品中碳酸钙的质量分数为_______________。
(3)计算所用稀盐酸溶质的质量分数。下学期期中学业水平质量调研试题
九年级化学参考答案
一、选择题(本题包括18小题,每小题只有一个选项符合题意,每题2分,共36分)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
D A C C D B A C B A D C D A C B D B
二、填空与简答题(每个化学方程式2分,其他每空1分,共40分)
19.(1)2H (2)3CO2- (3)4N (4)CH (5)Al (6)CO (7)NaCl (8)Ca(OH)
3 2 4 2
20.(1)Al3+ Cl (2)B C B、C (3)Al O
2 3
21.(1)3 9 (2)氧气(或O) 水蒸气(或HO) Fe O + 6HCl=2FeCl + 3HO
2 2 2 3 3 2
(3)乳化
22.蓝紫 2NaOH + SO =NaSO + HO
23.(1)元素 (2)+5 2 (3)2 2K 3 IO 2 2KI + 3O↑
3 2
△
24.(1)CO CuSO (2)2Cu + O 2CuO 化合反应
2 4 2
△
(3)CuO + CO Cu + CO↑ 还原性
2
△
25.(1)Ag、Cu、Fe(或银、铜、铁) Mg(NO)、Fe(NO )
3 2 3 2
(2)Fe + 2AgNO=2Ag + Fe(NO )
3 3 2
三、实验探究题(每个化学方程式2分,其他每空1分,共12分)
26.(1)2HCl + Mg(OH) =MgCl + 2HO (2)H (3)所用盐酸要适量(或不要过量)
2 2 2 2
27.(1)产生气泡(2)Ca(OH) + NaCO=CaCO ↓ + 2NaOH 溶液变浑浊(或产生白色
2 2 3 3
沉淀) CaCl + NaCO=CaCO ↓ + 2NaCl 稀盐酸 让NaCO 反应完全
2 2 3 3 2 3
四、计算题(本题共2小题,第28小题4分,第29小题8分,共12分)
28.(1)12+1×3+12+16+16+1=60
12×2
(2) ×100%=40%
60
29.(1)2.5 (2)80%
(3)解:设第一次参加反应的20g稀盐酸中氯化氢的质量为x
CaCO + 2HCl=CaCl + HO + CO↑
3 2 2 2
100 73
12.5g-8.5g x
100 4g
=
73 x
x=2.92g
稀 盐 酸溶质的质量分数为
2.92g
×100%=14.6%
20g
答:所用稀盐酸溶质的质量分数为14.6%。