文档内容
第 2 课时 海水资源的开发利用
学业要求 核心素养对接
1.了解海水资源及其利用。
2.掌握海水化学资源的开发和利用,即 通过学习海水资源的开发利用,培养学
海水制盐,海水提镁、提溴、提碘。 生科学态度与社会责任。
3.了解海水综合利用的重要方向。
[知 识 梳 理]
知识点一 海水水资源的开发利用
这是工业海水淡化的图片,那么海水淡化有哪些方法呢?请完成下列知识点:
1.直接利用:海水进行循环冷却。
2.海水淡化:主要方法有蒸馏法、电渗析法、离子交换法。
知识点二 海水化学资源的开发利用
这是海水晒盐、海水提镁的图片,海水化学资源究竟如何应用?请完成下列知识
点:
1.海水中的化学资源
海水中H、O两种元素,加上 Cl 、 Na 、 K 、 Ca 、 Mg 、 S 、 C 、 F 、 B 、 Br 、 Sr 等11种元素的
总量超过99%,其他为微量元素,共计含有80多种。
2.海水制盐
海水――→粗盐――→精盐。
3.海带提碘(1)流程:海带―→灼烧―→浸泡―→过滤――→氧化―→提纯―→碘单质。
(2)原理: 2I - + Cl == =I + 2C l - 。
2 2
4.海水提溴
(1)过程:浓缩―→氧化―→富集―→提取。
(2)原理: 2Br - + Cl == =Br + 2C l - 。
2 2
5.海水提镁
(1)过程:浓缩――→沉淀―→过滤――→溶解―→结晶(MgCl ·6H O)
2 2
――→MgCl 晶体――→金属镁。
2
(2)原理:① Mg 2 + + 2OH - == =Mg ( OH ) ↓。
2
②Mg(OH) +2HCl===MgCl +2H O。
2 2 2
③MgCl ·6H O=====MgCl +6H O。
2 2 2 2
④MgCl (熔融) ===== M g + C l ↑。
2 2
6.新能源的开发
(1)从海水中提取铀和重水,铀和重水是核能开发的重要原料。
(2)潮汐能、波浪能是待开发的新型能源。
微判断
(1)海水中含有Br ( )
2
(2)海带中含有碘,能使淀粉变蓝( )
(3)用SO 溶液吸收溴蒸气,是利用了SO 具有漂白性( )
2 2
答案 (1)× (2)× (3)×
微训练
1.海水是一个巨大的化学资源库,下列有关海水综合利用的说法错误的是
( )
A.海水中含有溴元素,需经过化学变化才可以得到溴单质
B.无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能
C.从海水中可以得到NaCl,电解熔融NaCl可制备金属钠
D.从海水中提取镁可以采用下列方法:海水―→苦卤――→Mg(OH)
――→MgCl 溶液―→无水MgCl ―→MgCl (熔融)――→Mg
2 2 2 2
解析 海水中的溴元素以离子形式存在,需要通过化学反应来转化成溴单质,A
项正确;在波浪发电和潮汐发电过程中机械能转化为电能,而不是化学能转化为电能,B项错误;从海水中可以得到NaCl固体,电解熔融NaCl可制备金属钠,C
项正确;依据海水提取镁的原理分析,卤水中加入氢氧化钙以沉淀镁离子,生成
氢氧化镁,过滤后加盐酸溶解、蒸发浓缩、冷却结晶析出晶体,然后得到氯化镁固
体,电解熔融氯化镁得到金属镁,该方法合理,D项正确。
答案 B
2.海水开发利用的部分过程如图所示。下列说法错误的是( )
A.向苦卤中通入Cl 是为了提取溴
2
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO 将其还原吸收
2
解析 A项,海水中通入氯气可置换出溴,正确;B项,粗盐提纯包括溶解、除杂、
过滤、结晶、重结晶等,正确;C项,氢氧化钠成本较高,工业上常用选用生石灰或
石灰水作沉淀剂,错误;D项,先吹出溴再用SO 吸收可实现溴的富集,正确。故
2
选B项。
答案 C
微思考
1.目前,海水制盐所采用的方法大部分仍为盐田蒸发法,利用风能和太阳能使海
水蒸发。这种古老方法有什么优点?(从经济效益方面考虑)
提示 盐田蒸发法具有产量高、耗能少、成本低、运输方便等优点。
2.结合P 思考与讨论
101
(1)通入空气,将溴吹入吸收塔,是利用了溴的什么性质?
(2)除通过蒸馏提取液溴外,还有什么方法可提取液溴?
提示 (1)溴的沸点低,易挥发。
(2)由于溴易溶于有机溶剂,还可用萃取的方法提取液溴。
学习任务 (核心素养)海水化学资源的开发利用一、知识要点
1.海水提溴
海水提溴的主要方法是空气吹出法。
(1)主要流程:
――→――→――→――→
(2)主要反应:
Cl +2Br-===Br +2Cl-(氧化)
2 2
Br +SO +2H O===2HBr+H SO (富集)
2 2 2 2 4
Cl +2Br-===Br +2Cl-(提取)
2 2
2.海带中提碘
(1)海带中含有碘元素的检验
①关键反应的反应原理:2H++2I-+H O ===I +2H O。
2 2 2 2
②实验步骤及证明方法:
(2)海带中提碘
①流程:海带→浸泡→氧化→过滤→提纯→碘单质。
②主要的化学反应原理:Cl +2KI===2KCl+I 。
2 2
3.海水提镁
(1)主要反应原理:
CaCO =====CaO+CO ↑
3 2
CaO+H O===Ca(OH)
2 2
Ca(OH) +MgCl ===Mg(OH) ↓+CaCl
2 2 2 2
Mg(OH) +2HCl===MgCl +2H O
2 2 2
MgCl (熔融)=====Mg+Cl ↑
2 2
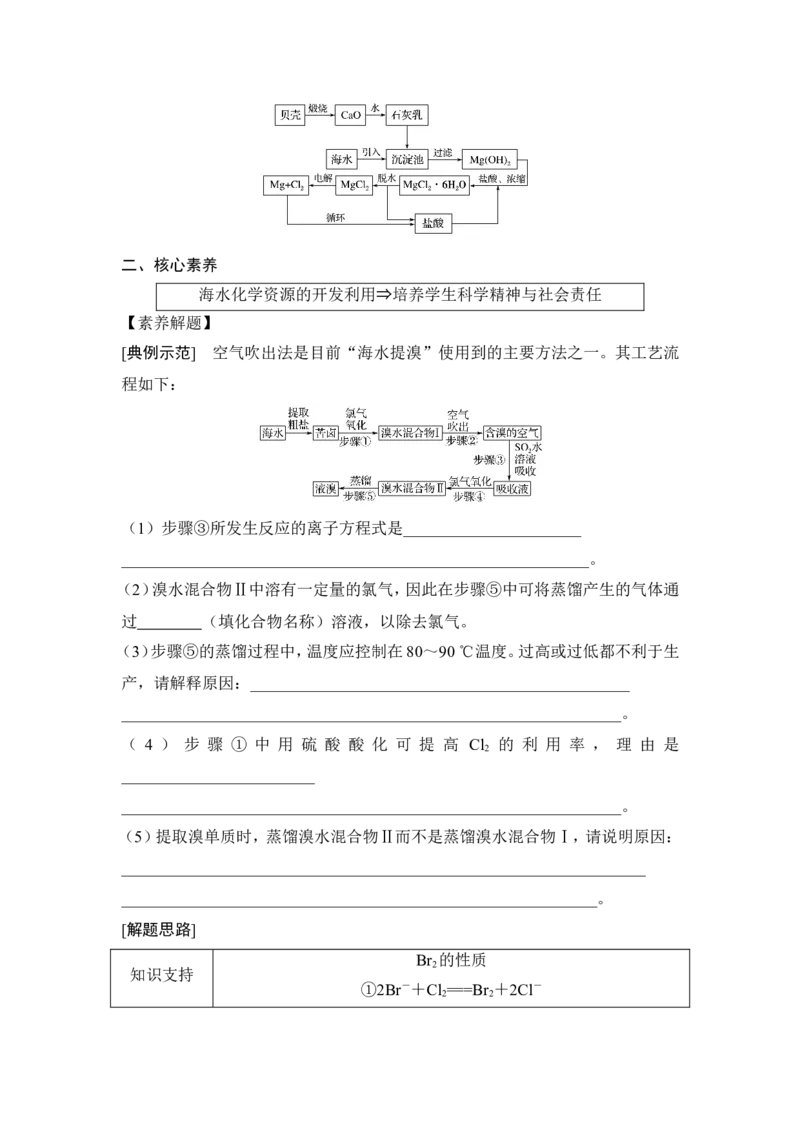
(2)工艺流程:二、核心素养
海水化学资源的开发利用⇒培养学生科学精神与社会责任
【素养解题】
[典例示范] 空气吹出法是目前“海水提溴”使用到的主要方法之一。其工艺流
程如下:
(1)步骤③所发生反应的离子方程式是______________________
__________________________________________________________。
(2)溴水混合物Ⅱ中溶有一定量的氯气,因此在步骤⑤中可将蒸馏产生的气体通
过 (填化合物名称)溶液,以除去氯气。
(3)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃温度。过高或过低都不利于生
产,请解释原因:_______________________________________________
______________________________________________________________。
( 4 ) 步 骤 ① 中 用 硫 酸 酸 化 可 提 高 Cl 的 利 用 率 , 理 由 是
2
________________________
______________________________________________________________。
(5)提取溴单质时,蒸馏溴水混合物Ⅱ而不是蒸馏溴水混合物Ⅰ,请说明原因:
_________________________________________________________________
___________________________________________________________。
[解题思路]
Br 的性质
2
知识支持
①2Br-+Cl ===Br +2Cl-
2 2②Br +SO +2H O===2HBr+H SO
2 2 2 2 4
③Br 的沸点低、易挥发
2
从海水中提取溴,一般要经过浓缩、氧化、提取三个步骤。步骤①发
生的反应是Cl +2Br-===2Cl-+Br ,生成的溴仍溶解在海水中,依
2 2
据溴的沸点比水低,鼓入热空气(步骤②),使溴和热空气一起挥发
选项分析
出来,再用SO 水溶液吸收(步骤③):Br +SO +2H O===4H++
2 2 2 2
2Br-+SO,这样可以得到Br-浓度较大的溶液,进一步用氯气氧化
(步骤④),可得到含Br 的水溶液,然后蒸馏即得到液溴。
2
(1)Br +SO +2H O===4H++2Br-+SO
2 2 2
(2)溴化铁(或其他含Br-的盐)
(3)温度过高,大量水蒸气被蒸出;温度过低,溴不能被完全蒸出
得出答案
(4)酸化可抑制Cl 、Br 与水反应
2 2
(5)将溴水混合物Ⅰ转变为溴水混合物Ⅱ是Br 的富集浓缩过程,
2
蒸馏溴水混合物Ⅱ可提高效率,减少能耗,降低成本
三、对点训练
1.从海水中提取镁的工艺流程可表示如下:
下列说法不正确的是( )
A.用此法提取镁的优点之一是原料来源丰富
B.步骤⑥电解MgCl 时阴极产生氯气
2
C.步骤⑤可将晶体置于HCl气体氛围中脱水
D.上述工艺流程中涉及化合、分解和复分解反应
解析 海水中含有大量的镁元素,从海水中提取镁的优点之一是原料来源丰富,
A项正确;电解熔融的MgCl 时,阳极产生Cl ,阴极产生金属镁,B项错误;因
2 2
MgCl 能水解:MgCl +2H OMg(OH)+2HCl,所以将MgCl ·6H O晶体在
2 2 2 2 2 2
HCl气体氛围中加热脱水,其目的是抑制MgCl 水解生成Mg(OH),C项正确;
2 2
步骤①涉及 CaCO 的分解反应得到 CaO,CaO 与 H O 发生化合反应得到 Ca
3 2
(OH),步骤⑥是电解涉及分解反应,步骤③涉及MgCl 与Ca(OH)发生的复分
2 2 2
解反应得到Mg(OH) 和CaCl ,D项正确。
2 2
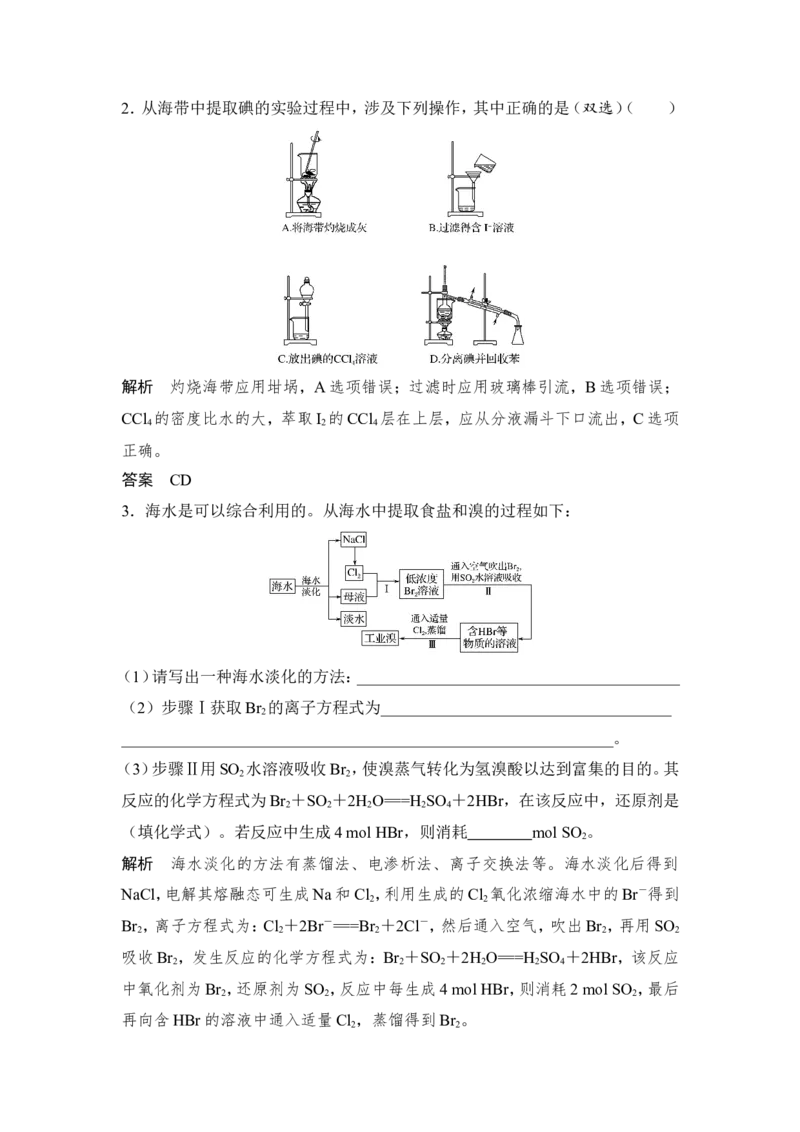
答案 B2.从海带中提取碘的实验过程中,涉及下列操作,其中正确的是(双选)( )
解析 灼烧海带应用坩埚,A选项错误;过滤时应用玻璃棒引流,B选项错误;
CCl 的密度比水的大,萃取I 的CCl 层在上层,应从分液漏斗下口流出,C选项
4 2 4
正确。
答案 CD
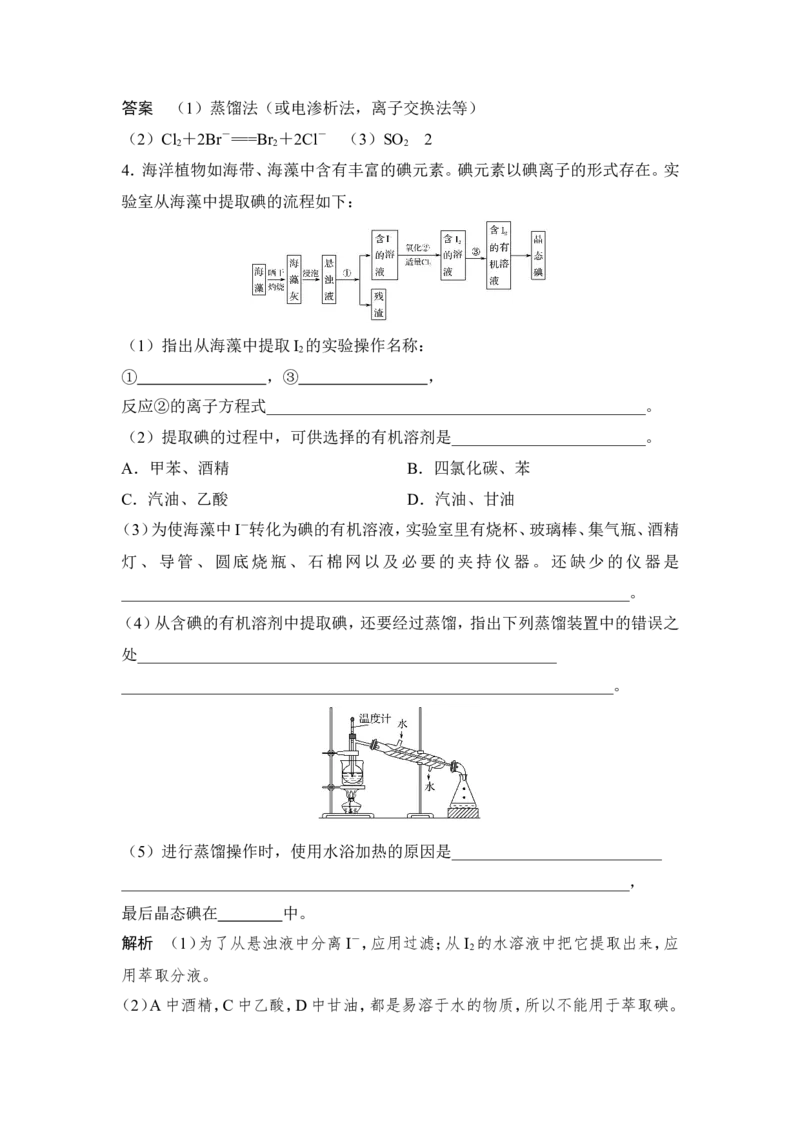
3.海水是可以综合利用的。从海水中提取食盐和溴的过程如下:
(1)请写出一种海水淡化的方法:________________________________________
(2)步骤Ⅰ获取Br 的离子方程式为____________________________________
2
_____________________________________________________________。
(3)步骤Ⅱ用SO 水溶液吸收Br ,使溴蒸气转化为氢溴酸以达到富集的目的。其
2 2
反应的化学方程式为Br +SO +2H O===H SO +2HBr,在该反应中,还原剂是
2 2 2 2 4
(填化学式)。若反应中生成4 mol HBr,则消耗 mol SO 。
2
解析 海水淡化的方法有蒸馏法、电渗析法、离子交换法等。海水淡化后得到
NaCl,电解其熔融态可生成Na和Cl ,利用生成的Cl 氧化浓缩海水中的Br-得到
2 2
Br ,离子方程式为:Cl +2Br-===Br +2Cl-,然后通入空气,吹出Br ,再用SO
2 2 2 2 2
吸收Br ,发生反应的化学方程式为:Br +SO +2H O===H SO +2HBr,该反应
2 2 2 2 2 4
中氧化剂为Br ,还原剂为SO ,反应中每生成4 mol HBr,则消耗2 mol SO ,最后
2 2 2
再向含HBr的溶液中通入适量Cl ,蒸馏得到Br 。
2 2答案 (1)蒸馏法(或电渗析法,离子交换法等)
(2)Cl +2Br-===Br +2Cl- (3)SO 2
2 2 2
4.海洋植物如海带、海藻中含有丰富的碘元素。碘元素以碘离子的形式存在。实
验室从海藻中提取碘的流程如下:
(1)指出从海藻中提取I 的实验操作名称:
2
① ,③ ,
反应②的离子方程式_______________________________________________。
(2)提取碘的过程中,可供选择的有机溶剂是________________________。
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
(3)为使海藻中I-转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精
灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器。还缺少的仪器是
_______________________________________________________________。
(4)从含碘的有机溶剂中提取碘,还要经过蒸馏,指出下列蒸馏装置中的错误之
处____________________________________________________
_____________________________________________________________。
(5)进行蒸馏操作时,使用水浴加热的原因是__________________________
_______________________________________________________________,
最后晶态碘在 中。
解析 (1)为了从悬浊液中分离I-,应用过滤;从I 的水溶液中把它提取出来,应
2
用萃取分液。
(2)A中酒精,C中乙酸,D中甘油,都是易溶于水的物质,所以不能用于萃取碘。(3)萃取分液所必需的仪器是分液漏斗,过滤时所需仪器必有普通漏斗。
答案 (1)过滤 萃取分液 2I-+Cl ===I +2Cl-
2 2
(2)B (3)分液漏斗,普通漏斗
(4)①没有石棉网;②温度计插入液面以下;③冷凝管进、出水方向颠倒
(5)萃取剂沸点较低,I 易升华 蒸馏烧瓶
2
[学 考 练]
1.许多国家十分重视海水资源的综合利用,不需要化学变化就能够从海水中获
得的物质是( )
A.氯、溴、碘 B.钠、镁、铝
C.烧碱、氢气 D.食盐、淡水
解析 海水中的各种元素都以化合态存在,要生成单质必然发生化学反应,A、
B、C均错。海水晒盐得NaCl,蒸馏海水得淡水只发生物理变化。
答案 D
2.随着人口增长、工业发展,淡水供应出现危机。若实行海水淡化来供应饮用水,
下列方法在原理上完全不可行的是( )
A.加入明矾,使海水中的泥沙沉淀并淡化
B.利用太阳能,将海水蒸馏淡化
C.将海水通过离子交换膜除去其所含的盐分
D.利用电渗析法使海水淡化
答案 A
3.下列关于海水的知识不正确的是( )
A.海水资源的利用包括海水水资源利用和化学资源利用
B.海水既苦又涩,不能直接利用
C.海水中某些金属元素总储量很大,但富集程度却很低
D.海水淡化应同化工生产结合,同能源技术结合
解析 海水可直接利用,如冲厕、作冷却水等。
答案 B
4.海水提镁的主要流程如下,下列说法正确的是( )①试剂M是盐酸 ②流程中的反应全部都是非氧化还原反应 ③操作b只是过
滤 ④用海水晒盐后的饱和溶液加石灰乳制Mg(OH) ⑤采用电解法冶炼镁是
2
因为镁很活泼
A.①②③④⑤ B.②③
C.④⑤ D.①④⑤
解析 生石灰溶于水生成Ca(OH),加入沉淀池沉淀Mg2+生成Mg(OH),过滤
2 2
后加入试剂M为盐酸,Mg(OH)溶解得到MgCl 溶液,通过浓缩蒸发,冷却结晶,
2 2
过滤洗涤得到MgCl 晶体,在HCl气体中加热失去结晶水得到固体MgCl ,通电
2 2
电解熔融MgCl 生成Mg。分析判断 M是盐酸用来溶解Mg(OH)沉淀,①正确;
2 2
电解MgCl 生成Mg和Cl 的反应是氧化还原反应,流程中的反应不全部都是非
2 2
氧化还原反应,②错误;操作b是蒸发浓缩,冷却结晶,过滤洗涤得到MgCl 晶体
2
的过程,③错误;用海水晒盐后的饱和溶液中主要是MgCl ,加石灰乳可以制Mg
2
(OH) ,④正确;依据金属活动顺序表中金属性可知,采用电解法冶炼Mg是因
2
为Mg很活泼,⑤正确,D项正确。
答案 D
5.海水提溴过程中将Br-氧化成Br ,可向其中加入氧化剂,合适的是( )
2
A.酸性KMnO 溶液 B.氯水
4
C.FeCl 溶液 D.碘水
3
解析 Fe3+和I 的氧化性都不如Br 的强,C、D不正确;酸性KMnO 溶液能氧化
2 2 4
Br-,但KMnO 价格比较贵,不适合工业生产用。
4
答案 B
6.某同学设计实验从海带中提取碘:
①滴加稀硫酸和双氧水 ②在海带中加入少量酒精,点燃使其燃烧为灰烬,在灰
烬中加水搅拌 ③加四氯化碳并振荡 ④过滤 ⑤分液
该实验的合理操作顺序是( )
A.①③⑤②④ B.②①③④⑤
C.②④①③⑤ D.③①②⑤④解析 从海带中提取I 的流程为
2
海带(加少量酒精)――→海带灰――→含 I-的水溶液――→I 的水溶
2
液――→I 的有机溶液,故正确步骤为②④①③⑤,选C。
2
答案 C
7.从海水中可以提取溴,但得到的液溴中常常有少量氯气,除去氯气应该采用的
方法是( )
A.加入适量的Na CO 溶液
2 3
B.通入溴蒸气
C.加入适量的NaOH溶液
D.加入适量的NaBr溶液
解析 Na CO 溶液和NaOH溶液都能与溴反应,不能用于除杂。
2 3
答案 D
8.某课外小组将灼烧海带产生的灰烬浸泡后过滤,得到澄清的滤液。他们设计了
如下的几个方案,你认为能证明海带的灰烬中含有碘元素的是(双选)( )
A.取适量滤液,蒸干,观察是否有紫色固体生成
B.取适量滤液,加入苯,振荡,静置,苯层无色,证明不含碘元素
C.取适量滤液,向其中先加氯水,再加入淀粉溶液,呈蓝色,证明含碘元素
D.取适量滤液,加入酸化的H O ,再加入淀粉溶液,呈蓝色,证明含有碘元素
2 2
解析 海带的灰烬中含有的碘元素,是以I-形式存在的,不是以单质形式存在,
所以A、B均不正确;C中2I-+Cl ===I +2Cl- ,产生了I ;D中发生了氧化还原
2 2 2
反应:H O +2I-+2H+===I +2H O,产生了I ,使淀粉溶液呈蓝色。
2 2 2 2 2
答案 CD
9.从淡化海水中提取溴的流程如下:
下列有关说法不正确的是(双选)( )
A.X试剂可用Na SO 饱和溶液
2 3
B.步骤Ⅲ的离子反应: Cl +Br-===Br +Cl-
2 2
C.工业上每获得1 mol Br ,需要消耗Cl 44.8L
2 2
D.步骤Ⅳ包含萃取、分液和蒸馏解析 Na SO +Br +H O===Na SO +2HBr,A正确;步骤Ⅲ利用氯的非金属性
2 3 2 2 2 4
比溴强,可以利用置换反应制取Br ,得失电子不守恒,B不正确;反应Ⅰ和反应
2
Ⅲ均使用到Cl ,故制取1 mol Br 消耗2 mol氯气,但未标明氯气所处的温度和压
2 2
强,C错误;从浓溴水中提取溴,可利用有机溶剂(如苯)萃取溴,然后分液得到溴
的有机溶液,再经蒸馏可得到纯净的溴,D正确。
答案 BC
10.海水中可以提取镁,其方法是首先使海水中的Mg2+转化为Mg(OH)沉淀。
2
从化学知识的角度和经济效益的角度考虑,可在海水中加入的物质是( )
A.NaOH B.KOH
C.CaO D.Na O
2
解析 若使Mg2+转化为Mg(OH)沉淀,须在海水中加入碱,理论上加入NaOH、
2
KOH、CaO、Na O都可实现上述转化,但NaOH、KOH、Na O为重要的化工原料,
2 2
其成本较高,而CaO可由石灰石或贝壳等分解而获得,原料易得,成本较低,故可
加入CaO,CaO+H O===Ca(OH) ,从而使Mg2+转化为Mg(OH) 沉淀。
2 2 2
答案 C
11.从海水中提取金属镁的生产步骤有:①浓缩结晶 ②加熟石灰 ③加盐酸
④过滤 ⑤熔融电解,正确的操作顺序是( )
A.①②③④⑤ B.⑤④③①②
C.②④③①⑤ D.③④②①⑤
解析 海水中含有Mg2+,加入Ca(OH)可生成Mg(OH)沉淀:Mg2++2OH-
2 2
===Mg(OH)↓,过滤可得到Mg(OH)固体。再将Mg(OH)转化为MgCl ,
2 2 2 2
MgCl 熔点低,电解熔融MgCl 可得金属镁:MgCl (熔融)=====Mg+Cl ↑。
2 2 2 2
答案 C
12.工业上海水资源合理开发利用的部分工艺流程如图所示:
(1)该工艺流程中先后制得Br 、CaSO 和Mg(OH),能否按Br 、Mg(OH)、
2 4 2 2 2CaSO 的 顺 序 制 备 ? ( 填 “ 能 ” 或 “ 不 能 ”) , 原 因 是
4
_______________________________________________________________
__________________________________________________________。
(2)溴单质在四氯化碳中的溶解度比其在水中的大得多,四氯化碳与水不互溶。
但在上述工艺中却不用四氯化碳,原因是________________________________
_________________________________________________________________。
(3)写出②③④反应的离子方程式。
_____________________________________________________________________
________________________________________________________________
________________________________________________________________。
解析 (1)CaSO 和Mg(OH)制备顺序与加入的试剂顺序有关,要求每次加入
4 2
试剂后只能得到一种物质,如果先沉淀Mg(OH),则沉淀中会夹杂有CaSO 和
2 4
Ca(OH) 沉淀,产品不纯。
2
(2)属于对试剂使用的评价问题,四氯化碳与水相比,无论是从价格上还是环境
污染问题上,都超过水。
答案 (1)不能 若先沉淀Mg(OH),则沉淀中会夹杂有CaSO 和Ca(OH)沉
2 4 2
淀,使产品不纯
(2)四氯化碳萃取法工艺复杂、设备投资大、经济效益低、环境污染严重
(3)②Cl +2Br-===Br +2Cl-
2 2
③Ca2++SO===CaSO ↓
4
④Mg2++2OH-===Mg(OH) ↓
2
[能 力 练]
13.海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺
流程如图:
(1)步骤①反应的离子方程式是_______________________________________
____________________________________________________________,步骤③反应的化学方程式是_____________________________________________
__________________________________________________________。
(2)从理论上考虑,下列物质也能吸收Br 的是___________________________。
2
A.NaOH B.FeCl
2
C.Na SO D.H O
2 3 2
(3)步骤③中氧化剂是 ,若反应中生成2 mol HBr,则消耗 mol
SO 。
2
(4)根据上述反应判断 SO 、Cl 、Br 三种物质氧化性由强到弱的顺序是
2 2 2
__________________________________________________________________。
解析 (1)读懂流程图,可以写出 2Br-+Cl ===Br +2Cl-,SO +Br +
2 2 2 2
2H O===2HBr+H SO 。(2)只从理论上考虑,NaOH具有强碱性,能吸收Br ,Fe2
2 2 4 2
+、SO具有还原性也能吸收Br ,但Br 在水中的溶解度较小,不能充分吸收。(3)
2 2
Br +SO +2H O===H SO +2HBr,该反应中氧化剂为Br ,还原剂为SO ,反应中
2 2 2 2 4 2 2
每生成2 mol HBr,则消耗1 mol SO 。(4)最后再向含HBr的溶液中通入适量
2
Cl ,蒸馏得到Br 。经过上述反应过程知氧化性由强到弱的顺序为Cl >Br >SO 。
2 2 2 2 2
答案 (1)2Br-+Cl ===Br +2Cl- SO +Br +2H O===H SO +2HBr
2 2 2 2 2 2 4
(2)ABC (3)Br 1 (4)Cl >Br >SO
2 2 2 2
14.海水占地球总储水量的97.2%,若把海水淡化和化工生产结合起来,既可解决
淡水资源缺乏的问题,又可充分利用海洋资源。
(1)海水中存在大量的氯化钠,氯化钠中的金属元素位于元素周期表第
族。
(2)目前,国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水
变成蒸气,蒸气经冷却而得高纯度淡水。由此可判断蒸馏法是 (填“物
理变化”或“化学变化”)。
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应式:食盐+
H O―→NaOH+H ↑+Cl ↑(未配平),该反应中食盐的化学式是
2 2 2
_________________________________________________________________;
利用电解所得气体制36.5%的浓盐酸1 000 t,最少需消耗食盐 t。
(4)近年来,有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废
气并回收二氧化硫的方法。该方法流程如下:请写出②④的化学反应方程式:_________________________________,
_______________________________________________________________。
解析 (1)Na位于第ⅠA族。(2)蒸馏法属于物理变化。
(3)2NaCl+2H O=====2NaOH+H ↑+Cl ↑,H +Cl =====2HCl,由n(HCl)=
2 2 2 2 2
=107 mol,可知m(NaCl)=107 mol×58.5 g·mol-1=585×106 g=585 t。
答案 (1)ⅠA (2)物理变化
(3)NaCl 585
(4)NaOH+SO ===NaHSO NaHSO +HCl===NaCl+H O+SO ↑
2 3 3 2 2