文档内容
第二章 烃
第二节 烯烃 炔烃
第 1 课时 烯烃
【即时训练】
一、单选题
1.化学与人类生活、科技发展密切相关,下列有关说法正确的是
A.华为 5G 芯片巴龙 5000 的主要材料是硅酸盐
B.生产 N95 口罩的聚丙烯能使酸性高锰酸钾溶液褪色
C.推广使用聚碳酸酯可降解塑料有利于保护环境,减少白色污染
D.中国天眼用到的高性能材料碳化硅是一种新型的有机高分子材料
2.目前丙烷和丙烯的工业分离主要依赖于低温蒸馏。下列说法错误的是
A.丙烯可以由丙烷催化脱氢制得 B.丙烯和乙烯互为同分异构体
C.丙烯能使溴的四氯化碳溶液褪色 D.丙烯可以发生加聚反应生成聚丙烯塑料
3.通常含有 的物质能使溴水褪色,下列物质能使溴水褪色的是
A.CH B.CH=CH C.CHCH D.CHCOOH
4 2 2 3 3 3
4.有关化合物HO-CH-CH=CH-CH -OH,下列说法不正确的是
2 2
A.分子式为C HO,1mol该物质充分燃烧需消耗氧气为5mol
4 8 2
B.该有机物能发生酯化反应、取代、加成、氧化、加聚反应
C.1mol该有机物和足量的金属钠反应,产生22.4L的氢气(标准状况下)
D.该有机物能使溴水褪色,但不能使酸性KMnO 溶液褪色
4
5.两种气态烃以任意比例混合,在150℃时2L该混合烃与12L氧气混合,充分燃烧后恢复到原状态,所
得气体体积为14L。下列各组混合烃中符合此条件的是
A.乙烯、乙烷 B.甲烷、乙烷 C.乙烷、丙烯 D.甲烷、乙烯
6.聚氯乙烯塑料在工农业生产中广泛应用,其结构简式为 ,它是由CH≡CH、HCl两种小
分子经过系列反应形成的,由聚氯乙烯分析合成过程中发生的反应类型有①取代反应②加成反应③加聚反应④氧化反应
A.①③ B.②③ C.①②③ D.①③④
7.为了提纯下列物质(括号内为杂质) ,有关除杂试剂和分离方法的选择均正确的是
选项 被提纯的物质 除杂试剂 分离方法
A 己烷(己烯) 溴水 分液
B 淀粉溶液(NaCl) 水 过滤
C 酒精(水) CaO 蒸馏
D 甲烷(乙烯) 酸性KMnO 溶液 洗气
4
A.A B.B C.C D.D
8.下列化合物中存在顺反异构的是
A.CH=CHCl B.CH=CCl C.CHCH=CHCH CH D.(CH)C=CHCH
2 2 2 3 2 3 3 2 3
9.1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应。由此可断定原
气态烃是(气体体积均在相同条件下测定)
A.丙炔 B.乙炔 C.乙烯 D.丁二烯
10. 表示阿伏加德罗常数,下列叙述正确的是
A. 与足量氯气反应时转移的电子数为
B. 硫酸钾溶液中阴离子所带电荷数为
C. 固体中含离子总数为
D.丙烯和环丙烷组成的 混合气体中氢原子的个数为
11.1mol某烃能与2molHCl加成,加成后产物上的氢原子最多能被8molCl 取代,则该烃可能为
2
A.2-丁烯 B.1,3-丁二烯 C.苯 D.乙烯
12.烯烃被酸性高锰酸钾溶液氧化的规律是烯烃中双键断裂:双键两端的基团=CH 变成 CO;=CHR
2 2
变成 RCOOH;=CRR'变成 R'RC=O。现有某溴代烷 A,分子式为 C HBr,在 NaOH醇溶液中加
4 9
热得到有机物 B,B 被酸性KMnO 溶液氧化后不可能得到的产物是
4
A.CHCOOH
3
B.CO 和CHCOCH
2 3 3
C.CO 和CHCHCOOH
2 3 2
22
D.HCOOH和CHCHCOOH
3 2
二、实验题
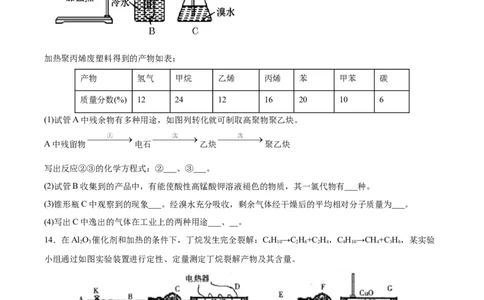
13.某废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图。
加热聚丙烯废塑料得到的产物如表:
产物 氢气 甲烷 乙烯 丙烯 苯 甲苯 碳
质量分数(%) 12 24 12 16 20 10 6
(1)试管A中残余物有多种用途,如图列转化就可制取高聚物聚乙炔。
A中残留物 电石 乙炔 聚乙炔
写出反应②③的化学方程式:②___、③___。
(2)试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,其一氯代物有___种。
(3)锥形瓶C中观察到的现象___。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为___。
(4)写出C中逸出的气体在工业上的两种用途___、__。
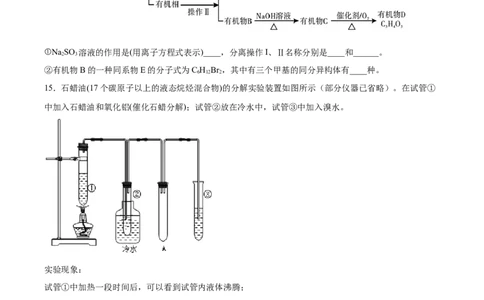
14.在Al O 催化剂和加热的条件下,丁烷发生完全裂解:C H →C H+C H,C H →CH+C H,某实验
2 3 4 10 2 6 2 4 4 10 4 3 6
小组通过如图实验装置进行定性、定量测定丁烷裂解产物及其含量。
(1)C和F玻璃仪器的名称是________。
(2)参考装置图,连接好各仪器,________,加入各试剂,排除装置中的空气,加热D和G装置,B装置所
起的作用是________。
(3)E装置中的实验现象是________;写出G装置中的反应的化学方程式_______。(写出一个即可)(4)E和F装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷的摩
尔分数是x=_____%
(提示1:x= ×100%;提示2:假定流经D、G装置中的气体能完全反应)
(5)对E装置中的混合物再按以下流程实验:
①Na SO 溶液的作用是(用离子方程式表示)____,分离操作I、Ⅱ名称分别是____和______。
2 3
②有机物B的一种同系物E的分子式为C H Br ,其中有三个甲基的同分异构体有____种。
6 12 2
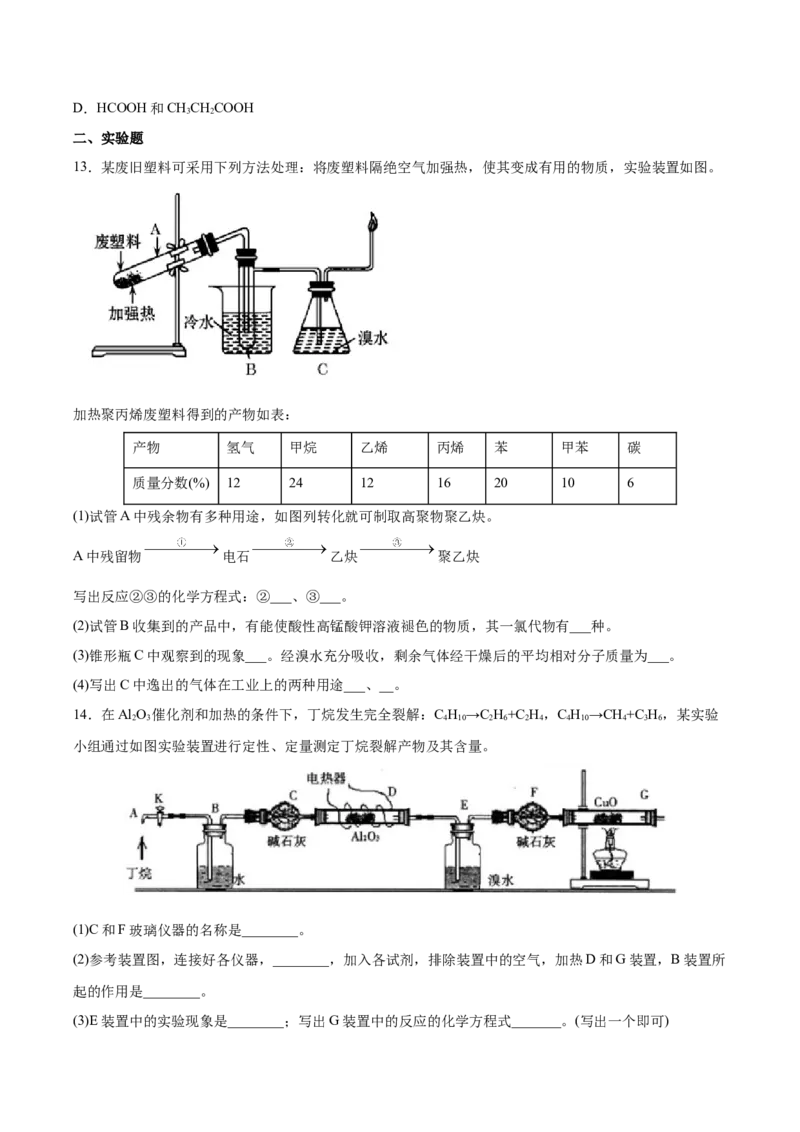
15.石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。在试管①
中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水。
实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。根据实验现
象回答下列问题:
(1)装置A的作用是______________________________;
(2)试管①中发生的主要反应有:
C H C H +C H C H C H +C H
17 36 8 18 9 18 8 18 4 10 4 8
丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为_________和
________,这两种有机物混合后在一定条件下可聚合成高分子化合物,其反应类型属于______反应。其可
44
能结构为______(填序号)
(3)写出试管③中反应的一个化学方程式_____________________________,该反应的类型为__________反
应。
(4)试管②中的少量液体的组成是____________(填序号)
A.甲烷 B.乙烯 C.液态烷烃 D.液态烯烃
三、填空题
16.(1)写出以氯乙烯(CH=CHCl)制备PVC(聚氯乙烯)发生反应的化学反应方程式及反应类型:
2
___________、___________。
PE(聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。辨别PE和PVC有二种方法,
一是测密度法:密度大的应是___________;二是燃烧法:PE和PVC在足量空气中燃烧的实验现象的明显
区别是___________。
(2)PVDC(CH —CCl )是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品
2 2
等的包装。写出合成PVDC的小分子的结构简式:___________。
(3)“白色污染”是指各种塑料制品对环境的污染。焚烧塑料会生成有毒物质二 英,二 英是含有如图所
示母体的系列化合物,下列关于如图所示物质的说法不正确的是___________(填字母)。
a该物质在氧气中完全燃烧的产物是CO 和HO
2 2
b该物质属于烃
c该物质的一卤代物只有2种参考答案
1.C
【详解】
A.芯片的主要材料为高纯硅,而不是硅酸盐,A错误;
B.聚丙烯中不含碳碳双键(丙烯加聚时断裂),故不能使KMnO 溶液褪色,B错误;
4
C.白色污染主要由难降解的塑料形成,故推广使用可降解塑料有利于减少白色污染,C正确;
D.碳化硅属于新型无机非金属材料,D错误;
故答案选C。
2.B
【详解】
A.丙烯 ,丙烷为 ,丙烯可通过丙烷脱两个氢原子得到,故A正确
B.丙烯分子式为C H,乙烯分子式为C H,两者分子式不同,不是同分异构体,故B错误;
3 6 2 4
C.丙烯 ,含有碳碳双键能与溴单质发生加成反应从而使溴的四氯化碳溶液褪色,故C正确;
D.丙烯含有碳碳双键,通过加成聚合反应可得到聚丙烯,故D正确;
故选:B。
3.B
【详解】
A.CH 属于烷烃,不含 ,不能使溴水褪色,故A不符合题意;
4
B.CH=CH 属于烯烃,含 ,可以使溴水褪色,故B符合题意;
2 2
C.CHCH 属于烷烃,不含 ,不能使溴水褪色,故C不符合题意;
3 3
D.CHCOOH属于羧酸,不含 ,不能使溴水褪色,故D不符合题意;
3
故答案为B。
4.D
【详解】
A.根据结构简式知,分子式为C HO,可写成C H(H O) ,只有C H 消耗氧气,故1mol物质充分燃烧
4 8 2 4 4 2 2 4 4
消耗O 为5mol,故A正确;
2
B.分子含有羟基和碳碳双键,因此可以发生取代反应、加成反应、氧化反应和加聚反应,故B正确;
C.1mol该物质和足量钠反应会生成1molH ,在标准状况下为22.4L,故C正确;
2
D.分子中含有醇羟基和碳碳双键,能和Br 发生加成反应,也能被酸性KMnO 氧化,故D错误;
2 4
11
答案选D。
5.D
【详解】
设该混合物的平均分子式为C H,由燃烧通式: ,得燃
x y
烧前后气体体积变化△V=1+x+ -x- =1- ,由题意知△V=0,即1- =0,解得y=4,即该混合烃的平均
分子式为C H,选项A、B、C相关烃混合后氢原子数不可能为4个,故A、B、C不符合题意;甲烷(CH)
x 4 4
与乙烯(C H)均含4个氢原子,故混合后平均每个分子含4个氢原子,D符合题意,故答案选D。
2 4
6.B
【详解】
由聚氯乙烯的结构简式可知,其单体为 ,据题给原料, 应由CH≡CH和HCl加成反
应制得,因此制聚氯乙烯的过程应有加成反应和加聚反应,故选B。
7.C
【详解】
A.己烯与溴水反应,而己烷不能,但反应后的产物及过量的溴溶于己烷,不能分液除杂,故A错误;
B.二者均可透过滤纸,应利用渗析法分离,故B错误;
C.CaO与水反应生成沸点高的氢氧化钙,蒸馏分离出乙醇,故C正确;
D.乙烯被高锰酸钾氧化后生成二氧化碳,引入新杂质,应利用溴水和洗气法除杂,故D错误;
故选C。
8.C
【分析】
顺反异构产生的条件:①分子中至少有一个键不能自由旋转(如碳碳双键);②每个不能自由旋转的同一碳
原子上(如碳碳双键两端的碳原子)不能有相同的基团,必须连有两个不同原子或原子团。
【详解】
A.CH=CHCl中碳碳双键两端的碳原子上连接2个氢原子,不存在顺反异构,A与题意不符;
2
B.CH=CCl 中碳碳双键两端的碳原子分别连接2个氢原子、2个氯原子,不存在顺反异构,B与题意不符;
2 2
C.CHCH=CHCH 符合条件,存在顺反异构,C符合题意;
3 3
22
D.(CH)C=CHCH 中碳碳双键两端的碳原子上连接2个甲基,不存在顺反异构,D与题意不符;
3 2 3
答案为C。
9.A
【详解】
1体积某气态烃和2体积氯化氢发生加成反应,说明该气态烃分子中含2个双键或1个C≡C。生成的1体积
该卤代烷最多能和6体积氯气发生取代,说该明该1个卤代烷分子中含有6个H原子。气态烃与氯化氢加
成时1个烃分子引入2个H原子,所以该气态烃分子中原本含有4个H原子。通过题意可知,若该烃与氢
气加成,生成的烷烃分子中含有氢原子数应为8个,根据烷烃通式,则该烷烃所含的碳原子数为(8-2)÷2
=3,则该气态烃所含的碳原子数也为3,氢原子数为4,则丙炔符合题意,故答案选A。
10.D
【详解】
A.FeI 中Fe2+和I-都具有较强的还原性,都能和Cl(氧化性)发生反应,1molFeI 中有1molFe2+和2molI-,
2 2 2
1molFe2+生成Fe3+,转移电子数为N ,2molI-生成I,转移电子数为2N ,所以转移电子总数为3N ,A项
A 2 A A
不符合题意;
B.硫酸钾的物质的量为 ,其中的阴离子为 ,物质的量为1mol,所带电荷数为
2N ,但是溶液中还有水电离出来的氢氧根,所以阴离子的物质的量无法确定,阴离子所带电荷也无法确
A
定,B项不符合题意;
C.1个NaO 中的离子为2个Na+和1个 ,1molNa O 中离子总数为3N ,C项不符合题意;
2 2 2 2 A
D.丙烯和环丙烷的分子式相同,都是C H,则氢原子数为 ,D项符合题意;
3 6
故正确选项为D
11.B
【详解】
气态烃1mol能和2molHCl加成,说明烃分子中含有1个C C键或2个C= C键,加成后产物分子上的氢
原子又可被8molCl 完全取代,说明1mol氯代烃中含有6molH原子,最终的产物中1mol氯代烃含有含有
2
4molC原子,10mol氯原子,又因原烃并含有1个C C键或2个C= C键,所以原烃分子式为C H,可能
4 6
为1,3-丁二烯或1-丁炔或2-丁炔。
故选:B。
12.D
33
【详解】
某溴代烷A的分子式为 C HBr,在NaOH醇溶液中加热得到有机物B,B为烯烃C H,C H 有如下三种
4 9 4 8 4 8
同分异构体(不考虑顺反异构):CH═CHCH CH、CH-CH═CH-CH 、CH═C(CH ),根据题中信息,
2 2 3 3 3 2 3 2
C H 双键被氧化断裂的情况如下: 、 、
4 8
,三种烯烃被氧化得到的产物有:CO、CHCHCOOH、CHCOOH、 ,
2 3 2 3
则不可能有HCOOH,故选D。
13.CaC +2H O→Ca(OH) +C H↑ nCH≡CH 4 棕黄色溶液变无
2 2 2 2 2
色或褪色 4.8 合成氨原料 作燃料或其他化工原料
【分析】
碳的沸点高,A中剩余固体是碳;常温下,碳原子1~4的烃为气体,碳原子数小于等于4的烃为气体,碳
原子数5~16的烃为液体,所以B中收集到的物质是苯和甲苯;氢气、甲烷、乙烯、丙烯进入C,乙烯、丙
烯被溴水吸收,最后剩余气体是氢气和甲烷。
【详解】
(1)②是电石和水反应生成氢氧化钙和乙炔,反应方程式是CaC +2H O→Ca(OH) +C H↑;③是乙炔发生加
2 2 2 2 2
聚反应生成聚乙炔,反应的化学方程式是nCH≡CH ;
(2)试管B收集到的产品是苯和甲苯,其中甲苯能使酸性高锰酸钾溶液褪色,甲苯分子中有4种等效氢,其
一氯代物有4种;
(3)氢气、甲烷、乙烯、丙烯进入C,乙烯、丙烯和溴水发生加成反应,锥形瓶C中观察到的现象是棕黄色
溶液变无色或褪色。经溴水充分吸收,最后剩余气体是氢气和甲烷,剩余气体经干燥后的平均相对分子质
量为 ;
(4)C中逸出的气体是氢气和甲烷,在工业上的用途有合成氨原料、作燃料或其他化工原料。
44
14.球形干燥管 检查装置的气密性 观察、控制丁烷的流速 溴水褪色 CH+4CuO
4
CO+2H O+4Cu或C H+7CuO 2CO+3H O+7Cu 25% Br + +H O=2Br-+2H++ 分液
2 2 2 6 2 2 2 2
蒸馏 15
【分析】
首先将丁烷蒸气通过盛有水的集气瓶,根据集气瓶中产生气泡的速率控制丁烷蒸气的气流速度;然后经碱
石灰干燥通入装置D中,在Al O 催化剂和加热的条件下,丁烷发生裂解生成乙烯、丙烯、甲烷和乙烷,E
2 3
中溴水用于吸收烯烃,且根据溴水是否褪色可以判断是否发生裂解反应,F干燥烷烃,G中CuO能将烃氧
化成CO 和HO。
2 2
E装置中主要有BrCHCHBr、CHCHBrCH Br以及未反应的溴水;加入亚硫酸钠将溴单质还原,分液得到
2 2 3 2
的有机相为BrCHCHBr和CHCHBrCH Br的混合物,蒸馏分离二者,有机物A可以水解得到
2 2 3 2
HOCH CHOH,所以A为BrCHCHBr,则B为CHCHBrCH Br,B在NaOH水溶液中水解得到C,C为
2 2 2 2 3 2
CHCHOHCH OH,羟基可以被催化氧化,结合D的分子式可知D为CHCOCOOH,由此分析解答。
3 2 3
【详解】
(1)根据C和F的结构特点可知其为球形干燥管;
(2)该反应中有气体参与反应、有气体生成,所以连接好各仪器后要检验装置的气密性;B装置中盛有水,
可以通过观察B中产生的气泡快慢来控制气体的流速;
(3)丁烷裂解产生乙烯、丙烯,烯烃可以和溴水发生加成反应从而使溴水的颜色变浅,相关的化学反应方程
式为CH=CH +Br ⟶BrCH CHBr,CHCH=CH+Br ⟶CH CHBrCH Br;从F中出来的气体含有甲烷和乙
2 2 2 2 2 3 2 2 3 2
烷,G装置中发生甲烷或乙烷和氧化铜反应生成铜、二氧化碳和水的反应,化学反应方程式为CH+4CuO
4
CO+2H O+4Cu或C H+7CuO 2CO+3H O+7Cu;
2 2 2 6 2 2
(4)丁烷的裂解中生成的乙烯和乙烷的物质的量相等,生成的甲烷和丙烯的物质的量相等,E、F吸收的是
烯烃;G中氧化铜和烷烃反应生成Cu、CO 和HO,所以G减少的质量是氧化铜中的氧元素质量;设x为
2 2
甲烷的物质的量,y为乙烷的物质的量,则丙烯和乙烯的物质的量分别是x、y,则:42x+28y=0.7;甲烷、
55
乙烷与氧化铜反应需要的氧原子的物质的量为:(2x+2x)+(4y+3y)= ,解得:x=0.01mol,
y=0.01mol,所以甲烷的摩尔分数为 =25%;
(5)①亚硫酸钠溶液的作用是除去溴单质,反应的离子方程式为Br + +H O=2Br-+2H++ ;根据分析
2 2
可知分离操作I名称为分液,分离操作Ⅱ为蒸馏;
②B为CHCHBrCH Br,B的一种同系物E的分子式为C H Br ,己烷有:CHCHCHCHCHCH、
3 2 6 12 2 3 2 2 2 2 3
CHCH(CH )CHCHCH、CHCHCH(CH )CHCH、CHC (CH )CHCH;CHCH(CH )CH(CH )CH,含有
3 3 2 2 3 3 2 3 2 3 3 3 2 2 3 3 3 3 3
三个甲基,二溴代物分别为:CHCH (CH )CBr CHCH、CHCH(CH )CHCBr CH、
3 3 2 2 3 3 3 2 2 3
CHCBr(CH)CHCHBrCH 、CHCBr(CH)CHBrCH CH、CHCH(CH )CHBrCHBrCH 、
3 3 2 3 3 3 2 3 3 3 3
CHCBr CH(CH )CHCH、CHCHBrCBr(CH )CHCH、CHCHBrC(CH )CHBrCH 、CHC(CH)CBr CH、
3 2 3 2 3 3 3 2 3 3 3 3 3 3 2 2 3
CHC(CH)CHCHBr 、CHC(CH)CHBrCH Br、CHBr CH(CH )CH(CH )CH、CHBrCBr
3 3 2 2 3 3 2 2 2 3 3 3
(CH)CH(CH )CH、CHBrCH(CH )CBr(CH )CH、CHCBr(CH)CBr(CH )CH 共15种同分异构体。
3 3 3 3 3 3 3 3 3 3
【点睛】
难点是计算甲烷的摩尔分数,明确质量增加的量和质量减少的量分别是什么物质是解本题的关键。
15.防止试管③中的液体倒吸到试管②中 CH=CH CH CH=CH 加聚 AC
2 2 3 2
CH=CH +Br →CHBrCHBr(CHCH=CH+Br →CHCHBrCH Br) 加成 CD
2 2 2 2 2 3 2 2 3 2
【详解】
(1)CH=CH-CH 和CH=CH 能与溴水发生加成反应,使气压降低,发生倒吸,装置A的作用是防止试
2 3 2 2
管③中液体倒吸回试管②中;
(2)丁烷的两种裂解方式为:C H →CH+CH =CHCH,C H →C H+CH =CH ,如果是乙烯和丙烯之间
4 10 4 2 3 4 10 2 6 2 2
发生加聚反应,由于碳原子之间的连接顺序可以有 和
两种结构简式,分别为A、C结构,故答案为AC;
(3)CH=CH-CH 和CH=CH 能与溴水发生加成反应,反应方程式为
2 3 2 2
66
;
(4)石蜡在催化剂氧化铝存在下,加热可以裂化为短链的气态饱和烃和不饱和烃,还有液态的饱和烃和
不饱和烃,故答案为CD。
16.nCH=CHCl 加聚反应 聚氯乙烯 聚乙烯更易燃烧,聚氯乙烯燃烧产
2
生刺激性气味气体(HCl),有白雾 CH=CCl b
2 2
【详解】
(1)氯乙烯(CH=CHCl)制备PVC(聚氯乙烯)发生反应的化学反应方程式为:nCH=CHCl
2 2
,反应类型为加聚反应;聚氯乙烯中含有相对原子质量相对较大的氯原子,其密度比聚乙
烯大,聚氯乙烯不易燃烧,燃烧时产生具有刺激性气味的HCl,有白雾(含有HCl的小液滴)生成。故答案
为:nCH=CHCl ;加聚反应;聚氯乙烯;聚乙烯更易燃烧,聚氯乙烯燃烧产生刺激
2
性气味气体(HCl),有白雾;
(2)PVDC(CH —CCl )是一种加聚反应产物,单体为CH=CCl ,故答案为:CH=CCl ;
2 2 2 2 2 2
(3)该物质含有碳、氢、氧三种元素,不属于烃;完全燃烧的产物是CO 和HO;且其一卤代物只有2种,
2 2
故答案为:b。
7