文档内容
第二章 烃
第二节 烯烃 炔烃
第 2 课时 炔烃
【即时训练】
一、单选题
1.下列表示物质结构的化学用语或模型正确的是
A.乙烷的分子式:CHCH B.CH 分子的球棍模型:
3 3 4
C.乙醇的结构式:CHCHOH D.乙烯的结构简式:CH=CH
3 2 2 2
2.下列有关化学用语表示正确的是
A.NH 的电子式
3
B.聚丙烯的结构简式:
C.丙烷分子的空间填充模型:
D.2-乙基-1,3-丁二烯分子的键线式:
3.下列方法既可以用于鉴别乙烷和乙烯,又可以除去乙烷中的乙烯的是
A.NaOH溶液 B.通入H C.酸性KMnO 溶液 D.溴水
2 4
4.含有一个双键的烯烃和H 加成后的产物结构简式如图,此烯烃可能有的结构
2
A.6种 B.7种 C.5种 D.8种5.氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业。实验室用加热
NH Cl 和Ca(OH) 固体混合物的方法制取少量氨气。侯氏制碱法以氯化钠、二氧化碳、氨和水为原料,发
4 2
生反应NaCl + NH +CO +H O= NaHCO↓+ NH Cl。将析出的固体灼烧获取纯碱,向析出固体后的母液中加
3 2 2 3 4
入食盐可获得副产品氯化铵。下列说法正确的是
A.室温不,下列物质在水中的溶解度:丙三醇>苯
B.乙苯的一氯取代物只有4种
C.分子式为CHO和C HO的物质一定互为同系物
4 2 6
D.CHCH = C(CH )CH(CH ) 的名称: 2,3-二甲基-3-戊烯
3 3 3 2
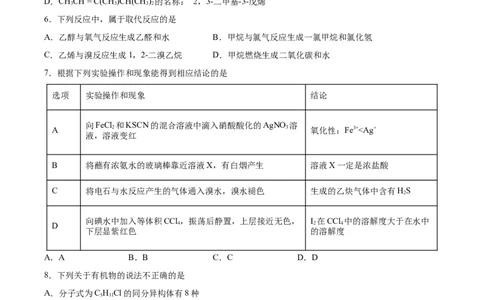
6.下列反应中,属于取代反应的是
A.乙醇与氧气反应生成乙醛和水 B.甲烷与氯气反应生成一氯甲烷和氯化氢
C.乙烯与溴反应生成1,2-二溴乙烷 D.甲烷燃烧生成二氧化碳和水
7.根据下列实验操作和现象能得到相应结论的是
选项 实验操作和现象 结论
向FeCl 和KSCN的混合溶液中滴入硝酸酸化的AgNO 溶
A 2 3 氧化性:Fe3+苯,故A正确;
B.乙苯一共有5种等效氢,所以乙苯的一氯取代物有5种,故B错误;
C.分子式为CHO的化合物为甲醇,分子式为C HO的化合物可以为 或者
4 2 6
,所以分子式为CHO和C HO的物质不一定互为同系物,故C错误;
4 2 6
D.CHCH = C(CH )CH(CH ) 的命名应该近官能团编号,所以正确的命名为: 3,4-二甲基-2-戊烯,故D
3 3 3 2
错误;
综上答案为A。
22
6.B
【详解】
A.乙醇与氧气反应生成乙醛属于氧化反应,故A错误;
B.取代反应是有机物的分子内某些原子或原子团被其它原子或原子团取代的反应,甲烷与氯气反应生成
一氯甲烷和氯化氢,属于取代反应,故B错误;
C.加成反应是双键两端的碳原子直接与其它原子相连,乙烯与溴反应生成1,2-二溴乙烷属于加成反应,
故C正确;
D.甲烷燃烧生成二氧化碳和水,是氧化反应,故D错误;
答案选B。
7.D
【详解】
A.向FeCl 和KSCN的混合溶液中滴入硝酸酸化的AgNO 溶液,溶液变红,说明亚铁离子被氧化为铁离
2 3
子,由于酸性溶液中硝酸根也能氧化亚铁离子,所以不能得出氧化性:Fe3+<Ag+,A错误;
B.将蘸有浓氨水的玻璃棒靠近溶液X,有白烟产生,溶液X不一定是浓盐酸,也可能是浓硝酸,B错误;
C.将电石与水反应产生的气体通入溴水,溴水褪色,不能说明生成的乙炔气体中含有HS,因为乙炔就
2
能使溴水褪色,C错误;
D.向碘水中加入等体积CCl ,振荡后静置,上层接近无色,下层显紫红色,四氯化碳密度大于水的,这
4
说明I 在CCl 中的溶解度大于在水中的溶解度发生了萃取,D正确;
2 4
答案选D。
8.D
【详解】
A.C H Cl相当于1个Cl原子取代戊烷上的H,戊烷有正戊烷、异戊烷、新戊烷三种结构,分别有3、
5 11
4、1中H原子,则C H Cl的同分异构体由8种,故A正确;
5 11
B.4−甲基−2−己醇,先写主链的碳原子,在写官能团羟基,在写碳的支链,这样的键线式为
,故B正确;
C.乙烯和溴反应生成无色油状的1,2-二溴乙烷,因此甲烷中混有的乙烯可以用溴水除去,故C正确;
D. 是醇类,而 是酚类物质,它们不属于同系物,故D错误;
33
故选:D。
9.D
【详解】
A.石油裂化可以得到较多的轻质油;裂解得到较多的气态烯烃,A说法正确;
B.苯和乙炔的最简式均为CH,则总质量相等的任何比例苯和乙炔混合物完全燃烧时生成水的质量不变,
B说法正确;
C.使1mol乙烯与氯气先发生加成反应,消耗1mol氯气,加成反应的产物中含有4个氢原子,则其与氯
气在光照的条件下发生取代反应,消耗4mol氯气,则两个过程中消耗的氯气总的物质的量最多是5mol,C
说法正确;
D.常压分馏得到的汽油是混合物,没有固定的沸点,石油气是混合物,主要组成成分为丙烷、丙烯、丁
烷、丁烯中的一种或者两种,而且其还掺杂着少量戊烷、戊烯和微量的硫化物杂质,D说法错误;
答案为D。
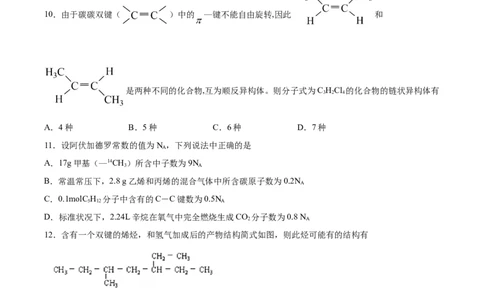
10.D
【详解】
C HCl 的2个Cl原子,根据一固定一游动原则,同分异构体存在CCl =CH-CH、CHCl=CCl-CH 、
3 4 2 2 3 3
CHCl=CH-CH Cl、CH=CCl-CH Cl、CH=CH-CHCl ,其中CHCl=CCl-CH 和CHCl=CH-CH Cl均存在顺反
2 2 2 2 2 3 2
异构体,共计有4+3=7种,C HCl 与C HCl 的同分异构体数目相等,答案选D。
3 2 4 3 4 2
11.B
【详解】
A.该甲基中中子数是14-6=8,A不正确;
B.乙烯和丙烯的最简式相同,都是CH,所以B正确;
2
C.戊烷中只有四个C—C,应该是0.4N ,不正确;
A
D.标准状况下,辛烷不是气体,不正确;
正确的答案选B。
12.C
【详解】
根据烯烃与H 加成反应的原理,推知该烷烃分子中相邻碳原子上均含有原子的碳原子间是对应烯烃存在
2
44
C=C的位置,该烷烃 中能形成双键键位置有:1和2之间、2和
3之间、3和4之间、3和5之间、5和6之间、6和7之间(6和9)、7和8之间(9和10),故该烯烃共有7种,
故选C。
13. 3 A ⑤ ⑥ CH C≡CCH
3 3
【详解】
(1)乙烯中含碳碳双键,电子式为 ,故答案为: ;
(2)2-甲基-1,3-丁二烯含有2个碳碳双键,且含有5个C原子,主链为4个C,结构简式为 ,
故答案为: ;
(3) 立方烷( )中只有1种等效H,二氯代物有一条棱、面对角线、体对角线上3种位置,二氯代物
有3种,故答案为:3;
(4)烷烃的沸点随着分子中碳原子数的递增逐渐升高;碳原子数相同的烃,支链越多,熔沸点越低。①、③
中碳原子都是4个,①无支链,沸点:①>③;②、④中碳原子数为5,比①、③中碳原子数都多,则沸
点较高,②无支链,沸点:②>④;故沸点由高到低的顺序是②④①③,故答案为:A;
(5)⑤ 的结构相似,分子式不同,互为同系物;⑥戊烯和环戊烷的结构不同,分子式
相同,互为同分异构体,故答案为:⑤; ⑥;
(6)乙炔为直线结构,若乙炔分子中的两个氢原子被碳原子代替,则四个碳原子均在一条直线上,所以分子
式为C H 的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为CHC≡CCH ,故答案为:
4 6 3 3
CHC≡CCH 。
3 3
14. 甲基 丁烯 甲基丁烷 5 4 d
55
【详解】
(1)烯烃命名时,选含官能团的最长的碳链为主链,故主链上有4个碳原子,故为丁烯,从离官能团近的一
端给主链上的碳原子进行编号,故碳碳双键在1号和2号碳原子之间,在3号碳原子上有一个甲基,故名
称为 甲基 丁烯;
其在催化剂存在下完全与氢气加成后,碳碳双键打开,H原子加到C原子的半键上所得的产物是烷烃,故
得到(CH)CHCH CH,为 甲基丁烷;
3 2 2 3
(2) ①戊烷的同分异构体有CH-CH-CH-CH-CH、 、 ,若为CH-CH-CH-
3 2 2 2 3 3 2 2
CH-CH,相应烯烃有CH═CH-CH -CH-CH、CH-CH═CH-CH -CH,(不考虑顺反异构),即有2种异
2 3 2 2 2 3 3 2 3
构;若为 ,相应烯烃有:CH═C(CH )CHCH;CHC(CH)═CHCH ;CHCH(CH )CH═CH ,
2 3 2 3 3 3 3 3 3 2
都不存在顺反异构,即有3种异构;若为 ,没有相应烯烃;所以分子式为C H 的烯烃共有
5 10
(不包括顺反异构)2+3=5种;
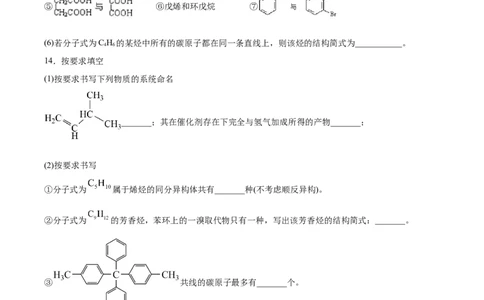
②分子式为 的芳香烃,苯环上的一溴取代物只有一种,说明苯环上只有一种氢原子,分子高度对称,
该芳香烃为1,3,5-三甲苯,结构简式为: ;
③ 可看成是甲烷上的4个氢原子被4个苯基取代,而左右两边的二个甲基为取代苯环
上的氢原子,根据甲烷为正四面体结构,苯上的12个原子共平面,苯上的对角上2个碳和2个氢原子共线,
66
故 共线的碳原子最多有4个;
(3) ①根据正四面体烷的每个顶点代表一个碳原子,碳可形成4对共用电子对,每个碳原子上都连有一个氢
原子,正四面体烷的分子式为C H;
4 4
②)a.因乙烯基乙炔为CH=CH-C≡CH,乙烯基乙炔分子中含有一个碳碳双键、一个碳碳三键,官能团碳
2
碳双键、碳碳三键都能使酸性 溶液褪色,选项a正确;
b.因乙烯基乙炔为CH=CH-C≡CH,乙烯基乙炔分子中含有一个碳碳双键、一个碳碳三键, 乙烯基
2
乙炔能与 ,发生加成反应,选项b正确;
c.乙烯基乙炔分子中含有的官能团有两种:碳碳双键、碳碳三键,选项c正确;
d.乙烯基乙炔为CH=CH-C≡CH最简式为CH,乙炔C H 的最简式为CH,二者最简式相同,质量相同时
2 2 2
消耗氧气一定相同,选项d错误;
答案选d;
③环辛四烯的分子式为C H,不饱和度为5,属于芳香烃的同分异构体,含有1个苯环,侧链不饱和度为
8 8
1,故含有1个侧链为-CH=CH,属于芳香烃的同分异构体的结构简式: 。
2
15.玻璃棒 防止暴沸 停止加热,冷却后再加入碎瓷片 装置丙中酸性 溶液紫色褪去
强氧化 乙 D中的品红溶液不褪色,E中澄清石灰水变浑浊 B中的品红溶液
褪色
【详解】
(1)将量好的浓硫酸和乙醇在烧杯中混合时,需要用玻璃棒进行搅拌,使溶液混合均匀,热量及时散发出去;
(2)给烧瓶中的混合液加热,加入碎瓷片是为了防止溶液暴沸;若实验中加热一段时间后发现忘记加碎瓷片,
要停止加热,冷却后再加入碎瓷片,以防发生危险;
(3)乙烯中含有碳碳双键,能够被酸性高锰酸钾溶液氧化,装置丙中酸性 溶液紫色褪去,此现象可
以证明乙烯具有还原性;
77
(4)因浓硫酸具有强氧化性,酒精脱水碳化后,碳与浓硫酸加热反应产生① 、② 气体;二氧化硫、
二氧化碳均能与氢氧化钠溶液反应产生亚硫酸钠和碳酸钠混合液;因此图2中,装置A中加入乙中的混合
液,加入盐酸后产生二氧化碳和二氧化硫混合气体;二氧化硫具有漂白性,能够使品红褪色,用浓溴水吸
收二氧化硫,再次用品红检验二氧化硫是否除尽,最后用澄清的石灰水检验二氧化碳气体;结合以上分析
可知,为检验可能产生的气体,设计如图2所示装置进行检验,将图1装置乙中溶液转移到图2的锥形瓶
中,打开分液漏斗活塞,进行实验,能说明有气体①二氧化碳产生的实验现象是:D中的品红溶液不褪色,
E中澄清石灰水变浑浊;能说明有气体②二氧化硫产生的实验现象是:B中的品红溶液褪色。
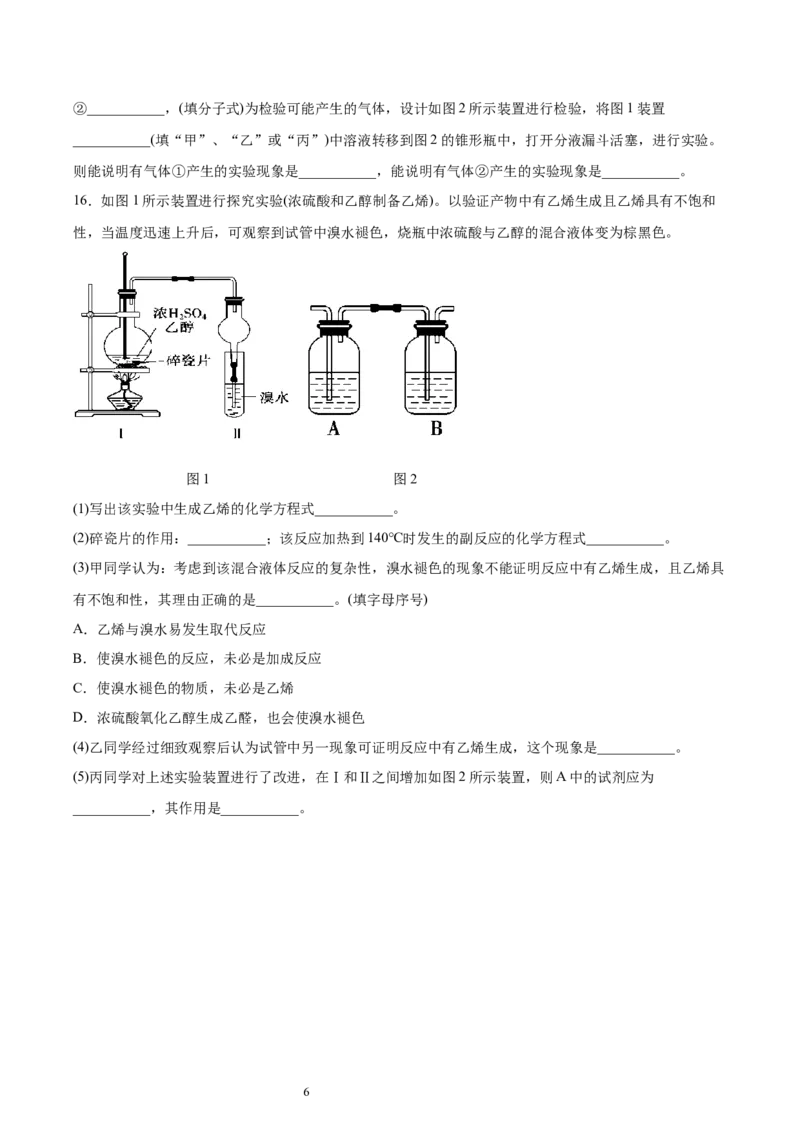
16.CHCHOH HO+CH=CH ↑ 防止液体发生爆沸 2C HOH →C HOC H + H O
3 2 2 2 2 2 5 2 5 2 5 2
BC 液体分两层,下层有油状液体 NaOH溶液 吸收二氧化硫
【详解】
(1)实验中生成乙烯的化学方程式CHCHOH HO+CH=CH ↑
3 2 2 2 2
;
(2)碎瓷片的作用:防止液体发生爆沸;该反应加热到140℃时发生的副反应的化学方程式2C HOH
2 5
→C HOC H + H O;
2 5 2 5 2
(3) A.乙烯与溴水易发生加成反应,故A错误;
B.使溴水褪色的反应,未必是加成反应,也可能是浓硫酸使乙醇碳化后的碳单质与浓硫酸加热生成的二
氧化硫,与溴单质发生氧化还原反应使溴水褪色,故B错误;
C.使溴水褪色的物质,未必是乙烯,也可能是二氧化硫,故C正确;
D.浓硫酸不能氧化乙醇生成乙醛,故D错误;
(4)乙同学经过细致观察后认为试管中另一现象可证明反应中有乙烯生成,因为乙烯与溴单质发生加成后生
成1,2-二溴-乙烷,该有机物不溶于水,则看到的现象是液体分两层,下层有油状液体;
(5)为了防止二氧化硫对乙烯的性质检验产生干扰,丙同学对上述实验装置进行了改进,应在Ⅰ和Ⅱ之间增
加如图2所示装置,除去二氧化硫,则A中的试剂应为NaOH溶液,其作用是吸收二氧化硫。
8