文档内容
一、选择题(每小题2分,共28分)
1.俗话说:“五谷杂粮壮身体,青菜萝卜保平安”,其中“萝卜青菜”富含的营养素是( )
A.糖类 B.脂肪 C.蛋白质 D.维生素
2.加油站内必须张贴的图标是( )
3.下列物质的用途中,利用其化学性质的是( )
A.氧气用于气焊 B.浓硫酸用作干燥剂
C.铜用于制导线 D.用活性炭除去冰箱异味
4.下列物质由分子构成的是( )
A.水 B.铝 C.金刚石 D.氯化钠
5.下列净水方法中,净化程度最高的是( )
A.吸附 B.沉淀 C.过滤 D.蒸馏
6.环境保护是我国的一项基本国策。下列行为有利于环境保护的是( )
A.焚烧废弃塑料 B.深埋处理废旧电池 C.控制企业排污 D.丢弃实验剩余药品
7.下列物质的化学式和俗名对应不相符的是( )
A.Hg—水银 B.NaHCO3 —苏打 C.NaOH—苛性钠 D.C
2
H
5
OH—酒精
8.溶液与我们的日常生活密切相关。下列关于溶液的说法正确的是( )
A.溶液一定是无色透明的 B.面粉与水混合可形成溶液
C.稀溶液也可能是饱和溶液 D.溶液的上层浓度小,下层浓度大
9.下列操作正确的是( )
10.下列区分物质的方法错误的是( )
A.用燃着的木条区分氮气和二氧化碳
B.用氯化钡溶液区分稀盐酸和稀硫酸C.用水区分硝酸铵固体和氢氧化钠固体
D.用点燃闻气味的方法区分羊毛纤维和合成纤维
11.生活中处处充满化学。下列说法正确的是( )
A.食用加碘盐可以预防人体贫血
B.用细沙灭火降低了可燃物着火点
C.洗洁精清除油污利用了乳化作用
D.施用大量的化肥农药以提供农作物的产量
12.下列事实的结论或解释错误的是( )
A.分离液态空气制氧气——说明分子可以再分
B.桂花开放时满园飘香——说明分子在不断运动
C.气体可压缩储存于钢瓶中——说明分子之间有间隔
D.酸碱中和反应都能生成水——实质是H+与OH—结合生产了HO
2
13.下列各组物质中,能相互反应且反应后溶液总质量增加的是( )
A.铁和硫酸铜溶液 B.氧化铁固体和稀硫酸
C.盐酸和澄清石灰水 D.氯化钠溶液和硝酸钾溶液
14.下列实验方案合理的是( )
选项 实验目的 所用试剂或方法
A 实验室制取二氧化碳 块状大理石与稀硫酸
B 鉴别硬水和软水 观察液体是否浑浊
C 鉴别水、氯化钾溶液 硝酸银溶液
D 除去二氧化碳中少量的一氧化碳 通入氧气,点燃
二、填空题(包括5小题,共21分)
15(. 4分)用化学用语填空:空气中含量最多的气体 ;氧化铝中铝元素显+3价
;硝酸铵中的阳离子 ;人体内含量最高的金属元素 。
16.(5分)请根据下图中的信息回答问题。
⑴硫属于 (填“金属”或“非金属”)元素;硫元素的原子序数为 。
⑵图乙所表示粒子的化学符号是 。
⑶硫在空气中燃烧的化学方程式为 。
17.(4分)下图为某反应的微观模拟示意图。
⑴图中的氧化物有 种。
⑵该反应的化学方程式为 ,属于 (填基本反应类
型)。18.(4分)为减少汽车尾气对空气的污染,目前在燃料使用和汽车制造技术方面采取了一些
措施。
⑴有些城市的部分汽车改用压缩天然气(CNG),天然气的主要成分是 。
⑵氢化镁(化学式:MgH )固体看作为氢动力汽车的能源提供剂,提供能源时氢化镁与水反
2
应生成一种碱和氢气,反应的化学方程式为 。选用氢气作为能
源的一个优点是 。
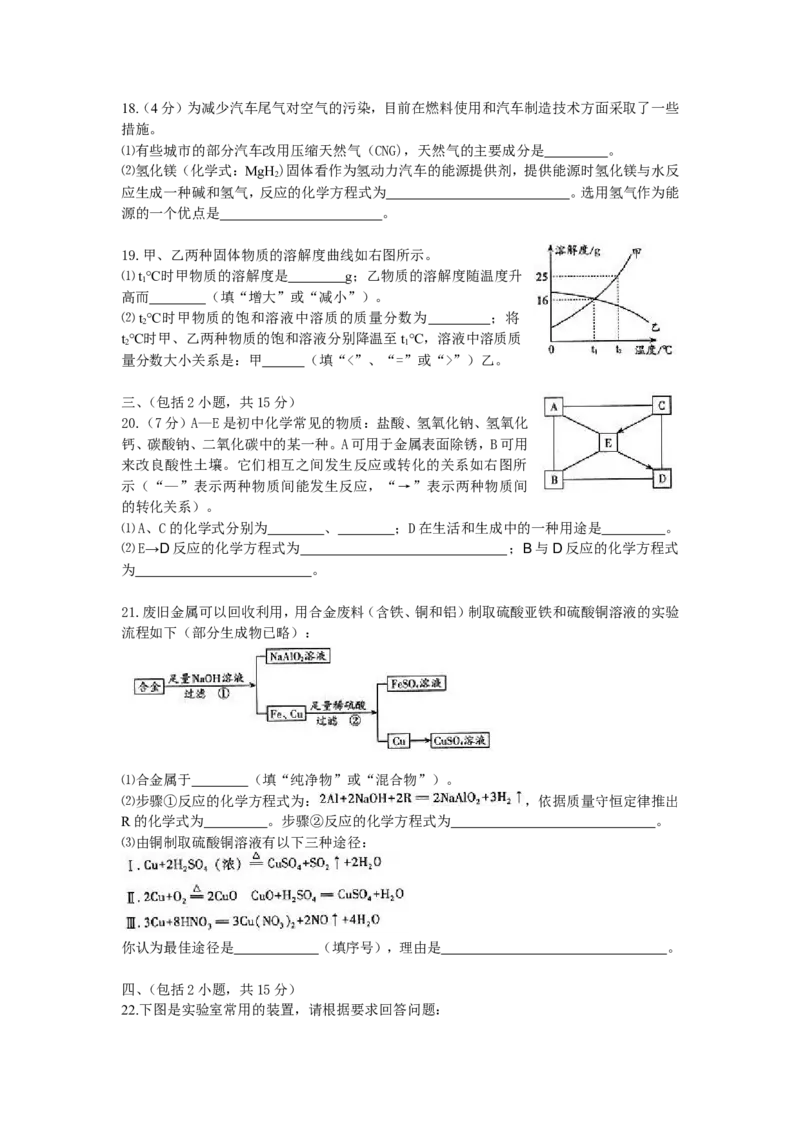
19.甲、乙两种固体物质的溶解度曲线如右图所示。
⑴t℃时甲物质的溶解度是 g;乙物质的溶解度随温度升
1
高而 (填“增大”或“减小”)。
⑵t℃时甲物质的饱和溶液中溶质的质量分数为 ;将
2
t℃时甲、乙两种物质的饱和溶液分别降温至t℃,溶液中溶质质
2 1
量分数大小关系是:甲 (填“<”、“=”或“>”)乙。
三、(包括2小题,共15分)
20.(7分)A—E是初中化学常见的物质:盐酸、氢氧化钠、氢氧化
钙、碳酸钠、二氧化碳中的某一种。A可用于金属表面除锈,B可用
来改良酸性土壤。它们相互之间发生反应或转化的关系如右图所
示(“—”表示两种物质间能发生反应,“→”表示两种物质间
的转化关系)。
⑴A、C的化学式分别为 、 ;D在生活和生成中的一种用途是 。
⑵E→D反应的化学方程式为 ;B与D反应的化学方程式
为 。
21.废旧金属可以回收利用,用合金废料(含铁、铜和铝)制取硫酸亚铁和硫酸铜溶液的实验
流程如下(部分生成物已略):
⑴合金属于 (填“纯净物”或“混合物”)。
⑵步骤①反应的化学方程式为: ,依据质量守恒定律推出
R的化学式为 。步骤②反应的化学方程式为 。
⑶由铜制取硫酸铜溶液有以下三种途径:
你认为最佳途径是 (填序号),理由是 。
四、(包括2小题,共15分)
22.下图是实验室常用的装置,请根据要求回答问题:⑴实验室用氯酸钾和二氧化锰制取氧气的化学方程式为 ,选用
的气体发生装置是 (填装置序号)。反应结束后,若要过滤分离出二氧化锰,除了玻
璃棒外,还需要补充的玻璃仪器名称是 、 。
⑵实验室可用氧化钙固体与浓氨水在常温下混合制取氨气(NH ),选用的气体发生装置是
3
(填装置序号)。
⑶上图中的C、D、E三种装置,均可用右图的F装置代替。若用F装置进行排空
气法收集二氧化碳,二氧化碳行F装置的 (填“a”或“b”,下同)口
通入;若用F装置进行排水法收集氧气,可先在F装置中装满水,然后将氧气从
F装置的 口通入。
⑷将二氧化碳通入紫色石蕊溶液中,溶液变成红色,加热后溶液又变成紫色。用
化学方程式表示加热后溶液又变成紫色的原因是 。
23.NaCO、NaHCO 是生活在常见的盐,某实验小组通过以下实验了探究这两种物质的性质
2 3 3
(已知:NaCO、NaHCO 的水溶液均呈碱性;NaHCO 受热易分解生成NaCO、HO和
2 3 3 3 2 3 2
CO)。
2
⑴称取两种固体各1g分别放入两支试管中,在各加入5mL水,振荡。固体成分溶解,并恢复
至室温。
①发现NaCO 完全溶解,而NaHCO 有剩余。由此得出结论:
2 3 3
在相同温度下, 。②向所得溶液中各滴入1—2滴酚
酞溶液后,溶液均显 色。
⑵①取少量NaHCO 按右图装置进行实验。可观察到的现象
3
是:大试管口有水珠生成, 。
②用 的方法除去混在NaCO 粉末中少量的
2 3
NaHCO。
3
⑶测定NaCO 样品(含氯化钠杂质)中NaCO 的质量分数:
2 3 2 3
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为 ;证明反应后
氯化钙有剩余的方法是 。
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中NaCO 的质量分数为 。
2 3
五(包括2小题,共15分)
24(. 4分)科学家发现,中草药成分中提取的“汗防己碱”能有效避免病毒进入细胞,有助于
预防埃博拉感染,其分子式为C H NO。请回答:
38 42 2 6
⑴汗防己碱属于 (填“无机物”或“有机物”)。
⑵汗防己碱由 种元素组成,分子中氢、氧的原子个数比为 (填最简整数比)
⑶汗防己碱中 元素的质量分数最小。
25.(11分)取盐酸与氯化铜的混合溶液27g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液质量关系如图
所示。
⑴滴入氢氧化钠溶液的质量在0—4g时,发生反应的化学方程式为
。
⑵与氯化铜反应的氢氧化钠的质量为 g。
⑶求原盐酸与氯化铜的混合溶液中氯化铜的质量分数(写出计算过程)。
2015-2016年汕尾市初中毕业生学业考试
化学试题参考答案
一、选择题(每小题2分,共28分)
1、D 2、B 3、A 4、A 5、D 6、C 7、B
8、C 9、D 10、A 11、C 12、A 13、B 14、C
二、填空题(包括5小题,共21分)
15.(4分)
+3
N ,AlO ,NH+ , Ca2+
2 2 3 4
16.(5分)
⑴非金属元素,16
⑵S2-
⑶ S+O 点燃 SO
2 2
17.(4分)
⑴两种
⑵ H2O+C 高温 H2 + CO, 置换
18.(4分)
⑴
⑵ MgH+HO=Mg(OH)+H↑ ,携带方便,使用安全
2 2 2 2
19. (4分)
⑴16g ,减少
⑵20% ,甲>乙
三、(包括2小题,共15分)
20.(7分)
⑴HCl 、Ca(OH)2 ,光合作用的原料 、灭火
⑵Na2CO3+2HCl=2NaCl+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O
21. (8分)
⑴混合物
⑵H2O ,Fe+H2SO4==CFeSO4 +H
2
↑
⑶ I, II会产生污染物二氧化硫,污染空气,并且硫酸的利用率低,III不产生硫酸铜,还产生
污染物:一氧化氮四、(包括2小题,共21分)
22. (10分)
⑴ 2KClO MnO 、 △ 2KCl+3O ↑ ,A ,烧杯、漏斗
3 2. 2
⑵ B
⑶ b,a
⑷ H2CO3 ∆ H2O+CO2↑
23. (11分)
⑴①碳酸钠的溶解度比碳酸氢钠的大 ②红色
⑵①澄清的石灰水变浑浊 ②加热
⑶②CaCl2+Na
2
CO
3
=CaCO3↓+2NaCl,向反应后所得溶液中加入碳酸钠,有沉淀生成
③ %
CaCl2+Na
2
CO
3
=CaCO3↓+2NaCl
106 100
x n
x=106n/100 样品中碳酸钠的质量分数为 %
五(包括2小题,共15分)
25.(4分)
⑴ 有机物
⑵ 四
⑶ 氮
27.(11分)
⑴NaOH+HCl=NaCl+H2O
⑵20g×20%= 1.6g
⑶设混合液中氯化铜的质量为x
2NaOH+CuCl2==Cu(OH)2 ↓+2NaCl
80 135
1.6g x
80 / 1.6g =135/x
x=2.7g
混合液中氯化铜的质量分数为:2.7g÷27g×100%=10%
答:略