文档内容
第 30 讲 碱金属元素
知识导航
知识精讲
一、碱金属元素概述
1. 定义
碱金属元素为第ⅠA族(除氢)的元素。包括锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs),钫
(Fr),其中钫为放射性元素。
2. 相似性
碱金属元素原子的最外层都有_____个电子,很容易_______,最高正价为_____价,最高价氧化物对应的
水化物均为_____碱,是典型的活泼金属元素。
3. 递变性
随着核电荷数的增加,碱金属元素原子的电子层数逐渐_______,原子半径逐渐______。
二、碱金属元素的物理性质
碱金属 颜色 状态 密度/g·cm-3 熔点/℃ 沸点/℃
锂 0.534 180.5 1347
钠 0.97 97.81 882.9
银白色
钾 柔软 0.86 63.65 774
铷 1.532 38.89 688
铯 略带金色光泽 1.879 28.40 678.4
1. 相似性
碱金属单质都有______色的金属光泽(但____略带金色光泽)、硬度小、有延展性,密度小、熔沸点较低,导电、导热性良好,液态钠钾合金可做原子反应堆的导热剂。
2. 递变性
随着核电荷数的增加,单质的熔点和沸点逐渐______,密度逐渐______,(但ρ ___ρ ),且Li、Na、K
K Na
的密度_____1,Rb、Cs的密度_____1。
三、碱金属与氧气的反应
碱金属 现象及产物 化学方程式
Li 不如Na剧烈,生成LiO 4Li + O ===== 2LiO
2 2 2
Na 剧烈燃烧,生成NaO 2Na + O ===== NaO
2 2 2 2 2
K 燃烧比Na剧烈,生成复杂的氧化物 K + O ===== KO (超氧化钾)
2 2
Rb 燃烧反应更剧烈,生成更复杂的氧化物
Cs 燃烧反应更剧烈,生成更复杂的氧化物
【实验结论】随着核电荷数的增加,碱金属与O 反应越来越_____,产物越来越_________。
2
四、碱金属与水的反应
碱金属 现象及产物 化学方程式
Li 反应较慢,生成H 2Li + 2H O === 2LiOH + H↑
2 2 2
Na 反应剧烈,生成H 2Na + 2H O === 2NaOH + H↑
2 2 2
K 反应剧烈,轻微爆炸,生成H 2K + 2H O === 2KOH + H↑
2 2 2
Rb 遇水立即燃烧,爆炸,生成H
2
Cs 遇水立即燃烧,爆炸,生成H
2
【实验结论】碱金属都能与水反应,反应的通式为2R + 2HO===2ROH + H↑ ,随着核电荷数的增加,
2 2
碱金属与水反应越来越______,生成的ROH(最高价氧化物对应的水化物)的碱性越来越______。
五、碱金属化学性质递变性的微观解释
核电荷数增加→电子层数增加→对电子引力降低→越容易失去电子→元素的金属性增强→单质的还原性增
强。
对点训练
题型一:碱金属的物理性质
【例1】(2021·云南省大姚县第一中学高一月考)下列不属于碱金属单质的通性的是
A.硬度小、密度小 B.熔点较低C.焰色反应相同 D.导热、导电性能强
题型二:碱金属的化学性质
【变2-7】(2019·山西·太原五中高三月考)下列关于碱金属及其化合物的叙述错误的是( )
A.金属钠投入Ca(HCO ) 溶液,反应后有白色沉淀析出
3 2
B.干粉灭火器能用于扑灭金属钠、钾的着火
C.生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl
D.取用金属钠、钾时,所需实验用品有小刀、镊子、滤纸、玻璃片
【变3】(2020·全国·高一课时练习)下列对碱金属的叙述正确的是
①K通常保存在煤油中以隔绝与空气的接触
②碱金属常温下呈固态,取用时可直接用手拿
③碱金属中还原性最弱的是锂
④碱金属阳离子中氧化性最强的是
⑤碱金属的原子半径随核电荷数的增大而增大
⑥从 到 ,碱金属的密度越来越大,熔、沸点越来越低
A.①③④⑤ B.②③⑤⑥ C.①②③④ D.①②③⑤
题型三:推测碱金属的性质
【变4-4】(2021·全国·高一专题练习)可能存在的第119号未知元素,有人称为“类钫”,它位于碱金属
族,根据元素周期表结构及元素性质变化趋势,下列关于碱金属某些元素原子结构和性质的判断,错误的
是( )
①锂与水反应比钠剧烈 ②金属单质都可以密封保存在煤油中
③锂的氧化物暴露在空气中易吸收二氧化碳 ④锂的阳离子的最外层电子数和钠的相同
⑤“类钫”单质是强还原剂 ⑥“类钫”在化合物中显+1价
⑦推测“类钫”单质的密度应该大于 ⑧“类钫”单质有较高的熔点
A.①②④⑧ B.①②③⑦ C.③④⑤⑧ D.①③④⑥
【例5】(2021·湖南长郡中学高一月考)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,
该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答
下列问题:
(1)铷位于元素周期表的第________周期________族。(2)关于铷的下列说法中不正确的是________(填数字序号)。
①与水反应比钠更剧烈
②Rb O在空气中易吸收水和二氧化碳
2
③Rb O 与水能剧烈反应并释放出O
2 2 2
④它是极强的还原剂
⑤RbOH的碱性比同浓度的NaOH弱
(3)现有铷和另一种碱金属形成的合金5 g,与足量水反应时生成标准状况下的气体2.24 L,则另一碱金属
可能是_______________(填元素符号)。
(4)铷久置于空气中,最终变成产物是_____________。
A.Rb O B.Rb O C.Rb CO D.RbHCO
2 2 2 2 3 3
提分特训
【题1】(2021·全国·模拟预测)“铷(Rb)原子钟”被誉为卫星的“心脏”。下列说法正确的是
A.金属铷的熔点高于钾 B. 的中子数为48
C. 和 化学性质不同 D.铷元素属于ⅠB族
【题2】(2020·全国·高一课时练习)下列关于Li、Na、K、Rb、Cs的叙述均正确的一组是
①金属性最强的是锂②氧化性最强的是锂离子③在自然界中均以化合态形式存在④Li的密度最大⑤铯与水
反应十分剧烈,甚至会发生爆炸
A.①②③ B.④⑤ C.②④ D.②③⑤
【题3】(2021·上海金山·二模)已知有钠、钾及钠钾合金,对于它们三者熔点高低比较正确的是
A.钠钾合金>钠>钾 B.钠>钾>钠钾合金
C.钠>钠钾合金>钾 D.钾>钠钾合金>钠
【题4】(2021·全国·高一课时练习)下列关于碱金属元素的叙述错误的是( )
A.随核电荷数递增,碱金属单质的熔点依次降低
B.随核电荷数递增,碱金属单质的密度依次增大
C.碱金属单质都是密度较小的有色金属
D.碱金属元素的原子最外层都只有一个电子
【题5】(2020·福建省泰宁第一中学高一月考)2019年诺贝尔化学奖颁给几位在锂离子电池研发领域做出
贡献的科学家,锂单质化学性质与钠类似,活泼性比钠略弱。它的密度为0.534g/cm3,锂元素的焰色为紫
红色,将绿豆大的锂投入水中,下列实验现象合理的有①锂沉入水中
②锂浮在水面上
③水中有大量气泡
④反应后在水中加入几滴石蕊试液,溶液变红
⑤反应剧烈,发出紫红色火焰
⑥锂四处游动
A.②③ B.①③ C.②③⑤ D.②④⑤⑥
【题6】(2018·河北张家口·高一月考)钾、钠及其化合物的性质都类似。回答下列问题:
(1)单质钾与钠相比,熔沸点:K ____(填“>”“<” 或“=”,下同) Na;密度:K____Na。
(2)超氧化钾(KO )与过氧化钠都能吸收CO 生成碳酸盐和氧气,因此均可用作急救供氧剂。写出超氧化钾
2 2
与CO 反应的化学方程式:________
2
(3)若KO 和NaO 分别与CO 反应时,欲得到等量的氧气,则所需KO 与NaO 的物质的量之比为
2 2 2 2 2 2 2
________,此时两反应转移的电子数之比为_________。
【题7】碱金属元素按原子序数增大,依次为:锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、
钫(Fr,放射性元素)。请回答:
(1)常温常压下,将一定量锂单质投入到一定量重水中,锂完全反应,产生1.6g气体,过滤得到6.75g沉
淀和100mL澄清溶液。则得到的澄清溶液中溶质的物质的量浓度为____________。
(2)钠钾合金许多特殊反应中有着非常重要的应用。取59.80g钠钾合金和一定量四氯化碳在一定条件下
恰好完全反应,制造出5.40g纳米级金刚石粉末。则该钠钾合金中钠元素和钾元素的质量比为_________。
(3)某同学在实验室模拟制备纯碱。0.600 mol NH 和35.100g食盐混合,得到氨盐水总质量为105.300
3
g。向该溶液通入CO 至反应完全,过滤,得到滤液88.200g,则NaHCO 的产率为______________。(保
2 3
留三位小数)
(4)一定条件下,85.5g铷与氧气和臭氧的混合气体22.4L(已折算为标况,且该混合气体对相同状况下
氢气的相对密度为20.8)恰好完全反应,得到两种离子化合物A和B的固体混合物。A和B中,阴阳离子
个数比均为1:1且均存在两种微粒间作用力,A的含氧量为0.3596。则化合物A的化学式为_____________。
将上述固体混合物加热,A可分解生成B和氧气。加热一段时间后,固体混合物中两种阴离子的物质的量
相等,则分解产生的氧气在标况下的体积为_________。
【题8】(2021·静宁县第一中学高一月考)科学家对碱金属的认识始终在不断的探索中前进。
(1)1807年,英国化学家戴维在在无氧条件下电解熔融的KOH,最后成功地得到了银白色的金属钾,实验
中产生的金属液珠一接触水就剧烈反应,放出___________色气体,向溶液中滴入紫色石蕊试液,显
______色,因为_______(写出化学方程式)。
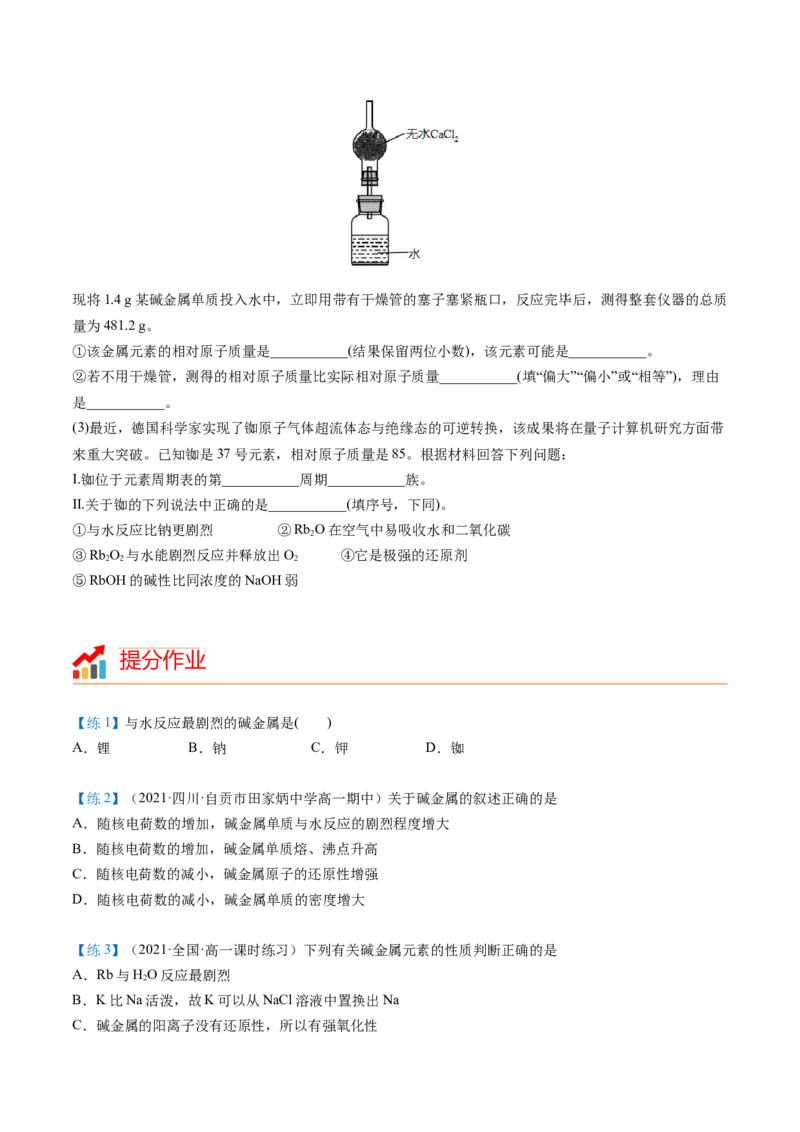
(2)利用碱金属与水的反应可测定某碱金属的相对原子质量。如下图所示,仪器本身连同水和干燥管以及其
内的无水氯化钙的总质量为480.0g。现将1.4 g某碱金属单质投入水中,立即用带有干燥管的塞子塞紧瓶口,反应完毕后,测得整套仪器的总质
量为481.2 g。
①该金属元素的相对原子质量是___________(结果保留两位小数),该元素可能是___________。
②若不用干燥管,测得的相对原子质量比实际相对原子质量___________(填“偏大”“偏小”或“相等”),理由
是___________。
(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带
来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
Ⅰ.铷位于元素周期表的第___________周期___________族。
Ⅱ.关于铷的下列说法中正确的是___________(填序号,下同)。
①与水反应比钠更剧烈 ②Rb O在空气中易吸收水和二氧化碳
2
③Rb O 与水能剧烈反应并释放出O ④它是极强的还原剂
2 2 2
⑤RbOH的碱性比同浓度的NaOH弱
提分作业
【练1】与水反应最剧烈的碱金属是( )
A.锂 B.钠 C.钾 D.铷
【练2】(2021·四川·自贡市田家炳中学高一期中)关于碱金属的叙述正确的是
A.随核电荷数的增加,碱金属单质与水反应的剧烈程度增大
B.随核电荷数的增加,碱金属单质熔、沸点升高
C.随核电荷数的减小,碱金属原子的还原性增强
D.随核电荷数的减小,碱金属单质的密度增大
【练3】(2021·全国·高一课时练习)下列有关碱金属元素的性质判断正确的是
A.Rb与HO反应最剧烈
2
B.K比Na活泼,故K可以从NaCl溶液中置换出Na
C.碱金属的阳离子没有还原性,所以有强氧化性D.从Li到Cs都易失去最外层1个电子,且失电子能力逐渐增强
【练4】下列关于碱金属的叙述中正确的是( )
A.碱金属单质与水反应都能生成碱和H
2
B.碱金属单质都是质软、电和热的良导体,焰色反应都呈现黄色
C.碱金属的密度都小于1g/cm3,因此碱金属单质都可以保存在煤油中
D.碱金属单质在空气中燃烧都生成过氧化物
【练5】(2020·全国·高一)以下关于锂、钠、钾、铷、铯的叙述不正确的是( )
①对应的氢氧化物中,碱性最强的是
②单质熔点最高的是铯
③与 反应均可得到多种氧化物
④单质的密度依次增大
⑤单质的还原性依次增强
⑥对应阳离子的氧化性依次增强
A.①③⑤ B.②④⑥ C.②③④⑥ D.①⑤
【练6】(2019·黑龙江绥化市高一期末)下列有关碱金属的叙述正确的是
A.碱金属单质和氧气反应时都会生成同类产物
B.碱金属单质的硬度都较大
C.液态的钠可用作核反应堆的传热介质
D.碱金属单质都是银白色的固体
【练7】(2020·全国·高一课时练习)可能存在的第119号元素被称为“类钫”,据元素周期表结构及元素
性质变化趋势,有关“类钫”的预测说法正确的是( )
A.“类钫”在化合物中呈 价
B.“类钫”属过渡元素,具有放射性
C.“类钫”单质的密度小于
D.“类钫”单质有较高的熔点
【练8】(2020·全国·高一课时练习)下列关于碱金属元素的说法正确的是( )
A.碱金属元素中,锂原子失去电子的能力最强
B.碱金属单质可将铜从其盐溶液中置换出来
C.金属钾具有强还原性, 具有强氧化性
D.常温下Cs与水反应会发生爆炸【练9】碱金属元素是指ⅠA族中除H以外的金属元素,完成下列问题:
(1)下列有关比较不正确的是__________(填序号)。
①原子半径: ②单质还原性:
③离子氧化性: ④碱性:
(2)铯位于元素周期表第六周期ⅠA族,根据铯在元素周期表中的位置,推断下列内容:
①铯原子核外共有__________个电子层,最外层电子数为__________。
②铯单质与水剧烈反应,放出_________色气体,生成的溶液可使紫色石蕊溶液显_________色。
③预测铯单质的还原性比钠单质的还原性__________(填“弱”或“强”)。关注更新免费领取,淘宝唯一每月更新店铺:知二教育