文档内容
第 2 课时 硫酸 不同价态含硫物质的转化
学业要求 核心素养对接
1.能列举、描述、辨识硫酸的重要物理性
质、化学性质及实验现象。 1.从氧化还原的角度分析浓硫酸的强氧
化性,以提高学生宏观辨识与微观探析
2.能从氧化还原的角度分析浓硫酸的强
的素养水平。
氧化性。
2.通过不同价态硫元素之间的转化的研
3.SO的检验。
究提高学生证据推理和模型认知水平。
4.了解不同价态硫元素之间的转化。
[知 识 梳 理]
知识点一 硫酸
硫酸安全警示牌
警示牌中为什么注明硫酸是腐蚀品,硫酸有什么样的性质,使用时需要注意什么
请完成下列知识点,你就会明白:
1.硫酸的物理性质
纯硫酸是无色、黏稠、难挥发的油状液体,稀释时放出大量热。
2.稀硫酸——具有酸的通性
(1)电离方程式为H SO ===2H++SO。
2 4
(2)硫酸具有酸的通性,可与酸碱指示剂作用,也可与活泼金属、碱、碱性氧化物及
某些盐反应。
3.浓硫酸的特性
(1)吸水性:浓硫酸能够吸收气体、液体中的水分子,故常用做干燥剂。不能用于干燥碱性气体和还原性气体
(2)脱水性:浓硫酸能把有机物中的氧、氢元素按水的组成比脱去,留下黑色的炭。
如向蔗糖中加入浓硫酸时,蔗糖逐渐变黑,体积膨胀,形成疏松多孔的海绵状固
体,并放出有刺激性气味的气体。生成的气体有H O、CO 、SO
2 2 2
(3)强氧化性
①与金属的反应:除Au、Pt以外的绝大多数金属都能与浓硫酸作用,如与铜反应。
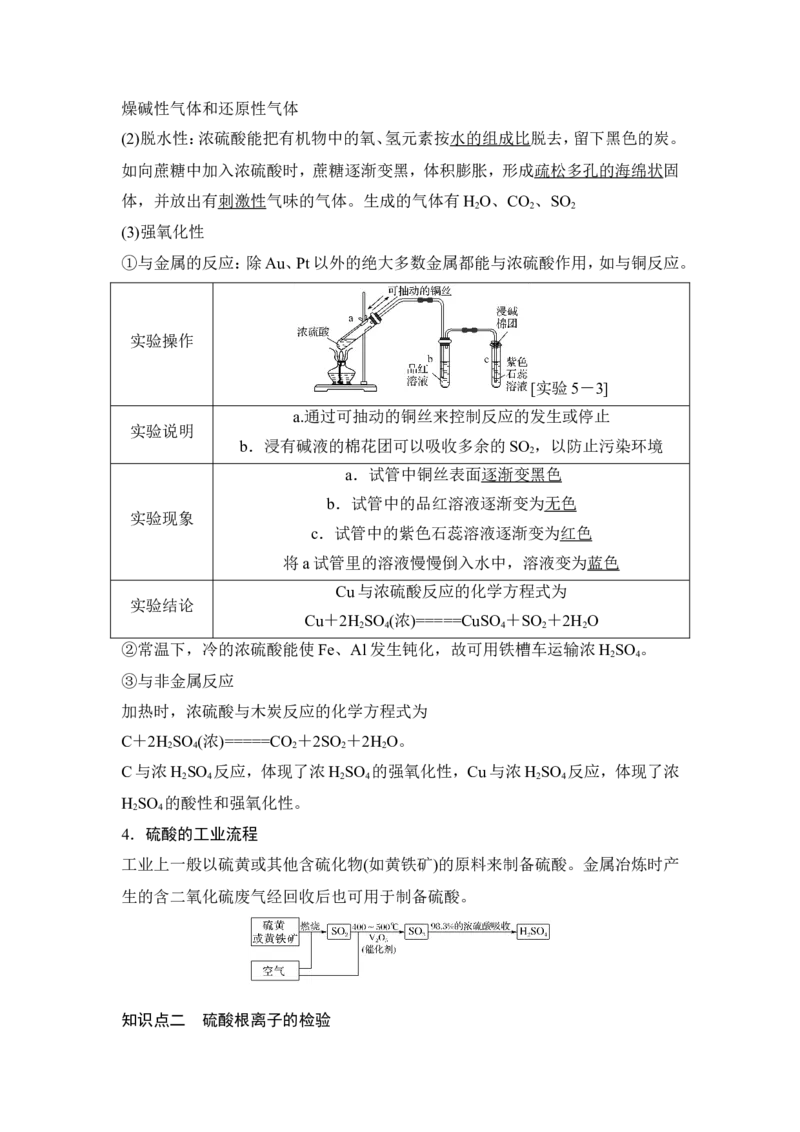
实验操作
[实验5-3]
a.通过可抽动的铜丝来控制反应的发生或停止
实验说明
b.浸有碱液的棉花团可以吸收多余的SO ,以防止污染环境
2
a.试管中铜丝表面逐渐变黑色
b.试管中的品红溶液逐渐变为无色
实验现象
c.试管中的紫色石蕊溶液逐渐变为红色
将a试管里的溶液慢慢倒入水中,溶液变为蓝色
Cu与浓硫酸反应的化学方程式为
实验结论
Cu+2H SO (浓)=====CuSO +SO +2H O
2 4 4 2 2
②常温下,冷的浓硫酸能使Fe、Al发生钝化,故可用铁槽车运输浓H SO 。
2 4
③与非金属反应
加热时,浓硫酸与木炭反应的化学方程式为
C+2H SO (浓)=====CO +2SO +2H O。
2 4 2 2 2
C与浓H SO 反应,体现了浓H SO 的强氧化性,Cu与浓H SO 反应,体现了浓
2 4 2 4 2 4
H SO 的酸性和强氧化性。
2 4
4.硫酸的工业流程
工业上一般以硫黄或其他含硫化物(如黄铁矿)的原料来制备硫酸。金属冶炼时产
生的含二氧化硫废气经回收后也可用于制备硫酸。
知识点二 硫酸根离子的检验在实验室里,通常将溶液先加稀盐酸酸化,以排除CO、Ag+等可能造成的干扰,
然后加入BaCl 溶液来检验SO的存在。
2
知识点三 不同价态含硫物质的转化
1.常见重要化合物
名称及化学式
石膏:CaSO ·2H O 熟石膏:2CaSO ·2H O
4 2 4 2
胆矾:CuSO ·5H O 黄铁矿:FeS 黄铜矿:CuFeS
4 2 2 2
芒硝:Na SO ·10H O
2 4 2
2.硫的常见化合价及代表物
化合价 代表物
-2价 H S 、S2-
2
0价 S
+4价 SO 、H SO 、Na SO
2 2 3 2 3
+6价 SO 、H SO 、Na SO
3 2 4 2 4
3.不同价态硫元素转化关系图
微判断
(1)一般把pH<5.6的雨水称为酸雨,酸雨中一般含有硝酸、硫酸等强酸( )
(2)在常温下,浓硫酸和浓硝酸与Fe和Al发生钝化,说明常温下浓H SO 和浓
2 4
HNO 与Fe和Al都不反应( )
3
(3)浓硫酸具有强氧化性,稀硫酸不具有氧化性( )
(4)常温下将铜片放入浓硫酸中,无明显变化,说明铜在浓硫酸中发生钝化( )
(5)将浓H SO 滴到湿的蔗糖表面,固体变黑膨胀,说明浓H SO 有脱水性、吸水
2 4 2 4
性和强氧化性( )
(6)浓H SO 具有强氧化性,SO 具有还原性,所以浓H SO 不能干燥SO ( )
2 4 2 2 4 2
(7)浓H SO 具有吸水性,所以浓H SO 可以干燥H 、CO、NH 、H S、HI、HBr等气
2 4 2 4 2 3 2体( )
答案 (1)√ (2)× (3)× (4)× (5)√ (6)× (7)×
微训练
用来鉴别浓硫酸和稀硫酸的操作错误的是( )
A.分别取10 mL溶液,质量大的是浓硫酸,质量小的是稀硫酸
B.观察液体流动性,流动性好的是稀硫酸,油状黏稠的是浓硫酸
C.把CuSO ·5H O晶体投入溶液中,逐渐变为白色粉末的是浓硫酸,晶体溶解的
4 2
是稀硫酸
D.将铝片分别投入溶液,快速放出气体的是浓硫酸,放出气体慢的是稀硫酸
解析 硫酸浓度越大密度越大,故等体积的浓硫酸和稀硫酸相比,浓硫酸的质量
大于稀硫酸,A项正确。浓硫酸是黏稠的液体,流动性不如稀硫酸,B项正确。浓
硫酸有吸水性,能吸收结晶水合物中的结晶水,故胆矾投入浓硫酸会变为白色粉
末,投入稀硫酸中胆矾晶体溶解,C项正确。常温下浓硫酸使铝片钝化无气体放
出,铝片投入稀硫酸中有气体(氢气)放出,D项错误。
答案 D
微思考
1.浓硫酸如何稀释?
提示 浓硫酸稀释时放出大量的热,故浓硫酸稀释应将浓H SO 沿烧杯的内壁缓
2 4
缓注入H O中,并不断地搅拌。
2
2.实验室制CO ,用HCl与CaCO 反应,为什么不用H SO 与CaCO 反应?
2 3 2 4 3
提示 H SO 与CaCO 反应生成CaSO 微溶于水,覆盖在CaCO 表面,阻止反应
2 4 3 4 3
的进一步发生,而CaCl 溶于水,不存在这个问题。
2
学习任务1 浓H SO 的特性
2 4
情景:很多人使用硫酸的时候不小心,或者是不当的使用硫酸,再或者是不小心触碰到
了硫酸,那么就会造成很多的伤害,任何皮肤在接触了硫酸的时候都是很容易烧
伤的,如果把皮肤烧伤了,那么很有可能会伤害到皮肤,导致皮肤出现化脓的现
象,硫酸有腐蚀性。
(1)浓硫酸的急救措施有哪些呢?
提示 马上用大量的冷水冲洗。
(2)如果浓H SO 滴到蔗糖上,会出现什么现象?
2 4
提示 会使庶糖变黑,体现了脱水性。
(3)如果滴到蓝矾上呢?
提示 蓝矾变成白色粉末,体现了吸水性。
1.浓硫酸吸水性和脱水性的区别
→
|
→
二者的根本区别在于物质本身是否存在水分子
2.浓硫酸强氧化性
(1)本质:浓硫酸具有强氧化性,是因为H SO 分子中+6价的硫元素具有很强的
2 4
得电子能力。
(2)反应规律:
①Fe、Al的钝化,常温下,当Fe、Al遇到浓硫酸时,会与浓硫酸发生反应,表面生
成一层致密的氧化物薄膜而出现钝化现象。过程中发生了氧化还原反应
②常温下与活泼金属反应(铁、铝除外)表现强氧化性和酸性,生成硫酸盐和SO ,
2
硫酸变稀后,生成的气体为H 。
2
③与不活泼金属和非金属反应的规律
a.反应需要加热,否则不反应。
b.还原产物一般是SO ,一般金属被氧化为高价态的硫酸盐,非金属被氧化为高
2
价态氧化物或含氧酸。
c.浓硫酸与金属反应时,既表现酸性又表现强氧化性,而与非金属反应时,只表现强氧化性。
d.随着反应的进行,浓硫酸浓度变小,一旦变为稀硫酸,反应就停止。
④与具有还原性的化合物反应,如与H S、HI、HBr、FeCl 等物质反应。
2 2
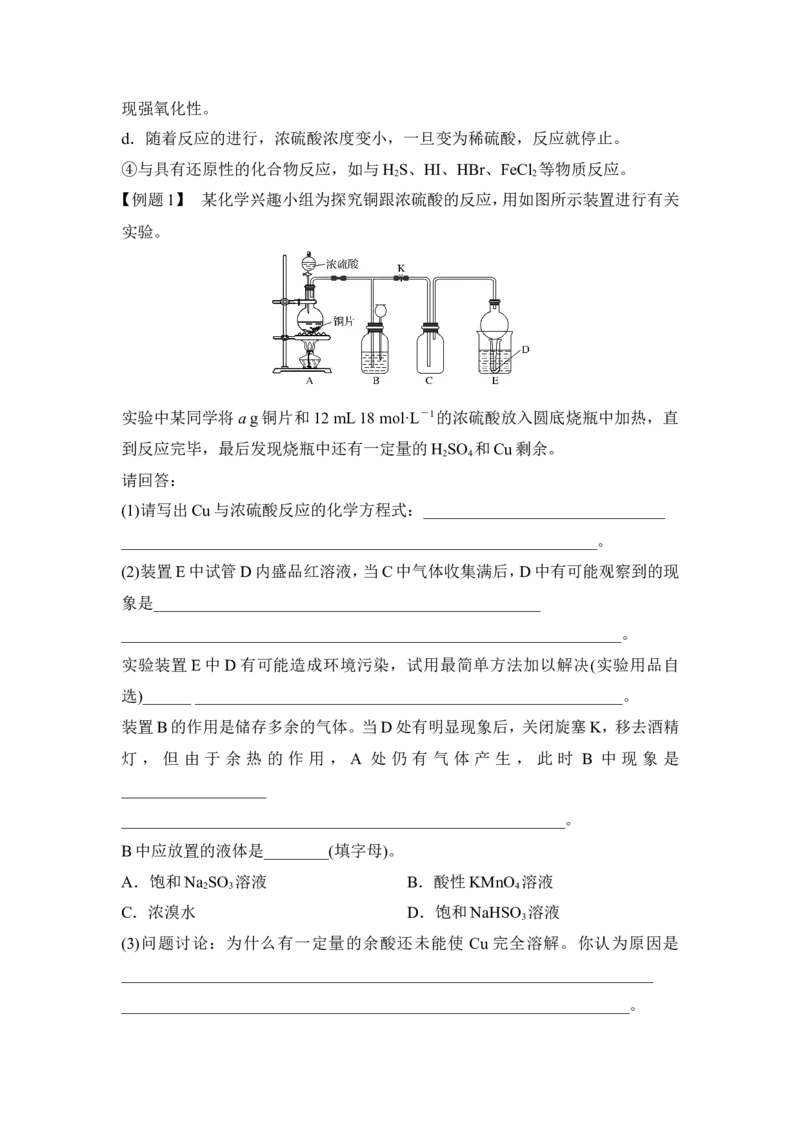
【例题1】 某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关
实验。
实验中某同学将a g铜片和12 mL 18 mol·L-1的浓硫酸放入圆底烧瓶中加热,直
到反应完毕,最后发现烧瓶中还有一定量的H SO 和Cu剩余。
2 4
请回答:
(1)请写出Cu与浓硫酸反应的化学方程式:______________________________
___________________________________________________________。
(2)装置E中试管D内盛品红溶液,当C中气体收集满后,D中有可能观察到的现
象是________________________________________________
______________________________________________________________。
实验装置E中D有可能造成环境污染,试用最简单方法加以解决(实验用品自
选)______ _____________________________________________________。
装置B的作用是储存多余的气体。当D处有明显现象后,关闭旋塞K,移去酒精
灯 , 但 由 于 余 热 的 作 用 , A 处 仍 有 气 体 产 生 , 此 时 B 中 现 象 是
__________________
_______________________________________________________。
B中应放置的液体是________(填字母)。
A.饱和Na SO 溶液 B.酸性KMnO 溶液
2 3 4
C.浓溴水 D.饱和NaHSO 溶液
3
(3)问题讨论:为什么有一定量的余酸还未能使 Cu 完全溶解。你认为原因是
__________________________________________________________________
_______________________________________________________________。足量下列药品能够用来证明反应结束后的烧瓶中的确有余酸的是________(填字
母)。考虑与H+反应的物质
A.Fe B.BaCl 溶液
2
C.Ag D.Na CO 溶液
2 3
(4)实验中该同学向A中反应后溶液中通入一种气体单质,使铜片全部溶解且仅
生成硫酸铜溶液,请问该气体单质是__________(填名称),反应的化学方程式是
__________________________________________________________
_________________________________________________________________。
解析 (1)Cu与浓H SO 反应需加热。(2)SO 能使品红溶液褪色,为防止环境污染
2 4 2
可用的简单方法是用浸有 NaOH 溶液的棉花团塞在试管口,则 SO +
2
2NaOH===Na SO +H O。关闭K,装置内气体压强增大,B广口瓶内液面下降,长
2 3 2
颈漏斗内液面上升。B中的液体应不能与SO 反应,而且要防止SO 的溶解。A项
2 2
Na SO +H O+SO ===2NaHSO ;B 项,KMnO 氧化 SO ;C 项,Br +SO +
2 3 2 2 3 4 2 2 2
2H O===2HBr+H SO ;D项,SO 难溶于饱和NaHSO 溶液。应选D。(3)浓H SO
2 2 4 2 3 2 4
浓度降低,变为稀H SO ,Cu与稀H SO 不反应。检验余酸实质是检验H+的存在。
2 4 2 4
Fe+2H+===Fe2++H ↑,CO+2H+===H O+CO ↑,Fe和Na CO 溶液能证明H
2 2 2 2 3
+的存在;BaCl 溶液不能证明H SO 剩余,因为产物CuSO 也能电离出SO;Ag与
2 2 4 4
H+不反应,不能证明H+的存在。故选AD。(4)根据题目要求气体单质应为强氧化
剂,且仅生成CuSO 溶液,该氧化剂为O 。
4 2
答案 (1)Cu+2H SO (浓)=====CuSO +SO ↑+2H O
2 4 4 2 2
(2)品红溶液褪色 用浸有NaOH溶液的棉花团塞在试管口 试剂瓶中液面下降,
长颈漏斗中液面上升 D
(3)随着H SO 的消耗,浓H SO 浓度逐渐变稀,稀硫酸与铜不反应 AD
2 4 2 4
(4)氧气 2Cu+2H SO +O =====2CuSO +2H O
2 4 2 4 2
变式训练1 下列叙述正确的是( )
A.浓硫酸是一种干燥剂,能够干燥氢气、氧气等气体,但不能干燥碱性气体和有
较强还原性的HI、H S等气体
2
B.浓硫酸与单质碳反应的化学方程式为 C+2H SO (浓)=====CO +2SO ↑+
2 4 2 2
2H O,在此反应中,浓硫酸既表现了强氧化性又表现了酸性
2
C.把足量铜粉投入到含2 mol H SO 的浓硫酸中,加热得到气体体积标准状况下
2 4为22.4 L
D.常温下能够用铁、铝等容器盛放浓硫酸,是因为浓硫酸与其不反应
解析 A项,浓硫酸具有吸水性,但由于其具有强氧化性和酸性,故不能用来干
燥具有还原性的气体和碱性气体(如NH );B项,浓硫酸与S、C等非金属单质作
3
用时,由于没有盐生成,故只显强氧化性;C项,Cu与浓硫酸反应时,浓硫酸浓度
逐渐降低,当反应到一定程度变为稀硫酸时,反应自行停止,故产生的SO 在标
2
况下不足22.4 L;D项是因为浓硫酸的强氧化性使其钝化。
答案 A
学习任务2 SO离子检验的应用
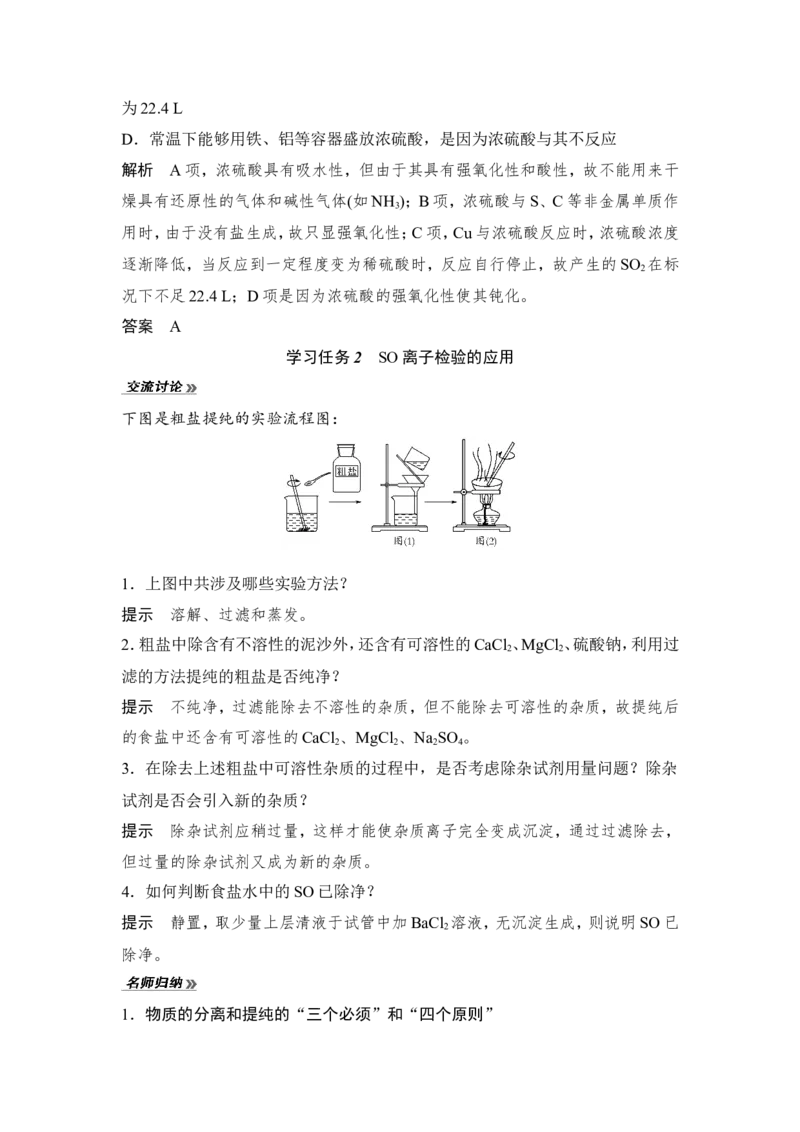
下图是粗盐提纯的实验流程图:
1.上图中共涉及哪些实验方法?
提示 溶解、过滤和蒸发。
2.粗盐中除含有不溶性的泥沙外,还含有可溶性的CaCl 、MgCl 、硫酸钠,利用过
2 2
滤的方法提纯的粗盐是否纯净?
提示 不纯净,过滤能除去不溶性的杂质,但不能除去可溶性的杂质,故提纯后
的食盐中还含有可溶性的CaCl 、MgCl 、Na SO 。
2 2 2 4
3.在除去上述粗盐中可溶性杂质的过程中,是否考虑除杂试剂用量问题?除杂
试剂是否会引入新的杂质?
提示 除杂试剂应稍过量,这样才能使杂质离子完全变成沉淀,通过过滤除去,
但过量的除杂试剂又成为新的杂质。
4.如何判断食盐水中的SO已除净?
提示 静置,取少量上层清液于试管中加BaCl 溶液,无沉淀生成,则说明SO已
2
除净。
1.物质的分离和提纯的“三个必须”和“四个原则”(1)三个必须:
①除杂试剂必须稍过量。
②过量试剂必须除尽,且容易除去。
③除杂途径选最佳,有多种杂质时除杂顺序必须合理。
(2)四个原则:
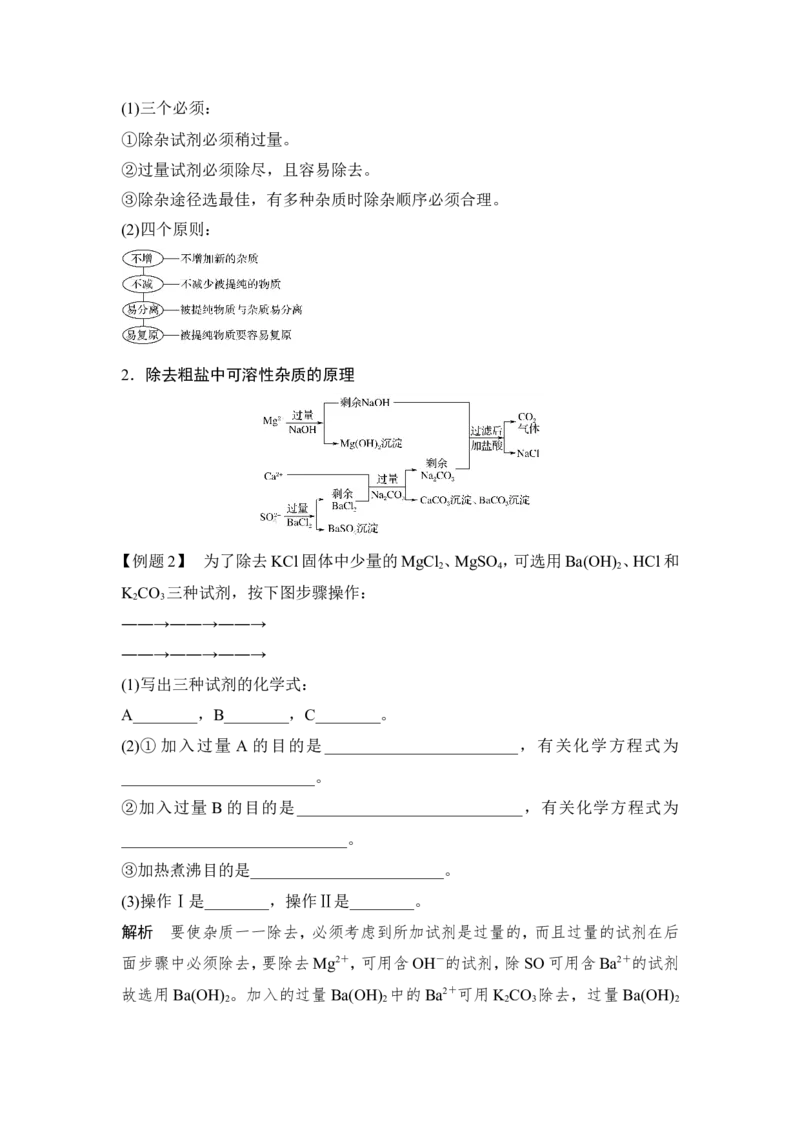
2.除去粗盐中可溶性杂质的原理
【例题2】 为了除去KCl固体中少量的MgCl 、MgSO ,可选用Ba(OH) 、HCl和
2 4 2
K CO 三种试剂,按下图步骤操作:
2 3
――→――→――→
――→――→――→
(1)写出三种试剂的化学式:
A________,B________,C________。
(2)① 加入过量 A 的目的是________________________,有关化学方程式为
________________________。
②加入过量 B 的目的是____________________________,有关化学方程式为
____________________________。
③加热煮沸目的是________________________。
(3)操作Ⅰ是________,操作Ⅱ是________。
解析 要使杂质一一除去,必须考虑到所加试剂是过量的,而且过量的试剂在后
面步骤中必须除去,要除去Mg2+,可用含OH-的试剂,除SO可用含Ba2+的试剂
故选用Ba(OH) 。加入的过量Ba(OH) 中的Ba2+可用K CO 除去,过量Ba(OH)
2 2 2 3 2中的OH-,以及过量K CO 中的CO,可用稀盐酸除去,最后加热煮沸可除去
2 3
HCl。
答案 (1)Ba(OH) K CO HCl
2 2 3
(2)①除尽MgCl 和MgSO MgCl +Ba(OH) ===BaCl +Mg(OH) ↓,MgSO +
2 4 2 2 2 2 4
Ba(OH) ===BaSO ↓+Mg(OH) ↓
2 4 2
②除尽过量 Ba(OH) 和生成的 BaCl Ba(OH) +K CO ===BaCO ↓+2KOH,
2 2 2 2 3 3
BaCl +K CO ===BaCO ↓+2KCl
2 2 3 3
③使HCl挥发
(3)过滤 蒸发
变式训练2 为了除去粗盐中的Ca2+、Mg2+、SO和泥沙,可将粗盐溶于水,然后
进行下列五项操作:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量
Na CO 溶液 ⑤加过量BaCl 溶液,正确的操作顺序是( )
2 3 2
A.①④②⑤③ B.④①②⑤③
C.②④⑤①③ D.⑤②④①③
解析 首先要明确除去粗盐中的Ca2+、Mg2+、SO,可分别加入Na CO 溶液、
2 3
NaOH溶液和BaCl 溶液,且三种溶液均过量,才能使杂质离子分别变成CaCO 、
2 3
Mg(OH) 、BaSO 沉淀,过量的BaCl 溶液只能用Na CO 溶液除去,故要先加入
2 4 2 2 3
BaCl 溶液,再加入Na CO 溶液,才能保证不引入新杂质Ba2+,而多余的NaOH
2 2 3
和Na CO 只需要在过滤后再加入盐酸即可,至于NaOH溶液的加入顺序,只要
2 3
在过滤前加入就可除去Mg2+,故D项正确。
答案 D
学习任务3 (核心素养)制取H SO 的工业流程及H SO 性质应用
2 4 2 4
一、知识要点
第一步:制取SO
2
S+O =====SO 或4FeS +11O =====2Fe O +8SO
2 2 2 2 2 3 2
第二步:制取SO
3
2SO +O 2SO
2 2 3
第三步:吸收SO (用98%的浓H SO 吸收)
3 2 4
SO +H O===H SO 若用水吸收易形成酸雾
3 2 2 4
二、核心素养工业流程⇒提高学生的实验探究与创新意识
【素养解题】
[典例示范] 用硫及其化合物制硫酸有下列三种反应途径,某些反应条件和产物
已省略,下列有关说法不正确的是( )
途径①:S――→H SO
2 4
途径②:S――→SO ――→SO ――→H SO
2 3 2 4
途径③:FeS ――→SO ――→SO ――→H SO
2 2 3 2 4
A.途径①的反应中体现了浓HNO 的强氧化性
3
B.途径②、③的第二步反应在实际生产中可以通过增大O 的浓度来降低成本
2
C.由途径①、②、③分别制取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol e
2 4
-
D.途径②、③比途径①污染相对小且原子利用率高,更能体现“绿色化学”的理
念
[解题思路]
读题干 三种途径,不正确
A项,(浓)HNO 强氧化性
3
B项,增大O 浓度降低成本
2
抽信息
C项,1 mol S转移6 mol e-
D项,绿色化学
注意点 硫元素的价态变化
途径①属于浓硝酸和非金属单质的反应,表现了浓硝酸的强氧化性,
A项正确;途径②、③的第二步反应为可逆反应,通过增大O 的浓度
2
细分析 来提高二氧化硫的转化率,降低成本,B项正确;由途径①、②分别制
取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol e-,而途径③转
2 4
移7.5 mol e-,C项错误。
得答案 C
三、对点训练
1.下列关于浓硫酸与稀硫酸的说法,不正确的是(双选)( )
A.浓硫酸稀硫酸都有脱水性
B.浓硫酸有氧化性,稀硫酸没有氧化性
C.浓硫酸和稀硫酸都有酸性D.常温下,浓硫酸和稀硫酸都不能与铜反应
解析 稀H SO 也有氧化性,能氧化活泼金属,本身被还原成H 。
2 4 2
答案 AB
2.下列现象或事实不能用同一原理解释的是( )
A.SO 和CO 都能使澄清石水变浑浊
2 2
B.硫化钠和亚硫酸钠固体长期暴露在空气中变质
C.常温下铁和铂都不溶于浓硫酸
D.SO 和Na SO 溶液都能使氯水褪色
2 2 3
解析 SO 和CO 都能与Ca(OH) 生成难溶或微溶于水的沉淀;A不选;硫化钠及
2 2 2
亚硫酸钠都具有还原性,易被空气中的氧气氧化而变质,B不选;常温下铁遇浓
硫酸,发生钝化;铂的活泼性较弱,不与浓硫酸反应,不能用同一原理解释,C可
选;SO 和Na SO 都具有还原性,都能与氯水发生氧化还原反应使氯水褪色,D
2 2 3
不选。
答案 C
3.将SO 通入BaCl 溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉淀
2 2
则通入的气体可能是( )
A.CO B.NH
2 3
C.SO D.Cl
3 2
解析 NH 、SO 、Cl 分别与溶有SO 的水溶液反应生成(NH ) SO 和H SO ,再与
3 3 2 2 4 2 3 2 4
BaCl 溶液反应生成白色沉淀;而 CO 不能与溶有 SO 的水溶液反应,也不与
2 2 2
BaCl 溶液反应,无沉淀生成。
2
答案 A
4.将浓H SO 表现的性质填入括号内。
2 4
A.酸性 B.强氧化性
C.脱水性 D.吸水性
(1)用磷矿粉[主要成分Ca (PO ) ]和硫酸反应制磷酸( )
3 4 2
(2)热的浓硫酸与铜片反应 ( )
(3)浓H SO 不能干燥NH 、H S、HI等气体( )
2 4 3 2
(4)浓H SO 能吸收H 或SO 气体中的水分( )
2 4 2 2
(5)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑( )解析 硫酸与Ca (PO ) 反应制磷酸利用了硫酸的强酸性;热的浓硫酸与Cu片反
3 4 2
应生成CuSO 和SO ,表现了浓硫酸的强氧化性和酸性;NH 为碱性气体,不能用
4 2 3
浓H SO 干燥,H S、HI为还原性气体,浓H SO 氧化这两种气体;浓H SO 可用
2 4 2 2 4 2 4
来干燥气体,表现了其吸水性;浓硫酸使湿润的蓝色石蕊试纸变红,表现其酸性,
后变黑,表现其脱水性。
答案 (1)A (2)AB (3)AB (4)D (5)AC
[学 考 练]
1.根据硫元素的化合价判断下列物质中的硫元素不能表现氧化性的是( )
A.Na S B.S
2
C.SO D.H SO
2 2 4
解析 处于最低价态的元素,无氧化性。
答案 A
2.在下列生成二氧化硫的反应中,反应物中的含硫物质被氧化的是 ( )
A.硫在空气中燃烧
B.铜片与浓硫酸共热
C.红热的木炭与浓硫酸反应
D.亚硫酸钠与较大浓度硫酸反应
解析 A选项中硫元素化合价升高,被氧化;B、C选项中浓硫酸中的硫元素化合
价均降低;D项中硫元素的价态不变,故选A。
答案 A
3.将浓硫酸与下列物质作用时,浓硫酸既表现氧化性,又表现酸性的是( )
①红热的木炭 ② H S 气体 ③ Cu ④ FeO ⑤ NH ⑥使木材碳化
2 3
⑦CuSO ·5H O ⑧对铁、铝的钝化
4 2
A.③④ B.①②⑤⑧
C.①②③④⑦ D.以上答案均不正确
解析 与木炭、H S反应及Fe、Al钝化时浓硫酸只表现氧化性;浓硫酸与NH 反
2 3
应时只表现酸性,⑥是浓硫酸的脱水性;⑦是吸水性。③和④符合题意。
答案 A4.下列反应中,调节反应物用量或浓度,不会改变反应产物的是( )
A.铁在硫蒸气中燃烧
B.H SO 与Cu反应
2 4
C.二氧化硫通入澄清石灰水
D.硫酸中加入锌粉
解析 A项中无论硫蒸气量如何,只发生反应:Fe+S=====FeS;B项中浓H SO
2 4
时产生 SO ,稀 H SO 时不反应;C 项中若 SO 少量,发生反应:SO +
2 2 4 2 2
Ca(OH) ===CaSO ↓ + H O , 若 SO 足 量 , 发 生 反 应 : 2SO +
2 3 2 2 2
Ca(OH) ===Ca(HSO ) ;D项中若为稀H SO ,发生反应:Zn+H SO ===ZnSO +
2 3 2 2 4 2 4 4
H ↑,若为浓H SO ,发生反应:Zn+2H SO (浓)=====ZnSO +SO ↑+2H O,故
2 2 4 2 4 4 2 2
选A项。
答案 A
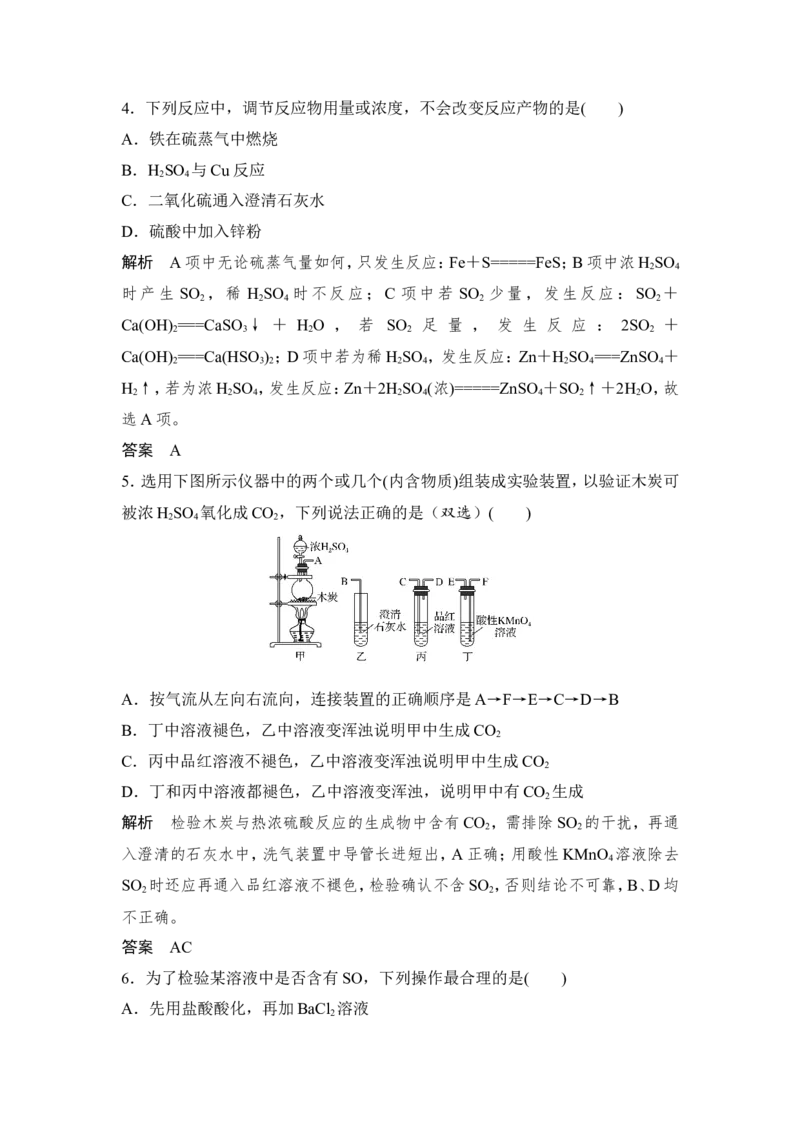
5.选用下图所示仪器中的两个或几个(内含物质)组装成实验装置,以验证木炭可
被浓H SO 氧化成CO ,下列说法正确的是(双选)( )
2 4 2
A.按气流从左向右流向,连接装置的正确顺序是A→F→E→C→D→B
B.丁中溶液褪色,乙中溶液变浑浊说明甲中生成CO
2
C.丙中品红溶液不褪色,乙中溶液变浑浊说明甲中生成CO
2
D.丁和丙中溶液都褪色,乙中溶液变浑浊,说明甲中有CO 生成
2
解析 检验木炭与热浓硫酸反应的生成物中含有CO ,需排除SO 的干扰,再通
2 2
入澄清的石灰水中,洗气装置中导管长进短出,A正确;用酸性KMnO 溶液除去
4
SO 时还应再通入品红溶液不褪色,检验确认不含SO ,否则结论不可靠,B、D均
2 2
不正确。
答案 AC
6.为了检验某溶液中是否含有SO,下列操作最合理的是( )
A.先用盐酸酸化,再加BaCl 溶液
2B.先用硝酸酸化,再加BaCl 溶液
2
C.加入用硝酸酸化的BaCl 溶液
2
D.先用盐酸酸化,再加Ba(NO ) 溶液
3 2
解析 检验SO时常用Ba2+,但是需要排除CO和SO的影响,CO可以通过将溶
液酸化排除影响,SO也可以通过将溶液酸化排除影响,但要注意不能用硝酸等
强氧化性酸,防止SO被氧化成SO,所以通常先用盐酸酸化溶液,排除CO、SO、
Ag+等的影响以后,再用BaCl 溶液检验SO。
2
答案 A
7.下列有关物质检验的实验结论正确的是( )
选项 实验操作及现象 实验结论
向某溶液中先加入盐酸酸化,再加BaCl 溶液,
A 2 该溶液中一定含有SO
有白色沉淀生成
向某溶液中加入盐酸,将生成的气体通入品红
B 该溶液一定含有SO
溶液中,品红溶液褪色
C 将某气体通入品红溶液中,品红溶液褪色 该气体一定是SO
2
将SO 通入Na CO 溶液中,将生成的气体,先
2 2 3
D 通入足量的酸性KMnO 溶液,再通入澄清石灰 说明酸性H SO >H CO
4 2 3 2 3
水中有浑浊
解析 A项,先用盐酸酸化,排除了CO、SO、Ag+等干扰;B项,该溶液中可能含
有HSO;C项,该气体可能是Cl 、O 等。
2 3
答案 AD
8.SO 被认为是造成大气污染的“首犯”。大气中的SO 主要来源于化石燃料(煤
2 2
石油)的燃烧。下列与SO 污染有关的是( )
2
①酸雨现象 ②伦敦“毒雾”事件 ③洛杉矶“光化学烟雾”事件 ④温室效
应
A.①③ B.②④
C.①② D.③④
解析 SO 在空气中遇水蒸气和O 形成亚硫酸、硫酸,随雨水降落到地面,形成
2 2
“酸雨”。1952年12月5日到8日,伦敦上空出现的“毒雾”4天内导致4 000人
死亡,事件过后的两个月内还陆续有8 000人死亡。这种“毒雾”就是工厂排出
的SO 气体引起的。SO 气体主要可引发气管炎、冠心病、肺结核等。洛杉矶“光
2 2
化学烟雾”是由汽车排放的尾气(含碳氢化合物和氮氧化物)造成的。“温室效应”是由CO 等引起的。故正确答案为C项。
2
答案 C
9.下列因果关系不正确的是( )
选项 原因 结果
A 植树造林 温室效应
B SO 和NO 大量排放 酸雨
2 2
C 汽车尾气的排放 光化学烟雾
含氮、磷等元素的生活废水的大量排
D 赤潮
放
解析 A项,温室效应是CO 的大量排放导致的,植树造林可降低空气中CO 的
2 2
浓度,缓解温室效应;B项,SO 和NO 等酸性气体的大量排放,会导致酸雨;C项,
2 2
汽车尾气中含氮氧化合物、碳氢化合物,可引起光化学烟雾;D项,氮、磷等营养
元素可使水体富营养化,引起赤潮。
答案 A
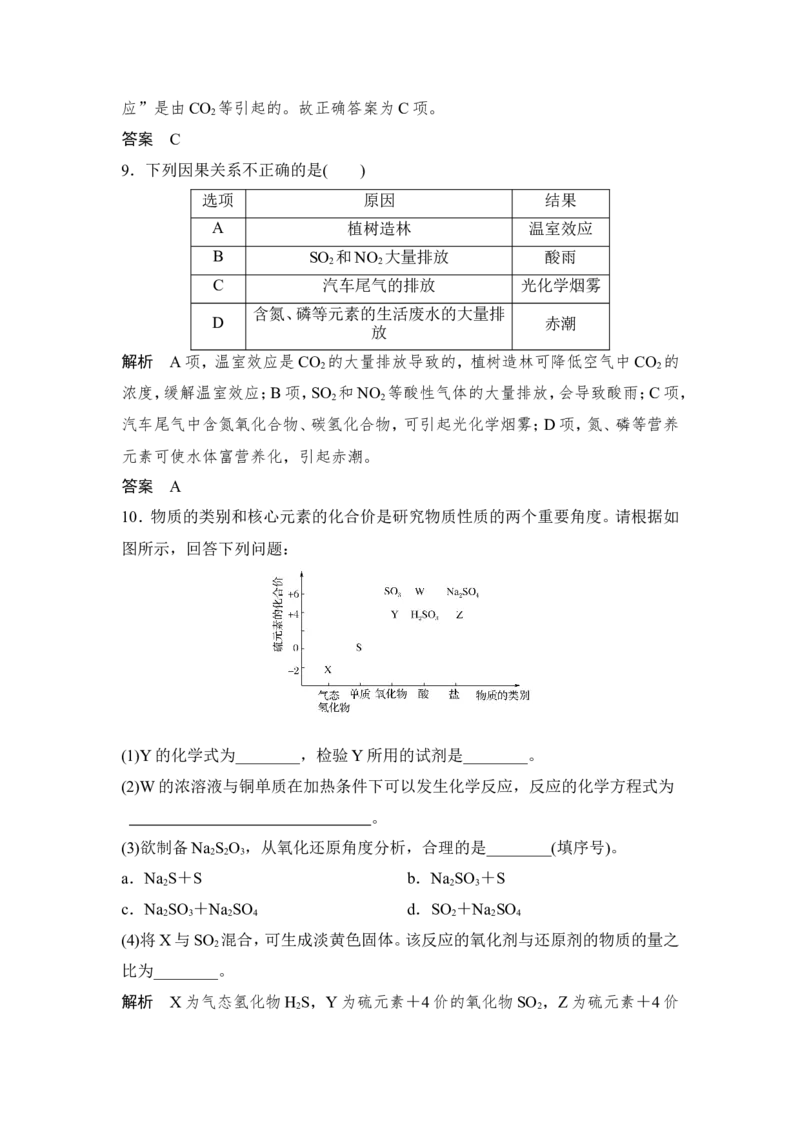
10.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据如
图所示,回答下列问题:
(1)Y的化学式为________,检验Y所用的试剂是________。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
。
(3)欲制备Na S O ,从氧化还原角度分析,合理的是________(填序号)。
2 2 3
a.Na S+S b.Na SO +S
2 2 3
c.Na SO +Na SO d.SO +Na SO
2 3 2 4 2 2 4
(4)将X与SO 混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之
2
比为________。
解析 X为气态氢化物H S,Y为硫元素+4价的氧化物SO ,Z为硫元素+4价
2 2的盐,可以为Na SO ,W为+6价的含氧酸H SO 。(1)由上述分析可知Y为二氧
2 3 2 4
化硫气体,二氧化硫具有漂白性可以使品红溶液褪色,加热恢复红色,所以检验
二氧化硫的试剂可以是品红溶液。(2)W的浓溶液是浓硫酸,与铜单质在加热条件
下可以发生化学反应,反应的化学方程式为:Cu+2H SO (浓)=====CuSO +
2 4 4
2H O+SO ↑。(3)Na S O 中S为+2价,从氧化还原的角度分析,反应物中S元
2 2 2 2 3
素化合价必须分别大于2和小于2,a中S化合价都小于2,c、d中S的化合价都
大于2,b符合题意。(4)将X即H S与SO 混合,可生成淡黄色固体,发生反应:
2 2
2H S+SO ===3S↓+2H O,反应中H S做还原剂,SO 做氧化剂,则该反应的氧
2 2 2 2 2
化剂与还原剂的物质的量之比为1∶2。
答案 (1)SO 品红溶液
2
(2)Cu+2H SO (浓)=====CuSO +2H O+SO ↑
2 4 4 2 2
(3)b (4)1∶2
11.盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就硫酸与金属铜反应的情
况,回答下列问题:
(1)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热条件下跟稀硫酸反应,有关
的化学方程式是__________________________________________________
_________________________________________________________________。
不采用铜跟浓硫酸反应来制取硫酸铜的原因是_________________________
______________________________________________________________。
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的
硫酸为 0.9 mol。则浓硫酸的实际体积________(填“大于”“等于”或“小
于”)180 mL。
(3)将8 g Fe O 投入150 mL某浓度的稀硫酸中,再投入7 g铁粉,充分反应后,收
2 3
集到1.68 L H (标准状况),同时,Fe和Fe O 均无剩余,为了中和过量的硫酸,且
2 2 3
使溶液中铁元素完全沉淀,共消耗4 mol·L-1的NaOH溶液150 mL。则原硫酸的
物质的量浓度为________。
解析 (1)加热条件下,Cu和氧气反应生成CuO:2Cu+O =====2CuO,CuO和稀
2
硫酸反应方程式为CuO+H SO ===CuSO +H O;浓硫酸和铜反应方程式为:Cu
2 4 4 2
+2H SO (浓)=====CuSO +SO ↑+2H O,生成等量的硫酸铜时需要浓硫酸较
2 4 4 2 2
多且生成的二氧化硫污染环境,所以不采用铜跟浓硫酸反应来制取硫酸铜。(2)在加热条件下,浓硫酸和铜反应生成二氧化硫,但浓硫酸浓度达到一定值后变为稀
硫酸,稀硫酸和铜不反应,所以当被还原的硫酸为0.9 mol时,则所用浓硫酸的实
际体积应大于180 mL。(3)该过程中发生的反应为:Fe O +3H SO ===Fe (SO ) +
2 3 2 4 2 4 3
3H O 、 Fe + H SO ===FeSO + H ↑ 、 Fe (SO ) + Fe===3FeSO 、 FeSO +
2 2 4 4 2 2 4 3 4 4
2NaOH===Fe(OH) ↓+Na SO 、2NaOH+H SO ===Na SO +2H O,最终溶液中
2 2 4 2 4 2 4 2
的溶质是Na SO ,由原子守恒得n(NaOH)=n(Na SO )=n(H SO ),则c(H SO )=
2 4 2 4 2 4 2 4
==2 mol·L-1。
答案 (1)2Cu+O =====2CuO、CuO+H SO ===CuSO +H O 生成等量的硫酸
2 2 4 4 2
铜需浓硫酸较多且生成的二氧化硫污染环境
(2)大于
(3)2 mol·L-1
[能 力 练]
12.某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,甲同学认为
产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为
了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示实验装置(锌与浓
硫酸共热时产生的气体为X,且该装置略去),试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为______________________________
___________________________________________________________。
(2)乙同学认为还可能产生氢气的理由是_______________________
_____________________________________________________________。
(3)丙同学在安装好装置后,必须首先进行的一步操作是
______________________________________________________________。
(4)A中加入的试剂可能是________,作用是_______________________________
______________________________________________________________;
B中加入的试剂可能是________,作用是_______________________________
___________________________________________________________;E中加入的试剂可能是________,作用是__________________________________
_______________________________________________________________。
(5)可以证明气体X中含有氢气的实验现象是:
C中:____________,D中:__________________________________________。
如果去掉装置 B,还能否根据 D中的现象判断气体 X中有氢气?________(填
“ 能 ” 或 “ 不 能 ” ) , 原 因 是
______________________________________________
________________________________________________________________。
解析 本题对Zn与浓H SO 反应的产物进行两种推测,而后设计装置进行验证。
2 4
设计时既要验证有无SO 生成,又要验证有无H 生成。验证SO ,可用品红溶液,
2 2 2
验证H 可利用它的还原性,在加热条件下让气体通过CuO,再通过无水硫酸铜,
2
同时必须注意验证H 时,应考虑空气中的水蒸气和从洗气装置中带出的水蒸气
2
对氢气检验的干扰。
答案 (1)Zn+2H SO (浓)=====ZnSO +SO ↑+2H O
2 4 4 2 2
(2)当Zn与浓H SO 反应时,浓H SO 浓度逐渐变稀,Zn与稀H SO 反应可产生
2 4 2 4 2 4
H
2
(3)检查装置的气密性
(4)品红溶液 检验SO 浓H SO 吸收水蒸气 碱石灰 防止空气中水蒸气
2 2 4
进入D中
(5)黑色(CuO)变成红色(Cu) 白色粉末变成蓝色 不能 因为混合气体中含
H O,会干扰H 的检验
2 2
13.SO 是常见的大气污染物,燃煤是产生SO 的主要原因。工业上有多种方法可
2 2
以减少SO 的排放。
2
(1)往煤中添加一些石灰石,可使燃煤过程中产生的SO 转化成硫酸钙。该反应的
2
化学方程式是____________________________________________________
__________________________________________________________。
(2)可用多种溶液做燃煤烟气中SO 的吸收液。
2
①分别用等物质的量浓度的Na SO 溶液和NaOH溶液做吸收液,当生成等物质
2 3
的 量 NaHSO 时 , 两 种 吸 收 液 体 积 比 V(Na SO )∶V(NaOH) =
3 2 3
________________________________________________________________。②NaOH溶液吸收了足量的SO 后会失效,可将这种失效的溶液与一定量的石灰
2
水溶液充分反应后过滤,使 NaOH 溶液再生,再生过程的离子方程式是
______________________________________________________________
___________________________________________________________。
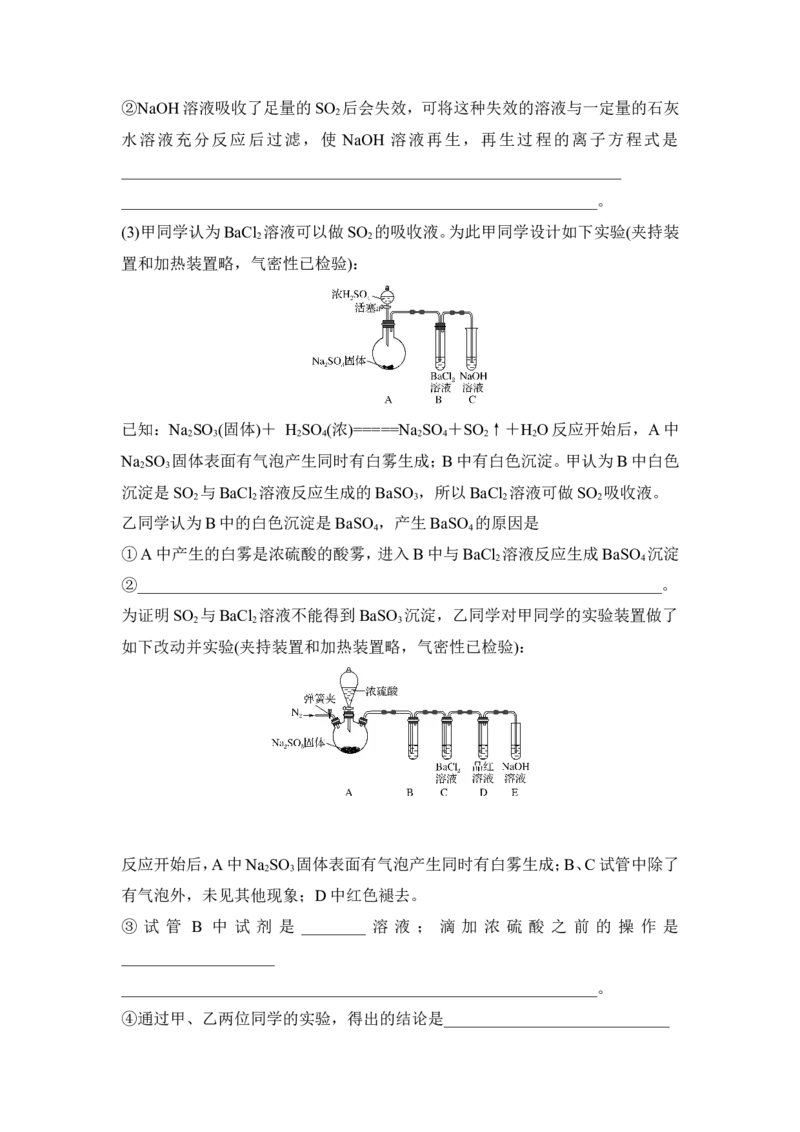
(3)甲同学认为BaCl 溶液可以做SO 的吸收液。为此甲同学设计如下实验(夹持装
2 2
置和加热装置略,气密性已检验):
已知:Na SO (固体)+ H SO (浓)=====Na SO +SO ↑+H O反应开始后,A中
2 3 2 4 2 4 2 2
Na SO 固体表面有气泡产生同时有白雾生成;B中有白色沉淀。甲认为B中白色
2 3
沉淀是SO 与BaCl 溶液反应生成的BaSO ,所以BaCl 溶液可做SO 吸收液。
2 2 3 2 2
乙同学认为B中的白色沉淀是BaSO ,产生BaSO 的原因是
4 4
① A中产生的白雾是浓硫酸的酸雾,进入B中与BaCl 溶液反应生成BaSO 沉淀
2 4
②_________________________________________________________________。
为证明SO 与BaCl 溶液不能得到BaSO 沉淀,乙同学对甲同学的实验装置做了
2 2 3
如下改动并实验(夹持装置和加热装置略,气密性已检验):
反应开始后,A中Na SO 固体表面有气泡产生同时有白雾生成;B、C试管中除了
2 3
有气泡外,未见其他现象;D中红色褪去。
③ 试 管 B 中 试 剂 是 ________ 溶 液 ; 滴 加 浓 硫 酸 之 前 的 操 作 是
___________________
___________________________________________________________。
④通过甲、乙两位同学的实验,得出的结论是__________________________________________________________________________________________。
解析 (1)根据题意,碳酸钙与二氧化硫、氧气在高温条件下反应生成硫酸钙,同
时生成二氧化碳,所以反应的化学方程式为2CaCO +2SO +O =====2CaSO +
3 2 2 4
2CO 。(2)① 假设生成的 NaHSO 物质的量都为 2 mol,Na SO +SO +
2 3 2 3 2
H O===2NaHSO ,吸收的二氧化硫的物质的量为1 mol,需1 mol Na SO ;NaOH
2 3 2 3
+SO ===NaHSO ,吸收的二氧化硫的物质的量为2 mol,需2 mol NaOH,假设
2 3
Na SO 溶液和NaOH溶液的物质的量浓度都为 c mol·L-1,两种吸收液体积比
2 3
V(Na SO )∶V(NaOH)=∶=1∶2。②NaOH溶液吸收了足量的SO 发生反应:
2 3 2
NaOH+SO ===NaHSO ,与一定量的石灰水溶液充分反应 NaHSO +
2 3 3
Ca(OH) ===CaSO ↓+NaOH+H O,离子反应为Ca2++OH-+HSO===CaSO ↓
2 3 2 3
+H O,使NaOH溶液再生。(3)②二氧化硫具有还原性,易被氧气氧化成三氧化
2
硫,三氧化硫与水反应生成硫酸,与BaCl 溶液反应,H SO +BaCl ===BaSO ↓
2 2 4 2 4
+2HCl。③滴加浓硫酸之前打开弹簧夹,通入N ,排出装置中的氧气,然后滴加
2
浓硫酸,Na SO +H SO (浓)===Na SO +SO ↑+H O,A中产生的白雾是浓硫酸
2 3 2 4 2 4 2 2
的酸雾,所以B中的试剂是饱和NaHSO 溶液,除去白雾。④通过甲、乙两位同学
3
的实验,得出的结论是SO 与BaCl 溶液不能得到BaSO 沉淀;不能用BaCl 溶液
2 2 3 2
做吸收SO 的吸收液。
2
答案 (1)2CaCO +2SO +O =====2CaSO +2CO
3 2 2 4 2
(2)① 1∶2 ② Ca2++OH-+HSO===CaSO ↓+H O
3 2
(3)②A 中产生的 SO 与装置内空气中的 O 进入 B 中与 BaCl 溶液反应生成
2 2 2
BaSO 沉淀
4
③饱和NaHSO 打开弹簧夹,通入N ,一段时间后关闭弹簧夹
3 2
④ SO 与BaCl 溶液不能得到BaSO 沉淀;不能用BaCl 溶液做吸收SO 的吸收
2 2 3 2 2
液