文档内容
可能用到的相对原子质量:H-1 O-16 S-32 Zn-65
一、 选择题(每小题只有一个正确答案,请填入下表内,每小题2分,共20分)
1.下列过程主要只涉及物理变化的是( )
A.浓硫酸使白纸变黑 B.石蕊溶液遇到酸溶液变成红色
C.生石灰遇水变成熟石灰 D.活性炭用于净水
2.硫酸二甲酯能与水发生反应,化学方程式为;C H O S+2H O═H SO +2X,则 X 的化学式(
2 6 4 2 2 4
)
A.CH B.CH O C.C H O D.C H O
4 4 2 8 2 8 2
3.(2012年山东滨州)化学中常常出现“1+1≠2”的有趣现象,但也有例外,下列符合“1+
1=2”的事实是( )
4.A.20 ℃,1 L水与1 L酒精混合后的体积等于2 L
B.20 ℃,1 g镁和1 g稀硫酸充分反应后所得的溶液质量为2 g
C.20 ℃,1 g硫粉在1 g氧气中完全燃烧后生成2 g二氧化硫
D.20 ℃,1 g硝酸钾饱和溶液中加入1 g硝酸钾固体能得到2 g硝酸钾溶液.
4.下列物质按单质、氧化物、化合物、混合物的顺序排列的是( )
A.金刚石、生石灰、粗食盐、冰水 B.水银、干冰、熟石灰、天然气
C.苛性钠、铁锈、纯碱、石油 D.硫磺、液态氧、粗食盐、胆矾
5.小科看到妈妈炒的一盘紫色高丽菜(一种紫色的卷心菜)的菜汁呈紫色,后来因为掺了醋
变成了红色,在洗盘子时遇到碱性洗涤剂又变成黄绿色。下列也能使紫色高丽菜汁呈现黄绿
色的物质是( )
A.柠檬汁 B.雪碧 C.食盐水 D.肥皂水
6.H 、CO、C分别与黑色的氧化铜反应,下列叙述中错误的是( )
2
A.反应都需要加热 B.都有红色铜生成
C.都属于置换反应 D.H 、CO、C都具有还原性
2
7.“低碳生活”目前已成为一种生活态度和时尚,指的是生活作息时所耗用的能量要尽量减
少,特别是减少二氧化碳的排放量,减缓生态恶化,下列行为中不符合“低碳生活”的精神的
是( )
A.避免购买不需要的物品,少穿化纤材质的服装 B.使用手绢代替餐巾纸
C.推广无纸化办公,使用再生纸且双面打印文印 D.夏天将空调开的很低
8.分析推理是化学常用的一种学习方法.下列推理正确的是( )
A.分子、原子是不带电的粒子,但不带电的粒子不一定是分子、原子
B.碱能使酚酞试液变红色,所以使酚酞试液变红色的一定是碱
C.酸能使紫色石蕊试液变红色,CO 也能使紫色石蕊试液变红色,所以 CO 是酸
2 2
D.燃烧要同时满足三个条件才能发生,所以灭火也一定要同时控制这三个条件
9.下列除去混合物中少量杂质(括号内为杂质)的方法中,合理的是( )
混合物 方法 选用物质
A.CO(CO ) 吸收 高温的氧化铜
2B.CaCl (HCl) 转化、过滤 过量的碳酸钙
2
C.H Cl(BaCl ) 沉淀、过滤 过量的硫酸铜溶液
2
D.FeSO (CuSO ) 置换、过滤 过量的铁粉
4 4
10.下面是对四个实验绘制的图形,其中实验结果与图形对应准确的是( )
A.图 1 是向一定量稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量
B.图 2 是用 H 还原 CuO 来测定 CuO 中铜元素的含量
2
C.图 3 是向饱和的 NaCl 溶液中不断加水
D.图 4 是用适量的 KClO 和 MnO 混合物加热制 O
3 2 2
二.填空题(每空1分,化学方程式2分,总分34分)
11.(5分)豆腐是人们喜爱的食物,其主要成分如表所示.请回答下列问题:
豆腐的主要成分:每 100g 含有:水 89.30g,蛋白质 4.70g,油脂 1.30,糖类 2.80g,维生
素 B 0.06mg,维生素 B 0.03mg,钙 0.24g,铁 1.40g,其他。
1 2
(1)其中的铁、钙是指
(填序号) .
①分子 ②原子 ③元素
(2)当人体缺钙时,可能引起的疾病是
(填序号) .
①骨质疏松症 ②贫血症 ③夜盲症
(3)豆腐中除了蛋白质、油脂、糖类、无机盐、水之外,还包括的营养物质是
.
(4)豆腐常用塑料袋包装,请指出使用塑料袋包装的利与弊(各答一条)
.
12.(5分)已知下列原子结构示意图:
请在上述元素中选择合适的元素,写出符合要求的化学式
①最轻的气体 . ②相对分子质量最小的氧化物 .
③含有氧元素的酸(只写一种) .④能用于治疗胃酸过多的碱 .
⑤由空气中含量最多的元素,地壳中含量最多的元素和金属元素组成
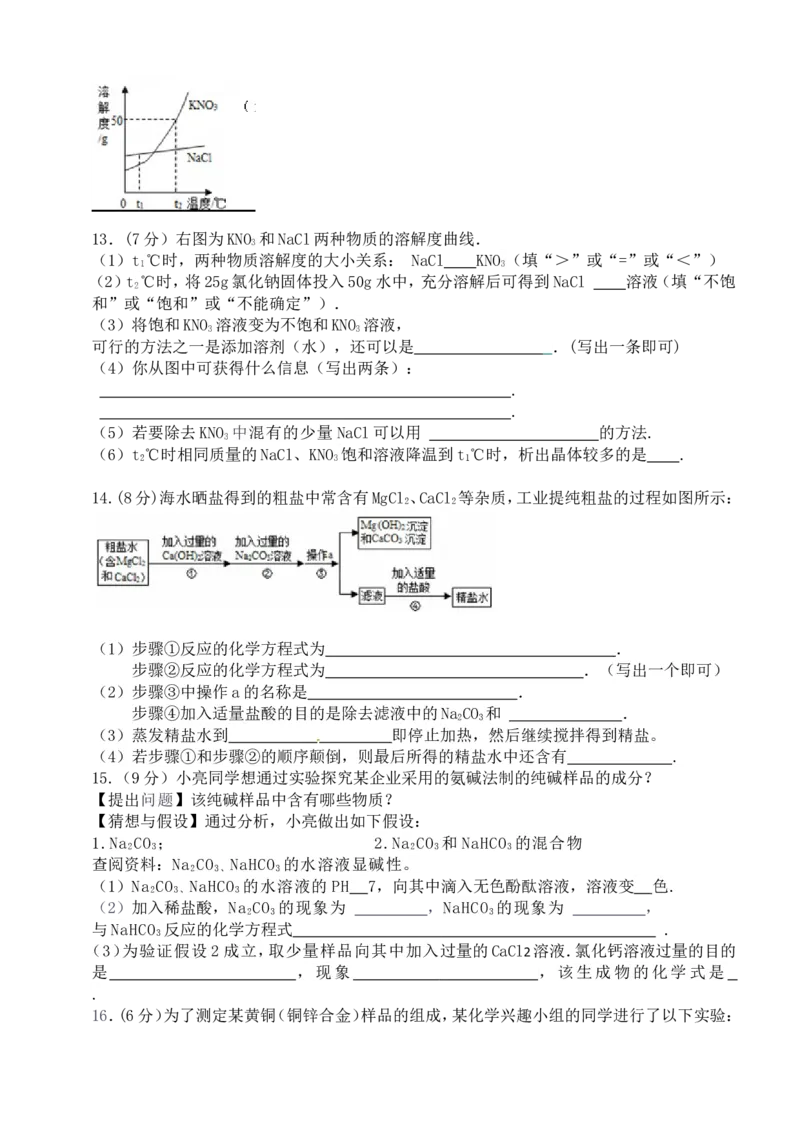
的盐 .13.(7分)右图为KNO 和NaCl两种物质的溶解度曲线.
3
(1)t ℃时,两种物质溶解度的大小关系: NaCl KNO (填“>”或“=”或“<”)
1 3
(2)t ℃时,将25g氯化钠固体投入50g水中,充分溶解后可得到NaCl 溶液(填“不饱
2
和”或“饱和”或“不能确定”).
(3)将饱和KNO 溶液变为不饱和KNO 溶液,
3 3
可行的方法之一是添加溶剂(水),还可以是 .(写出一条即可)
(4)你从图中可获得什么信息(写出两条):
.
.
(5)若要除去KNO 中混有的少量 NaCl可以用 的方法.
3
(6)t ℃时相同质量的NaCl、KNO 饱和溶液降温到t ℃时,析出晶体较多的是 .
2 3 1
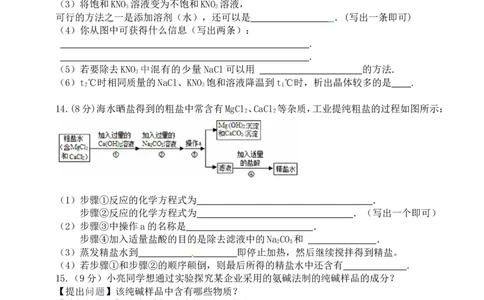
14.(8分)海水晒盐得到的粗盐中常含有MgCl 、CaCl 等杂质,工业提纯粗盐的过程如图所示:
2 2
(1)步骤①反应的化学方程式为 .X kB1.
步骤②反应的化学方程式为 .(写出一个即可)
(2)步骤③中操作a的名称是 .
步骤④加入适量盐酸的目的是除去滤液中的Na CO 和 .
2 3
(3)蒸发精盐水到 即停止加热,然后继续搅拌得到精盐。
(4)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有 .
15.(9分)小亮同学想通过实验探究某企业采用的氨碱法制的纯碱样品的成分?
【提出问题】该纯碱样品中含有哪些物质?
【猜想与假设】通过分析,小亮做出如下假设:
1.Na CO ; 2.Na CO 和 NaHCO 的混合物
2 3 2 3 3
查阅资料:Na CO NaHCO 的水溶液显碱性。
2 3、 3
(1)Na CO NaHCO 的水溶液的 PH 7,向其中滴入无色酚酞溶液,溶液变 色.
2 3、 3
(2)加入稀盐酸,Na CO 的现象为 ,NaHCO 的现象为 ,
2 3 3
与NaHCO 反应的化学方程式 .
3
(3)为验证假设 2 成立,取少量样品向其中加入过量的CaCl 溶液.氯化钙溶液过量的目的
2
是 ,现象 ,该生成物的化学式是
.
16.(6分)为了测定某黄铜(铜锌合金)样品的组成,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平
称量,记录实验数据如下:
试验次序 第1次 第2次 第3次 第4次
所取样品的
质量 50.0 50.0 50.0 50.0
/g
加入稀硫酸
20.0 40.0 60.0 80.0
的质量/g
生成气体的
0.2 0.4 0.5
质量/g
请回答下列问题并计算:
(1)经分析,在第1次实验结束后,反应物 完全反应完了.
(2)50.0g样品与80g稀硫酸反应最多能生成气体 。
(3)计算样品中锌的质量分数(写出具体计算过程)第二学期期中测
化学试卷参考答案
一、选择题:
二、 填空题: