文档内容
第 31 讲 卤族元素
知识导航
知识精讲
一、卤族元素概述
1. 定义
卤族元素为第VIIA族的元素,包括氟(F)、氯(Cl)、溴(Br)、碘(I)、砹(At)。
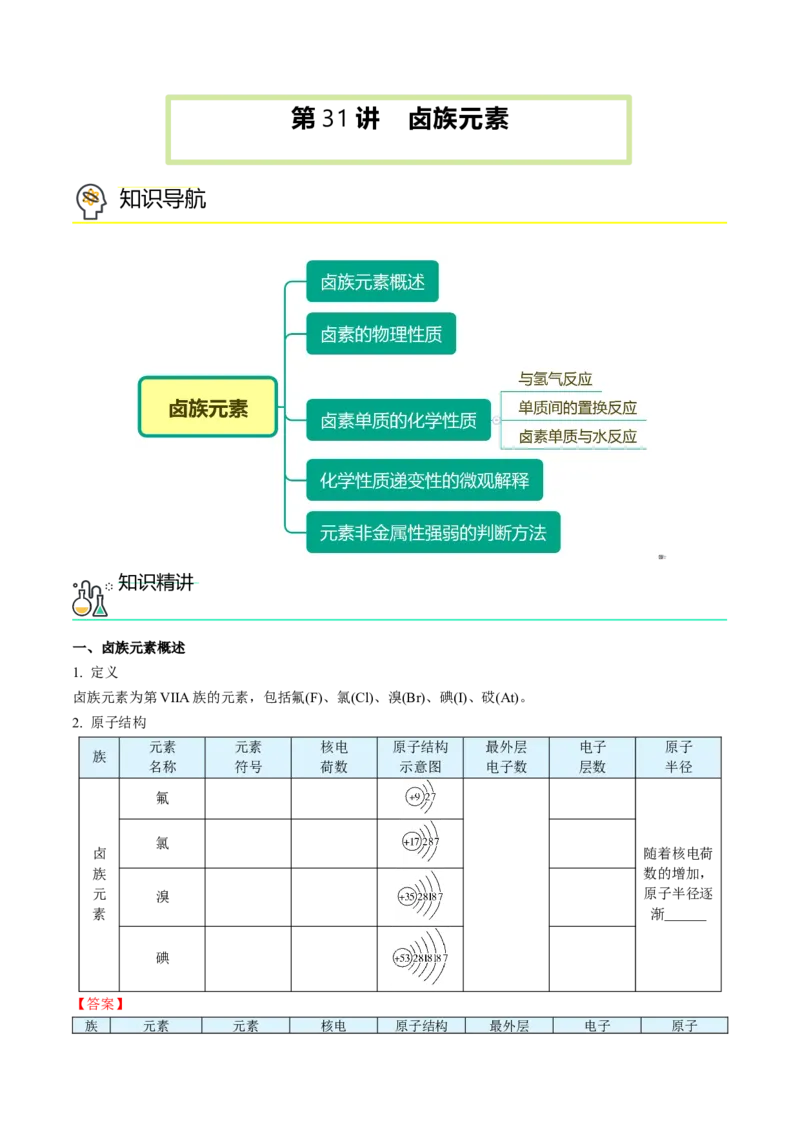
2. 原子结构
元素 元素 核电 原子结构 最外层 电子 原子
族
名称 符号 荷数 示意图 电子数 层数 半径
氟
氯
卤 随着核电荷
族 数的增加,
元 溴 原子半径逐
素 渐______
碘
【答案】
族 元素 元素 核电 原子结构 最外层 电子 原子层数
名称 符号 荷数 示意图 电子数 半径
氟 F 9 2
氯 Cl 17 3
卤 随着核电荷
族 数的增加,
7
元 溴 Br 35 4 原子半径逐
素 渐 增大
碘 I 53 5
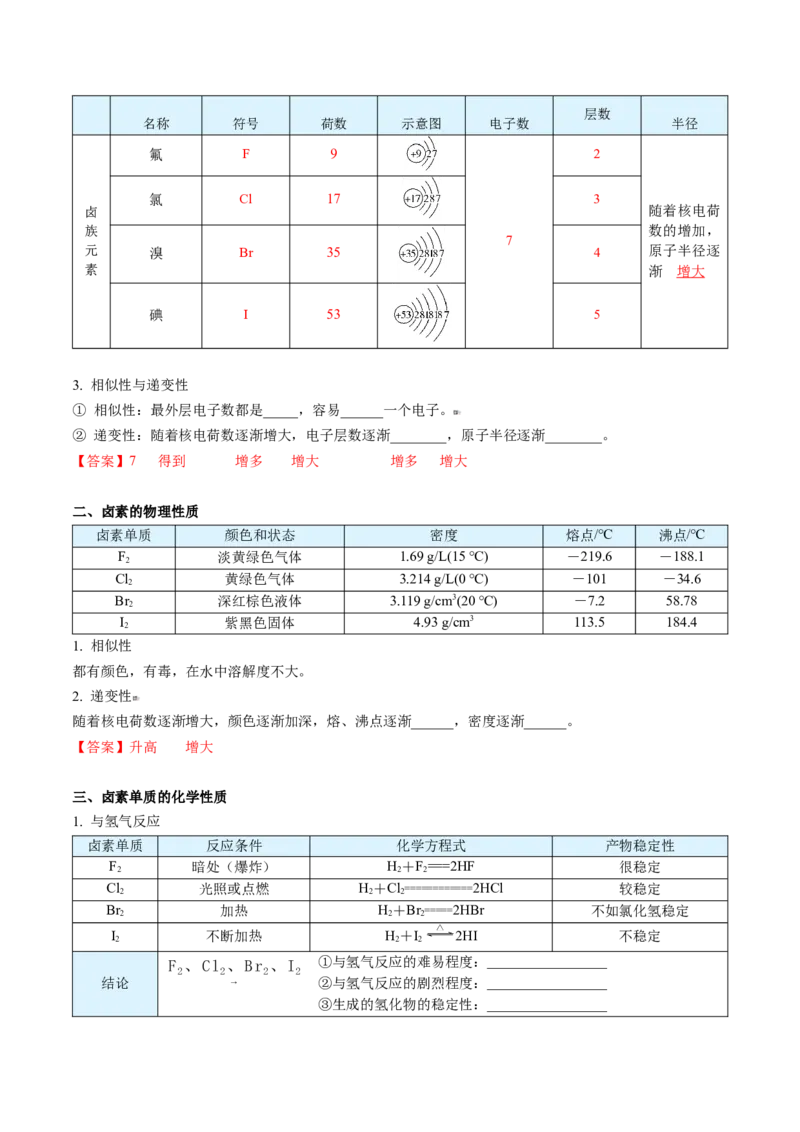
3. 相似性与递变性
① 相似性:最外层电子数都是_____,容易______一个电子。
② 递变性:随着核电荷数逐渐增大,电子层数逐渐________,原子半径逐渐________。
【答案】7 得到 增多 增大 增多 增大
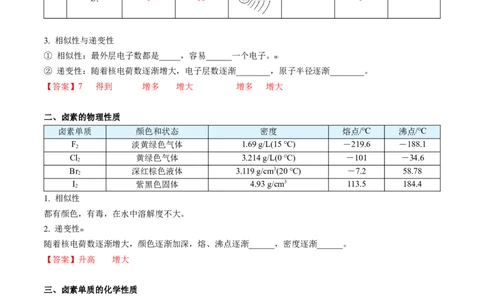
二、卤素的物理性质
卤素单质 颜色和状态 密度 熔点/℃ 沸点/℃
F 淡黄绿色气体 1.69 g/L(15 ℃) -219.6 -188.1
2
Cl 黄绿色气体 3.214 g/L(0 ℃) -101 -34.6
2
Br 深红棕色液体 3.119 g/cm3(20 ℃) -7.2 58.78
2
I 紫黑色固体 4.93 g/cm3 113.5 184.4
2
1. 相似性
都有颜色,有毒,在水中溶解度不大。
2. 递变性
随着核电荷数逐渐增大,颜色逐渐加深,熔、沸点逐渐______,密度逐渐______。
【答案】升高 增大
三、卤素单质的化学性质
1. 与氢气反应
卤素单质 反应条件 化学方程式 产物稳定性
F 暗处(爆炸) H+F===2HF 很稳定
2 2 2
Cl 光照或点燃 H+Cl============2HCl 较稳定
2 2 2
Br 加热 H+Br =====2HBr 不如氯化氢稳定
2 2 2
I 不断加热 H+I 2HI 不稳定
2 2 2
F 、Cl 、Br 、I ①与氢气反应的难易程度:_________________
2 2 2 2
结论 → ②与氢气反应的剧烈程度:_________________
③生成的氢化物的稳定性:_________________④卤素的非金属性强弱:___________________
【答案】越来越困难 越来越不剧烈 越来越不稳定 越来越弱
2. 卤素单质间的置换反应
实验操作 实验现象 实验原理(化学方程式)
将少量氯水滴入盛有KBr溶液
无色变_____色
的试管中,用力振荡试管
将少量氯水滴入盛有KI溶液的
无色变_____色
试管中,用力振荡试管
将少量溴水滴入盛有KI溶液的
无色变_____色
试管中,用力振荡试管
①卤素单质的氧化性顺序由强到弱依次是:____________________
实验结论
②卤素离子的还原性顺序由强到弱依次是:____________________
【答案】橙 Cl+2KBr===2KCl+Br 棕褐 Cl+2KI===2KCl+I 棕黄 Br +2KI===2KBr+I
2 2 2 2 2 2
Cl>Br >I I->Br->Cl-
2 2 2
3. 卤素单质与水反应
① 卤素单质与水发生的反应可用通式表示:X + H O === HX + HXO(X表示Cl、Br、I)
2 2
② F 与水反应的化学方程式为:2F + 2HO === 4HF + O
2 2 2 2
四、卤素化学性质递变性的微观解释
核电荷数减少→电子层数减少→对电子引力增强→越容易得到电子→元素的非金属性增强→单质的氧化性
增强。
五、元素非金属性强弱的判断方法
1. 与H 化合越_______,非金属性越强。
2
2. 与H 生成的气态氢化物越_______,非金属性越强。
2
3. _______氧化物对应水化物的酸性越_____,非金属性越强。
4. 单质氧化性越______或阴离子还原性越______,非金属性越强。
【答案】容易 稳定 最高价 强 强 弱
对点训练
题型一:卤素单质的结构与性质
【例1】(2021·莎车县第一中学高一期中)氯、溴、碘单质的化学性质相似,主要原因是( )A.单质均有颜色 B.均为双原子分子
C.原子最外层电子数均为7 D.均为非金属元素
【答案】C
【解析】A项,单质均有颜色,属于物质的性质,故A不符;B项, 均为双原子分子,属于物质的组成,
故B不符;C项,原子最外层电子数均为7,属于物质结构,结构上有相似,决定了氯、溴、碘单质的化
学性质相似,故C符合;D项, 均为非金属元素,属于物质的组成,故D不符;故选C。
题型二:卤素单质及化合物的性质
【例4】(2021·广东华侨中学高一期中)已知卤素单质的氧化性强弱为F>Cl>Br >I,排在前面的卤素
2 2 2 2
单质可将排在后面的卤素从它的盐溶液中置换出来,如Cl+2NaBr=2NaCl+Br 。下列说法或化学方程式不
2 2
成立的是
A.Cl 与I-在水溶液中不能大量共存
2
B.2NaF+I =2NaI+F
2 2
C.还原性:Cl-<Br-<I-
D.少量Cl 通入到NaBr和NaI的混合溶液中,Cl 优先氧化I-
2 2
【答案】B
【详解】
A.由氧化性:Cl>I 可知,Cl 与I-在水溶液中会发生反应生成I 和Cl-,不能大量共存,A正确;
2 2 2 2
B.由氧化性:F>I 可知,2NaF+I =2NaI+F 不能发生,B错误;
2 2 2 2
C.单质的氧化性越强,对应阴离子的还原性越弱,由氧化性:F>Cl>Br >I 可知,还原性:Cl-<Br-<
2 2 2 2
I-,C正确;
D.少量Cl 通入到NaBr和NaI的混合溶液中,由于还原性:Br-<I-,Cl 优先氧化I-,再氧化Br-,D正确;
2 2
故选B。
【例5】某学生往一支试管里按一定次序分别加入下列几种物质:A.KI溶液 B.淀粉溶液 C.NaOH
溶液 D.氯水,发现溶液颜色按下面次序变化:①无色→②棕黄色→③蓝色→④无色。依据溶液颜色的
变化回答下列问题:
(1)加入以上药品的顺序是___________________________________________________
(2)写出①→②的离子反应方程式:_____________________________________________
(3)写出③→④的化学反应方程式:_____________________________________________
【答案】(1)A、D、B、C
(2)2I-+Cl===I +2Cl-
2 2
(3)3I +6NaOH===5NaI+NaIO +3HO
2 3 2
题型三:类卤化合物/拟卤素的性质
【变6-2】(2021·全国·高三专题练习)BrCl是一种卤素互化物,与Cl 性质相似,也能与水或碱溶液反应。
2
下列说法正确的是A.BrCl与水反应生成HBrO和HCl,该反应属于氧化还原反应
B.1molBrCl与KBr溶液完全反应时转移的电子为1mol
C.BrCl可与Cl 反应得到Br
2 2
D.BrCl与稀氢氧化钠溶液反应可生成NaBr和NaClO
【答案】B
【详解】
A.BrCl+HO =HBrO+HCl,反应中化合价无变化,因此该反应属于非氧化还原反应,故A错误;
2
B.BrCl+KBr=KCl+Br ,BrCl中Br化合价降低1个价态变为Br ,因此1mol BrCl与KBr溶液完全反应
2 2
时转移的电子为1mol,故B正确;
C.Cl 氧化性比BrCl氧化性强,因此BrCl不与Cl 反应,故C错误;
2 2
D.BrCl中Br为+1价,因此BrCl与稀氢氧化钠溶液反应可生成NaCl和NaBrO,故D错误。
综上所述,答案为B。
【变7-1】(2021·全国·高三专题练习)(CN) 、(OCN) 、(SCN) 等化合物的性质与卤素单质相似,称为“类
2 2 2
卤素”。已知卤素单质和“类卤素”的氧化性由强到弱的顺序为:F、(OCN) 、Cl、Br 、(CN) 、(SCN) 、
2 2 2 2 2 2
I。下列叙述正确的是( )
2
A.反应I2SCN-2I-(SCN) 能自发进行
2 2
B.反应Cl2CN-2Cl-(CN) 不能自发进行
2 2
C.还原性:F-OCN-Br-SCN-
D.“类卤素”在碱性溶液中不能发生自身的氧化还原反应
【答案】C
【详解】
在氧化还原反应中,氧化剂的氧化性强于氧化产物;
A.根据I+2SCN-=2I-+(SCN) 可知氧化性I 强于(SCN) ,由信息可知,氧化性(SCN) 强于I,所以该反应
2 2 2 2 2 2
不能自发进行,故A错误;
B.Cl+2CN-=2Cl-+(CN) 可知,氧化性Cl 强于(CN) ,与信息一致,所以该反应可以自发进行,故B错误;
2 2 2 2
C.氧化性越强,则其对应的还原产物的还原性越弱,氧化性由强到弱为F、(OCN) 、Br 、(SCN) ,所以
2 2 2 2
还原性为F- M,说明非金属性N强于M,A
项不选;
B.M原子比N原子容易得到电子,说明非金属性M强于N,B项选;
C.非金属性强弱与氢化物的酸性没有关系,C项不选;
D.H MO 和HNO ,不一定是最高价含氧酸,不能比较非金属性强弱,D项不选;
m x n y
答案选B。
【变8-2】(2021·全国·高一课时练习)下列有关叙述:①非金属单质M能从N的化合物中置换出非金属
单质N;②M原子比N原子容易得到电子;③单质M跟H 反应比N跟H 反应容易得多;④气态氢化物水
2 2
溶液的酸性H M>HN;⑤氧化物对应水化物的酸性H MO>HNO;⑥熔点M>N,能说明M比N的非
m n m x n y
金属性强的是( )
A.①②③ B.②⑤
C.①②③④⑤ D.全部
【答案】A
【详解】
①根据非金属单质间的置换反应可推断M比N的非金属性强,①正确;
②根据得电子的难易程度可以推断M比N的非金属性强,②正确;
③根据单质与H 反应的难易程度可以推断M比N的非金属性强,③正确;
2
④根据气态氢化物水溶液的酸性不能推断M、N的非金属性强弱,如元素的非金属性:O>S,但水为中性
物质,HS的水溶液显酸性,④错误;
2
⑤如果不是元素最高价氧化物对应的水化物的酸性,则不能推断M、N的非金属性强弱,⑤错误;
⑥熔点属于物理性质,其高低与物质化学性质无关,不能用于比较元素非金属性的强弱,⑥错误;
综合分析可知:能够证明元素非金属性强弱的依据是①②③,故合理选项是A。
题型五:卤素的综合实验
【例10】某学生做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关实验现象。
请你帮助该学生整理并完成实验报告。
(1)实验目的:____________________________________________________。
(2)实验用品:仪器:①________;②________(请填写两种主要玻璃仪器)。
药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳。
(3)实验内容:序号 实验方案 实验现象
① 将少量氯水滴入盛有少量NaBr溶液的试管中,振荡; 加入氯水后,溶液由无色变为橙色
② 将少量溴水滴入盛有少量KI溶液的试管中,振荡; 加入溴水后,溶液由无色变为褐色
(4)实验结论:__________________________________________。
(5)问题和讨论:
同一主族元素,自上而下,元素原子的电子层数增多,原子半径________,原子核对最外层电子的吸引力
逐渐________。
【答案】(1)探究同一主族元素性质的递变规律 (2)①试管 ②胶头滴管
(4)同一主族元素,自上而下,元素的非金属性依次减弱 (5)增大减弱
【解析】(1)元素周期律包括同一周期与同一主族性质的变化规律。根据给出的实验药品不难看出,该学生
想以同一主族元素为例,设计实验验证同一主族元素性质的递变规律。(2)本实验属于试管实验,主要使用
试管和胶头滴管。(4)该小题具有一定的开放性,比如:Cl、Br 、I 的氧化性依次减弱或非金属性依次减弱
2 2 2
都可以,但最好与该实验的实验目的相对应:即同一主族元素,自上而下,元素的非金属性依次减弱。(5)
同一主族元素,自上而下,元素原子的电子层数增多,原子半径增大,原子核对最外层电子的吸引力逐渐
减弱。
提分特训
【题1】(2020·云南·陇川县民族中学高二期末)下列化学方程式或离子方程式书写有误的是( )
A.Cl+2I-===I +2CI- B.I+2Br-===Br +2I-
2 2 2 2
C.Cl+2Br-===Br +2Cl- D.Br +HO===HBr+HBrO
2 2 2 2
【答案】B
【详解】
A.由卤素间的置换反应规律可知,氧化性:Cl>I,该离子方程式正确,故A正确;
2 2
B.由卤素间的置换反应规律可知,氧化性:Br >I,该反应不能发生,故B错误;
2 2
C.由卤素间的置换反应规律可知,氧化性:Cl>Br ,该离子方程式正确,故C正确;
2 2
D.由Cl 与水反应进行类推,Br 和水反应生成溴化氢和次溴酸,该离子方程式正确,故D正确。
2 2
故选B。
【题2】(2021·甘肃省武威市民勤县第四中学高一期中)下列不能使湿润的淀粉碘化钾试纸变蓝的是( )
A.氯化钾 B.溴水 C.碘酒 D.氯气
【答案】A
【解析】A项,氯化钾与KI不反应,不存在I,试纸不会变蓝,故A符合题意;B项,溴水有强的氧化性,
2
与KI发生反应:Br +2KI=2KBr+I ,I 遇淀粉溶液变为蓝色,故B不符合题意;C项,碘酒中含有I,I 遇
2 2 2 2 2
淀粉溶液变为蓝色,故C不符合题意;D项,氯气有强的氧化性,与KI发生反应:Cl+2KI=2KCl+I ,I 遇
2 2 2
淀粉溶液变为蓝色,故D不符合题意;故选A。
【题3】(2020·全国·高三专题练习)氰 的化学性质与卤素 很相似,化学上称之为拟卤素,其氧化性介于 和 之间,下列有关反应方程式正确的是
A. 和KCN溶液之间不发生反应
B.向KCN溶液中加入碘水:
C. 和HCN反应: 浓
D.在NaI和KCl混合溶液中通入少量 :
【答案】C
【分析】
氰 的化学性质与卤素 很相似, 和水反应可生成HCN和HCNO; 的氧化性比 弱,
比 强,据此来分析即可。
【详解】
A.氰的氧化性介于 和 之间, 和KCN溶液之间可发生反应生成 和KBr,故A错误;
B.向KCN溶液中加入碘水, 的氧化性比 强:不能发生反应 ,故B错误;
C. 和HCN反应可以类推二氧化锰和浓盐酸的反应,所以反应的化学方程式为:
,故C正确;
D.在NaI和KCl混合溶液中通入少量 ,只能氧化碘离子,离子方程式为 ,故D
错误;
答案选C。
【题4】(2021·黔西南州同源中学高一期末)砹(At)是原子序数最大的卤族元素,对砹及其化合物的叙述,不
正确的是( )
A.与H 化合的能力:At Br >I ,且相对分子质量逐渐增大,氯气可与溴化钾反应生成溴,溴与碘化
2 2 2
钾反应生成碘,因此相对分子质量小的卤素单质可将相对分子质量大的卤素从它的卤化物溶液里置换出来,
故B正确;
C.氯气为黄绿色气体,溴为深红棕色液体,碘为紫黑色固体,且相对分子质量按照Cl、Br 、I 的顺序逐
2 2 2
渐增大,所以卤素单质的颜色随相对分子质量增大而加深,故C正确;
D.非金属性越强,氢化物越稳定;非金属性:Cl>Br>I,所以HX的热稳定性随核电荷数增加而减小,故
D错误;
故选D。
【练3】(2021·广西·平桂高中高一月考)下列关于卤化氢的说法中,不正确的是
A.卤化氢中HF最稳定
B.卤素原子序数越大,卤素单质越难与氢气反应
C.卤素原子序数越大,其氢化物越稳定
D.卤素单质与氢气越难反应,生成的氢化物越不稳定
【答案】C
【详解】
A.卤族元素中,F的非金属性最强,则在卤化氢中HF最稳定,故A正确;
B.卤素原子序数越大,非金属性越弱,卤素单质与氢气越难反应,故B正确;C.卤素原子序数越大,非金属性越弱,其氢化物越不稳定,故C错误;
D.非金属性越弱,卤素单质与氢气越难反应,生成的氢化物越不稳定,故D正确;
故选C。
【练4】(2021·全国·高一课时练习)溴化碘(IBr)的化学性质跟Cl、Br 和I 相似,下列有关溴化碘的叙述
2 2 2
中,错误的是
A.溴化碘通常作氧化剂
B.溴化碘跟水的反应属于氧化还原反应
C.溴化碘跟NaOH溶液反应后生成NaBr、NaIO和水
D.溴化碘能跟多数金属反应生成溴化物及碘化物
【答案】B
【详解】
A.由题给信息可知,溴化碘(IBr)的化学性质跟Cl、Br 和I 相似,而Cl、Br 和I 在反应中通常作氧化剂,
2 2 2 2 2 2
所以溴化碘通常作氧化剂,A正确;
B.溴化碘跟水反应的化学方程式为IBr+H O=HBr+HIO,元素的化合价没有发生改变,属于非氧化还原反
2
应,B错误;
C.溴化碘跟NaOH溶液反应,可认为溴化碘先跟水反应,反应的产物HBr、HIO再跟NaOH反应,所以
最终生成NaBr、NaIO和水,C正确;
D.溴化碘(IBr)的化学性质跟Cl、Br 和I 相似,所以溴化碘能跟多数金属反应,生成溴化物、碘化物等,
2 2 2
D正确;
故选B。
【练5】(2020·安徽·六安一中高一期末)氰 ,硫氰 等称为拟卤素,与卤素单质性质相似,它
们的阴离子与也卤素阴离子性质相似,阴离子的还原性顺序为: ,又知,拟卤
素形成的无氧酸和含氧酸一般为弱酸,下列反应中,不合理的是( )
A. 浓
B.
C.
D.
【答案】B
【分析】
由阴离子的还原性强弱为 ,可知氧化性顺序为 ,
结合氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性以及卤素单质的性质来解答。【详解】
A.浓盐酸可与二氧化锰在加热条件下生成氯气,因还原性Cl-