文档内容
第 35 讲 共价键
知识导航
知识精讲
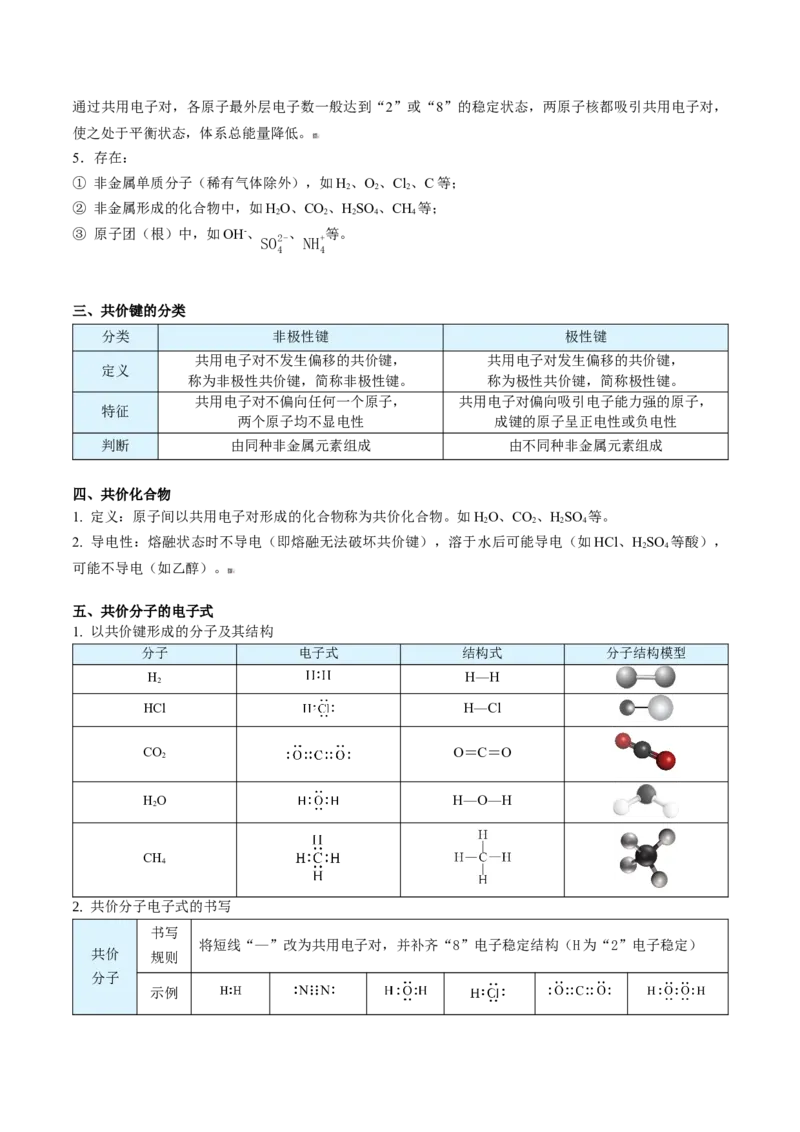
一、Cl、HCl的形成过程
2
过程分析
①氯原子的最外层有7个电子,要达到稳定的8电子结构,需获得1个电子;
Cl
2
②两个Cl原子相互接近时,各提供1个电子,形成共用电子对。
①氢原子、氯原子要达到稳定的电子结构,均需获得1个电子;
HCl ②H原子与Cl原子相互接近时,各提供1个电子,形成共用电子对;
③由于Cl原子对电子的吸引能力更强,共用电子对会偏向Cl原子
二、共价键
1. 定义:原子间通过共用电子对所形成的相互作用叫做共价键。
2.成键粒子:非金属元素的原子(稀有气体除外)。
3.成键实质:共用电子对对两个原子的电性作用。
4.成键原因:通过共用电子对,各原子最外层电子数一般达到“2”或“8”的稳定状态,两原子核都吸引共用电子对,
使之处于平衡状态,体系总能量降低。
5.存在:
① 非金属单质分子(稀有气体除外),如H、O、Cl、C等;
2 2 2
② 非金属形成的化合物中,如HO、CO、HSO 、CH 等;
2 2 2 4 4
③ 原子团(根)中,如OH-、 、 等。
SO2- NH+
4 4
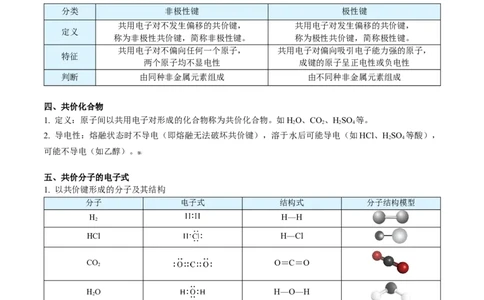
三、共价键的分类
分类 非极性键 极性键
共用电子对不发生偏移的共价键, 共用电子对发生偏移的共价键,
定义
称为非极性共价键,简称非极性键。 称为极性共价键,简称极性键。
共用电子对不偏向任何一个原子, 共用电子对偏向吸引电子能力强的原子,
特征
两个原子均不显电性 成键的原子呈正电性或负电性
判断 由同种非金属元素组成 由不同种非金属元素组成
四、共价化合物
1. 定义:原子间以共用电子对形成的化合物称为共价化合物。如HO、CO、HSO 等。
2 2 2 4
2. 导电性:熔融状态时不导电(即熔融无法破坏共价键),溶于水后可能导电(如HCl、HSO 等酸),
2 4
可能不导电(如乙醇)。
五、共价分子的电子式
1. 以共价键形成的分子及其结构
分子 电子式 结构式 分子结构模型
H H—H
2
HCl H—Cl
CO O=C=O
2
HO H—O—H
2
CH
4
2. 共价分子电子式的书写
书写
将短线“—”改为共用电子对,并补齐“8”电子稳定结构(H为“2”电子稳定)
共价 规则
分子
示例4.用电子式表示共价分子的形成过程
①反应物是原子的电子式; ②生成物是共价化合物的电子式; ③中间用“→”连接。
如: 、 。
六、化学键
1. 概念:使离子相结合或原子相结合的作用力。
2. 形成与分类:
七、化学反应的实质
化学反应的本质是旧化学键的断裂和新化学键的形成过程。
八、分子间作用力
1. 定义:把分子聚集在一起的作用力,叫分子间作用力,又称范德华力。
2. 特点:分子间作用力比化学键弱得多,主要影响物质的熔点、沸点等物理性质。
3. 影响:
一般来说,对于组成和结构相似的物质,相对分子质量越大,范德华力越大,克服范德华力所需消耗的能
量越大,物质的熔、沸点就越高。如:I > Br > Cl > F。
2 2 2 2
4. 氢键
(1)概念:分子间存在的一种比范德华力强的分子间作用力。
(2)形成条件:通常是N、O、F与H形成。
(3)影响:
①氢键会使物质的熔点和沸点升高。因为固体熔化或液体汽化时必须破坏分子间的氢键,消耗较多能量。
②水结成冰,体积增大,跟氢键有关。
③DNA的结构和生理活性都与氢键的作用有关。
对点训练
题型一:共价键、共价化合物的判断
【变1-3】(2021·四川省南充高级中学高二期中)下列各组化合物中,化学键类型完全相同的是
A.HCl和NaOH B.NaO 和Al O C.CO 和CaO D.MgCl 和KS
2 2 2 3 2 2 2
【答案】D【详解】
A.HCl中只有共价键,NaOH中除共价键外还有离子键,选项A不符合;
B.NaO 中除共价键外还有离子键,Al O 中只有离子键,选项B不符合;
2 2 2 3
C.CO 中只有共价键,CaO中只有离子键,选项C不符合;
2
D.MgCl 和KS中只含离子键,选项D符合。
2 2
故选D。
【变2-2】(2021·重庆·西南大学附中高一阶段练习)下列说法中错误的有
①化学键断裂的过程一定是化学变化
②离子化合物中一定含有金属元素
③单质中一定含有非极性共价键
④HCl溶于水电离出H+和Cl-,因此HCl中含有离子键
⑤含有共价键的化合物一定是共价化合物
⑥双原子单质分子中的共价键一定是非极性键
A.3个 B.4个 C.5个 D.6个
【答案】C
【详解】
①化学变化一定有旧化学键的断裂和新化学键的生成,但化学键断裂的过程不一定是化学变化,如氯化钠
溶解的过程中有离子键断裂,但没有新物质产生,不属于化学变化,故①错误;
②离子化合物中不一定含有金属元素,如氯化铵是不含有金属元素的离子化合物,故②错误;
③单质中不一定含有非极性共价键,如稀有气体分子是单原子分子,分子不含有非极性共价键,故③错误;
④氯化氢是共价化合物,不含离子键,溶于水能电离出氢离子和氯离子,故④错误;
⑤含有共价键的化合物不一定是共价化合物,如氢氧化钠是含有离子键和共价键的离子化合物,故⑤错误;
⑥由同种原子组成的双原子分子一定含有非极性共价键,故⑥正确;
综上所述,①②③④⑤错误,故选C。
题型二:电子式的书写
【例3】(2020·全国·高一课时练习)按要求回答下面问题。
(1)N 电子式________、结构式________。
2
(2)CO 电子式________、结构式________。
2
(3)Cl 电子式________、结构式________。
2
(4)CH 电子式________。
4
(5)H O+电子式________。
3
(6)F﹣电子式________。
(7)CaCl 电子式________。
2
【答案】 N≡N O=C=O Cl﹣Cl【详解】
(1)氮气分子中存在氮氮三键,氮原子最外层达到8电子,故N 的电子式为: ;故结构式为N≡N,
2
故答案为: ;N≡N;
(2)二氧化碳是由C与O组成的共价化合物,每个碳原子与两个氧原子各共用两对电子,结构式为O=C=
O,电子式为 ,
故答案为: ;O=C=O;
(3)Cl 为双原子分子,两个氯原子共用一对电子,形成一条共价键,电子式是 ;结构式为Cl﹣Cl,
2
故答案为: ;Cl﹣Cl;
(4)甲烷中C最外层只有4个电子,与4个H形成4对共用电子对,电子式为: ,
故答案为: ;
(5)水合氢离子中O原子还含有一个孤电子对,其电子式为: ,
故答案为: ;
(6)F﹣为阴离子,最外层达到8个电子,电子式 ,
故答案为: ;
(7)氯化钙为离子化合物,由钙离子和氯离子构成,电子式为 ,
故答案为: 。
题型三:8电子稳定结构
【变4】(2021·四川自贡·高二期末)下列分子中所有原子都满足最外层 电子结构的是A. B. C. D.
【答案】D
【详解】
A. 中H为1号元素,核外只有1个电子层K层,H原子与Cl所形成的HCl中Cl最外层满足8电子的
稳定结构而H原子不满足,故A错;
B. 为15号元素,最外层5个电子,Cl为17号元素,最外层由7个电子,则P与5个Cl原子形成5
个共用电子对,则P原子最外层为10电子不满足8电子的稳定结构,故B错;
C. 中B为5号元素,最外层为3个电子,B与3个F原子所形成的3个共用电子对,则B最外层未达
到8电子的稳定结构,故C错;
D. 中S为16号元素,最外层6个电子,F为9号元素,最外层7个电子,1个S原子与2个F原子形
成2个共用电子对,即均满足8电子稳定结构,故D正确;
答案选D。
题型四:微粒间的作用力
【变5-1】(2021·浙江·高二开学考试)下列物质溶于水,既有离子键断裂,又有非极性键断裂的是 A.
NaHSO B.CaH C.NaO D.KSCN
4 2 2 2
【答案】C
【详解】
A.硫酸氢钠电离出钠离子和氢离子和硫酸根离子,有离子键断裂和极性键断裂,A错误;
B.氢化钙溶于水反应生成氢氧化钙和氢气,有离子键断裂和极性键断裂,B错误;
C.过氧化钠和水反应生成氢氧化钠和氧气,有离子键断裂和非极性键断裂,C正确;
D.硫氰化钾溶于水,有离子键断裂,D错误;
故选C。
提分特训
【题1】(2021·云南·弥勒市第二中学高一期中)下列物质中只含有非极性共价键的是
A.C1 B.NaC1 C.HO D.KOH
2 2
【答案】A
【分析】
相同元素原子间的共价键其共用电子对不发生偏移,可判断为非极性共价键。
【详解】A.C1 中只含有Cl-Cl共价键,,A符合题意;
2
B.NaC1只含有离子键,B不符合题意;
C.HO只含有H-O共价键,C不符合题意;
2
D.KOH含有H-O共价键和离子键,D不符合题意;
故选A。
【题2】(2021·浙江·高三阶段练习)含有共价键的正盐的是
A. B. C. D.
【答案】C
【详解】
A. 为氧化物,A不符合题意;
B. 为正盐但不含共价键,B不符合题意;
C. 含有共价键且为正盐,C符合题意;
D. 含有共价键但属于酸式盐,D不符合题意;
故选C。
【题3】(2020·福建·莆田二中高一阶段练习)三氟化氮(NF )常用于微电子工业,可用以下反应制备:
3
4NH +3F =NF+3NHF,下列说法中,正确的是
3 2 3 4
A.NF 的电子式为F:N:F
3
B.在制备NF 的反应中,各物质均为共价化合物
3
C.NH F分子中仅含共价键
4
D.在制备NF 的反应中,NH 表现出还原性
3 3
【答案】D
【详解】
A.NF 中N原子与每个F原子共用一对电子,故其电子式为 ,A错误;
3
B.NH F是由铵根和氟离子形成的离子化合物,B错误;
4
C.NH F中含有铵根和氟离子形成的离子键,C错误;
4
D.该反应中NH 中部分N元素化合价升高为+3价,被氧化,NH 表现出还原性,D正确;
3 3
综上所述答案为D。
【题4】(2021·浙江浙江·高一阶段练习)下列说法正确的是
A.NH Cl属于离子化合物,该物质中只存在离子键
4
B.CO、CH 和HO 分子中只存在极性共价键
2 4 2 2
C.N 和C1 两种分子中,每个原子的最外层都具有8电子稳定结构
2 2D.干冰溶于水生成碳酸的过程只需克服分子间作用力
【答案】C
【详解】
A.NH Cl离子化合物,铵根离子和氯离子之间形成的是离子键,铵根离子中N原子和H原子之间形成的
4
是极性共价键,故A错误;
B.HO 中含有O-H极性键和O-O非极性键,故B错误;
2 2
C.N 和Cl 两种分子,结构式分别为N≡N、Cl-Cl,N最外层5个电子、Cl最外层7个电子,则两种分子
2 2
中每个原子的最外层都具有8电子稳定结构,故C正确;
D.干冰是分子晶体,溶于水生成碳酸,发生化学变化,则共价键破坏,故D错误;
故选:C。
【题7】(2021·全国·模拟预测)W、X、Y、Z是依次增大的短周期元素,W、X构成的一种气态化合物在
同条件下是氢气密度的8倍,Y、Z构成的两种化合物之间可无条件相互转化,根据题意下列说法正确的是
A.原子半径:Z>X>Y>W
B.简单氢化物沸点:Z>X>Y
C.W、Y形成最简化合物的水溶液显酸性
D.W、X与X、Z可构成密度相同的气体
【答案】D
【分析】
W、X构成化合物在同条件下是氢气密度的8倍,相对分子质量为16,即W、X构成的气体为甲烷,即W
为H,X为C;Y、Z构成的化合物可在无条件下相互转化,即NO 与NO,则Y为N、Z为O。
2 2 4
【详解】
A.C、N、O为同一周期元素,原子半径依次减小,A错误;
B.CH 分子间不能形成氢键,沸点最小,水常温下是液体,沸点最高,B错误;
4
C.W、Y形成最简化合物是氨气,其水溶液为氨水,氨水呈碱性,C错误;
D.在相同条件下,由阿伏伽德罗定理的推论可知,相对分子量相同的时候密度相同,CO与C H 相对分
2 4
子质量相同,所以它们可构成密度相同的气体,D正确;
故选D。
【题8】(2021·全国·高一课时练习)写出下列物质的电子式:
HF___________、F___________、HO___________、O ___________、NH ___________、
2 2 2 3
N___________、CH___________。
2 4
【答案】
【详解】
氟化氢是共价化合物,H原子和F原子间为共价键,氟原子最外层7个电子,与1个H原子共用一对电子,
故氟化氢的电子式为: ;氟气是非金属单质气体,F原子和F原子间为共价键,氟原子最外层7个电子,共用一对电子,故氟气的
电子式为: ;
水为共价化合物,氧原子最外层6个电子,分别与2个H原子共用一对电子,故水的电子式为: ;
氧气是非金属单质气体,O原子和O原子间为共价键,氧原子最外层6个电子,共用两对电子,故氧气的
电子式为: ;
氨气是非金属单质气体,N原子和H原子间为共价键,氮原子最外层5个电子,分别与3个H原子共用一
对电子,故氨气的电子式为: ;
氮气是非金属单质气体,N原子和N原子间为共价键,氮原子最外层5个电子,共用三对电子,故氮气的
电子式为: ;
甲烷分子中,C原子与4个H原子分别共用一对电子,形成4个C-H键,故甲烷的电子式为: 。
提分作业
【练1】(2021·浙江·绍兴市柯桥区教师发展中心模拟预测)下列含有共价键的盐是
A.MgCl B.Ba(OH) C.NaSO D.C HOH
2 2 2 4 2 5
【答案】C
【详解】
A.MgCl 属于离子化合物,Mg2+与Cl-通过离子键形成,其电子式为 ,只存在离子键,
2
无共价键,故A不符合题意;
B.Ba(OH) 电离出的阴离子全部是OH-,即Ba(OH) =Ba2++2OH-,属于碱,故B不符合题意;
2 2
C.NaSO 是由金属阳离子(Na+)和酸根离子( )组成,属于盐, 中S原子与O原子形成共价键,故
2 4
C符合题意;
D.C HOH属于有机化合物,不属于盐,故D不符合题意;
2 5
答案为C。
【练2】(2021·河南商丘·高一期末)下列物质中,既含有离子键又含有非极性共价键的是
A. B. C. D.
【答案】D
【详解】A. 是共价化合物,只含极性共价键,A不符合题意;
B. 是共价化合物,含有极性键和非极性共价键,B不符合题意;
C. 是离子化合物,其中铵根离子中含有极性共价键,铵根离子和氯离子之间存在离子键,C不符
合题意;
D.NaO 是离子化合物,钠离子和过氧根离子之间存在离子键,两个氧原子之间存在非极性共价键,D符
2 2
合题意。
综上所述,既含离子键,又含非极性共价键的是选项D。
答案选D。
【练3】(2021·上海市建平中学高一期中)下列各组物质中,化学键类型完全相同的是
A. 和 B. 和 C. 和 D. 和
【答案】B
【分析】
活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,同种非金属元素之间易形
成非极性键,不同非金属元素之间易形成极性键,据此分析解答。
【详解】
A.HI分子中H﹣I原子之间只存在共价键,NaI中钠离子和碘离子之间只存在离子键,所以化学键类型不
同,A错误;
B.硫化氢、二氧化碳分子中都只含共价键,且都是极性键,B正确;
C.氯气分子中Cl﹣Cl原子之间只存在非极性键,He分子中没有化学键,C错误;
D.氟气分子中F﹣F原子之间只存在非极性键,溴化钠中钠离子和溴离子之间只存在离子键,D错误;
故选B。
【练4】(2021·陕西·绥德中学高一阶段练习)下列说法正确的是
A.含有共价键的化合物一定是共价化合物
B.分子中只有共价键的化合物一定是共价化合物
C.离子键就是阴、阳离子间相互吸引
D.只有非金属原子间才能形成共价键
【答案】B
【详解】
A.含有共价键的化合物不一定是共价化合物,例如氢氧化钠,A错误;
B.分子中只有共价键的化合物一定是共价化合物,B正确;
C.离子键是指阴离子,阳离子间通过静电作用形成的化学键,C错误;
D.不一定只有非金属原子间才能形成共价键,例如氯化铝中含有共价键,D错误;答案选B。
【练5】(2021·重庆·高二期中)下列有关化学用语表示正确的是
A. 的结构式:
B. 的电子式:
C. 和 的结构示意图都表示为:
D.用电子式表示 的形成过程:
【答案】C
【详解】
A. 的结构式中 原子之间以单键结合,每个 原子与两个 原子形成共价键,故其结构式为
,故A错误;
B.氯离子是阴离子,应表示出其最外层电子,扩上中括号,标上所带负电荷,则氯化铵的电子式为
,故B错误;
C. 和 的核内均有 个质子,核外均有 个电子,结构简式均为 ,故C正确;
D.相同离子不能合并,用电子式表示氯化镁的形成过程为
,故D错误;
故选
【练7】(2021·上海市洋泾中学高一期中)下列电子式书写正确的是
A. B. C. D.
【答案】C【详解】
A.NaCl为离子化合物,由钠离子与氯离子构成,电子式为: ,故A错误;
B.二氧化碳为共价化合物,其分子中含有两个碳氧双键,二氧化碳正确的电子式为 ,故B错
误;
C.OH-中O与H形成1对共用电子对,O得到1个电子,电子式为 ,故C正确;
D.水是共价化合物,原子间通过共用电子对形成共价键,其正确的电子式为 ,故D错误;
故选:C。
【练9】(2017·甘肃·天水市第一中学高一阶段练习)现有下列物质:①Cl ②NaO ③NaOH ④HCl
2 2 2
⑤HO ⑥MgF ⑦NH Cl
2 2 2 4
(1)只由离子键构成的物质是________(填序号,下同)
(2)只由极性键构成的物质是_________
(3)由极性键和非极性键构成的物质是_______
(4)由离子键和非极性键构成的物质是_______
(5)属于离子化合物的物质是__________
(6)属于共价化合物的物质的是_______
(7)下列变化(填字母)A碘的升华B烧碱熔化C氯化钠溶于水D氯化氢溶于水E氧气溶于水F氯化铵
受热分解,未发生化学键破坏的是_______;仅发生离子键破坏的是_________;仅发生共价键破坏的是
___;
既发生离子键又发货所能共价键破坏的是_________。
【答案】⑥ ④ ⑤ ② ②③⑥⑦ ④⑤ AE BC D F
【详解】
考查化学键与物质类别,①只含非极性键,②含有离子键和非极性键,③含有离子键和极性键,④只含非
极性键,⑤含有极性键和非极性键,⑥只含离子键,⑦含有离子键和极性键,(1)只由离子键构成的物
质是⑥;(2)只由极性键构成的物质是④;(3)由离子键和非极性键构成的物质的⑤;(4)由离子键
和非极性键构成物质是②;(5)属于离子化合物是②③⑥⑦;(6)属于共价化合物的是④⑤;(7)A、
碘升华破坏的是分子间作用力;B、烧碱熔化破坏的是离子键;C、氯化钠溶于水破坏的是离子键;D、氯
化氢溶于水破坏的是极性键;E、氧气溶于水,未破坏化学键;F、NHCl分解破坏的是离子键和共价键,
4
未发生化学键破坏的是AE;只发生离子键破坏的是B和C;只发生共价键破坏的是D;既发生离子键破坏
又发生共价键破坏的是F。
点睛:分子间作用力、氢键不是化学键,这是学生易错的地方,熔化或水溶液中破坏什么作用力,需要判
断属于哪种化合物,从而确定断裂什么作用力。关注更新免费领取,淘宝唯一每月更新店铺:知二教育