文档内容
2021-2022学年高一上学期期末综合测试卷
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共45分)
1.(本题3分)分类是科学研究的重要方法,下列物质分类正确的是
A.碱性氧化物:NaO、Fe O、NaO
2 2 3 2 2
B.同素异形体:石墨、C 、金刚石
60
C.非电解质:乙醇、二氧化碳、氯气
D.碱:苛性钠、纯碱、一水合氨
2.(本题3分)在下列反应类型中,一定属于非氧化还原反应的是
A.分解反应 B.复分解反应 C.置换反应 D.化合反应
3.(本题3分)下列变化必须加入氧化剂才能发生的是
A. B. C. D.
4.(本题3分)化学知识在新冠肺炎疫情防控中发挥着重要作用。新冠病毒直径为60 140nm,下列说法正
确的是 ∼
A.新冠病毒是一种胶体
B.医用酒精不可杀灭新型冠状病毒
C.可用84消毒液直接喷洗双手消毒
D.勤洗手、戴口罩是防止病毒入侵的有效方法
5.(本题3分)下列溶液中离子能大量共存的是
A.使无色酚酞溶液呈红色的溶液中: 、 、 、
B.无色透明的溶液中: 、 、 、
C.含有大量 的溶液中: 、 、 、D.使紫色石蕊溶液呈红色的溶液中: 、 、 、
6.(本题3分)某溶液中含有 、 、 、Na+4种阴离子。向其中加入足量的NaO 固体后,溶液
2 2
中离子浓度变大的是(假设溶液体积无变化)
A. B. C. 、Na+ D. 、
7.(本题3分)下列有关钠及其化合物的说法不正确的是
A.高压钠灯可用于道路照明
B.NaO在空气中加热可得固体NaO
2 2 2
C.NaHCO 的热稳定性比NaCO 强
3 2 3
D.做焰色反应前,铂丝用稀盐酸清洗并灼烧至与原来的火焰颜色相同
8.(本题3分)设N 表示阿伏加德罗常数,下列说法正确的是
A
A.1 mol FeI 与足量的氯气反应时转移的的电子数为2N
2 A
B.常温下,34gNH 含有6N 个N-H共价键
3 A
C.1 mol Na O 中含有的离子总数为4N
2 2 A
D.标准状况下,16g CH 与22.4L H O含有的电子数均为10 N
4 2 A
9.(本题3分)现需要480 mL 0.1 mol/LNaOH溶液,下列选项正确的是
A.需用托盘天平在滤纸上称量药品2.0g
B.必须使用的玻璃仪器有500 mL容量瓶、烧杯、玻璃棒、量筒
C.将溶解后的溶液未冷却至室温立即转入容量瓶,会使所配溶液浓度偏高
D.定容时俯视刻度线会使所配溶液浓度偏低
10.(本题3分)下列化学用语表述正确的是
A.二氧化碳的比例模型: B.HO 的电子式:
2 2
C.氮气分子的结构式:N≡N D.14C的原子结构示意图:11.(本题3分)下列溶液能溶解铁且无新的固体和气体产生的是
A.CuSO 溶液 B.稀硫酸 C.FeCl 溶液 D.AgNO 溶液
4 3 3
12.(本题3分)下列关于元素周期表说法正确的是
A.元素周期表中最外层电子数为2的元素一定在第ⅡA族
B.在过渡元素中找优良催化剂和耐高温、耐腐蚀的合金材料
C.元素所在族序数等于元素原子最外层电子数
D.元素周期表有七个横行,分为七个周期,有18个纵行,分为18个族
13.(本题3分)下列关于铝及其化合物的性质、用途的说法不正确的是
A.铝粉和氢氧化钠混合物可用作下水道疏通剂
B.可用NaOH溶液除去Fe O 粉末中少量的Al O
2 3 2 3
C.铝的氧化膜致密且熔点高,从而能保护内部金属
D.铝制品廉价易得,适用于厨房制作和长期存放各类食物
14.(本题3分)下列关于物质性质变化的比较,正确的是
A.非金属性强弱: C>Si>P
B.原子半径大小: Na > S > O
C.金属性性强弱: Mg > Na> Li
D.还原性强弱: F- > Cl- > I-
15.(本题3分)以下关于锂、钠、钾、铷、铯的叙述正确的是( )
①氢氧化物中碱性最强的是CsOH ②单质熔点最高的是铯 ③它们都是热和电的良导体 ④它们的密度
依次增大,且都比水轻 ⑤它们的还原性依次增强 ⑥它们对应阳离子的氧化性依次增强
A.①③ B.②⑤ C.②④⑥ D.①③⑤
二、填空题(共10分)
16.(本题10分)按要求作答:
Ⅰ.现有以下8种物质:①熔融状态的NaCl、②NO 、③NaHCO 、④铜、⑤AgCl、⑥酒精、⑦NaOH溶
2 3液、⑧FeCl 溶液。
3
(1)上述物质中,属于电解质的是___________。(填序号)
(2)写出③溶于水的电离方程式:___________。
(3)写出③与⑦反应的离子方程式:___________。
Ⅱ.把Cl 通入浓氨水中,发生如下反应:3Cl+8NH=6NHCl+N
2 2 3 4 2
(4)用双线桥表示反应的电子转移方向和数目:___________。
(5)氧化剂与还原剂的分子数之比为:___________
(6)若反应中有6.8g氨发生氧化反应,则反应中生成氮气的质量为___________g.
三、元素或物质推断题(共14分)
17.(本题14分)A~D为核电荷数小于18的元素,其性质或结构信息如下表:
元素 A B C D
性质或 原子核内只有 海水中含量最多,其 其阴离子是构 其原子的M电子层
结构信息 1个质子 原子有2个电子层 成食盐的粒子 上只有1个电子
请根据表中的信息回答下列问题:
(1)四种元素名称为:A______;B______;C______;D________;
(2)B原子的结构示意图:________;
(3)由A、B、D三种元素构成的物质中含有的化学键类型___,写出该物质的电子式:___,写出该物质
在水中的电离方程式_____。D与硫元素形成的化合物水溶液跟单质C的水溶液混合发生置换反应,其离
子方程式为_______。
(4)AC的浓溶液与化合物DCB 的溶液反应生成C的单质,其中的还原反应为_____→_____(用化学式表
3
示),每有1molDCB 参加反应,电子转移______mol。
3
(5)有某AC的浓溶液,密度为1.19g/cm3,质量百分比浓度为36.5%,其物质的量浓度为____。
四、工业流程题(共15分)
18.(本题15分)铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有的少量铝粉,加入某试剂后反应的离子方程式为___________
(2)某同学在实验室用铝土矿(含有 和 ,不考虑其他杂质)取金属铝的流程如下:①操作Ⅰ所加物质a为___________(选填 或NaOH), 与a反应的离子方程式为___________。
②滤液Ⅱ中溶质的用途之一是___________。
③工业上在电解熔融的 时,还加入了冰晶石 作熔剂,其作用是降低 的熔点。冰晶石
在物质的分类中属于___________(填字母)。
a.酸 b.碱 c.盐 d.氧化物
(3)铝与 在酸性或碱性条件下均可反应,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
还原为 ,完善并配平该反应: ,
___________。每消耗 ,转移的电子数目为___________。
(4)已知:CCl 与水不相溶且密度比水大,Cl 的CCl 溶液呈黄绿色,Br 的CCl 溶液呈橙红色,且Br 易从
4 2 4 2 4 2
水溶液中溶入CCl 中。Cl 既能氧化 ,也能氧化 。
4 2
①取 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加
入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl ,振荡后,下层为无色液体。以上实验结
4
论表明还原性: ___________ (填“>”或“<”)。
②若在 溶液中通入标准状况下672mL的Cl,取少量反应后的溶液加入CCl ,振荡后
2 4
下层液体呈___________色,写出该反应的离子方程式___________。
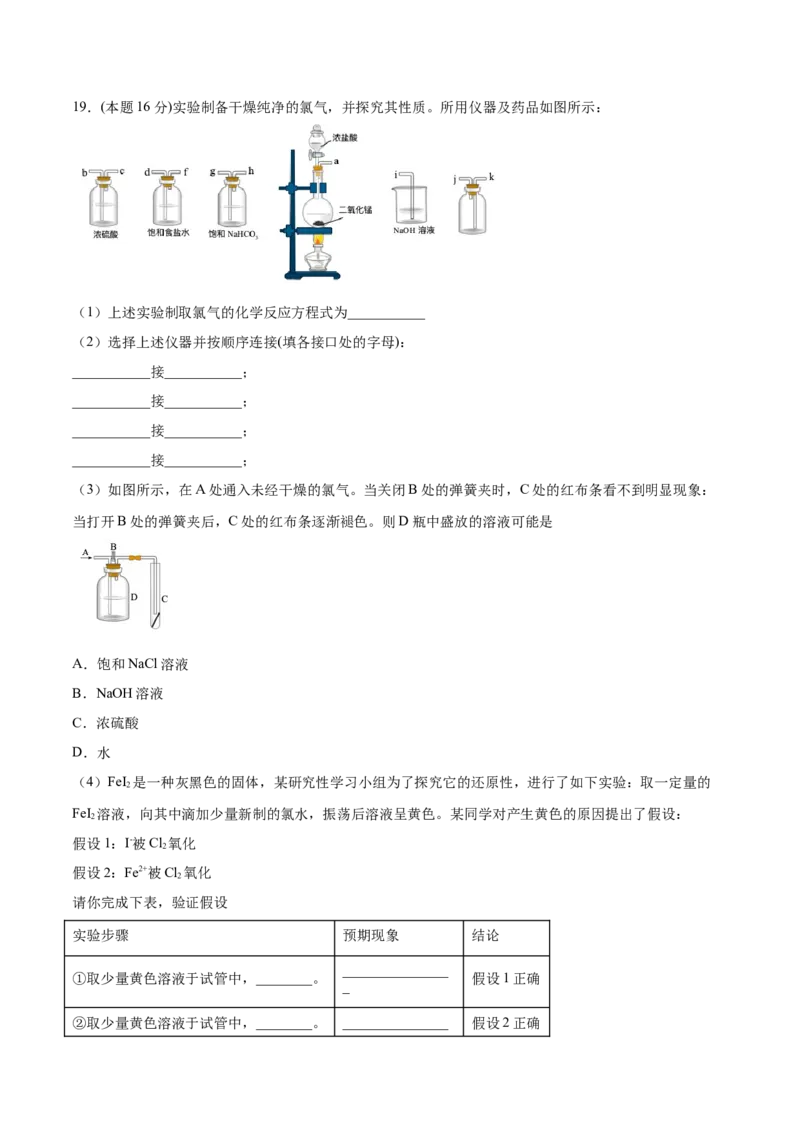
五、实验题(共16分)19.(本题16分)实验制备干燥纯净的氯气,并探究其性质。所用仪器及药品如图所示:
(1)上述实验制取氯气的化学反应方程式为___________
(2)选择上述仪器并按顺序连接(填各接口处的字母):
___________接___________;
___________接___________;
___________接___________;
___________接___________;
(3)如图所示,在A处通入未经干燥的氯气。当关闭B处的弹簧夹时,C处的红布条看不到明显现象:
当打开B处的弹簧夹后,C处的红布条逐渐褪色。则D瓶中盛放的溶液可能是
A.饱和NaCl溶液
B.NaOH溶液
C.浓硫酸
D.水
(4)FeI 是一种灰黑色的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:取一定量的
2
FeI 溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
2
假设1:I-被Cl 氧化
2
假设2:Fe2+被Cl 氧化
2
请你完成下表,验证假设
实验步骤 预期现象 结论
_______________
①取少量黄色溶液于试管中,________。 假设1正确
_
②取少量黄色溶液于试管中,________。 _______________ 假设2正确_关注更新免费领取,淘宝唯一每月更新店铺:知二教育