文档内容
2021-2022学年高一上学期期末综合测试卷
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共45分)
1.(本题3分)分类是科学研究的重要方法,下列物质分类正确的是
A.碱性氧化物:NaO、Fe O、NaO
2 2 3 2 2
B.同素异形体:石墨、C 、金刚石
60
C.非电解质:乙醇、二氧化碳、氯气
D.碱:苛性钠、纯碱、一水合氨
【答案】B
【详解】
A.过氧化钠与水反应生成氢氧化钠和氧气,不是碱性氧化物,故A错误;
B.石墨、C 、金刚石是碳元素的不同单质,属于碳元素的同素异形体,故B正确;
60
C.乙醇,四氯化碳是非电解质,氯气是单质,不是化合物,既不是电解质也不是非电解质,故C错误;
D.纯碱是碳酸钠的俗称,属于盐类,故D错误;
故选:B。
2.(本题3分)在下列反应类型中,一定属于非氧化还原反应的是
A.分解反应 B.复分解反应 C.置换反应 D.化合反应
【答案】B
【详解】
A.分解反应:由一种物质反应生成两种或两种以上新物质的反应,有可能为氧化还原反应,如水分解生
成氧气、氢气,A不符合题意;
B.复分解反应:由两种化合物互相交换成分,生成另外两种化合物的反应,实质是离子的重新组合,不
可能为氧化还原反应,B符合题意;
C.置换反应:是一种单质与一种化合物作用,生成另一种单质与另一种化合物的反应,一定属于氧化还
原反应,C不符合题意;
D.化合反应:指的是由两种或两种以上的物质反应生成一种新物质的反应,有可能为氧化还原反应,如
氢气和氧气化合生成水,D不符合题意;
综上所述答案为B。
3.(本题3分)下列变化必须加入氧化剂才能发生的是A. B. C. D.
【答案】B
【分析】
加入氧化剂才能发生反应,说明反应物发生氧化反应,在反应中化合价要升高。
【详解】
A.Cu2+→Cu ,铜离子得电子,发生还原反应,故A不符合题意;
B.Cl-→Cl,氯离子失去电子,发生氧化反应,故B符合题意;
2
C. ,氯气和水反应生成盐酸和次氯酸,不是必须加入氧化剂才能发生,故C不符合题意;
D. ,碳元素化合价未变,没有发生氧化还原反应,D不符合题意。
故选B。
4.(本题3分)化学知识在新冠肺炎疫情防控中发挥着重要作用。新冠病毒直径为60 140nm,下列说法正
确的是 ∼
A.新冠病毒是一种胶体
B.医用酒精不可杀灭新型冠状病毒
C.可用84消毒液直接喷洗双手消毒
D.勤洗手、戴口罩是防止病毒入侵的有效方法
【答案】D
【详解】
A.分散质粒子直径介于1-100nm之间的分散系为胶体,但新冠病毒不是分散系,故不是胶体,故A错误;
B.医用酒精能杀菌消毒,因此可杀灭新型冠状病毒,故B错误;
C.84消毒液有强氧化性,但不能直接喷洗双手消毒,否则容易腐蚀皮肤,故C错误;
D.勤洗手、戴口罩可以减少传播途径,是防止病毒入侵的有效方法,故D正确。
故选D。
5.(本题3分)下列溶液中离子能大量共存的是
A.使无色酚酞溶液呈红色的溶液中: 、 、 、
B.无色透明的溶液中: 、 、 、
C.含有大量 的溶液中: 、 、 、D.使紫色石蕊溶液呈红色的溶液中: 、 、 、
【答案】C
【详解】
A.使无色酚酞溶液呈红色的溶液为碱性溶液,碱性溶液中 与OH-反应生成氢氧化铁沉淀,不能大量
共存,故A不符合题意;
B.铜离子在溶液中为蓝色,无色透明的溶液中不可能存在铜离子,故B不符合题意;
C.含有大量Ba(NO ) 的溶液中, 、 、 、 互不反应且与硝酸钡均不反应,能大量共存,故
3 2
C符合题意;
D.使紫色石蕊溶液呈红色的溶液为酸性溶液,酸性溶液中碳酸根离子与氢离子反应生成二氧化碳和水,
不能大量共存,故D不符合题意;
故选C。
6.(本题3分)某溶液中含有 、 、 、Na+4种阴离子。向其中加入足量的NaO 固体后,溶液
2 2
中离子浓度变大的是(假设溶液体积无变化)
A. B. C. 、Na+ D. 、
【答案】C
【详解】
向溶液中加入过量的过氧化钠固体,过氧化钠与水反应生成氢氧化钠和氧气,
A.CHCOO-与氢氧根离子和氧气均不反应,离子浓度基本保持不变,选项A错误;
3
B.反应生成的氢氧根离子与碳酸氢根离子反应生成碳酸根和水,溶液中碳酸氢根离子减少,选项B错误;
C.反应生成的氢氧根离子与碳酸氢根离子反应生成碳酸根和水,溶液中碳酸根离子浓度增大,NaO 与水
2 2
反应后Na+浓度也增大,,选项C正确;
D.反应生成的氢氧根离子与碳酸氢根离子反应生成碳酸根和水,溶液中碳酸氢根离子减少, 浓度不
变,选项D错误;
答案选C。
7.(本题3分)下列有关钠及其化合物的说法不正确的是
A.高压钠灯可用于道路照明
B.NaO在空气中加热可得固体NaO
2 2 2C.NaHCO 的热稳定性比NaCO 强
3 2 3
D.做焰色反应前,铂丝用稀盐酸清洗并灼烧至与原来的火焰颜色相同
【答案】C
【详解】
A.高压钠灯发出的黄光射程远、透雾能力强,所以高压钠灯常用于道路照明,故A正确;
B.氧化钠在加热条件下与空气中的氧气反应生成过氧化钠,故B正确;
C.碳酸氢钠受热分解可产生碳酸钠、水和二氧化碳,则稳定性:NaHCO Si>P
B.原子半径大小: Na > S > O
C.金属性性强弱: Mg > Na> Li
D.还原性强弱: F- > Cl- > I-
【答案】B
【详解】
A.同周期从左到右元素非金属性递增,同主族从上到下元素非金属性递减,则非金属性强弱:P >Si,A错误;
B.同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则原子半径大小: Na > S >
O,B正确;
C.同周期从左到右元素金属性递减,同主族从上到下元素金属性递增,则金属性性强弱: Na> Mg,C错
误;
D.同主族从上到下元素非金属性递减,非金属性越强,相应阴离子的还原性越弱,则还原性强弱:I->Cl
-> F-,D错误;
答案选B。
15.(本题3分)以下关于锂、钠、钾、铷、铯的叙述正确的是( )
①氢氧化物中碱性最强的是CsOH ②单质熔点最高的是铯 ③它们都是热和电的良导体 ④它们的密度
依次增大,且都比水轻 ⑤它们的还原性依次增强 ⑥它们对应阳离子的氧化性依次增强
A.①③ B.②⑤ C.②④⑥ D.①③⑤
【答案】D
【详解】
①碱金属从上到下,金属性增强,最高价氧化物对应水化物碱性越强,因此氢氧化物中碱性最强的是
CsOH,故①正确;②从上到下,金属的熔点逐渐降低,因此单质熔点最高的是Li,故②错误;③碱金属
是是热和电的良导体,故③正确;④碱金属密度具有增大趋势,但钠的密度大于钾的密度,铷、铯密度比
水大,故④错误;⑤从上到下金属性增强,它们的还原性依次增强,故⑤正确;⑥从上到下金属性增强,
还原性增强,它们对应阳离子的氧化性依次减弱,故⑥错误;因此①③⑤正确,故D正确。
答案为D。
二、填空题(共10分)
16.(本题10分)按要求作答:
Ⅰ.现有以下8种物质:①熔融状态的NaCl、②NO 、③NaHCO 、④铜、⑤AgCl、⑥酒精、⑦NaOH溶
2 3
液、⑧FeCl 溶液。
3
(1)上述物质中,属于电解质的是___________。(填序号)
(2)写出③溶于水的电离方程式:___________。
(3)写出③与⑦反应的离子方程式:___________。
Ⅱ.把Cl 通入浓氨水中,发生如下反应:3Cl+8NH=6NHCl+N
2 2 3 4 2
(4)用双线桥表示反应的电子转移方向和数目:___________。
(5)氧化剂与还原剂的分子数之比为:___________(6)若反应中有6.8g氨发生氧化反应,则反应中生成氮气的质量为___________g.
【答案】
(1)①③⑤
(2)NaHCO =Na++HCO
3
(3)HCO +OH-=H O+CO
2
(4)
(5)3:2
(6)5.6
【解析】
(1)
①熔融状态的NaCl有自由移动的离子,可以导电,属于电解质;
②NO 自身不能电离出离子而导电,属于非电解质;
2
③NaHCO 属于盐,在水溶液中能导电,属于电解质;
3
④铜为金属单质,既不是电解质,也不是非电解质;
⑤AgCl属于盐,熔融状态下能导电,属于电解质;
⑥酒精在水溶液和熔融状态下均不能导电,属于非电解质;
⑦NaOH溶液属于混合物,既不是电解质,也不是非电解质;
⑧FeCl 溶液属于混合物,既不是电解质,也不是非电解质;
3
综上,属于电解质的是①③⑤。
(2)
NaHCO 属于盐,在水溶液中完全电离生成Na+和 ,电离方程式为:NaHCO =Na++HCO 。
3 3
(3)
NaHCO 和NaOH反应生成NaCO 和HO,反应的离子方程式为:HCO +OH-=H O+CO 。
3 2 3 2 2
(4)
反应3Cl+8NH=6NHCl+N 中,Cl元素的化合价由0价降低至-1价,得到电子被还原,N元素的化合价
2 3 4 2
由-3价升高至0价,失去电子被氧化,故用双线桥表示电子转移方向和数目为:。
(5)
由(4)可知,氧化剂为Cl,还原剂为NH ,但8分子NH 中只有2分子NH 作还原剂,故氧化剂和还原剂的
2 3 3 3
分子数之比为3:2。
(6)
6.8gNH 的物质的量为 ,根据方程式,0.4mol NH 被氧化时,可生成0.2molN,因此生成
3 3 2
氮气的质量为0.2mol×28g/mol=5.6g。
三、元素或物质推断题(共14分)
17.(本题14分)A~D为核电荷数小于18的元素,其性质或结构信息如下表:
元素 A B C D
性质或 原子核内只有 海水中含量最多,其 其阴离子是构 其原子的M电子层
结构信息 1个质子 原子有2个电子层 成食盐的粒子 上只有1个电子
请根据表中的信息回答下列问题:
(1)四种元素名称为:A______;B______;C______;D________;
(2)B原子的结构示意图:________;
(3)由A、B、D三种元素构成的物质中含有的化学键类型___,写出该物质的电子式:___,写出该物质
在水中的电离方程式_____。D与硫元素形成的化合物水溶液跟单质C的水溶液混合发生置换反应,其离
子方程式为_______。
(4)AC的浓溶液与化合物DCB 的溶液反应生成C的单质,其中的还原反应为_____→_____(用化学式表
3
示),每有1molDCB 参加反应,电子转移______mol。
3
(5)有某AC的浓溶液,密度为1.19g/cm3,质量百分比浓度为36.5%,其物质的量浓度为____。
【答案】
(1) 氢 氧 氯 钠
(2)(3) 离子键和共价键 NaOH=Na++OH- Cl+S2-=2Cl-+S↓
2
(4) NaClO Cl 5
3 2
(5)11.9mol/L
【分析】
A:原子核内只有1个质子,则为氢元素;
B:海水中含量最多,其原子有2个电子层,则为水中的氧元素;
C:其阴离子是构成食盐的粒子,为氯离子,则C为氯元素;
D:其原子的M电子层上只有1个电子,则各电子层中电子数为2、8、1,为钠元素;
(1)
根据上述分析可知,四种元素的名称分别为氢、氧、氯、钠;
(2)
B为氧,原子的结构示意图为 ;
(3)
由A、B、D三种元素构成的物质NaOH中含有的化学键类型离子键、极性共价键;
NaOH的电子式为 ;
NaOH在水中的电离方程式为NaOH=Na++OH-;
D与硫元素形成的化合物NaS水溶液跟单质C(Cl)的水溶液混合发生置换反应生成硫和氯化钠,其离子
2 2
方程式为Cl+S2-=2Cl-+S↓;
2
(4)
AC的浓溶液浓盐酸与化合物NaClO 的溶液反应生成C的单质氯气,其中氯元素由+5价降为0价,发生的
3
还原反应为NaClO→Cl,每有1mol NaClO 参加反应,电子转移5mol;
3 2 3
(5)
有某AC的浓溶液,密度为1.19g/cm3,质量百分比浓度为36.5%,其物质的量浓度为c= =
=11.9mol/L。
四、工业流程题(共15分)
18.(本题15分)铝和铝合金是一类重要的金属材料。回答下列问题:(1)除去镁粉中混有的少量铝粉,加入某试剂后反应的离子方程式为___________
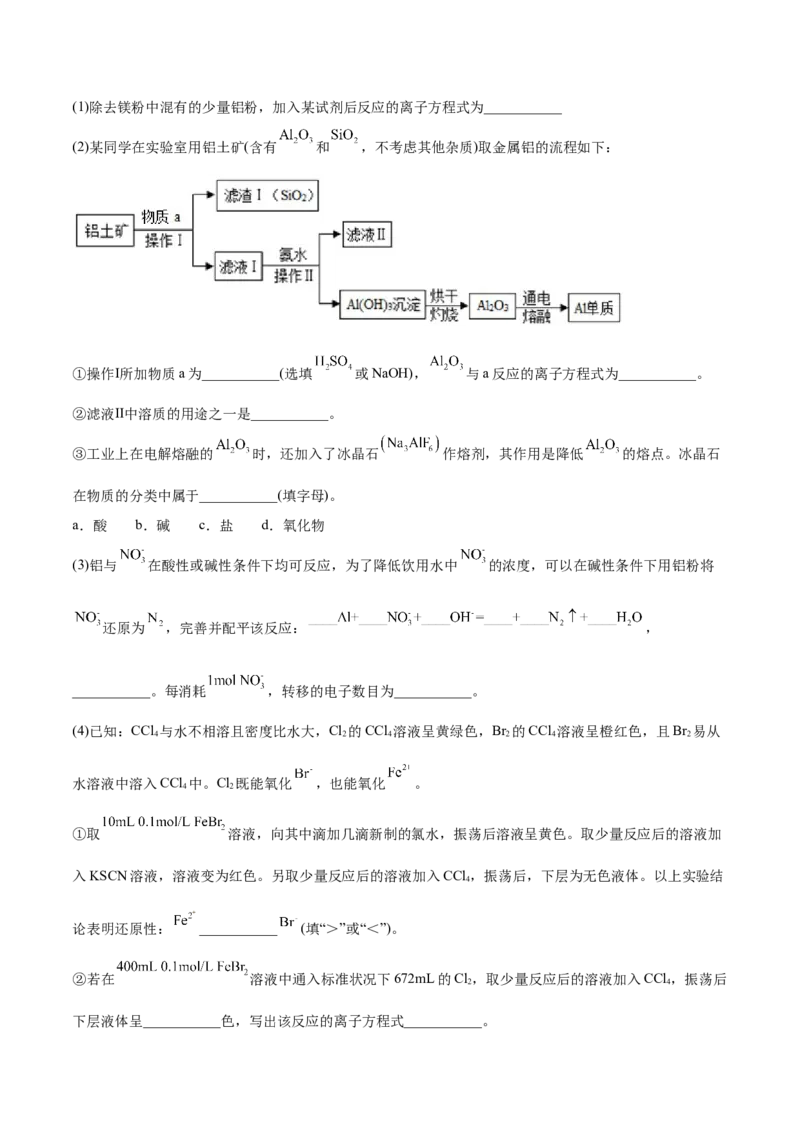
(2)某同学在实验室用铝土矿(含有 和 ,不考虑其他杂质)取金属铝的流程如下:
①操作Ⅰ所加物质a为___________(选填 或NaOH), 与a反应的离子方程式为___________。
②滤液Ⅱ中溶质的用途之一是___________。
③工业上在电解熔融的 时,还加入了冰晶石 作熔剂,其作用是降低 的熔点。冰晶石
在物质的分类中属于___________(填字母)。
a.酸 b.碱 c.盐 d.氧化物
(3)铝与 在酸性或碱性条件下均可反应,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
还原为 ,完善并配平该反应: ,
___________。每消耗 ,转移的电子数目为___________。
(4)已知:CCl 与水不相溶且密度比水大,Cl 的CCl 溶液呈黄绿色,Br 的CCl 溶液呈橙红色,且Br 易从
4 2 4 2 4 2
水溶液中溶入CCl 中。Cl 既能氧化 ,也能氧化 。
4 2
①取 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加
入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl ,振荡后,下层为无色液体。以上实验结
4
论表明还原性: ___________ (填“>”或“<”)。
②若在 溶液中通入标准状况下672mL的Cl,取少量反应后的溶液加入CCl ,振荡后
2 4
下层液体呈___________色,写出该反应的离子方程式___________。【答案】2Al+2OH -+2H O=2AlO + 3H ↑ 制氮肥 c
2 2
5N > 橙红
A
【分析】
铝土矿(含有Al O 和SiO,不考虑其他杂质)加入物质a,过滤得到滤渣(二氧化硅)和滤液,说明a与二氧
2 3 2
化硅不反应,因此a选硫酸,滤液I中主要含有硫酸铝,向滤液中加入氨水,反应生成氢氧化铝沉淀,过
滤分离,滤液Ⅱ中主要含有硫酸铵,氢氧化铝烘干、灼烧分解生成氧化铝,电解熔融氧化铝生成铝单质与
氧气;铝与碱反应生成偏铝酸盐,结合氧化还原反应的规律分析解答;根据实验现象结合题示信息分析解
答。
【详解】
(1)铝能够与氢氧化钠溶液反应,而镁不能,因此除去镁粉中混有的少量铝粉,可以加入氢氧化钠溶液,反
应的离子方程式为2Al + 2OH -+2H O=2AlO + 3H ↑,故答案为:2Al + 2OH -+2H O=2AlO + 3H ↑;
2 2 2 2
(2)①根据流程图,加入物质a,过滤得到滤渣(二氧化硅)和滤液,说明a与二氧化硅不反应,因此a选硫酸,
与硫酸反应的离子方程式为 ,故答案为: ; ;
②滤液Ⅱ中的溶质的硫酸铵,可以用作氮肥,故答案为:制氮肥;
③冰晶石(Na AlF)属于盐,故答案为:c;
3 6
(3)反应物为:铝、NO 、OH-,生成物为:N、HO,碱性条件下铝参加反应生成物还有AlO 。反应中
2 2
Al→AlO ,Al元素化合价由0价升高为+3价,共升高3价,NO →N↑,氮元素化合价由+5价降低为0价,
2
共降低10价,化合价升降的最小公倍数为30,故Al的系数为10,N 系数为3,由氮元素守恒可知系数为
2
6,由Al元素守恒可知系数为10,由电荷守恒可知OH-系数为4,由H元素守恒可知HO前面的系数为
2
2,故配平后的离子方程式为10Al+6NO +4OH-=10AlO +3N ↑+2H O;NO →N↑,氮元素化合价由+5价
2 2 2
降低为0价,每转移5mol电子会消耗1mol NO ,即每消耗1mol NO ,转移的电子数目为5N ,故答案为:
A
10Al+6NO +4OH-=10AlO +3N ↑+2H O;5N ;
2 2 A(4)①FeBr 溶液中滴加几滴新制的氯水,振荡后溶液呈黄色,取少量反应后的溶液加入KSCN溶液,溶液
2
变为血红色。另取少量反应后的溶液加入CCl ,振荡后,下层为无色液体,可知Fe2+被氧化为Fe3+,而Br-
4
未被氧化,因此还原性:Fe2+>Br-,故答案为:>;
②n(FeBr)=0.4L×0.1mol/L=0.04mol,n(Cl )= =0.03mol,因为还原性:Fe2+>Br-,氯气首先氧化
2 2
Fe2+,2Fe2+ + Cl =2Fe3+ + 2Cl-,Fe2+完全被氧化,消耗氯气0.02mol,剩余的0.01mol氯气再氧化Br-,Cl +
2 2
2Br-=2Cl-+ Br,0.01mol氯气能够氧化0.02mol Br-,因此总反应为3Cl+4Fe2++2Br-=4Fe3++Br +6Cl-,生成溴
2 2 2
易溶于四氯化碳,取少量反应后的溶液加入CCl ,振荡后下层液体呈橙红色,故答案为:橙红;
4
3Cl+4Fe2++2Br-=4Fe3++Br +6Cl-。
2 2
五、实验题(共16分)
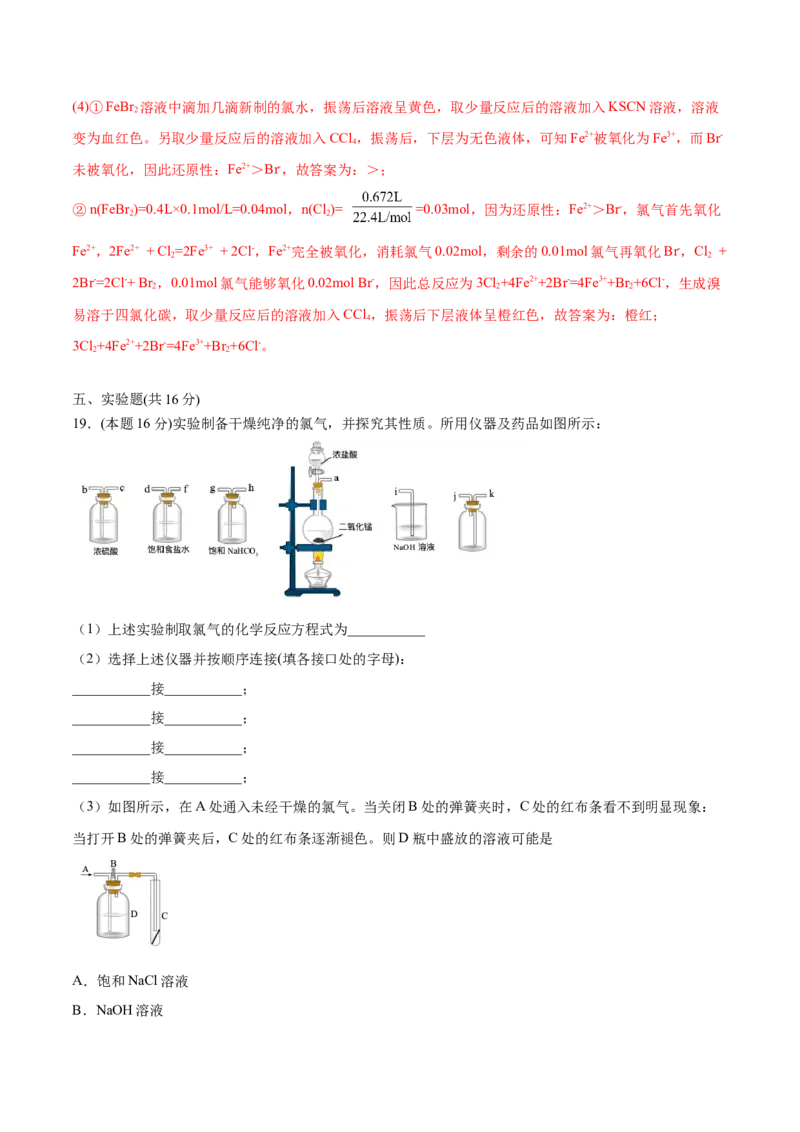
19.(本题16分)实验制备干燥纯净的氯气,并探究其性质。所用仪器及药品如图所示:
(1)上述实验制取氯气的化学反应方程式为___________
(2)选择上述仪器并按顺序连接(填各接口处的字母):
___________接___________;
___________接___________;
___________接___________;
___________接___________;
(3)如图所示,在A处通入未经干燥的氯气。当关闭B处的弹簧夹时,C处的红布条看不到明显现象:
当打开B处的弹簧夹后,C处的红布条逐渐褪色。则D瓶中盛放的溶液可能是
A.饱和NaCl溶液
B.NaOH溶液C.浓硫酸
D.水
(4)FeI 是一种灰黑色的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:取一定量的
2
FeI 溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
2
假设1:I-被Cl 氧化
2
假设2:Fe2+被Cl 氧化
2
请你完成下表,验证假设
实验步骤 预期现象 结论
_______________
①取少量黄色溶液于试管中,________。 假设1正确
_
_______________
②取少量黄色溶液于试管中,________。 假设2正确
_
【答案】
(1)
(2) ad fb ck ji
(3)C
(4) 淀粉溶液 溶液变成蓝色 KSCN溶液 出现血红色
【解析】
(1)
图示可知,是用浓盐酸与二氧化锰加热下反应生成氯气,化学反应方程式为
。
(2)
依题意需制取干燥纯净氯气并探究其性质,a出来的氯气带有HCl,经饱和食盐水除去后,用浓硫酸干燥
即得干燥纯净氯气,用向上排空气法收集观察其颜色,尾气用NaOH溶液处理。故圆底烧瓶接饱和食盐水:
ad,饱和食盐水接浓硫酸:fb,浓硫酸接收集装置:ck,收集装置接氢氧化钠溶液:ji。
(3)
分析题中信息,D瓶的作用是使湿润的氯气得到干燥,故选用浓硫酸,答案选C。
(4)
I-被Cl 氧化生成I,可使淀粉溶液变蓝,得到检验;Fe2+被Cl 氧化生成Fe3+,使KSCN溶液变血红色,得
2 2 2到检验。关注更新免费领取,淘宝唯一每月更新店铺:知二教育