文档内容
1.下列有关铁的化学反应的叙述正确的是( )
A.室温下,过量Fe与浓硫酸反应生成FeSO
4
B.铁钉置于稀硫酸中,表面产生大量气泡,溶液由无色变蓝色
C.高温下,铁与水蒸气反应有Fe O 生成
3 4
D.高温下,铁粉与氧化铝粉末反应生成单质铝
2.下列对铁元素的认识正确的是( )
A.铁有两种不溶于水的氢氧化物
B.铁在自然界中不存在单质形态
C.铁元素是地壳中含量最多的金属元素
D.自然界存在的铁元素均显+3价
3.下列关于氧化铁、氧化亚铁、四氧化三铁三种氧化物的说法不正确的是( )
A.铁元素的化合价不完全相同
B.氧元素的化合价完全相同
C.氧化亚铁俗称铁红,为红棕色固体
D.铁在氧气中燃烧的产物为黑色固体
4.某同学设计的制备氯化铁溶液的方案中,分别采用下列物品,其中能实现的是( )
A.氢氧化铁和硫酸 B.铁和盐酸
C.氧化亚铁和盐酸 D.氧化铁和盐酸
5.实验室用FeCl 溶液和烧碱制备Fe(OH) ,为使生成的产物不被氧化,下列采取的措施错
2 2
误的是( )
A.配制FeCl 溶液和烧碱溶液所用的蒸馏水要煮沸
2
B.可在FeCl 溶液的上面加一层苯,以隔绝空气
2
C.向FeCl 溶液中滴加烧碱溶液时,胶头滴管尖嘴不能伸入试管中
2
D.产生Fe(OH) 沉淀后,不能振荡试管
2
6.根据Fe(OH) 的物质类别和元素化合价推测,下列物质不与其反应的是(不考虑溶解氧)(
3
)
A.潮湿的空气 B.盐酸
C.新制氯水 D.烧碱溶液
7.(2023·长春模拟)某黑色粉末可能是Fe O 或Fe O 与FeO的混合物,为进一步确认该黑色
3 4 3 4
粉末的成分,下列实验方案不可行的是( )
A.准确称量一定质量的黑色粉末,用H 充分还原,并用干燥剂收集所得水,获得水的准
2
确质量,进行计算
B.准确称量一定质量的黑色粉末,溶解于足量盐酸,加热蒸干溶液并在空气中灼烧至质量不变,称量所得粉末质量,进行计算
C.准确称量一定质量的黑色粉末,用CO充分还原,在CO气流中冷却后准确称量剩余固
体的质量,计算
D.准确称量一定质量的黑色粉末,与一定量铝粉混合后点燃,充分反应后冷却,准确称量
剩余固体质量,进行计算
8.混合下列各组物质使之充分反应,加热蒸干产物并在 300 ℃下灼烧至质量不变,最终残
留固体不是纯净物的是( )
A.向红褐色的Fe(OH) 固体中加入过量盐酸
3
B.等物质的量浓度、等体积的(NH )SO 与BaCl 溶液
4 2 4 2
C.等物质的量的NaHCO 与NaO 固体溶于水
3 2 2
D.向NaBr溶液中通入过量氯气
9.废铁屑制Fe O 的一种流程如图:
2 3
下列说法不正确的是( )
A.热的纯碱溶液可去除废铁屑表面的油污
B.操作a是萃取
C.冰水既可洗去杂质又可减少固体的溶解
D.Fe O 可用作红色颜料
2 3
10.如图所示装置,可用以制取Fe(OH) 且观察其在空气中被氧化时颜色的变化。下列说法
2
错误的是( )
A.实验前,应先煮沸溶液除去溶解氧
B.装置Ⅰ可制取FeSO 溶液并排尽装置内空气
4
C.关闭止水夹可观察到装置Ⅱ中溶液进入装置Ⅰ中
D.取下装置Ⅱ的橡皮塞可观察沉淀颜色变化
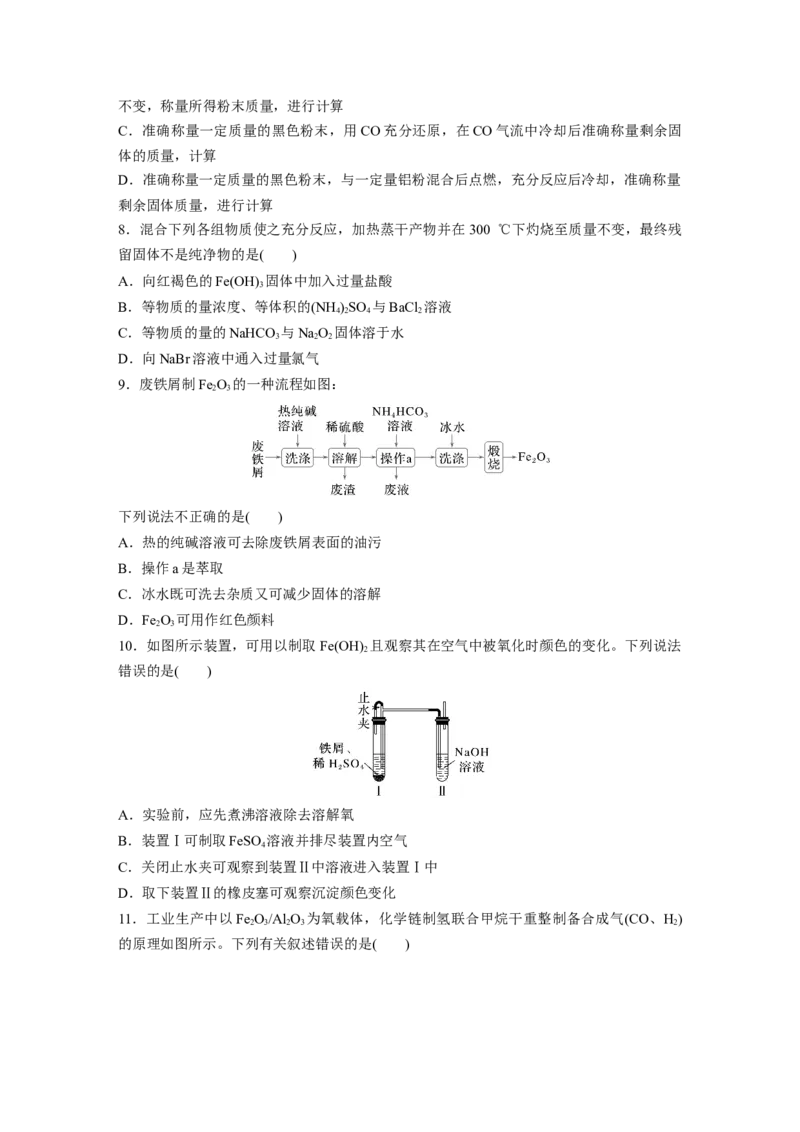
11.工业生产中以Fe O/Al O 为氧载体,化学链制氢联合甲烷干重整制备合成气(CO、H)
2 3 2 3 2
的原理如图所示。下列有关叙述错误的是( )A.M为Fe O
3 4
B.“干重整”时,装置中可能出现积碳
C.“氧化Ⅱ”中发生的主要反应是2Fe(OH) =====Fe O+3HO
3 2 3 2
D.该过程能有效实现温室气体(CH、CO)的回收利用
4 2
12.已知:普通铁+水蒸气―――→铁的氧化物+氢气,铁的氧化物+氢气―――→“引火铁”+
水蒸气,“引火铁”为颗粒很细、反应活性很高的铁粉。某实验小组使用普通铁粉、20%的
盐酸及其他试剂制备“引火铁”,装置(铁架台、铁夹、铁网、陶土网、加热仪器等略去)如
图所示。
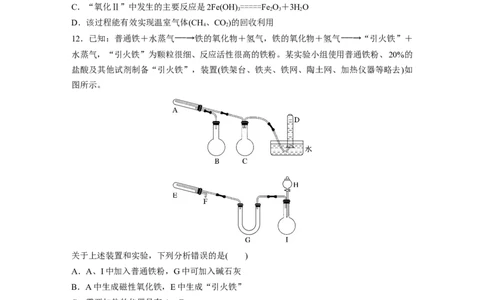
关于上述装置和实验,下列分析错误的是( )
A.A、I中加入普通铁粉,G中可加入碱石灰
B.A中生成磁性氧化铁,E中生成“引火铁”
C.需要加热的仪器只有A、E
D.D用于收集氢气
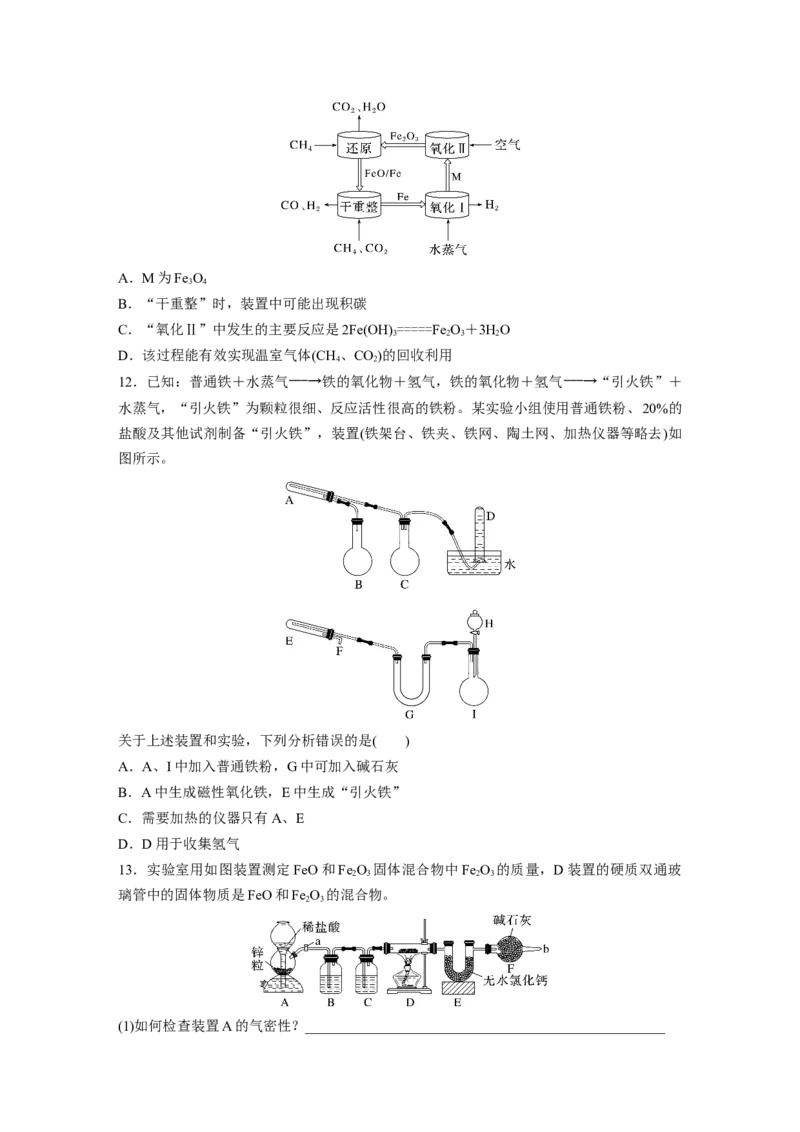
13.实验室用如图装置测定FeO和Fe O 固体混合物中Fe O 的质量,D装置的硬质双通玻
2 3 2 3
璃管中的固体物质是FeO和Fe O 的混合物。
2 3
(1)如何检查装置A的气密性?_________________________________________________________________________________________________________________________________。
(2)为了安全,在点燃D处的酒精灯之前,必须进行的操作是__________________________
______________________________________________________________________________。
(3)装置B的作用是______________________。装置C中装的液体是__________,所起的作
用是____________。
(4)点燃 D 处的酒精灯,写出在硬质双通玻璃管中发生反应的化学方程式:
________________
______________________________________________________________________________。
(5)若FeO和Fe O 固体混合物的质量为23.2 g,反应完全后U形管的质量增加7.2 g,则混合
2 3
物中Fe O 的质量为____________。
2 3
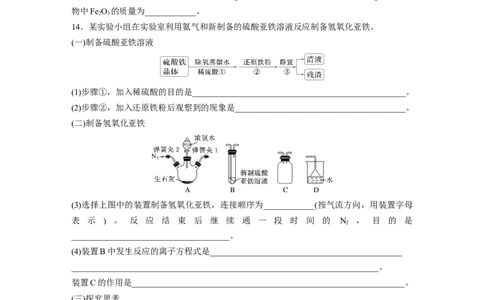
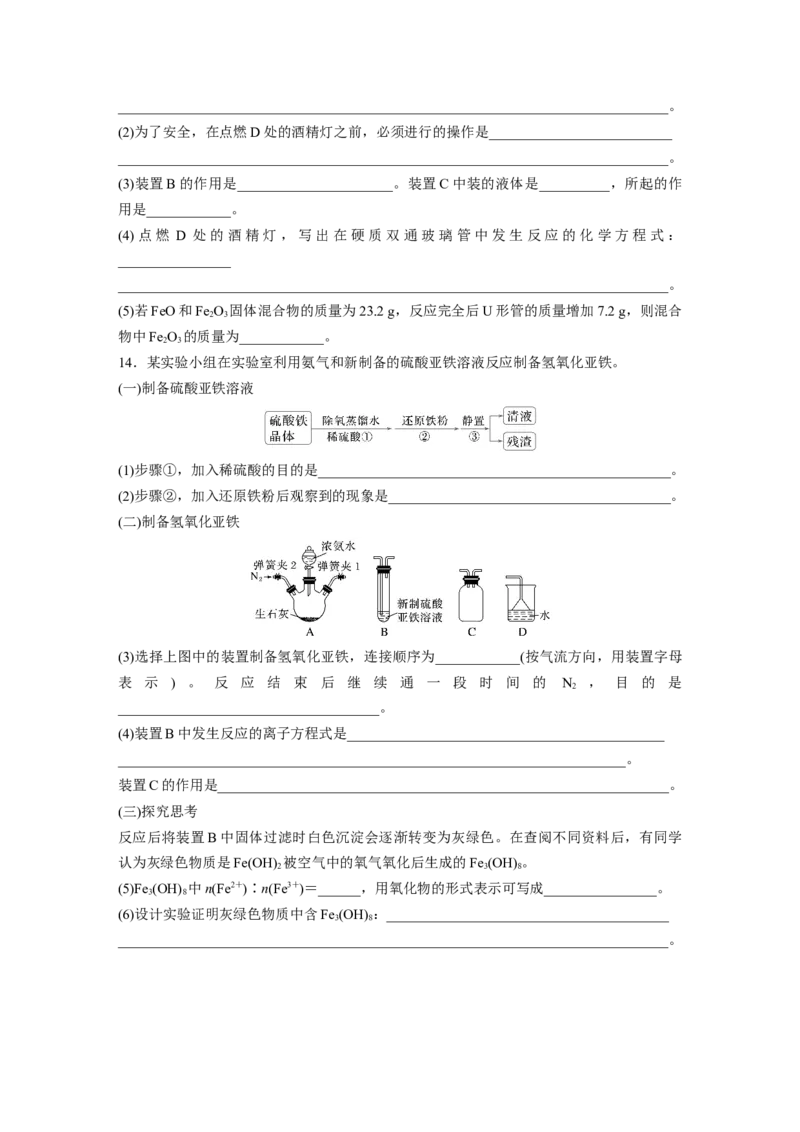
14.某实验小组在实验室利用氨气和新制备的硫酸亚铁溶液反应制备氢氧化亚铁。
(一)制备硫酸亚铁溶液
(1)步骤①,加入稀硫酸的目的是__________________________________________________。
(2)步骤②,加入还原铁粉后观察到的现象是________________________________________。
(二)制备氢氧化亚铁
(3)选择上图中的装置制备氢氧化亚铁,连接顺序为____________(按气流方向,用装置字母
表 示 ) 。 反 应 结 束 后 继 续 通 一 段 时 间 的 N , 目 的 是
2
_____________________________________。
(4)装置B中发生反应的离子方程式是_____________________________________________
________________________________________________________________________。
装置C的作用是________________________________________________________________。
(三)探究思考
反应后将装置B中固体过滤时白色沉淀会逐渐转变为灰绿色。在查阅不同资料后,有同学
认为灰绿色物质是Fe(OH) 被空气中的氧气氧化后生成的Fe (OH) 。
2 3 8
(5)Fe (OH) 中n(Fe2+)∶n(Fe3+)=______,用氧化物的形式表示可写成________________。
3 8
(6)设计实验证明灰绿色物质中含Fe (OH) :________________________________________
3 8
______________________________________________________________________________。