文档内容
1.(2023·大连模拟)青矾矿石(主要成分为FeSO ·7H O)在《唐本草》中记载:“本来绿色,
4 2
新出窟未见风者,正如琉璃……烧之赤色……”。下列关于FeSO ·7H O的说法正确的是(
4 2
)
A.可用于制净水剂
B.溶于水形成无色溶液
C.在干燥空气中稳定存在
D.在空气中加热转化为Fe O
3 4
2.铁及其化合物在生产、生活中应用广泛。下列铁及其化合物的性质与用途具有对应关系
的是( )
A.Fe有导电性,可用于湿法炼铜
B.FeCl 有氧化性,可用于净水
3
C.Fe O 呈红棕色,可用于制作颜料
2 3
D.KFeO 易溶于水,可用于杀菌消毒
2 4
3.下列事实不能证明Fe3+有氧化性的是( )
A.电子工业上用FeCl 溶液腐蚀电路板上的铜
3
B.FeCl 溶液滴在淀粉-KI试纸上,试纸变为蓝色
3
C.将KSCN溶液加入FeCl 溶液中,溶液变为红色
3
D.向FeCl 溶液中滴加适量NaS溶液,出现淡黄色浑浊,溶液变成浅绿色
3 2
4.下列离子方程式书写正确的是( )
A.铁与稀盐酸反应:Fe+6H+===Fe3++3H↑
2
B.氯气与氯化亚铁溶液反应:Cl+Fe2+===Fe3++2Cl-
2
C.氯化铁溶液与铜反应:3Cu+2Fe3+===2Fe+3Cu2+
D.氯化铁溶液与氨水反应:Fe3++3NH ·H O===Fe(OH) ↓+3NH
3 2 3
5.(2023·太原模拟)将NaS溶液逐滴加入等物质的量浓度的FeCl 溶液中,发生反应:2Fe3+
2 3
+S2-===2Fe2++S↓;将FeCl 溶液逐滴加入等物质的量浓度的NaS溶液中,发生反应:
3 2
2Fe3++3S2-===Fe S↓。则下列叙述错误的是( )
2 3
A.Fe3+在酸性环境中氧化性较强
B.S2-在碱性环境中还原性较强
C.相同温度下Fe(OH) 的溶解度比Fe S 的大
3 2 3
D.向FeCl 溶液中通入HS,有硫析出
3 2
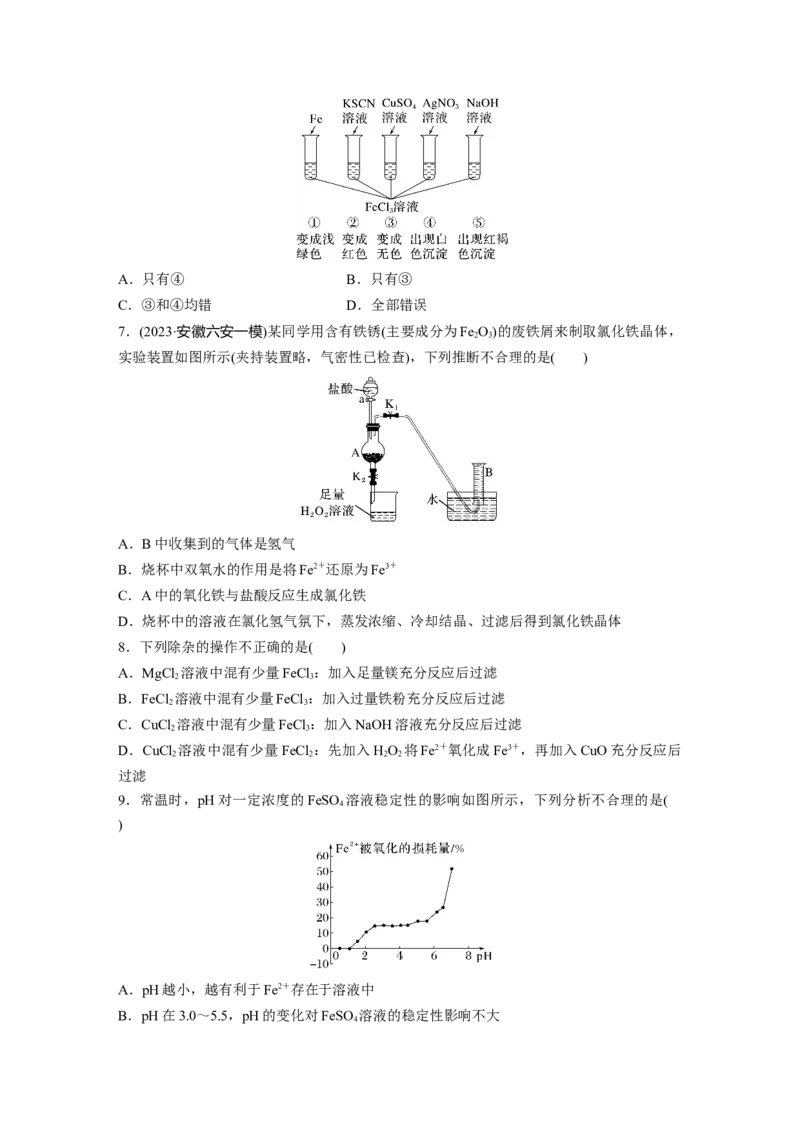
6.为了验证Fe3+的性质,某化学兴趣小组设计了如图所示的一组实验,其中实验方案设计
错误的是( )A.只有④ B.只有③
C.③和④均错 D.全部错误
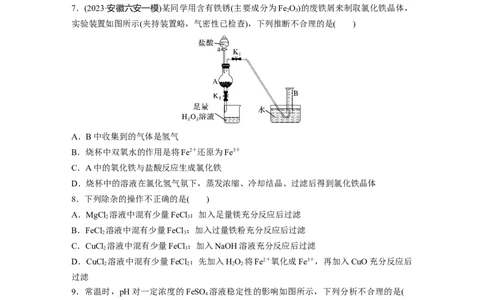
7.(2023·安徽六安一模)某同学用含有铁锈(主要成分为Fe O)的废铁屑来制取氯化铁晶体,
2 3
实验装置如图所示(夹持装置略,气密性已检查),下列推断不合理的是( )
A.B中收集到的气体是氢气
B.烧杯中双氧水的作用是将Fe2+还原为Fe3+
C.A中的氧化铁与盐酸反应生成氯化铁
D.烧杯中的溶液在氯化氢气氛下,蒸发浓缩、冷却结晶、过滤后得到氯化铁晶体
8.下列除杂的操作不正确的是( )
A.MgCl 溶液中混有少量FeCl :加入足量镁充分反应后过滤
2 3
B.FeCl 溶液中混有少量FeCl :加入过量铁粉充分反应后过滤
2 3
C.CuCl 溶液中混有少量FeCl :加入NaOH溶液充分反应后过滤
2 3
D.CuCl 溶液中混有少量FeCl :先加入HO 将Fe2+氧化成Fe3+,再加入CuO充分反应后
2 2 2 2
过滤
9.常温时,pH对一定浓度的FeSO 溶液稳定性的影响如图所示,下列分析不合理的是(
4
)
A.pH越小,越有利于Fe2+存在于溶液中
B.pH在3.0~5.5,pH的变化对FeSO 溶液的稳定性影响不大
4C.pH=6时,通入一定量的氯气,溶液酸性增强,有利于Fe2+存在于溶液中
D.保持溶液的pH始终为6.5时,可能发生的反应为4Fe2++O+10HO4Fe(OH) +8H+
2 2 3
10.硫酸亚铁是一种重要的化工原料,部分转化如图所示。下列说法正确的是( )
A.只用KSCN溶液不可以检验FeSO 是否变质
4
B.制纳米Fe O 时通入的O 需过量
3 4 2
C.制FeCO 时应将饱和NaCO 溶液加入FeSO 溶液中
3 2 3 4
D.生成(NH )Fe(SO )·6H O的反应为氧化还原反应
4 2 4 2 2
11.向含有Cu(NO ) 、Zn(NO ) 、Fe(NO ) 、AgNO 各0.1 mol的混合溶液中加入 0.1 mol
3 2 3 2 3 3 3
Fe,充分搅拌后Fe溶解,溶液中不存在Fe3+,同时析出0.1 mol Ag。下列结论错误的是(
)
A.氧化性:Zn2+>Cu2+>Fe3+>Ag+
B.Fe3+的氧化性大于Cu2+
C.溶液中Cu2+与Fe2+的物质的量之比为1∶2
D.1 mol Fe可还原2 mol Fe3+
12.无水FeCl 常作为芳烃氯代反应的催化剂。某研究小组设计了如图流程,以废铁屑(含有
3
少量碳和SiO 杂质)为原料制备无水FeCl (s):
2 3
已知:氯化亚砜( )熔点:-101 ℃,沸点:76 ℃,易水解。
下列有关说法不正确的是( )
A.操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和漏斗
B.反应D→E的化学方程式为FeCl ·6H O+6SOCl =====FeCl +6SO ↑+12HCl↑
3 2 2 3 2
C.该制备流程中试剂B可选用高锰酸钾溶液或稀硝酸
D.由D转化成E的过程中可能产生少量亚铁盐,其原因可能是生成的SO 将Fe3+还原成Fe2
2
+,为了验证是SO 将Fe3+还原应进行的实验操作和现象是:取样溶解后,先加盐酸酸化,
2
再加入BaCl 溶液,生成白色沉淀
2
13.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液。在FeCl 溶液中需加
2入少量铁屑,其目的是________________________________________________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明
2
Cl 可将Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为__________________________。
2 2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl 溶液中先加入0.5 mL 煤油,
2
再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是____________
____________________________________________________________________________。
(4)丙组同学取10 mL 0.1 mol·L-1KI溶液,加入6 mL 0.1 mol·L-1 FeCl 溶液混合。分别取 2
3
mL 此溶液于3支试管中进行如下实验:
①第一支试管中加入1 mL CCl 充分振荡、静置,CCl 层显紫色;②第二支试管中加入1滴
4 4
K[Fe(CN) ]溶液,生成蓝色沉淀;③第三支试管中加入1滴KSCN溶液,溶液变红。
3 6
实验②检验的离子是________(填离子符号,下同);实验①和③说明:在I-过量的情况下,
溶液中仍含有________,由此可以证明该氧化还原反应为____________。
(5)丁组同学向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,发生
2 2 2
反 应 的 离 子 方 程 式 为
_______________________________________________________________;
一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是
______________________________________________________________,生成沉淀的原因是
__________________________________________________(用平衡移动原理解释)。
14.(2022·河北,15)以焙烧黄铁矿 FeS(杂质为石英等)产生的红渣为原料制备铵铁蓝
2
Fe(NH )Fe(CN) 颜料。工艺流程如下:
4 6
回答下列问题:
(1)红渣的主要成分为______________(填化学式,下同),滤渣①的主要成分为__________。
(2)黄铁矿研细的目的是________________________________________________________
____________________________________________________________________________。
(3)还原工序中,不生成S单质的反应的化学方程式为______________________________。
(4)工序①的名称为______________________,所得母液循环使用。
(5)沉铁工序产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为__________,氧化工序发生反
4 2 6
应的离子方程式为____________________________________________________________
____________________________________________________________________________。
(6)若用还原工序得到的滤液制备 Fe O·xHO 和(NH )SO ,所加试剂为__________和
2 3 2 4 2 4________(填化学式,不引入杂质)。