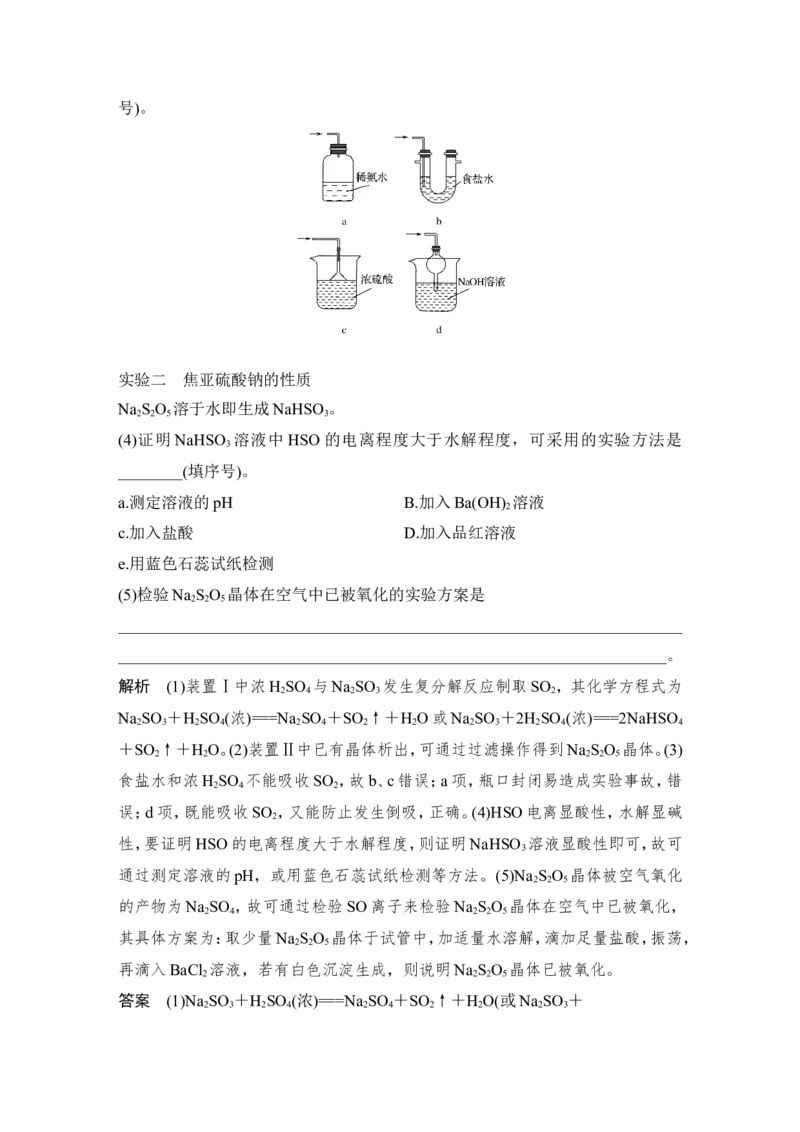
文档内容
第3讲 硫及其重要化合物
【2020·备考】
最新考纲:1.掌握硫元素的单质及其重要化合物的主要性质及应用。2.了解硫元素
的单质及其重要化合物的制备方法。3.了解二氧化硫对环境质量的影响。
核心素养:1.宏观辨识与微观探析:能从不同层次认识硫单质及化合物的多样性,
并对其进行分类。2.科学探究与创新意识:能根据硫单质及化合物的性质提出有探
究价值的问题;能从问题和假设出发,确定探究目的,设计探究方案,进行实验探
究。
考点一 硫及其氧化物的性质
(频数:★☆☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点主要考查硫及二氧化硫的性质判断,特别是二氧化硫的实验探究,是高考重
点,要重点落实。
1.自然界中硫元素的存在2.硫的物理性质
溶解性
俗称 颜色状态
水 酒精 CS
2
黄色或淡
硫黄 不溶 微溶 易溶
黄色固体
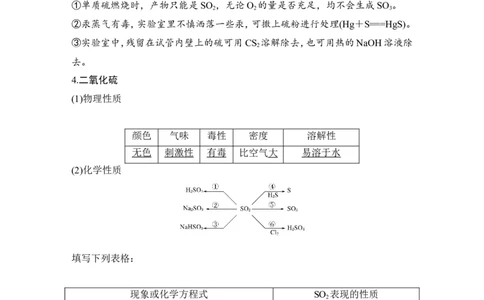
3.硫的化学性质
(3)与强氧化剂反应(如浓硫酸): S + 2H SO ( 浓 ) INCLUDEPICTURE "F:\\ 方正文
2 4
件 \\201 9 文件 \ \ 课件 \\202 0 版 创新设计 高考总复习 化学 人教版 \ \ 反应三角 .TIF "
\* MERGEFORMATINET 3SO ↑ + 2H O,表现还原性。
2 2(4)与碱溶液反应: 3S + 6NaOH INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课
件 \\2020 版 创新设计 高考总复习 化学 人教版 \ \ 反应三角 .TIF" \*
MERGEFORMATINET 2Na S + Na SO + 3H O,表现氧化性和还原性。
2 2 3 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
①单质硫燃烧时,产物只能是SO ,无论O 的量是否充足,均不会生成SO 。
2 2 3
②汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理(Hg+S===HgS)。
③实验室中,残留在试管内壁上的硫可用CS 溶解除去,也可用热的NaOH溶液除
2
去。
4.二氧化硫
(1)物理性质
颜色 气味 毒性 密度 溶解性
无色 刺激性 有毒 比空气大 易溶于水
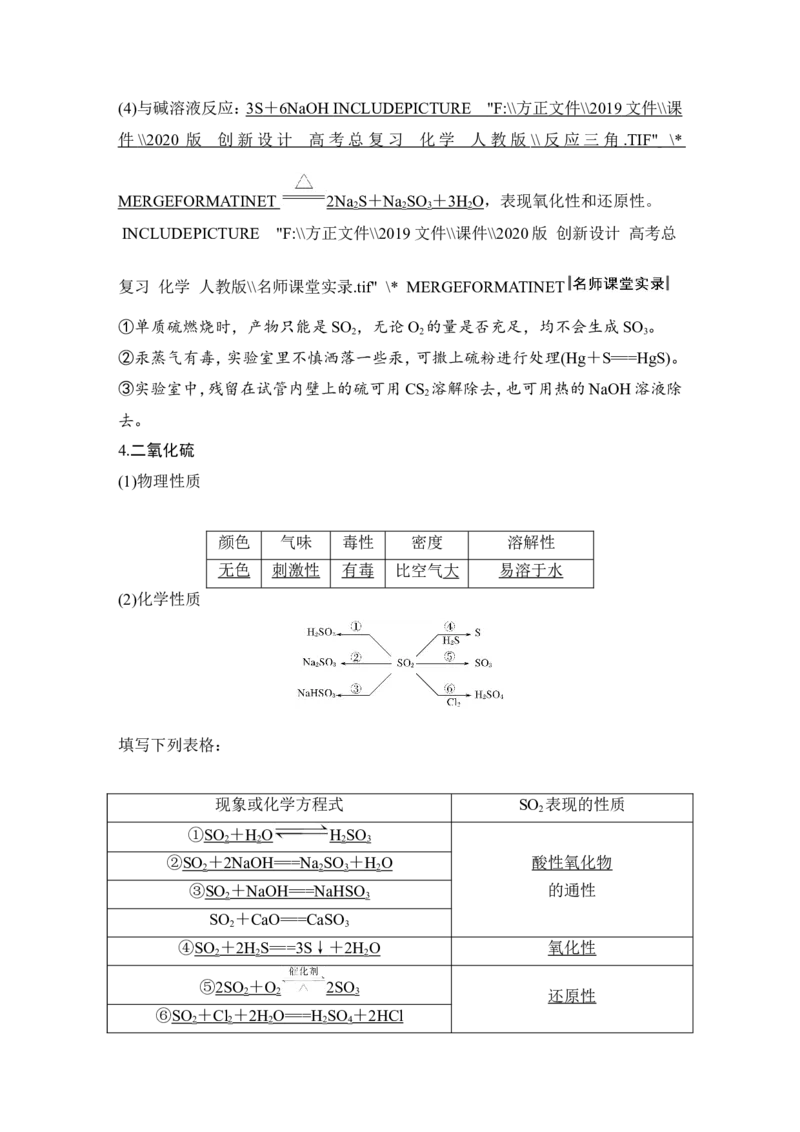
(2)化学性质
填写下列表格:
现象或化学方程式 SO 表现的性质
2
①SO + H O H SO
2 2 2 3
②SO + 2NaOH == =N a SO + H O 酸性氧化物
2 2 3 2
③SO + NaOH == =NaHSO 的通性
2 3
SO +CaO===CaSO
2 3
④SO + 2H S == =3S ↓ + 2H O 氧化性
2 2 2
⑤2SO + O 2SO
2 2 3 还原性
⑥SO + C l + 2H O == =H SO + 2HC l
2 2 2 2 4使酸性高锰酸钾溶液、溴水褪色
使品红溶液褪色 漂白性
(3)SO 对大气的污染与防治
2
①酸雨的形成过程:
②SO 对大气的污染与防治:
2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
(1)SO 不能漂白酸、碱指示剂,如:SO 使紫色的石蕊溶液只变红,不褪色。
2 2
(2)SO 能使溴水、酸性KMnO 溶液褪色,体现了SO 的还原性而不是漂白性。
2 4 2
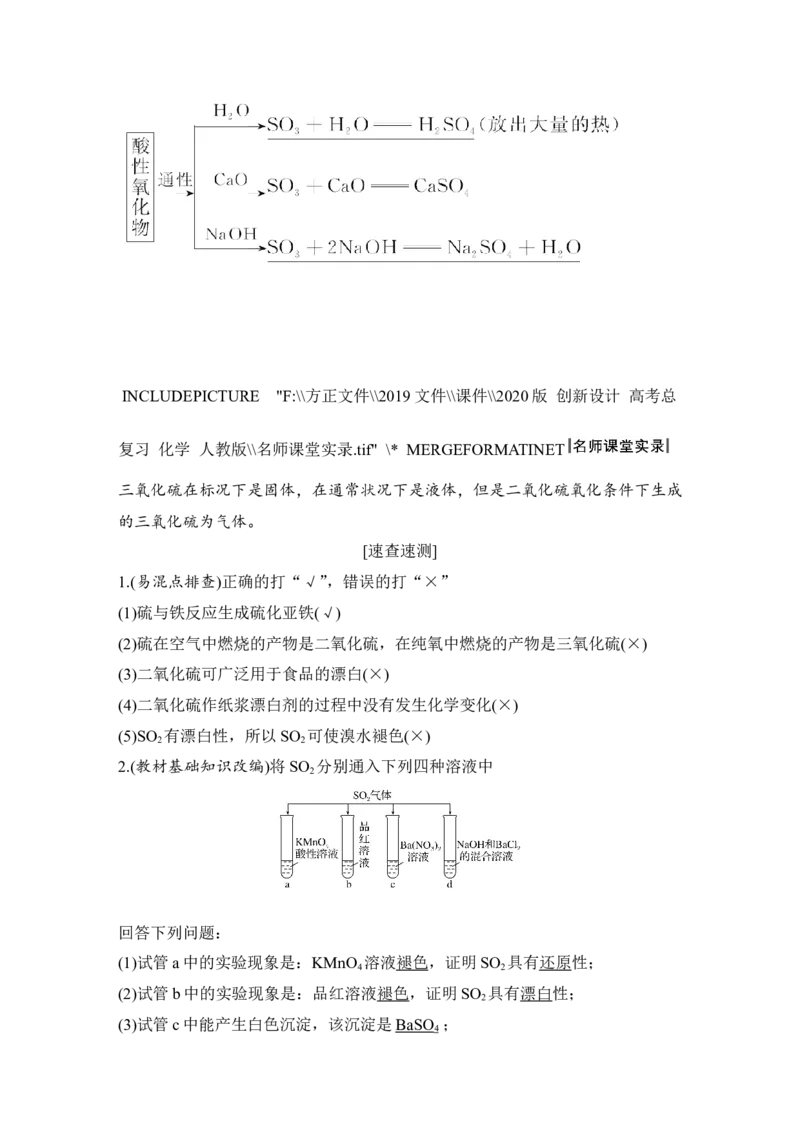
5.三氧化硫
(1)物理性质:熔点16.8 ℃,沸点44.8 ℃,在常温下为液态,在标准状况下为固态。
(2)化学性质INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
三氧化硫在标况下是固体,在通常状况下是液体,但是二氧化硫氧化条件下生成
的三氧化硫为气体。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)硫与铁反应生成硫化亚铁(√)
(2)硫在空气中燃烧的产物是二氧化硫,在纯氧中燃烧的产物是三氧化硫(×)
(3)二氧化硫可广泛用于食品的漂白(×)
(4)二氧化硫作纸浆漂白剂的过程中没有发生化学变化(×)
(5)SO 有漂白性,所以SO 可使溴水褪色(×)
2 2
2.(教材基础知识改编)将SO 分别通入下列四种溶液中
2
回答下列问题:
(1)试管a中的实验现象是:KMnO 溶液褪色,证明SO 具有还原性;
4 2
(2)试管b中的实验现象是:品红溶液褪色,证明SO 具有漂白性;
2
(3)试管c中能产生白色沉淀,该沉淀是BaSO ;
4(4)试管d中能产生白色沉淀,该沉淀是BaSO 。
3
3.(思维探究题)总结SO 和CO 的鉴别方法,并指出下列溶液能够区分SO 和CO
2 2 2 2
的是________。
①澄清石灰水 ②H S溶液 ③酸性KMnO 溶液 ④氯水 ⑤品红溶液
2 4
解析 通常可用以下方法鉴别SO 和CO :
2 2
答案 ②③④⑤
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2018·厦门模拟)下列说法不正确的是( )
A.改燃煤为燃气,可以减少废气中SO 等有害物质的排放量,是治理“雾霾”等
2
灾害天气的一种措施
B.向煤中加入适量石灰石,使煤燃烧产生的SO 最终生成CaSO ,可减少对大气的
2 3
污染
C.大量燃烧化石燃料排放的废气中含SO ,从而使雨水的pH<5.6形成酸雨
2
D.硫和氮的氧化物是形成酸雨的主要物质答案 B
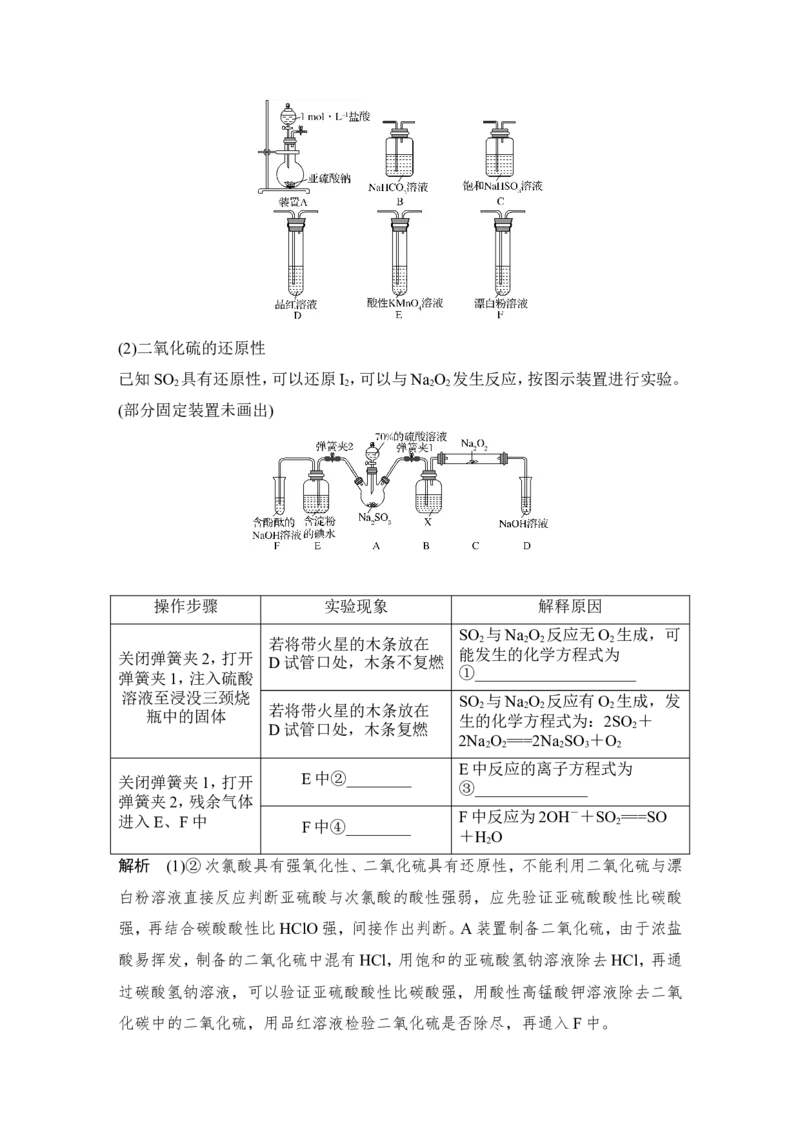
2.如图,利用培养皿探究SO 的性质。实验时向Na SO 固体上滴几滴浓硫酸,立即
2 2 3
用另一表面皿扣在上面。
下表中对实验现象的描述或所做的解释不正确的是( )
选项 实验现象 解释
A BaCl 溶液变浑浊 SO 与BaCl 溶液反应产生了BaSO 沉淀
2 2 2 3
B Na S溶液变浑浊 SO 与Na S溶液反应产生了S单质
2 2 2
C 酸性KMnO 溶液褪色 SO 具有还原性
4 2
D 品红溶液褪色 SO 具有漂白性
2
解析 SO 与水反应生成H SO ,H SO 为中强酸,不与BaCl 溶液反应。
2 2 3 2 3 2
答案 A
3.(2018·安徽安庆二模)SO 虽是大气污染物之一,但也是重要的工业原料,某同学
2
在实验室设计如下实验,对SO 的部分性质进行了探究。
2
(1)二氧化硫的水溶液
①SO 易溶于水,常温常压下溶解度为1∶40,其中有H SO 生成。向SO 的饱和溶
2 2 3 2
液 中 加 入 NaHSO 固 体 , 有 气 体 冒 出 , 原 因 是
3
_____________________________________________________________________
_____________________________________________________________________
。(结合有关平衡方程式简要说明)
②欲验证酸性:H SO >HClO,选用下面的装置,其连接顺序为:
2 3
A→________________________(按气流方向用大写字母表示即可)。能证明H SO
2 3
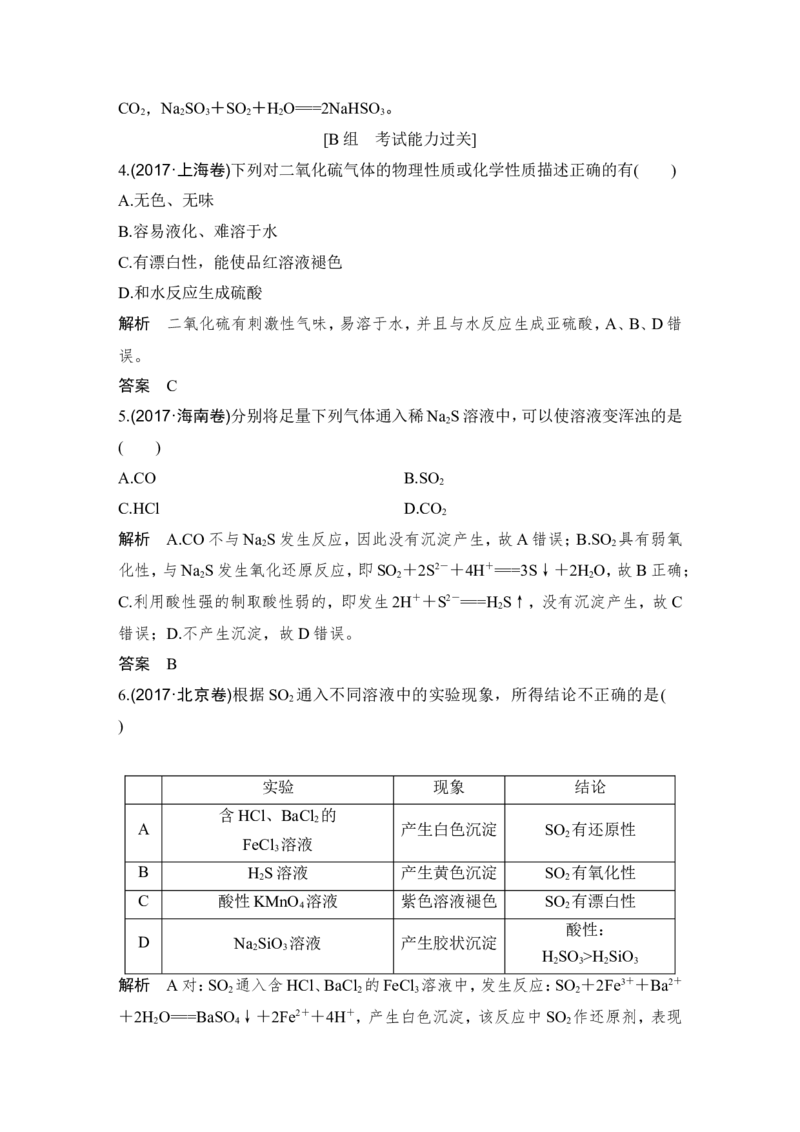
的酸性强于HClO的实验现象为_________________________________________。(2)二氧化硫的还原性
已知SO 具有还原性,可以还原I ,可以与Na O 发生反应,按图示装置进行实验。
2 2 2 2
(部分固定装置未画出)
操作步骤 实验现象 解释原因
SO 与Na O 反应无O 生成,可
若将带火星的木条放在 2 2 2 2
能发生的化学方程式为
关闭弹簧夹2,打开 D试管口处,木条不复燃
①____________________
弹簧夹1,注入硫酸
溶液至浸没三颈烧 SO 与Na O 反应有O 生成,发
若将带火星的木条放在 2 2 2 2
瓶中的固体
生的化学方程式为:2SO +
D试管口处,木条复燃 2
2Na O ===2Na SO +O
2 2 2 3 2
E中反应的离子方程式为
关闭弹簧夹1,打开 E中②________
③______________
弹簧夹2,残余气体
进入E、F中 F中④________ F中反应为2OH-+SO 2 ===SO
+H O
2
解析 (1)②次氯酸具有强氧化性、二氧化硫具有还原性,不能利用二氧化硫与漂
白粉溶液直接反应判断亚硫酸与次氯酸的酸性强弱,应先验证亚硫酸酸性比碳酸
强,再结合碳酸酸性比HClO强,间接作出判断。A装置制备二氧化硫,由于浓盐
酸易挥发,制备的二氧化硫中混有HCl,用饱和的亚硫酸氢钠溶液除去HCl,再通
过碳酸氢钠溶液,可以验证亚硫酸酸性比碳酸强,用酸性高锰酸钾溶液除去二氧
化碳中的二氧化硫,用品红溶液检验二氧化硫是否除尽,再通入F中。(2)A中制备二氧化硫,X干燥二氧化硫,C中是SO 与Na O 反应,D中氢氧化钠
2 2 2
溶液吸收剩余的二氧化硫,防止污染空气。E装置检验I-还原性弱于SO ,F装置
2
验证二氧化硫为酸性气体,并吸收二氧化硫,防止污染空气。
答案 (1)①SO 的水溶液中存在如下平衡:SO +H O H SO H++
2 2 2 2 3
HSO,加入NaHSO 固体增大了c(HSO),平衡左移,SO 增多,从饱和溶液中逸出
3 2
②C→B→E→D→F D中品红溶液不褪色,F中产生白色沉淀
(2)①Na O +SO ===Na SO ②溶液蓝色褪去
2 2 2 2 4
③SO +I +2H O===2I-+SO+4H+ ④红色变浅或褪色
2 2 2
【归纳总结】
工业上常见的SO 尾气处理方法
2
方法一:钙基固硫法
为防治酸雨,工业上常用生石灰和含硫的煤混合后燃烧,燃烧时硫、生石灰、O 共
2
同反应生成硫酸钙,从而使硫转移到煤渣中,反应原理为 CaO+SO
2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\反应三角.TIF" \* MERGEFORMATINET CaSO ,
3
2CaSO +O INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新
3 2
设计 高考总复习 化学 人教版\\反应三角.TIF" \* MERGEFORMATINET
2CaSO ,总反应方程式为2CaO+2SO +O INCLUDEPICTURE "F:\\方正文件\
4 2 2
\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\反应三角.TIF" \*
MERGEFORMATINET 2CaSO 。
4
方法二:氨水脱硫法
该脱硫法采用喷雾吸收法,雾化的氨水与烟气中的SO 直接接触吸收SO ,其反应
2 2
的化学方程式为2NH +SO +H O===(NH ) SO ,2(NH ) SO +O ===2(NH ) SO 。
3 2 2 4 2 3 4 2 3 2 4 2 4
(或生成NH HSO ,然后进一步氧化)
4 3
方法三:钠、碱脱硫法
钠、碱脱硫法是用NaOH/Na CO 吸收烟气中的SO ,得到Na SO 和NaHSO ,发生
2 3 2 2 3 3
反应的化学方程式为 2NaOH+SO ===Na SO +H O,Na CO +SO ===Na SO +
2 2 3 2 2 3 2 2 3CO ,Na SO +SO +H O===2NaHSO 。
2 2 3 2 2 3
[B组 考试能力过关]
4.(2017·上海卷)下列对二氧化硫气体的物理性质或化学性质描述正确的有( )
A.无色、无味
B.容易液化、难溶于水
C.有漂白性,能使品红溶液褪色
D.和水反应生成硫酸
解析 二氧化硫有刺激性气味,易溶于水,并且与水反应生成亚硫酸,A、B、D错
误。
答案 C
5.(2017·海南卷)分别将足量下列气体通入稀Na S溶液中,可以使溶液变浑浊的是
2
( )
A.CO B.SO
2
C.HCl D.CO
2
解析 A.CO不与Na S发生反应,因此没有沉淀产生,故A错误;B.SO 具有弱氧
2 2
化性,与Na S发生氧化还原反应,即SO +2S2-+4H+===3S↓+2H O,故B正确;
2 2 2
C.利用酸性强的制取酸性弱的,即发生2H++S2-===H S↑,没有沉淀产生,故C
2
错误;D.不产生沉淀,故D错误。
答案 B
6.(2017·北京卷)根据SO 通入不同溶液中的实验现象,所得结论不正确的是(
2
)
实验 现象 结论
含HCl、BaCl 的
2
A 产生白色沉淀 SO 有还原性
2
FeCl 溶液
3
B H S溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
酸性:
D Na SiO 溶液 产生胶状沉淀
2 3
H SO >H SiO
2 3 2 3
解析 A对:SO 通入含HCl、BaCl 的FeCl 溶液中,发生反应:SO +2Fe3++Ba2+
2 2 3 2
+2H O===BaSO ↓+2Fe2++4H+,产生白色沉淀,该反应中SO 作还原剂,表现
2 4 2出还原性。B对:SO 通入H S溶液中,发生反应:SO +2H S===3S↓+2H O,产生
2 2 2 2 2
黄色沉淀,该反应中SO 作氧化剂,表现出氧化性。C错:SO 通入酸性KMnO 溶
2 2 4
液中,发生反应:5SO +2MnO+2H O===5SO+2Mn2++4H+,该反应中,SO 作还
2 2 2
原剂,表现出还原性而不是漂白性。D对:SO 通入Na SiO 溶液中,发生反应:
2 2 3
Na SiO +SO +H O===H SiO ↓+Na SO ,该反应符合“强酸制弱酸”的反应规
2 3 2 2 2 3 2 3
律,则酸性:H SO >H SiO 。
2 3 2 3
答案 C
考点二 硫酸 硫酸根离子的检验
(频数:★★☆ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点主要考查角度有:(1)浓硫酸的特性。(2)硫酸根的检验。(3)陌生硫酸盐(或其他
硫的含氧酸盐)的制备或性质探究。
1.硫酸的物理性质
(1)纯硫酸是一种无色油状液体,沸点高,难挥发。利用浓H SO 的高沸点性可以制
2 4
取HCl,反应的化学方程式为: NaCl( 固体 ) + H SO ( 浓 ) ===== NaHSO + HC l ↑ 。
2 4 4
(2)溶解性:浓H SO 与水以任意比互溶,溶解时可放出大量的热,浓H SO 稀释的
2 4 2 4
方法是: 将浓 H SO 沿器壁慢慢注入水中并用玻璃棒不断搅拌。
2 4
2.稀H SO 具有酸的通性
2 4
硫酸是强电解质,在水溶液中的电离方程式为H SO == =2H + + SO ,能与酸碱指示
2 4
剂、金属、碱性氧化物、碱、盐等物质发生反应。
3.浓H SO 的特性
2 4
(1)填写下表
实验 实验现象 硫酸的特性
少量胆矾加入浓硫酸中 蓝色固体变白 吸水性用玻璃棒蘸取浓硫酸滴在滤
沾有浓 H SO 的滤纸变黑 脱水性
纸上 2 4
将铜片加入盛有浓硫酸的试 铜片逐渐溶解,产生无色刺
强氧化性
管中加热 激性气味的气体
(2)分别写出浓硫酸与Cu、C反应的化学方程式:
Cu + 2H SO ( 浓 ) INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版
2 4
创新设计 高考总复习 化学 人教版 \ \ 反应三角 .TIF " \* MERGEFORMATINET
CuSO + SO ↑ + 2H O、 C + 2H SO ( 浓 ) INCLUDEPICTURE "F:\\ 方正文
4 2 2 2 4
件 \\201 9 文件 \ \ 课件 \\202 0 版 创新设计 高考总复习 化学 人教版 \ \ 反应三角 .TIF "
\* MERGEFORMATINET CO ↑ + 2SO ↑ + 2H O。
2 2 2
(3)常温下,铁、铝遇浓H SO 钝化,可用铝槽车运输浓H SO 。
2 4 2 4
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
(1)浓硫酸与金属反应时体现了浓硫酸的氧化性和酸性,而与碳等非金属反应时只
体现了浓硫酸的氧化性。
(2)金属(如铜、铁、锌、铝等)与浓H SO 反应时,要动态地看待反应过程,注意
2 4
H SO 浓度的变化对反应的影响,开始阶段是浓H SO 反应产生SO 气体,但随着
2 4 2 4 2
反应的进行,最后变成稀硫酸,与Cu不反应,与铁、锌、铝等反应生成H 而不是
2
SO 。
2
4.硫酸的用途
(1)制取化肥、硫酸盐、挥发性酸。
(2)消除金属表面的氧化物。
(3)用于精炼石油,制造炸药、农药、染料等,是实验室里常用的试剂。
5.硫酸盐及SO的检验
(1)常见的硫酸盐及其化学式
①皓矾:ZnSO ·7H O
4 2
②钡餐,重晶石:BaSO
4③绿矾,皂矾,青矾:FeSO ·7H O
4 2
④芒硝,朴硝,皮硝:Na SO ·10H O
2 4 2
⑤明矾:KAl(SO ) ·12H O
4 2 2
⑥生石膏:CaSO ·2H O 熟石膏:2CaSO ·H O
4 2 4 2
⑦胆矾、蓝矾:CuSO ·5H O
4 2
⑧ 莫尔盐:(NH ) SO ·FeSO ·6H O
4 2 4 4 2
(2)SO的检验
检验SO的正确操作方法:被检液――→取清液――→有无白色沉淀产生(判断有
无SO)。
先加稀盐酸的目的是 防止 CO 、 SO 、 A g + 、 SiO 等离子干扰,再加BaCl 溶液,有白色
2
沉淀产生。整个过程中可能发生反应的离子方程式: CO + 2H + == =CO ↑ + H O、
2 2
SO + 2H + == =SO ↑ + H O、 Ag + + Cl - == =AgCl ↓ 、 Ba 2 + + SO == =BaSO ↓。
2 2 4
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)(四川高考)常温下,将铁片浸入足量浓硫酸中,铁片不溶解,说明常温下铁与浓
硫酸一定没有发生化学反应(×)
(2)(山东高考)浓H SO 溅到皮肤上时立即用稀NaOH溶液冲洗(×)
2 4
(3)(全国卷Ⅰ)浓H SO 滴入蔗糖固体中,将产生的气体通入溴水,溴水褪色,说明
2 4
浓硫酸具有脱水性、氧化性(√)
(4)(海南高考)用浓H SO 除去HCl中的H O(g)(√)
2 4 2
(5)(浙江高考)在未知液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,
2
说明该未知液中存在SO或SO(×)
2.(教材基础知识改编题)硫酸是中学化学实验室的常见药品,其性质有①酸性 ②
吸水性 ③脱水性 ④强氧化性 ⑤催化作用。请将序号填在相应的横线上:
(1)锌和稀H SO 制H ________________________________________________。
2 4 2
(2)浓硫酸作干燥剂___________________________________________________。
(3) 浓 硫 酸 与 蔗 糖 的 炭 化 实 验 ( 黑 面 包 实
验)________________________________________________________________
__________________________________________________________________。(4)实验室用乙醇和冰醋酸制取乙酸乙酯_______________________________。
(5)浓硫酸与铜的反应_________________________________________________。
(6)浓硫酸使湿润石蕊试纸先变红,后来又变黑__________________________。
答案 (1)① (2)② (3)②③④ (4)②⑤ (5)①④ (6)①③
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.对下列事实的解释正确的是( )
A.蘸有浓硫酸和蘸有浓氨水的玻璃棒靠近没有白烟,说明硫酸与氨气不反应
B.医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡不溶于酸
C.向50 mL 18 mol·L-1的H SO 溶液中加入足量的铜片加热充分反应后,被还原
2 4
的H SO 的物质的量等于0.45 mol
2 4
D.常温下,浓H SO 可以用铝制容器贮存,说明铝与浓硫酸不反应
2 4
解析 氨与挥发性酸反应可形成白烟,硫酸难挥发,A错误;随着反应的进行,硫
酸的浓度降低,稀硫酸不能与铜反应,C错误;常温下浓硫酸使铝钝化(化学变化),
形成致密的氧化膜阻碍了反应的继续进行,D错误。
答案 B
2.下列过程中,最终的白色沉淀物不一定是BaSO 的是( )
4
A.Fe(NO ) 溶液――→白色沉淀
3 2
B.Ba(NO ) 溶液――→白色沉淀
3 2
C.无色溶液――→白色沉淀
D.无色溶液――→无色溶液――→白色沉淀
解析 A项,二氧化硫被硝酸氧化为硫酸,加氯化钡一定生成硫酸钡沉淀;B项,
亚硫酸根被硝酸氧化为硫酸根,沉淀也是硫酸钡;C项,所得沉淀可能是氯化银;D
项,先加过量盐酸无沉淀,再加氯化钡产生的白色沉淀一定是硫酸钡。
答案 C
3.红热木炭与浓H SO 反应的化学方程式是C+2H SO (浓)=====CO ↑+2SO ↑
2 4 2 4 2 2
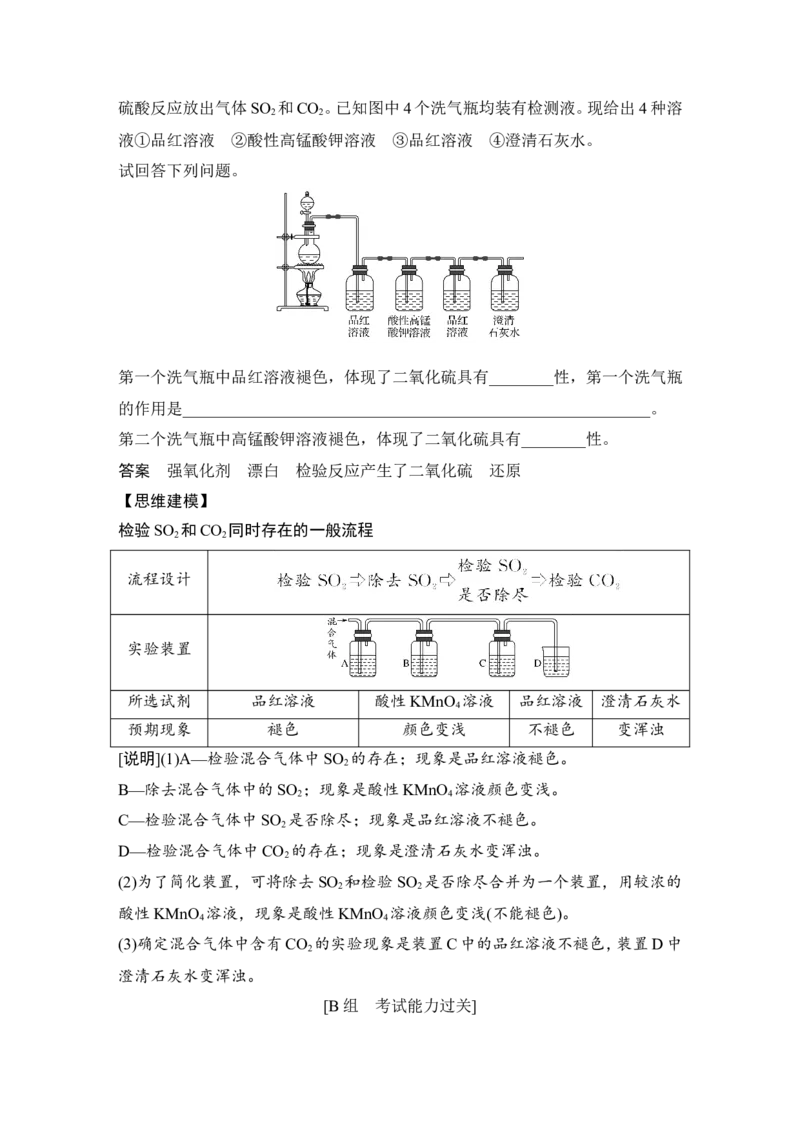
+2H O,该反应中浓硫酸的作用是________。按下图装置进行实验,可证明碳和浓
2硫酸反应放出气体SO 和CO 。已知图中4个洗气瓶均装有检测液。现给出4种溶
2 2
液①品红溶液 ②酸性高锰酸钾溶液 ③品红溶液 ④澄清石灰水。
试回答下列问题。
第一个洗气瓶中品红溶液褪色,体现了二氧化硫具有________性,第一个洗气瓶
的作用是__________________________________________________________。
第二个洗气瓶中高锰酸钾溶液褪色,体现了二氧化硫具有________性。
答案 强氧化剂 漂白 检验反应产生了二氧化硫 还原
【思维建模】
检验SO 和CO 同时存在的一般流程
2 2
流程设计
实验装置
所选试剂 品红溶液 酸性KMnO 溶液 品红溶液 澄清石灰水
4
预期现象 褪色 颜色变浅 不褪色 变浑浊
[说明](1)A—检验混合气体中SO 的存在;现象是品红溶液褪色。
2
B—除去混合气体中的SO ;现象是酸性KMnO 溶液颜色变浅。
2 4
C—检验混合气体中SO 是否除尽;现象是品红溶液不褪色。
2
D—检验混合气体中CO 的存在;现象是澄清石灰水变浑浊。
2
(2)为了简化装置,可将除去SO 和检验SO 是否除尽合并为一个装置,用较浓的
2 2
酸性KMnO 溶液,现象是酸性KMnO 溶液颜色变浅(不能褪色)。
4 4
(3)确定混合气体中含有CO 的实验现象是装置C中的品红溶液不褪色,装置D中
2
澄清石灰水变浑浊。
[B组 考试能力过关]4.(上海高考改编)一定条件下,一种反应物过量,另一种反应物仍不能完全反应的
是( )
A.过量的铁与稀硫酸
B.过量的浓盐酸与二氧化锰
C.过量的铜与浓硫酸
D.过量的锌与18 mol·L-1硫酸
解析 过量的铁与稀硫酸反应,硫酸完全反应,A项不符合题意;过量的浓盐酸与
二氧化锰反应,二氧化锰可以完全反应,B项不符合题意;过量的铜与浓硫酸反应
随着反应的进行,浓硫酸变为稀硫酸反应停止,C项符合题意;过量的锌与 18
mol·L-1硫酸反应,先生成二氧化硫,变为稀硫酸后生成氢气,硫酸可以完全反应,
D项不符合题意。
答案 C
5.(福建高考)焦亚硫酸钠(Na S O )是常用的食品抗氧化剂之一。某研究小组进行如
2 2 5
下实验:
实验一 焦亚硫酸钠的制取
采用下图装置(实验前已除尽装置内的空气)制取Na S O 。装置Ⅱ中有Na S O 晶
2 2 5 2 2 5
体析出,发生的反应为Na SO +SO ===Na S O
2 3 2 2 2 5
(1) 装 置 Ⅰ 中 产 生 气 体 的 化 学 方 程 式 为
______________________________________________________________________
_____________________________________________________________________
。
(2) 要 从 装 置 Ⅱ 中 获 得 已 析 出 的 晶 体 , 可 采 取 的 分 离 方 法 是
_____________________________________________________________________。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。
实验二 焦亚硫酸钠的性质
Na S O 溶于水即生成NaHSO 。
2 2 5 3
(4)证明 NaHSO 溶液中 HSO 的电离程度大于水解程度,可采用的实验方法是
3
________(填序号)。
a.测定溶液的pH B.加入Ba(OH) 溶液
2
c.加入盐酸 D.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检验Na S O 晶体在空气中已被氧化的实验方案是
2 2 5
______________________________________________________________________
____________________________________________________________________。
解析 (1)装置Ⅰ中浓H SO 与Na SO 发生复分解反应制取SO ,其化学方程式为
2 4 2 3 2
Na SO +H SO (浓)===Na SO +SO ↑+H O或Na SO +2H SO (浓)===2NaHSO
2 3 2 4 2 4 2 2 2 3 2 4 4
+SO ↑+H O。(2)装置Ⅱ中已有晶体析出,可通过过滤操作得到Na S O 晶体。(3)
2 2 2 2 5
食盐水和浓H SO 不能吸收SO ,故b、c错误;a项,瓶口封闭易造成实验事故,错
2 4 2
误;d项,既能吸收SO ,又能防止发生倒吸,正确。(4)HSO电离显酸性,水解显碱
2
性,要证明HSO的电离程度大于水解程度,则证明NaHSO 溶液显酸性即可,故可
3
通过测定溶液的pH,或用蓝色石蕊试纸检测等方法。(5)Na S O 晶体被空气氧化
2 2 5
的产物为Na SO ,故可通过检验SO离子来检验Na S O 晶体在空气中已被氧化,
2 4 2 2 5
其具体方案为:取少量Na S O 晶体于试管中,加适量水溶解,滴加足量盐酸,振荡,
2 2 5
再滴入BaCl 溶液,若有白色沉淀生成,则说明Na S O 晶体已被氧化。
2 2 2 5
答案 (1)Na SO +H SO (浓)===Na SO +SO ↑+H O(或Na SO +
2 3 2 4 2 4 2 2 2 32H SO (浓)===2NaHSO +SO ↑+H O) (2)过滤 (3)d (4)a、e (5)取少量
2 4 4 2 2
Na S O 晶体于试管中,加适量水溶解,滴加足量盐酸,振荡,再滴入氯化钡溶
2 2 5
液,有白色沉淀生成
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET
[A级 全员必做题]
1.(2018·天津红桥期中,2)酸雨形成的示意图如下。下列说法中,不正确的是( )
A.汽车尾气是导致酸雨的原因之一
B.酸雨会使土壤、湖泊酸化
C.酸雨形成中不涉及氧化还原反应
D.燃煤中加入生石灰可防治酸雨
解析 NO →HNO 、SO →H SO 等过程中均发生了氧化还原反应。
2 3 2 2 4
答案 C
2.探究浓硫酸和铜的反应,下列装置或操作正确的是( )
A.用装置甲进行铜和浓硫酸的反应
B.用装置乙收集二氧化硫并吸收尾气
C.用装置丙稀释反应后的混合液
D.用装置丁测定余酸的浓度
解析 A项,浓硫酸和铜反应Cu+2H SO (浓)=====CuSO +SO ↑+2H O,由原
2 4 4 2 2理知应选固+液――→装置类型,错误;B项,SO 比空气重,收集时应从长管进气,
2
错误;C项,由于甲中有剩余的浓硫酸,故稀释时应将残液缓缓加入水中,边加边
搅拌,正确;D项,测定余酸浓度,标准液为NaOH溶液,故应选碱式滴定管,错误
答案 C
3.(2019·辽宁大连模拟)以下每个选项中的两组物质都能反应,且能放出同一种气
体的是( )
A.铜与稀硫酸,铜与浓硫酸
B.铁与稀硫酸,铁与浓硫酸
C.硫化钠与稀硫酸,亚硫酸钠与稀硫酸
D.硫化钠与稀硫酸,硫化钠与稀盐酸
解析 Cu与稀H SO 不反应,A项错误;Fe与稀H SO 反应生成的气体为H ,Fe
2 4 2 4 2
与浓H SO 在加热的条件下反应生成的气体为SO ,B项错误;Na S与稀H SO 反
2 4 2 2 2 4
应生成的气体为H S,Na SO 与稀H SO 反应生成的气体为SO ,C项错误。
2 2 3 2 4 2
答案 D
4.(2019·湖南益阳、湘潭联考,7)下列有关说法错误的是( )
A.金属Mg与稀硫酸、CO 均能反应,但其反应类型不同
2
B.浓硫酸与铜反应既体现了其强氧化性又体现了其酸性
C.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe O
3 4
D.SO 气体通入Ba(NO ) 溶液中,有白色沉淀生成
2 3 2
解析 镁与稀硫酸、CO 反应均为置换反应:Mg+H SO ===MgSO +H ↑、2Mg+
2 2 4 4 2
CO =====2MgO+C,A项错误。
2
答案 A
5.(2018·湖南雅礼中学月考)含硫煤燃烧会产生大气污染物,为防治该污染,某工
厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不
正确的是( )
A.该过程中可得到化工产品H SO
2 4B.该工艺流程是除去煤燃烧时产生的SO
2
C.该过程中化合价发生改变的元素只有Fe和S
D.图中涉及的反应之一为Fe (SO ) +SO +2H O===2FeSO +2H SO
2 4 3 2 2 4 2 4
解析 根据工艺流程图可知,该工艺中 Fe (SO ) 溶液吸收 SO 生成 FeSO 和
2 4 3 2 4
H SO ,该反应的化学方程式为Fe (SO ) +SO +2H O===2FeSO +2H SO ,该工
2 4 2 4 3 2 2 4 2 4
艺不仅吸收了二氧化硫,还得到了化工产品硫酸,A、D两项正确;根据A中分析
可知该工艺流程是除去煤燃烧时产生的SO ,B项正确;该过程中化合价发生变化
2
的元素有氧、铁、硫,C项错误。
答案 C
6.下列叙述Ⅰ和叙述Ⅱ均正确且有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A H 有还原性,浓硫酸有强氧化性 不能用浓硫酸干燥H
2 2
反应H S+CuSO ===CuS↓+H SO
B CuS难溶于水和硫酸 2 4 2 4
可以发生
C 浓H SO 有吸水性 浓H SO 可用于干燥氨气
2 4 2 4
Na S O 能与H SO 反应生成沉淀S
D Na S O 溶液显碱性 2 2 3 2 4
2 2 3 和气体SO
2
解析 氢气与浓硫酸不反应,可以用浓硫酸干燥氢气,A错误;因为CuS难溶于水
和硫酸,所以H S+CuSO ===CuS↓+H SO 可以发生,B正确;浓硫酸具有酸性,
2 4 2 4
氨气具有碱性,二者能发生化学反应,C错误;叙述Ⅰ与叙述Ⅱ没有因果关系,D
错误。
答案 B
7.(2019·河北张家口模拟)SO 通入足量的Fe(NO ) 稀溶液中,溶液由棕色变为浅
2 3 3
绿色,但立即又变成棕黄色,这时若滴入BaCl 溶液,会产生白色沉淀。针对上述一
2
系列变化,下列说法不正确的是( )
A.上述过程中,最终被还原的是NO
B.从上述反应可以得出结论,氧化性:HNO >Fe3+>稀硫酸
3
C.上述过程中,会产生一种无色难溶于水的气体
D.假设通入的SO 完全反应,则同温同压下,SO 和逸出气体的体积比为1∶1
2 2
解析 溶液由棕色变为浅绿色,但立即又变为棕黄色,Fe3+被还原变为Fe2+,后又
被氧化为Fe3+,所以最终被还原的是NO,A正确;溶液由棕色变为浅绿色,说明Fe3+的氧化性强于稀硫酸,但在硝酸存在的前提下立即又变成棕黄色,说明 Fe2+
迅速被氧化成Fe3+,故硝酸的氧化性强于Fe3+,综上所述氧化性:HNO >Fe3+>
3
稀H SO ,B正确;硝酸根离子和二氧化硫被氧化后产生的氢离子构成强氧化性体
2 4
系,氧化Fe2+时生成无色的NO气体,该气体是一种无色难溶于水的物质,C正确;
上述过程中,最终被还原的是NO,故相当于二氧化硫与NO之间的氧化还原,根
据电子守恒可知 3SO ~2NO,反应消耗的 SO 与逸出的NO的物质的量之比是
2 2
3∶2,由于气体的体积之比等于它们的物质的量之比,D错误。
答案 D
8.(2019·福建六校联考,13)用下列两种途径制取H SO ,某些反应条件和产物已
2 4
省略,下列有关说法不正确的是( )
途径①:S――→H SO
2 4
途径②:S――→SO ――→SO ――→H SO
2 3 2 4
A.途径②与途径①相比较更能体现“绿色化学”的理念,因为途径②比途径①的
污染相对较小且原子利用率较高
B.由途径①和②分别制取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol电子
2 4
C.途径①反应中体现了浓HNO 的强氧化性和酸性
3
D.途径②的第二步反应在实际生产中可以通过增大O 的浓度来提高SO 的转化
2 2
率
解析 途径①S与浓硝酸反应生成硫酸、二氧化氮和水,有副产物二氧化氮,而且
二氧化氮会污染大气,所以途径②与途径①相比更能体现“绿色化学”的理念 ,
A项正确;途径①和②都是由S来制备H SO ,S的化合价从0价升高到+6价,制
2 4
取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol e-,B项正确;途径①反应的
2 4
化学方程式可表示为S+6HNO (浓)===H SO +6NO ↑+2H O,属于浓硝酸和非
3 2 4 2 2
金属单质的反应,产物中无盐生成,因此浓硝酸只表现氧化性而不表现酸性,C项
错误;增大一种反应物的浓度,可以提高另一种反应物的转化率,所以途径②的第
二步反应在实际生产中可以通过增大O 浓度来提高二氧化硫的转化率,从而降低
2
成本,D项正确。
答案 C
9.已知某溶液中可能含有SO、SO及其他未知离子,某同学取适量试液加入四支试
管中,然后分别进行如下实验并得出相应的结论,其中合理的是( )①若加入BaCl 溶液得到白色沉淀,然后加入足量的稀硝酸,沉淀不消失,说明原
2
溶液中一定含有SO ②若加入BaCl 溶液得到白色沉淀,然后加入足量的稀盐酸
2
沉淀溶解并产生刺激性气味的气体,说明原溶液中一定含有 SO ③若先加入盐
酸无现象,再加入BaCl 溶液得到白色沉淀,说明原溶液中一定有SO ④若做焰
2
色反应实验时,火焰呈黄色,说明溶液中一定有Na+,但不能确定是否有K+
A.①②③④ B.①④
C.②③④ D.②③
解析 ①无法排除SO及Ag+的干扰;④确定是否存在钾元素需要透过蓝色钴玻
璃观察焰色。
答案 C
10.H O 被称为绿色氧化剂,在生产工艺中应用广泛,请回答下列有关过氧化氢的
2 2
问题:
(1)Fe3 + 可 以 催 化 H O 分 解 , 请 写 出 该 反 应 的 化 学 方 程 式
2 2
____________________________________________________________________。
(2)酸性条件下,在FeCl 和FeCl 的混合溶液中加入H O 以除去Fe2+,反应的离子
3 2 2 2
方程式为____________________________________。
(3)H O 可 用 于 SO 的 尾 气 处 理 , 请 写 出 反 应 的 化 学 方 程 式
2 2 2
____________________________________。
(4)可以用酸性 KMnO 溶液测定溶液中的 H O 含量,反应的离子方程式为
4 2 2
____________________________________________________________________。
解析 (1)H O 经催化分解得O 和H O。(2)酸性环境下,Fe2+被H O 氧化为Fe3+,
2 2 2 2 2 2
H O 被还原,酸性环境下生成H O。(3)SO 具有还原性,H O 具有氧化性,二者发
2 2 2 2 2 2
生氧化还原反应,该反应也属于化合反应。(4)H O 遇到强的氧化剂时表现出还原
2 2
性,酸性环境下MnO被还原为Mn2+,由电荷守恒和原子守恒可写出反应的离子
方程式。
答案 (1)2H O =====2H O+O ↑
2 2 2 2
(2)2H++H O +2Fe2+===2Fe3++2H O
2 2 2
(3)SO +H O ===H SO
2 2 2 2 4
(4)6H++5H O +2MnO===2Mn2++5O ↑+8H O
2 2 2 2
11.(2018·山东淄博摸底)已知硫酸铜加热分解生成CuO、O 、SO 和SO (g)。通过测
2 2 3定产生的三种气体的量可确定该反应的方程式。实验用到的仪器如下图所示。
有关操作和结果如下(已知:H++HSO===SO ↑+H O)。
2 2
①准确称取一定质量的无水CuSO 固体充分加热到完全分解。
4
②实验后测得装置F总质量比实验前减少了0.96 g(忽略水蒸气的损失和SO 的溶
2
解)。
③干燥管C在实验后质量增加3.84 g。
④由量筒中水的体积,折算出标准状况下相应气体的体积为224 mL。
试回答下列问题:
(1)装置C的作用是___________________________________________________,
装置F的作用是__________________________________________________。
(2)使用上图所给仪器装置(可重复使用),按从左至右的方向连接各仪器,接口顺序
为:①→⑨⑩→⑥⑤→________→________→________→②。(填序号)
(3) 装 置 F 中 发 生 反 应 的 化 学 方 程 式 为 :
_____________________________________________________________________
_____________________________________________________________________
。
(4)请通过计算,推断出该条件下反应的化学方程式:
____________________________________________________________________。
解析 (1)~(3)已知硫酸铜加热分解生成CuO、O 、SO 和SO ,根据题中所给各仪
2 2 3
器的特点及所盛装的药品可知,实验过程为:无水CuSO 固体在A装置中加热分
4
解,所得混合气体中有O 、SO 和SO ;将混合气体通过F装置,发生反应SO +
2 2 3 3
2NaHSO ===Na SO +2SO +H O,此时混合气体(SO 和O )中会带入水蒸气,需
3 2 4 2 2 2 2
要经过装置D进行干燥处理;将混合气体通过C装置,碱石灰吸收SO 后,就得到
2
纯净的O ;最后利用排水法测量混合气体中O 的量,为减少实验误差,C装置和E
2 2装置之间要连接除水蒸气的装置(C或D装置均可)。(4)设F装置中参加反应的
SO 的物质的量为x mol,则生成的SO 为2x mol,故64×2x-80x=0.96,解得x=
3 2
0.02。干燥管C吸收的是分解产生的SO 和F中反应得到的SO ,则分解产生的
2 2
SO 的物质的量为=0.02 mol。量筒中水的体积为分解生成的氧气的体积,在标准
2
状况下氧气的体积为224 mL,则分解得到的O 的物质的量是0.01 mol。根据分解
2
生成的n(SO )=0.02 mol、n(SO )=0.02 mol、n(O )=0.01 mol,结合质量守恒定律
3 2 2
可配平方程式:4CuSO =====4CuO+2SO ↑+2SO ↑+O ↑。
4 3 2 2
答案 (1)吸收SO 吸收SO
2 3
(2)③④ ⑥⑤(或③④) ⑧⑦
(3)SO +2NaHSO ===Na SO +2SO +H O(或 SO +H O===H SO 、H SO +
3 3 2 4 2 2 3 2 2 4 2 4
2NaHSO ===Na SO +2SO ↑+2H O)
3 2 4 2 2
(4)4CuSO =====4CuO+2SO ↑+2SO ↑+O ↑
4 3 2 2
[B级 拔高选做题]
12.(2019·贵阳一测)下图是用电解法处理石油炼制过程中产生的大量 H S废气的
2
工艺流程。该方法对H S的吸收率达99%以上,并可制取H 和S。下列说法正确的
2 2
是( )
A.吸收H S发生反应的离子方程式为:2Fe3++H S===2Fe2++S↓+2H+
2 2
B.滤液的主要成分有盐酸、氯化亚铁和H S
2
C.若X含Fe3+,说明还原性Fe2+>Cl-;若X含Fe3+和少量Cl ,说明氧化性Fe3+
2
>Cl
2
D.实验室可用点燃的方法使H S完全燃烧以消除对环境的污染
2
解析 FeCl 具有氧化性,H S具有还原性,吸收H S时,二者发生氧化还原反应:
3 2 2
2Fe3++H S===2Fe2++S↓+2H+,A项正确;滤液的主要成分为盐酸、氯化亚铁,
2
B项错误;若X含少量Cl ,说明Fe2+先放电,Cl-后放电,则还原性:Fe2+>Cl-,故
2
氧化性:Fe3+