文档内容
第2讲 富集在海水中的元素——卤素
【2020·备考】
最新考纲:1.掌握氯单质及其重要化合物的主要性质及应用。2.了解氯单质及其重
要化合物对环境质量的影响。3.掌握氯气的实验室制法(包括所用试剂、仪器、反应
原理和收集方法)。4.了解卤族元素单质及其重要化合物的主要性质及应用。
核心素养:1.宏观辨识与微观探析:能从宏观和微观相结合的视角分析与解决实际
问题,在卤素学习过程中,使用“宏观-微观-结合”来认识物质及其递变规律,
形成科学的方法论。2.科学精神与社会责任:将化学知识与技能的学习、创新意识
和社会责任感的形成等方面的要求融为一体,充分认识海水资源的重要性。考点
一 氯及其重要化合物
(频数:★★☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 氯
及其重要化合物常见的考查点有:氯及其重要化合物的性质判断;氯及其重要化
合物的实验探究;特别是陌生含氯化合物的制取更是近几年的考查重点,复习时
要加以关注。
1.氯气的物理性质
2.从氯的原子结构认识氯气的化学性质——氧化性(1)与金属反应:与变价金属反应生成高价金属氯化物。
①与铁反应: 2Fe + 3Cl INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \
2
\2020 版 创 新 设 计 高 考 总 复 习 化 学 人 教 版 \\ 反 应 点 燃 .TIF" \*
MERGEFORMATINET 2FeCl 。
3
②与铜反应: Cu + Cl INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020
2
版 创 新 设 计 高 考 总 复 习 化 学 人 教 版 \\ 反 应 点 燃 .TIF" \*
MERGEFORMATINET CuCl 。
2
(2)与非金属反应。
与H 反应:H + C l ===== 2HCl ,
2 2 2
(3)与还原性无机化合物反应。
①与碘化钾溶液反应:Cl + 2K I == =2KC l + I 。
2 2
②与SO 水溶液反应:Cl + SO + 2H O == =H SO + 2HC l。
2 2 2 2 2 4
③与FeCl 溶液反应:
2
离子方程式为Cl + 2F e 2 + == =2F e 3 + + 2C l - 。
2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
Cl 具有强氧化性,与变价金属反应时均生成高价态的金属氯化物,如 FeCl 不能
2 2
由两种单质化合而成。
3.从化合价的角度认识Cl 的化学性质——歧化反应
2
氯气与水或碱反应,氯的化合价既有降低又有升高,因而氯气既表现氧化性又表
现还原性。
Cl +2NaOH===NaCl+NaClO+H O(84消毒液)
2 2
2Cl +2Ca(OH) ===CaCl +Ca(ClO) +2H O(制漂白粉)
2 2 2 2 2
4.从平衡的角度理解氯水的成分和性质
(1)氯水中存在三个平衡关系:
①Cl +H O HCl+HClO
2 2
②HClO H++ClO-
③H O H++OH-
2
(2)根据可逆反应的特点,即可得出氯水中存在的各种微粒。
①三种分子H O、Cl 、HClO;
2 2
②四种离子 H + 、 Cl - 、 ClO - 和 OH - 。
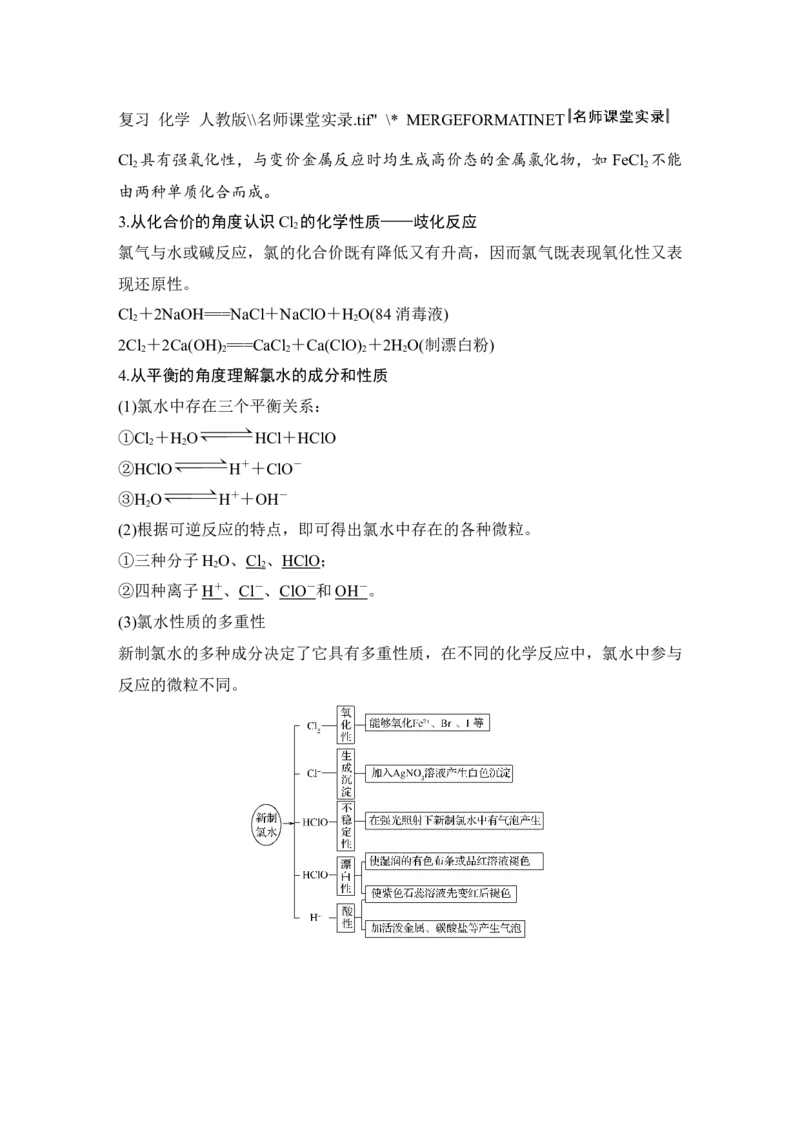
(3)氯水性质的多重性
新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与
反应的微粒不同。INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
(1)干燥的Cl 没有漂白性,但Cl 能使湿润的有色布条褪色,漂白粉也没有漂白性,
2 2
起漂白作用的是HClO,故不能用pH试纸测量氯水的pH。
(2)1 mol Cl 与强碱完全反应转移电子数为N ,而1 mol Cl 与水充分反应转移电
2 A 2
子数小于N (可逆反应)。
A
5.氯的重要化合物
(1)次氯酸
(2)漂白粉
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
(1)HClO不稳定,不能单独存在,只存在于氯水、次氯酸盐溶液或次氯酸盐与酸反
应的混合物中。
(2)不能用pH试纸测量氯水的pH,原因是氯水中的HClO具有漂白性。
(3)“84”消毒液的主要成分为NaClO,漂粉精的有效成分为Ca(ClO) 。“84”消毒液
2
和洁厕灵不能混合使用,其原因是ClO-+Cl-+2H+===Cl ↑+H O。
2 2
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)过量的铁粉在少量氯气中加热,充分反应后产物为FeCl (×)
2(2)标准状况下,11.2 L Cl 与水充分反应转移电子数为0.5N (×)
2 A
(3)Cl 能使湿润的淀粉碘化钾试纸变蓝,说明Cl 具有氧化性(√)
2 2
(4)氯气作水的杀菌消毒剂时没有发生化学变化(×)
(5)新制取的漂白粉是混合物(√)
2.(教材改编题)(RJ必修1·P 2改编)下列物质能使干燥的蓝色石蕊试纸先变红后
87
褪色的是( )
①氯气 ②液氯 ③新制的氯水 ④氯气的酒精溶液 ⑤盐酸 ⑥盐酸酸化的漂
白粉溶液
A.①②③ B.①②③⑥
C.③⑥ D.②④⑤⑥
答案 C
3.(思维探究题 )含氯消毒剂的共同特点是利用本身的强氧化性,或与水反应产生
HClO,杀灭具有生命活性的病菌微生物。其消毒效率通常是指单位质量的消毒剂
所得到的电子数,例如ClO 的消毒效率是Cl 的消毒效率的________________ 倍
2 2
答案 2.63
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不
正确的是( )
A.红热的铜丝在氯气里剧烈燃烧,产生棕黄色的烟
B.通常状况下,干燥的氯气能和Fe反应
C.纯净的H 在Cl 中安静地燃烧,发出苍白色火焰,集气瓶瓶口呈现雾状;光照H
2 2 2
和Cl 的混合气体时,因迅速化合而爆炸
2
D.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸
解析 Cl 与Fe反应需要点燃或加热,通常状况下,Fe与干燥Cl 不反应。
2 2
答案 B
2.在新制饱和氯水中,若只改变某一条件,下列叙述正确的是( )A.再通入少量氯气,减小
B.通入少量SO ,溶液漂白性增强
2
C.加入少量的碳酸钠粉末,pH增大,溶液漂白性增强
D.光照过程中,有气泡冒出,溶液的导电性减弱
解析 饱和氯水不能再溶解氯气,各成分的浓度不变,A 项错;SO +Cl +
2 2
2H O===2HCl+H SO ,Cl +H O H++Cl-+HClO的平衡左移,HClO的
2 2 4 2 2
浓度减小,漂白性减弱,B项错;加入少量的碳酸钠粉末,消耗H+,使上述平衡正
向移动,HClO的浓度增大,C项正确;光照过程中,HClO分解,生成O 和HCl,溶
2
液中的离子浓度增大,导电性增强,D项错误。
答案 C
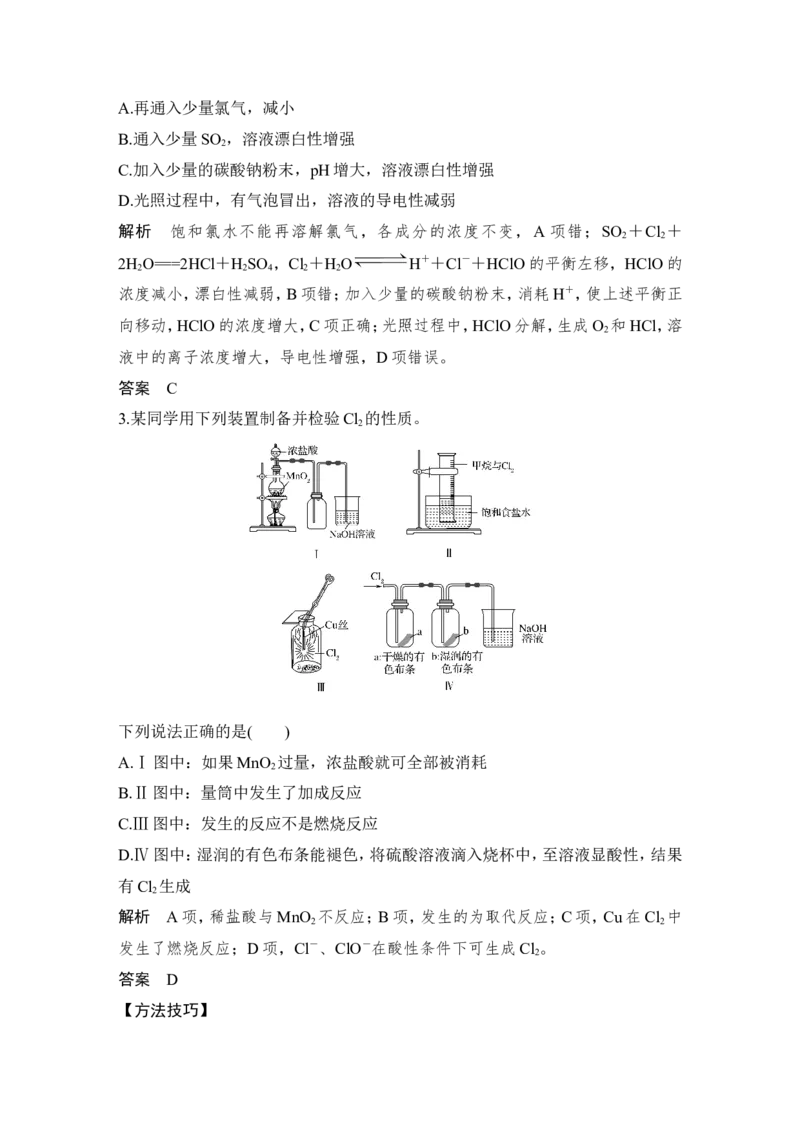
3.某同学用下列装置制备并检验Cl 的性质。
2
下列说法正确的是( )
A.Ⅰ图中:如果MnO 过量,浓盐酸就可全部被消耗
2
B.Ⅱ图中:量筒中发生了加成反应
C.Ⅲ图中:发生的反应不是燃烧反应
D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果
有Cl 生成
2
解析 A项,稀盐酸与MnO 不反应;B项,发生的为取代反应;C项,Cu在Cl 中
2 2
发生了燃烧反应;D项,Cl-、ClO-在酸性条件下可生成Cl 。
2
答案 D
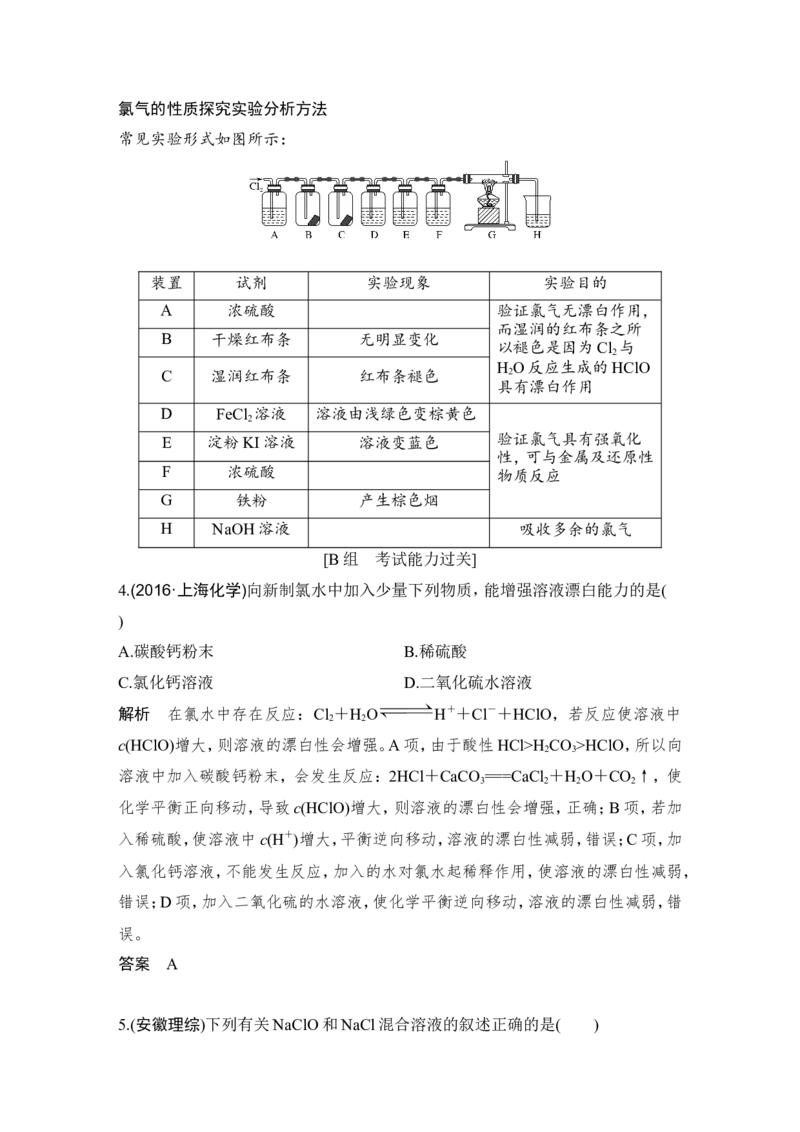
【方法技巧】氯气的性质探究实验分析方法
常见实验形式如图所示:
装置 试剂 实验现象 实验目的
A 浓硫酸 验证氯气无漂白作用,
而湿润的红布条之所
B 干燥红布条 无明显变化
以褪色是因为Cl 与
2
H O反应生成的HClO
C 湿润红布条 红布条褪色 2
具有漂白作用
D FeCl 溶液 溶液由浅绿色变棕黄色
2
E 淀粉KI溶液 溶液变蓝色 验证氯气具有强氧化
性,可与金属及还原性
F 浓硫酸 物质反应
G 铁粉 产生棕色烟
H NaOH溶液 吸收多余的氯气
[B组 考试能力过关]
4.(2016·上海化学)向新制氯水中加入少量下列物质,能增强溶液漂白能力的是(
)
A.碳酸钙粉末 B.稀硫酸
C.氯化钙溶液 D.二氧化硫水溶液
解析 在氯水中存在反应:Cl +H O H++Cl-+HClO,若反应使溶液中
2 2
c(HClO)增大,则溶液的漂白性会增强。A项,由于酸性HCl>H CO >HClO,所以向
2 3
溶液中加入碳酸钙粉末,会发生反应:2HCl+CaCO ===CaCl +H O+CO ↑,使
3 2 2 2
化学平衡正向移动,导致c(HClO)增大,则溶液的漂白性会增强,正确;B项,若加
入稀硫酸,使溶液中c(H+)增大,平衡逆向移动,溶液的漂白性减弱,错误;C项,加
入氯化钙溶液,不能发生反应,加入的水对氯水起稀释作用,使溶液的漂白性减弱,
错误;D项,加入二氧化硫的水溶液,使化学平衡逆向移动,溶液的漂白性减弱,错
误。
答案 A
5.(安徽理综)下列有关NaClO和NaCl混合溶液的叙述正确的是( )A.该溶液中,H+、NH、SO、Br-可以大量共存
B.该溶液中,Ag+、K+、NO、CH CHO可以大量共存
3
C.向该溶液中滴入少量 FeSO 溶液,反应的离子方程式为 2Fe2++ClO-+2H+
4
===Cl-+2Fe3++H O
2
D.向该溶液中加入浓盐酸,每产生1 mol Cl ,转移电子约为6.02×1023个
2
解析 A项ClO-能氧化Br-,且ClO-与H+反应能生成弱电解质HClO,不能大量
共存,错误;B项,Ag+与Cl-能生成难溶物AgCl而不能共存,且ClO-能氧化
CH CHO, 错误;C项,因NaClO水解,溶液呈弱碱性,滴加FeSO 溶液反应的离子
3 4
方程式为2Fe2++ClO-+4OH-+H O===2Fe(OH) ↓+Cl-,错误;D项,加入浓盐
2 3
酸后反应的离子方程式为Cl-+ClO-+2H+===Cl ↑+H O,每生成1 mol Cl ,转
2 2 2
移电子约为6.02×1023个,正确。
答案 D
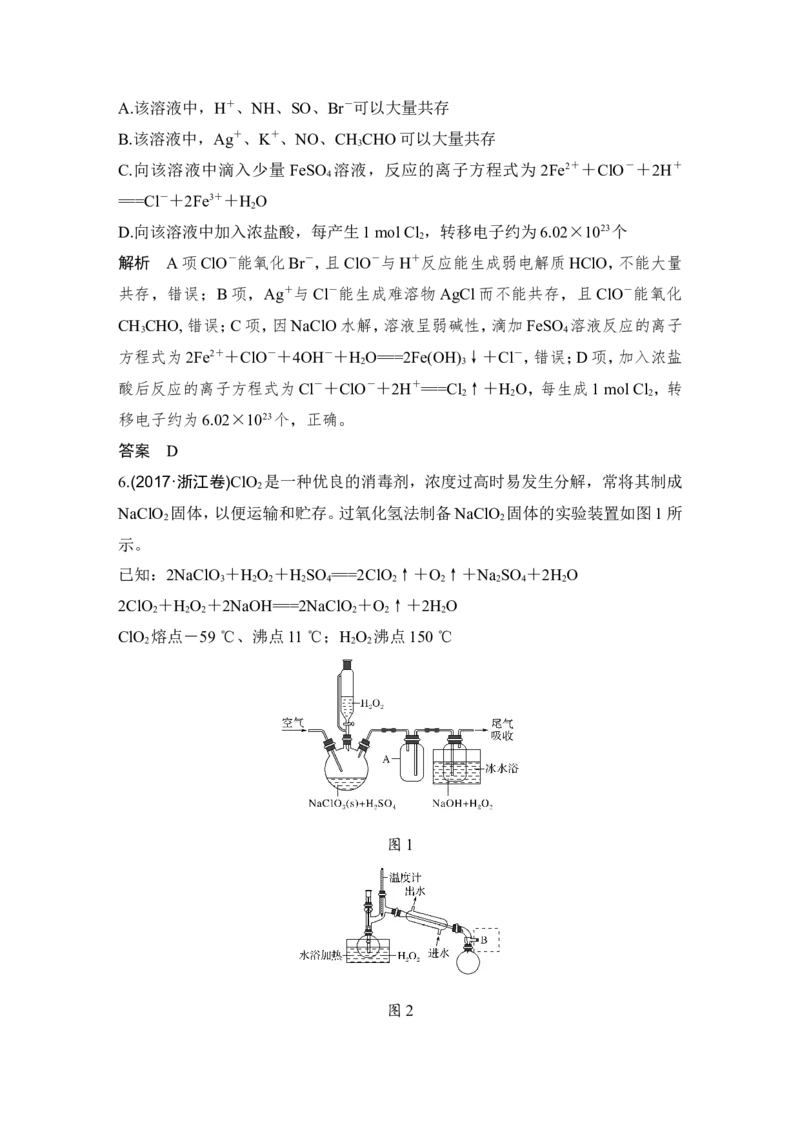
6.(2017·浙江卷)ClO 是一种优良的消毒剂,浓度过高时易发生分解,常将其制成
2
NaClO 固体,以便运输和贮存。过氧化氢法制备NaClO 固体的实验装置如图1所
2 2
示。
已知:2NaClO +H O +H SO ===2ClO ↑+O ↑+Na SO +2H O
3 2 2 2 4 2 2 2 4 2
2ClO +H O +2NaOH===2NaClO +O ↑+2H O
2 2 2 2 2 2
ClO 熔点-59 ℃、沸点11 ℃;H O 沸点150 ℃
2 2 2
图1
图2请回答:
(1)仪器A的作用是____________________________________________;
冰水浴冷却的目的是_______________________________________________
____________________________________________________________(写两种)。
(2) 空 气 流 速 过 快 或 过 慢 , 均 降 低 NaClO 产 率 , 试 解 释 其 原 因
2
____________________________________________________________________。
(3)Cl-存在时会催化ClO 的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO
2 2
的生成速率大大提高,并产生微量氯气。该过程可能经两步反应完成,将其补充完
整:
①___________________________________________________________________
(用离子方程式表示),②H O +Cl ===2Cl-+O +2H+。
2 2 2 2
(4)H O 浓度对反应速率有影响。通过图2所示装置将少量30% H O 溶液浓缩至
2 2 2 2
40% , B 处 应 增 加 一 个 设 备 。 该 设 备 的 作 用 是
____________________________________________________________________,
馏出物是________。
(5)抽滤法分离NaClO 过程中,下列操作不正确的是________。
2
A.为防止滤纸被腐蚀,用玻璃纤维代替滤纸进行抽滤
B.先转移溶液至漏斗,待溶液快流尽时再转移沉淀
C.洗涤沉淀时,应使洗涤剂快速通过沉淀
D.抽滤完毕,断开水泵与吸滤瓶间的橡皮管后,关闭水龙头
解析 (1)A瓶的特点是“短进长出”的空集气瓶,作安全瓶,防止倒吸。ClO 沸点
2
11 ℃,用冰水浴,可以防止挥发。同时防止H O 的分解。(2)空气流速过快,会带出
2 2
ClO 气体,使其与H O 反应不充分;空气流速过慢,ClO 的浓度过高,由题给信息
2 2 2 2
“浓度过高易分解”。(3)Cl-在酸性条件下被ClO氧化为Cl (归中反应)。(4)由题信
2
息“H O 沸点150 ℃”,馏出物为H O。
2 2 2
答案 (1)作安全瓶,防止倒吸 防止ClO 挥发,防止双氧水分解
2
(2)空气流速过快反应不充分,空气流速过慢,ClO 浓度过高易发生分解
2
(3)2ClO+2Cl-+4H+===2ClO ↑+Cl ↑+2H O
2 2 2
(4)降低体系压强,减少双氧水分解 H O (5)C
2考点二 氯气的实验室制法
(频数:★★☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 氯
气的制法的常考点有:制备原理,注意除二氧化锰外,重铬酸钾、高锰酸钾、氯酸钾
次氯酸钙、二氧化铅等氧化剂也能氧化浓盐酸制取氯气;实验装置分析,包括发生
装置、净化装置、尾气处理装置等,以氯气的实验室制备、性质探究为素材的实验
题目在高考实验类试题中占有较大的比重,复习时加以关注。
1.实验装置
2.制取过程INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
充分利用早读10分钟,掌握一些识记的知识要点。
其他制取Cl 的反应原理:
2
①14HCl(浓)+K Cr O ===2KCl+2CrCl +7H O+3Cl ↑
2 2 7 3 2 2
②16HCl(浓)+2KMnO ===2KCl+2MnCl +8H O+5Cl ↑
4 2 2 2
③6HCl(浓)+KClO ===KCl+3H O+3Cl ↑
3 2 2
④4HCl(浓)+Ca(ClO) ===CaCl +2H O+2Cl ↑
2 2 2 2
⑤PbO +4HCl(浓)=====PbCl +Cl ↑+2H O
2 2 2 2
3.注意事项(1)必须用浓盐酸,MnO 与稀盐酸不反应。
2
(2)为了减少制得的Cl 中HCl的含量,所以加热温度不宜过高,减少HCl的挥发。
2
(3)实验结束后,先使反应停止并排出装置中残留的Cl ,再拆卸装置,避免污染空
2
气。
(4)尾气吸收时,不能用澄清石灰水吸收Cl ,因为溶液中Ca(OH) 浓度小,吸收不
2 2
完全。
(5)酸化KMnO 溶液,用的是H SO 酸化而不是盐酸。
4 2 4
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)将Cl 与HCl混合气体通过饱和食盐水可得到纯净的Cl (×)
2 2
(2)为了减少制得的Cl 中HCl的含量,所以加热温度不宜过高,以减少HCl的挥
2
发(√)
(3)除去Cl 中少量HCl气体,可用饱和食盐水,也可用饱和碳酸氢钠溶液(×)
2
(4)过量浓盐酸与一定量的二氧化锰反应,MnO 能完全反应(√)
2
(5)检验氯气可用湿润的淀粉碘化钾试纸(√)
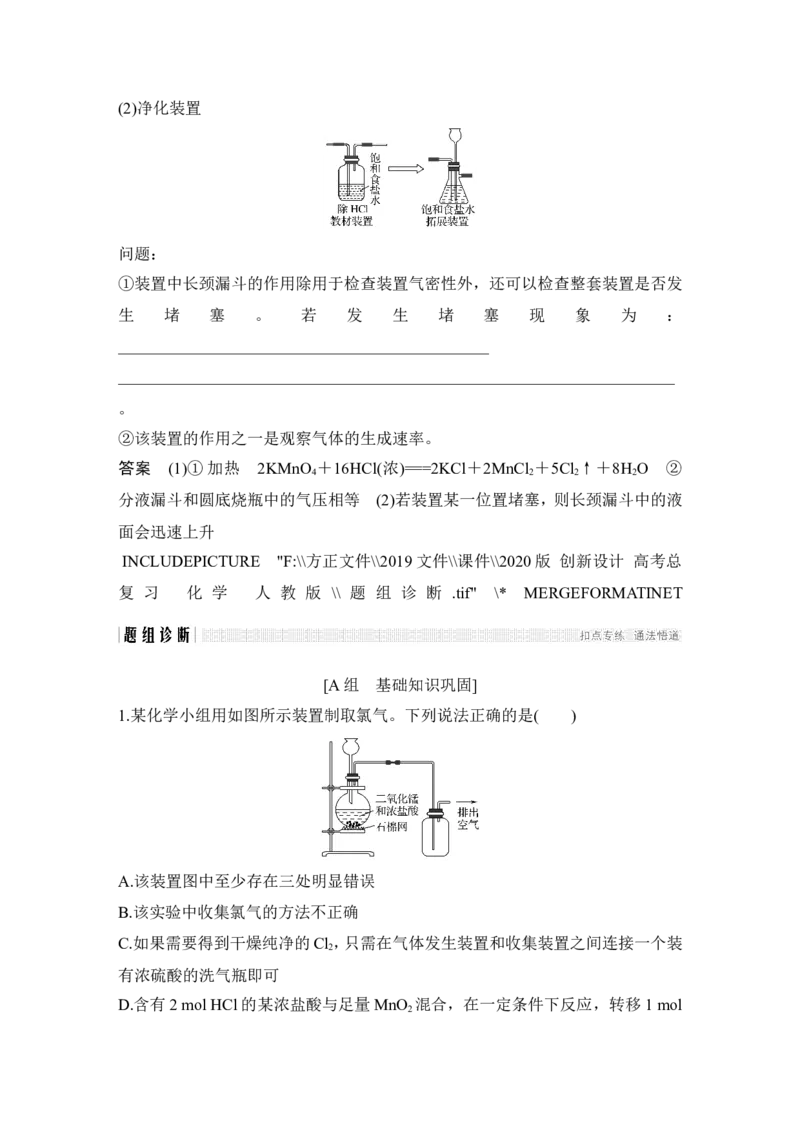
2.(教材制备装置创新探究题)
(1)制备装置
问题:
①用 KMnO 代替 MnO ,常温下即可反应,故不需要________,反应原理为
4 2
______________________________________________________________________
_____________________________________________________________________
。
②图中橡皮管a的作用是使__________________________________________
___________________________________________________________________,
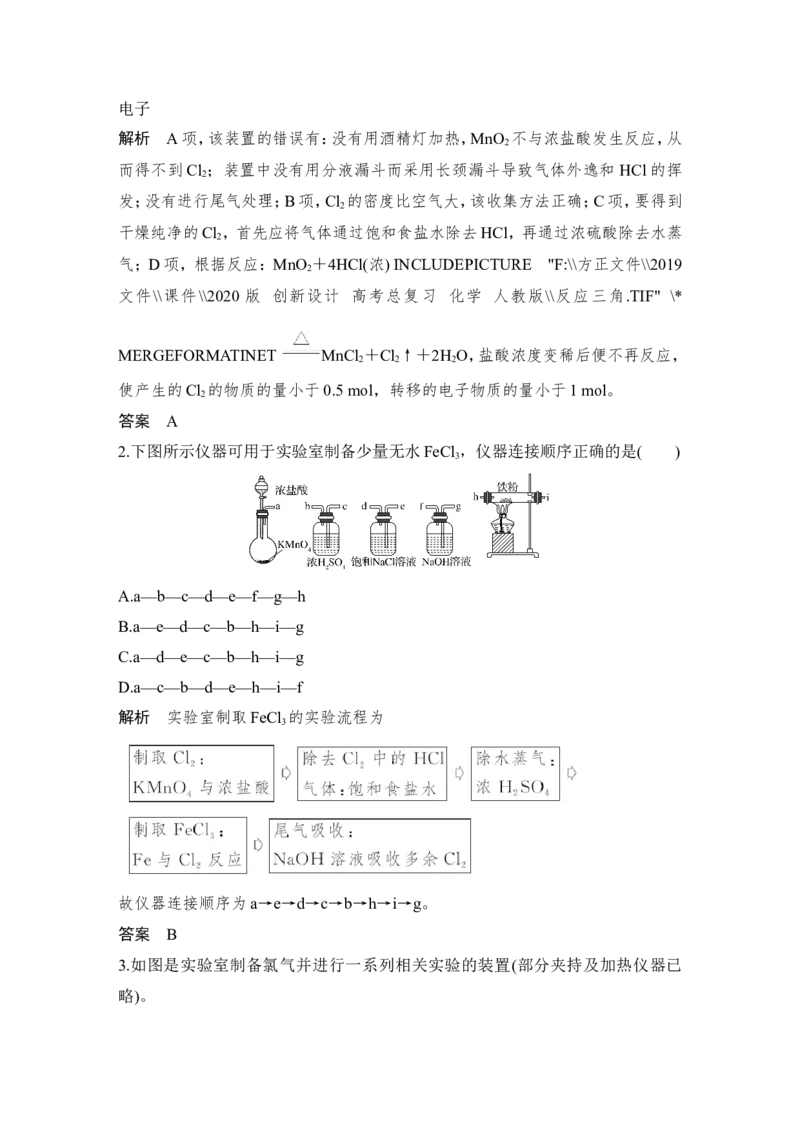
便于分液漏斗中的液体流下。(2)净化装置
问题:
①装置中长颈漏斗的作用除用于检查装置气密性外,还可以检查整套装置是否发
生 堵 塞 。 若 发 生 堵 塞 现 象 为 :
______________________________________________
_____________________________________________________________________
。
②该装置的作用之一是观察气体的生成速率。
答案 (1)①加热 2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl ↑+8H O ②
4 2 2 2
分液漏斗和圆底烧瓶中的气压相等 (2)若装置某一位置堵塞,则长颈漏斗中的液
面会迅速上升
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
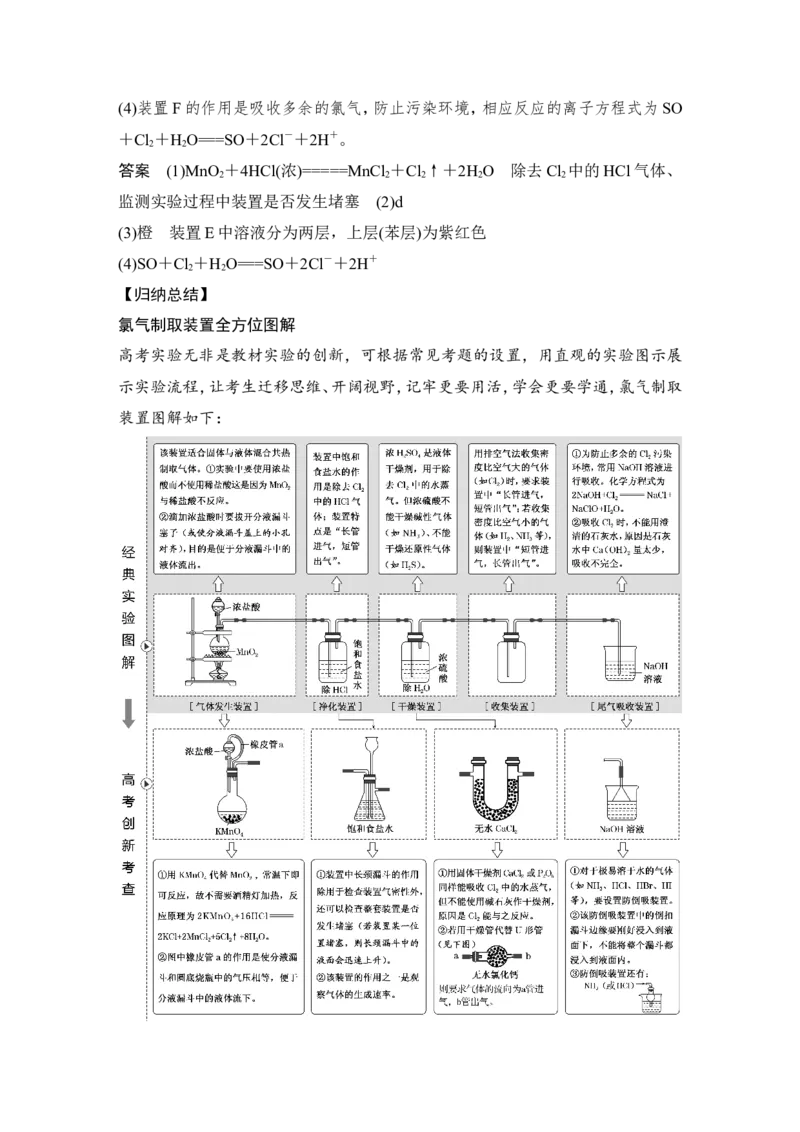
1.某化学小组用如图所示装置制取氯气。下列说法正确的是( )
A.该装置图中至少存在三处明显错误
B.该实验中收集氯气的方法不正确
C.如果需要得到干燥纯净的Cl ,只需在气体发生装置和收集装置之间连接一个装
2
有浓硫酸的洗气瓶即可
D.含有2 mol HCl的某浓盐酸与足量MnO 混合,在一定条件下反应,转移1 mol
2电子
解析 A项,该装置的错误有:没有用酒精灯加热,MnO 不与浓盐酸发生反应,从
2
而得不到Cl ;装置中没有用分液漏斗而采用长颈漏斗导致气体外逸和 HCl的挥
2
发;没有进行尾气处理;B项,Cl 的密度比空气大,该收集方法正确;C项,要得到
2
干燥纯净的Cl ,首先应将气体通过饱和食盐水除去HCl,再通过浓硫酸除去水蒸
2
气;D项,根据反应:MnO +4HCl(浓) INCLUDEPICTURE "F:\\方正文件\\2019
2
文件\\课件\\2020 版 创新设计 高考总复习 化学 人教版\\反应三角.TIF" \*
MERGEFORMATINET MnCl +Cl ↑+2H O,盐酸浓度变稀后便不再反应,
2 2 2
使产生的Cl 的物质的量小于0.5 mol,转移的电子物质的量小于1 mol。
2
答案 A
2.下图所示仪器可用于实验室制备少量无水FeCl ,仪器连接顺序正确的是( )
3
A.a—b—c—d—e—f—g—h
B.a—e—d—c—b—h—i—g
C.a—d—e—c—b—h—i—g
D.a—c—b—d—e—h—i—f
解析 实验室制取FeCl 的实验流程为
3
故仪器连接顺序为a→e→d→c→b→h→i→g。
答案 B
3.如图是实验室制备氯气并进行一系列相关实验的装置(部分夹持及加热仪器已
略)。(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关反应的化学方程式为
____________________________________________________________________。
装置B的作用是_____________________________________________________。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放
入的物质为________(填字母)。
选项 a b c d
干燥的有色 干燥的有色 湿润的有 湿润的有
Ⅰ
布条 布条 色布条 色布条
无水氯化
Ⅱ 碱石灰 硅胶 浓硫酸
钙
湿润的有色 湿润的有色 干燥的有 干燥的有
Ⅲ
布条 布条 色布条 色布条
(3)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入少量氯
气时,可以看到无色溶液逐渐变为________色,说明氯的非金属性大于溴。打开活
塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是
_____________________________________________________________________
。
(4)装置F中用足量的Na SO 溶液吸收多余氯气,试写出相应反应的离子方程式:
2 3
____________________________________________________________________。
解 析 (1)A 装 置 中 固 体 药 品 为 MnO , 其 化 学 方 程 式 为 MnO +
2 2
4HCl(浓)=====MnCl +Cl ↑+2H O;装置B用饱和食盐水吸收氯化氢;如果实验
2 2 2
过程中装置C发生堵塞,则装置B中长颈漏斗中的液面就会上升,所以装置B的
作用是既能除去氯气中混有的氯化氢,还能监测实验过程中装置C是否发生堵塞
(2)装置C的作用是验证氯气是否具有漂白性,Ⅰ处是湿润的有色布条,则Ⅱ处应
加入固态干燥剂且不能吸收氯气,Ⅲ处放置干燥的有色布条。
(3)设计装置D、E的目的是比较氯、溴、碘的非金属性,利用氯气、溴、碘之间的置
换反应验证。(4)装置F的作用是吸收多余的氯气,防止污染环境,相应反应的离子方程式为SO
+Cl +H O===SO+2Cl-+2H+。
2 2
答案 (1)MnO +4HCl(浓)=====MnCl +Cl ↑+2H O 除去Cl 中的HCl气体、
2 2 2 2 2
监测实验过程中装置是否发生堵塞 (2)d
(3)橙 装置E中溶液分为两层,上层(苯层)为紫红色
(4)SO+Cl +H O===SO+2Cl-+2H+
2 2
【归纳总结】
氯气制取装置全方位图解
高考实验无非是教材实验的创新,可根据常见考题的设置,用直观的实验图示展
示实验流程,让考生迁移思维、开阔视野,记牢更要用活,学会更要学通,氯气制取
装置图解如下:[B组 考试能力过关]
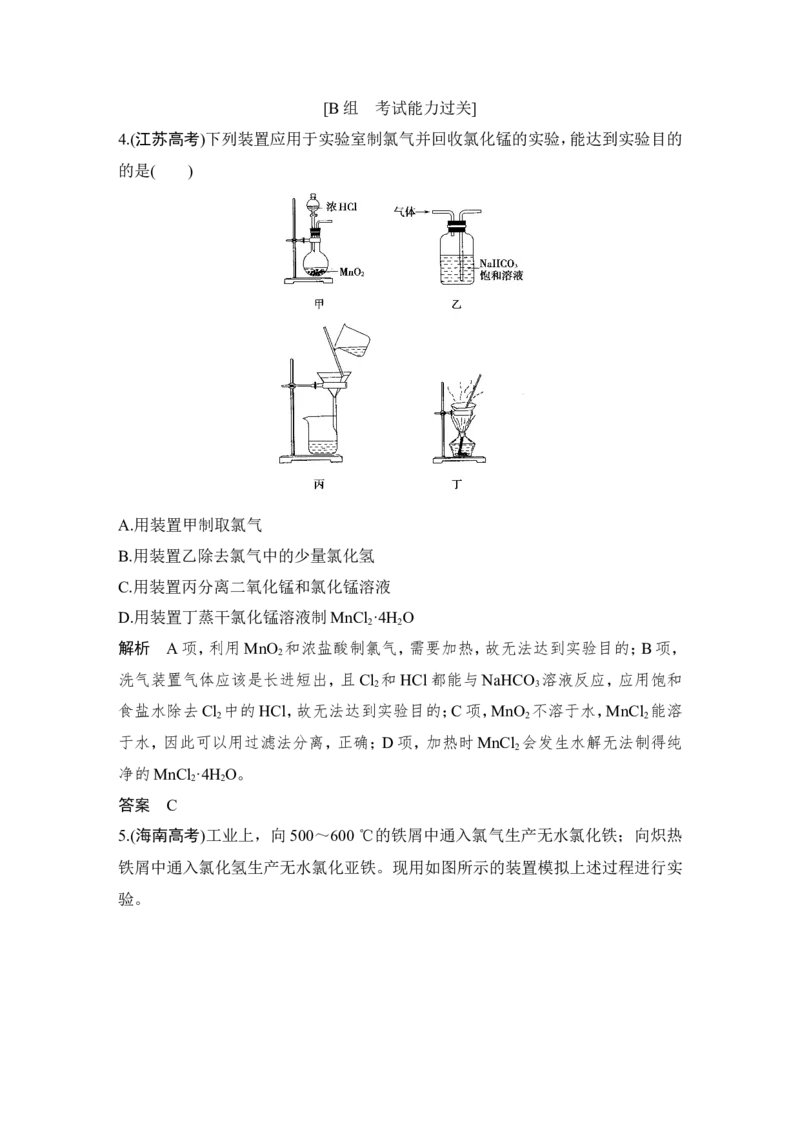
4.(江苏高考)下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的
的是( )
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl ·4H O
2 2
解析 A项,利用MnO 和浓盐酸制氯气,需要加热,故无法达到实验目的;B项,
2
洗气装置气体应该是长进短出,且Cl 和HCl都能与NaHCO 溶液反应,应用饱和
2 3
食盐水除去Cl 中的HCl,故无法达到实验目的;C项,MnO 不溶于水,MnCl 能溶
2 2 2
于水,因此可以用过滤法分离,正确;D项,加热时MnCl 会发生水解无法制得纯
2
净的MnCl ·4H O。
2 2
答案 C
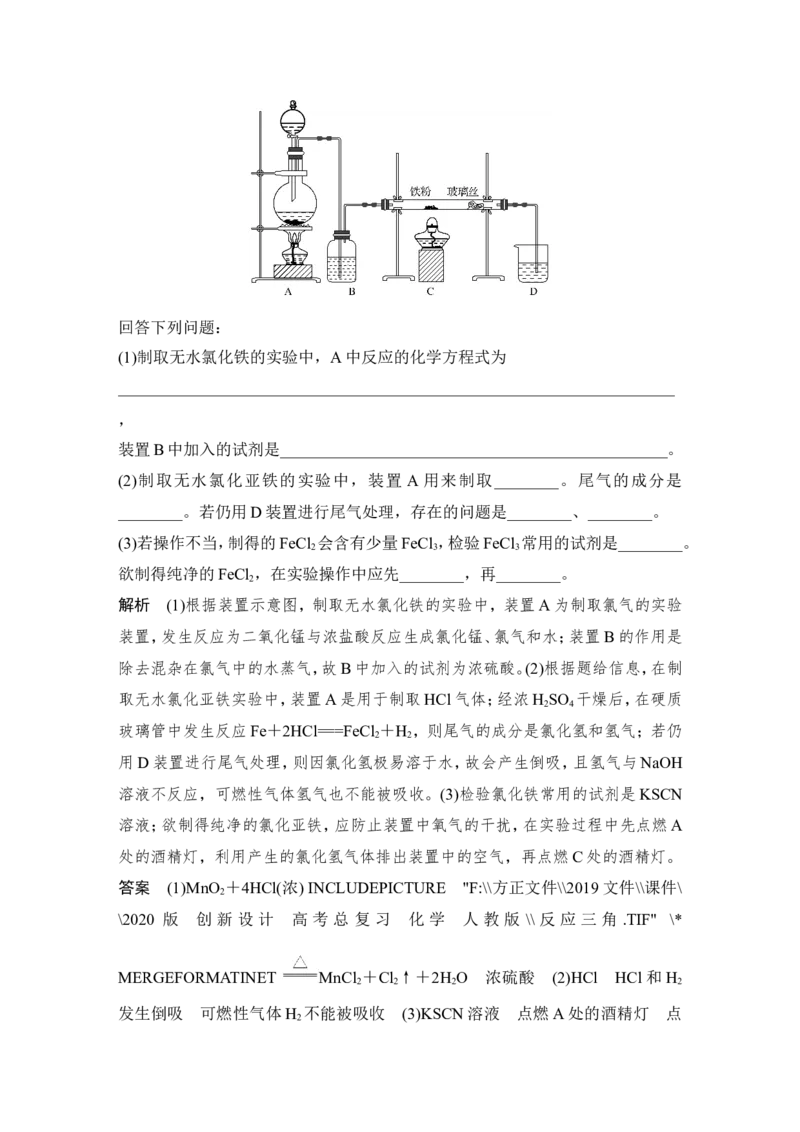
5.(海南高考)工业上,向500~600 ℃的铁屑中通入氯气生产无水氯化铁;向炽热
铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行实
验。回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为
_____________________________________________________________________
,
装置B中加入的试剂是________________________________________________。
(2)制取无水氯化亚铁的实验中,装置 A 用来制取________。尾气的成分是
________。若仍用D装置进行尾气处理,存在的问题是________、________。
(3)若操作不当,制得的FeCl 会含有少量FeCl ,检验FeCl 常用的试剂是________。
2 3 3
欲制得纯净的FeCl ,在实验操作中应先________,再________。
2
解析 (1)根据装置示意图,制取无水氯化铁的实验中,装置A为制取氯气的实验
装置,发生反应为二氧化锰与浓盐酸反应生成氯化锰、氯气和水;装置B的作用是
除去混杂在氯气中的水蒸气,故B中加入的试剂为浓硫酸。(2)根据题给信息,在制
取无水氯化亚铁实验中,装置A是用于制取HCl气体;经浓H SO 干燥后,在硬质
2 4
玻璃管中发生反应Fe+2HCl===FeCl +H ,则尾气的成分是氯化氢和氢气;若仍
2 2
用D装置进行尾气处理,则因氯化氢极易溶于水,故会产生倒吸,且氢气与NaOH
溶液不反应,可燃性气体氢气也不能被吸收。(3)检验氯化铁常用的试剂是KSCN
溶液;欲制得纯净的氯化亚铁,应防止装置中氧气的干扰,在实验过程中先点燃A
处的酒精灯,利用产生的氯化氢气体排出装置中的空气,再点燃C处的酒精灯。
答案 (1)MnO +4HCl(浓) INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\
2
\2020 版 创 新 设 计 高 考 总 复 习 化 学 人 教 版 \\ 反 应 三 角 .TIF" \*
MERGEFORMATINET MnCl +Cl ↑+2H O 浓硫酸 (2)HCl HCl和H
2 2 2 2
发生倒吸 可燃性气体H 不能被吸收 (3)KSCN溶液 点燃A处的酒精灯 点
2燃C处的酒精灯考点三 卤素的来源及性质
(频数:★☆☆ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点应掌握:海水中提取氯、溴、碘的化学工艺;借助元素周期律掌握卤素的递变
规律;卤素离子的检验。特别是卤素离子的检验在高考中经常涉及,复习时加以关
注。
1.卤素的来源
(1)氯的提取——氯碱工业
海水―→粗盐――→饱和食盐水――→
化学方程式为 2NaCl + 2H O ===== 2NaOH + H ↑ + C l ↑。
2 2 2
(2)海水提取溴
①流程
②发生反应的化学方程式
a. 2NaBr + Cl == =Br + 2NaC l;
2 2
b.Br + SO + 2H O == =2HBr + H SO ;
2 2 2 2 4c. 2HBr + Cl == =2HCl + Br 。
2 2
(3)海带中提取碘
①流程
②发生反应的离子方程式:Cl + 2 I - == = I + 2C l - 。
2 2
2.卤素单质的性质
(1)递变性
颜色
熔、沸点
密度 ――→
水溶性
氧化性
还原性(X -) ――→
(2)相似性
①都能与大多数金属反应: 2Fe + 3Br == =2FeBr ;
2 3
I + F e == =Fe I ;
2 2
②都能与H 反应:H + X == =2HX ;
2 2 2
③都能与H O反应:X + H O HX + HXO (F 例外);
2 2 2 2④都能与碱液反应:X + 2NaOH == =NaX + NaXO + H O(F 例外)。
2 2 2
(3)特殊性
①无正价,非金属性最强,F-的还原性最弱
氟 ②2F +2H O===4HF+O ,与H 反应在暗处即爆炸
2 2 2 2
③氢氟酸是弱酸,能腐蚀玻璃,故应保存在塑料瓶中
①Br 是深红棕色液体,易挥发
2
溴
②盛溴的试剂瓶中加水,进行水封,保存液溴不能用橡胶塞
①淀粉遇I 变蓝色
2
碘
②I 加热时易升华
2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
(1)卤族元素单质能将同主族原子序数大的元素从其盐溶液中置换出来,但氟不能
进行相应的置换,原因是F 能与水发生反应。
2
(2)卤族元素的单质F 、Cl 、Br 均能将Fe氧化为Fe3+,而I 只能将铁氧化为
2 2 2 2
Fe2+。
(3)卤素氢化物的两大性质:①酸性:氢氟酸是弱酸,盐酸、氢溴酸、氢碘酸是强酸。
②沸点:HClBr >I 的是( )
2 2 2
A.氯水分别滴入KBr、NaI溶液中颜色加深,而溴水滴入NaCl溶液中无明显变化,
滴入KI淀粉溶液中,溶液变蓝
B.H 和Cl 的混合气体光照爆炸,H 和Br 的混合气体加热才能反应,而H 和I 反
2 2 2 2 2 2
应更困难
C.Fe分别与Cl 、Br 、I 反应生成Fe的化合物的化合价高低
2 2 2
D.HCl、HBr、HI的热稳定性越来越差
答案 C
3.(思维探究题)设计实验检验食用盐是否为加碘盐,并写出所发生反应的离子方程
式。___________________________________________________________
_______________________________________________________________。
答案 将少量食用盐溶于白醋中,然后滴到淀粉KI试纸上,若试纸变蓝色,说明
此食用盐为加碘食盐。(其他合理答案也可)IO+5I-+6H+===3I +3H O
2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2019·盐城期中)利用海洋资源获得的部分物质如图所示,下列有关说法正确的
是( )
A.在化学反应中,H O可转变为D O
2 2
B.“加碘食盐”生产中碘添加剂为单质I
2
C.实验室用带玻璃塞的棕色瓶贮存液溴
D.电解饱和MgCl 溶液时在阴极得到Mg
2
解析 海水中存在重水,海水蒸馏是物理变化不能实现水变化为重水的分子变化,
故A错误;加碘食盐是添加了碘酸钾,不是碘单质,故B错误;溴单质具有强氧化
性和腐蚀性,不能用橡胶塞而用玻璃塞,易挥发,密度比水大,所以应保存在棕色
瓶中,避免光照,放在阴凉处,同时在液溴表层加水,就是所谓的液封,防止其挥发
实验室用带玻璃塞的棕色瓶贮存液溴,故C正确;依据电解原理分析,电解氯化镁
溶液,阳离子是氢离子在阴极得到电子生成氢气,镁离子不能放电,工业上是通过
电解熔融氯化镁得到金属镁,故D错误。
答案 C
2.下列叙述中正确的是( )
A.加碘食盐可用淀粉溶液检验其中的碘
B.某溶液加入氯水后振荡,再加入CCl 振荡,下层显示紫色,说明原溶液中一定含
4
有I-
C.某溶液中滴加AgNO 溶液和稀硝酸,产生淡黄色沉淀,说明原溶液中一定含有
3
Br-D.要除去KBr溶液中混有的单质Br ,可用酒精萃取除去
2
解析 食盐加碘加入的是KIO ,KIO 不能使淀粉变蓝,A错误。B中若原溶液中含
3 3
有I ,也会产生同样现象,B错误。由于酒精与水互溶,因此不能用酒精萃取溶液
2
中的Br ,D错误。
2
答案 C
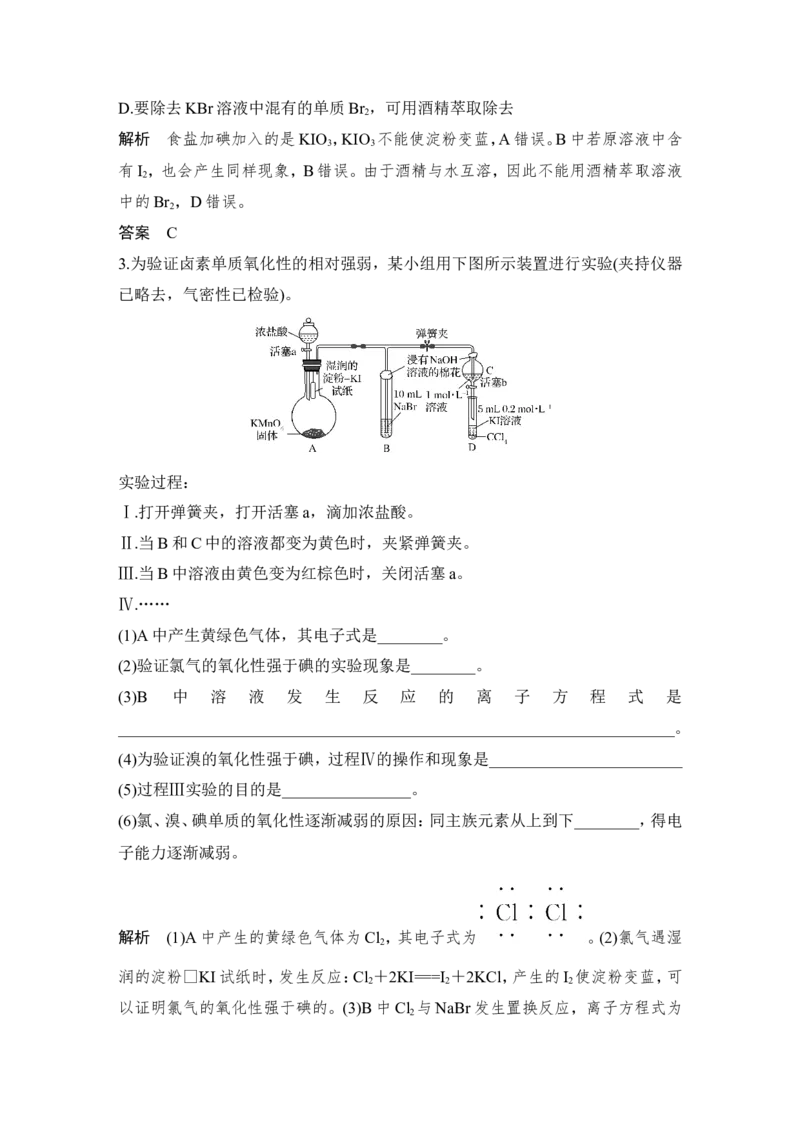
3.为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器
已略去,气密性已检验)。
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是________。
(2)验证氯气的氧化性强于碘的实验现象是________。
(3)B 中 溶 液 发 生 反 应 的 离 子 方 程 式 是
_____________________________________________________________________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是________________________
(5)过程Ⅲ实验的目的是________________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下________,得电
子能力逐渐减弱。
解析 (1)A中产生的黄绿色气体为Cl ,其电子式为 。(2)氯气遇湿
2
润的淀粉KI试纸时,发生反应:Cl +2KI===I +2KCl,产生的I 使淀粉变蓝,可
2 2 2
以证明氯气的氧化性强于碘的。(3)B中Cl 与NaBr发生置换反应,离子方程式为
2Cl +2Br-===2Cl-+Br 。(4)C中NaBr与氯气反应生成NaCl和Br ,将C中溶液
2 2 2
滴入D中,振荡,发生反应:Br +2KI===I +2KBr,静置后D中溶液分层,下层为
2 2
碘的四氯化碳溶液,显紫红色,可以说明溴的氧化性强于碘的。(5)过程Ⅲ主要是为
了确认C的黄色溶液中无Cl ,排除对溴置换碘实验的干扰。(6)氯、溴、碘单质的氧
2
化性逐渐减弱,是因为从Cl到I,原子半径逐渐增大,得电子能力逐渐减弱。
答案 (1)
(2)淀粉KI试纸变蓝
(3)Cl +2Br-===Br +2Cl-
2 2
(4)打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静置后CCl
4
层溶液变为紫红色
(5)确认C的黄色溶液中无Cl ,排除Cl 对溴置换碘实验的干扰
2 2
(6)原子半径逐渐增大
【思维建模】
海水中物质提取的思路
海水中提取溴和碘的反应都是将其-1价离子氧化成单质。涉及工业实际,最主要
的问题是如何将大量海水中分布很稀的元素富集起来。溴的制取一般是氧化→吹
出→吸收→再氧化的路线,碘一般是由海带提取,主要是灼烧→溶解→过滤→氧
化→萃取的路线。工艺模式如图所示:
[B组 考试能力过关]
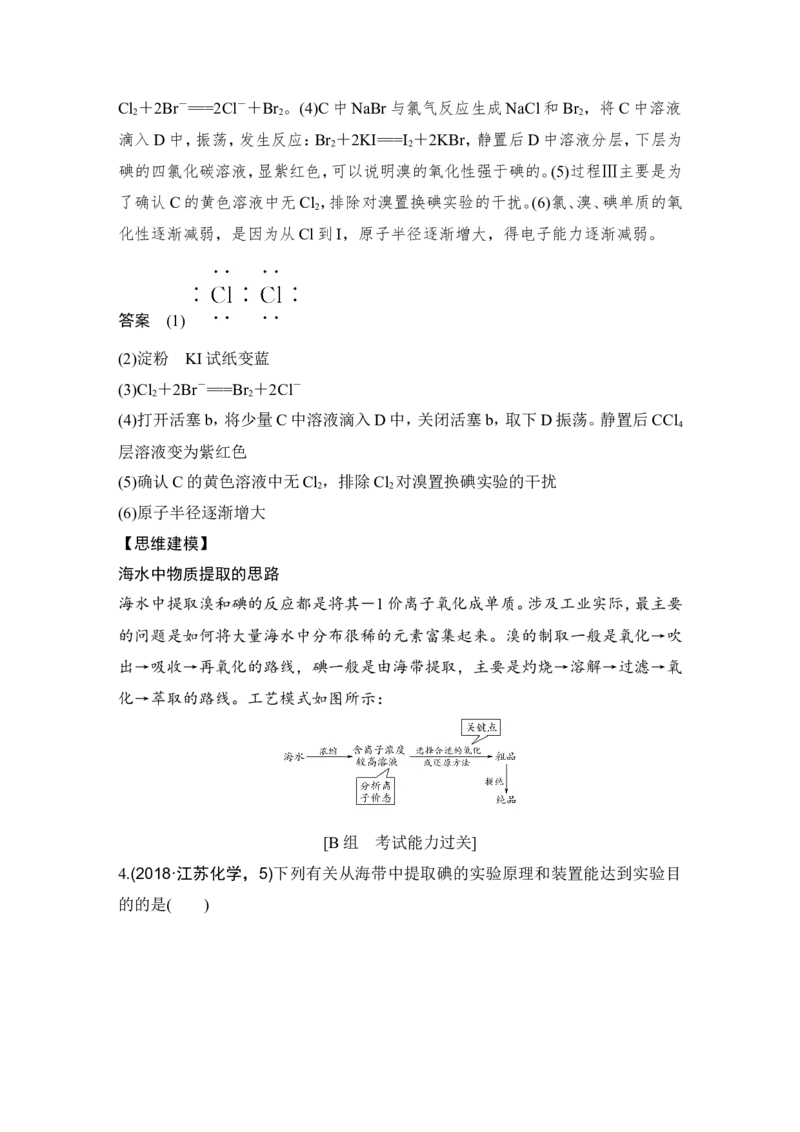
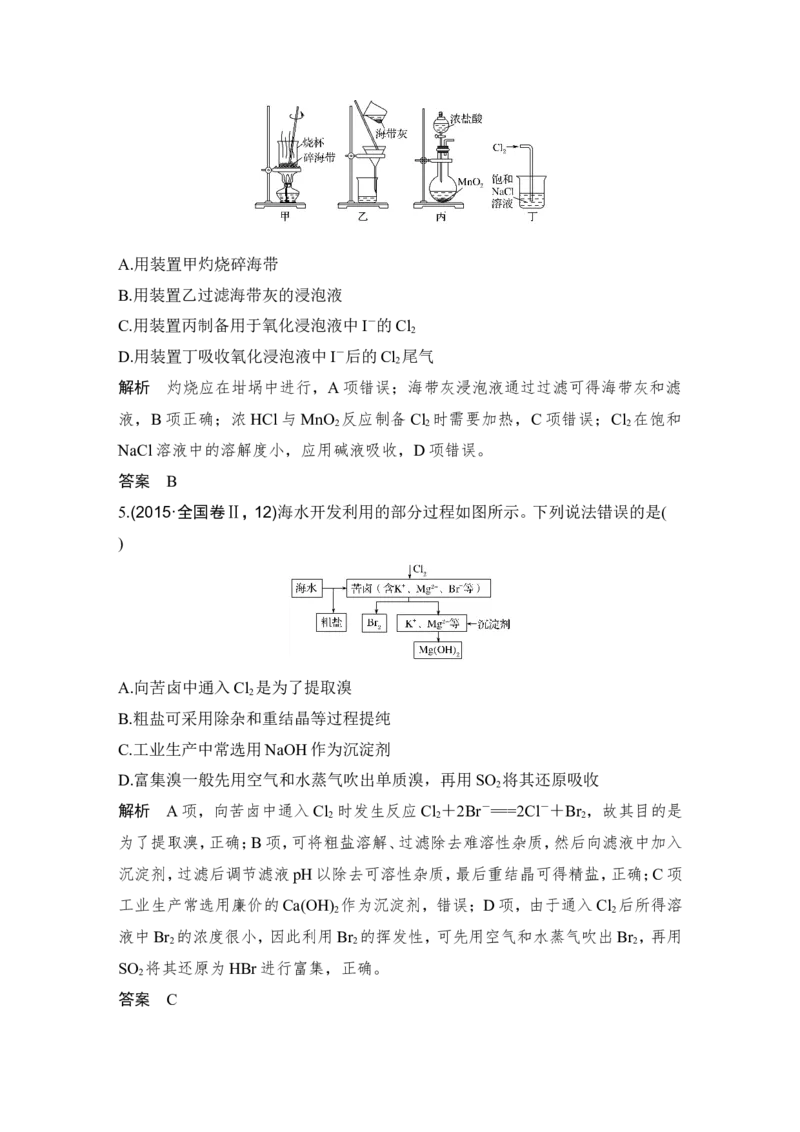
4.(2018·江苏化学,5)下列有关从海带中提取碘的实验原理和装置能达到实验目
的的是( )A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中I-的Cl
2
D.用装置丁吸收氧化浸泡液中I-后的Cl 尾气
2
解析 灼烧应在坩埚中进行,A项错误;海带灰浸泡液通过过滤可得海带灰和滤
液,B项正确;浓HCl与MnO 反应制备Cl 时需要加热,C项错误;Cl 在饱和
2 2 2
NaCl溶液中的溶解度小,应用碱液吸收,D项错误。
答案 B
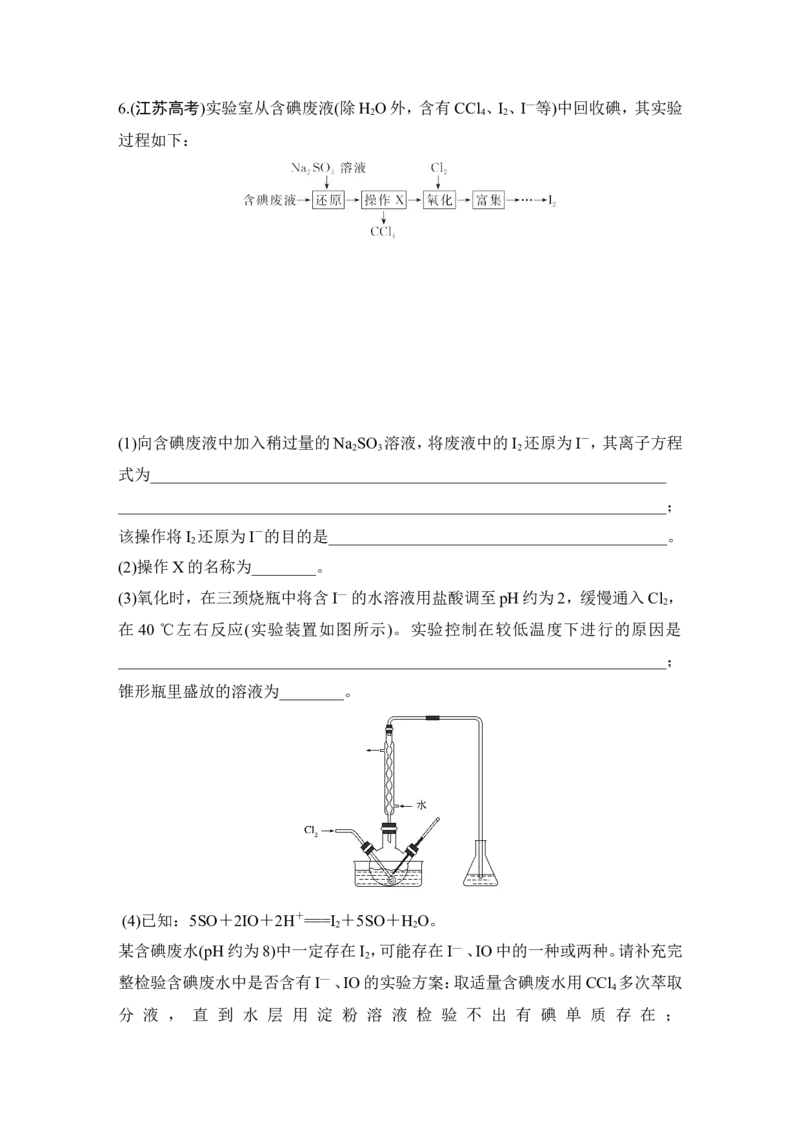
5.(2015·全国卷Ⅱ,12)海水开发利用的部分过程如图所示。下列说法错误的是(
)
A.向苦卤中通入Cl 是为了提取溴
2
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO 将其还原吸收
2
解析 A项,向苦卤中通入Cl 时发生反应Cl +2Br-===2Cl-+Br ,故其目的是
2 2 2
为了提取溴,正确;B项,可将粗盐溶解、过滤除去难溶性杂质,然后向滤液中加入
沉淀剂,过滤后调节滤液pH以除去可溶性杂质,最后重结晶可得精盐,正确;C项
工业生产常选用廉价的Ca(OH) 作为沉淀剂,错误;D项,由于通入Cl 后所得溶
2 2
液中Br 的浓度很小,因此利用Br 的挥发性,可先用空气和水蒸气吹出Br ,再用
2 2 2
SO 将其还原为HBr进行富集,正确。
2
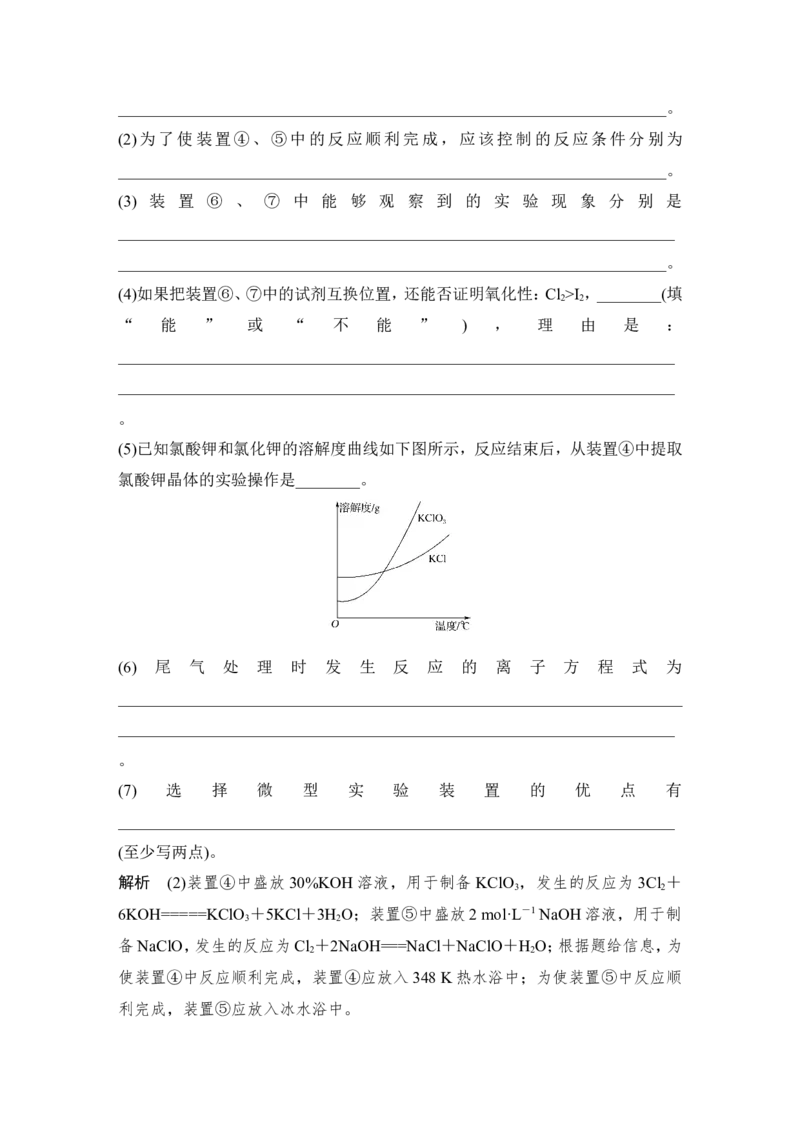
答案 C6.(江苏高考)实验室从含碘废液(除H O外,含有CCl 、I 、I—等)中回收碘,其实验
2 4 2
过程如下:
(1)向含碘废液中加入稍过量的Na SO 溶液,将废液中的I 还原为I-,其离子方程
2 3 2
式为________________________________________________________________
____________________________________________________________________;
该操作将I 还原为I-的目的是__________________________________________。
2
(2)操作X的名称为________。
(3)氧化时,在三颈烧瓶中将含I— 的水溶液用盐酸调至pH约为2,缓慢通入Cl ,
2
在 40 ℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是
____________________________________________________________________;
锥形瓶里盛放的溶液为________。
(4)已知:5SO+2IO+2H+===I +5SO+H O。
2 2
某含碘废水(pH约为8)中一定存在I ,可能存在I— 、IO中的一种或两种。请补充完
2
整检验含碘废水中是否含有I— 、IO的实验方案:取适量含碘废水用CCl 多次萃取
4
分 液 , 直 到 水 层 用 淀 粉 溶 液 检 验 不 出 有 碘 单 质 存 在 ;______________________________________________________________________
_____________________________________________________________________
_____________________________________________________________________
_____________________________________________________________________
。
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl 溶液、Na SO 溶液。
3 2 3
解析 (1)SO 具有还原性,I 具有氧化性,二者发生氧化还原反应:SO+I +
2 2
H O===SO+2I-+2H+。由流程图可知还原I 的下一步操作是分离出CCl ,由于I
2 2 4 2
易溶于CCl 而难溶于水,而I-易溶于水而难溶于CCl ,所以将I 还原为I-的目的
4 4 2
是使CCl 中的I 进入水溶液中。(2)由于CCl 与水互不相溶,故分离出CCl 的操作
4 2 4 4
X为分液。(3)若温度高了,氯气在水中的溶解度小,不利于将I-氧化为I ,且生成
2
的I 易升华,也可能进一步被氯气氧化为其他物质。锥形瓶中液体的作用是吸收
2
没有反应完的氯气或升华出去的碘蒸气,故应用氢氧化钠溶液吸收。(4)检验I-应
加入氧化剂(如Fe3+、H O 等)将I-氧化成I ,再用淀粉溶液检验I 的存在;由题给
2 2 2 2
反应可知,检验IO应利用SO将IO还原为I ,再用淀粉溶液检验I 的存在。
2 2
答案 (1)SO+I +H O===2I-+SO+2H+ 使CCl 中的碘进入水层
2 2 4
(2)分液
(3)使氯气在溶液中有较大的溶解度(或防止 I 升华或防止 I 进一步被氧化)
2 2
NaOH溶液
(4)从水层取少量溶液,加入1~2 mL淀粉溶液,加盐酸酸化,滴加FeCl 溶液,若
3
溶液变蓝,说明废水中含有I-;若溶液不变蓝,说明废水中不含有I-。另从水层取
少量溶液,加入1~2 mL淀粉溶液,加盐酸酸化,滴加Na SO 溶液,若溶液变蓝,
2 3
说明废水中含有IO;若溶液不变蓝,说明废水中不含有IO
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET
[A级 全员必做题]
1.下列有关物质的性质及应用说法正确的是( )
A.干燥的Cl 和氯水均能使鲜花褪色
2B.久置的氯水仍具有漂白性
C.明矾和漂白粉常用于自来水的处理,两者的作用原理相同
D.无色溶液C加入AgNO 溶液,产生白色沉淀,再加入稀盐酸,沉淀不消失,则C
3
必含Cl-
解析 鲜花中含有水分,氯气与水发生反应 Cl +H O HCl+HClO,产生
2 2
HClO,氯水中也含HClO,HClO具有漂白作用,因此可以使鲜花褪色,A项正确;
久置的氯水最终变为稀盐酸,B项错误;明矾溶于水形成胶体利用胶体的吸附性
净水,漂白粉是利用其强氧化性杀菌消毒,C项错误;加入稀盐酸时混入了Cl-,无
法确定原溶液中是否含有Cl-,D项错误。
答案 A
2.下列说法正确的是( )
①氯气的性质活泼,它与氢气混合后立即发生爆炸 ②实验室制取氯气时,为了
防止环境污染,多余的氯气可以用氢氧化钙溶液吸收 ③新制氯水的氧化性强于
久置氯水的 ④检验 HCl气体中是否混有 Cl ,方法是将气体通入硝酸银溶液
2
⑤除去HCl气体中的Cl ,可将气体通入饱和食盐水中
2
A.①②③ B.②③④
C.③ D.③⑤
解析 氯气与氢气混合,达到爆炸极限,在光照的条件下才能发生爆炸,①错,氢
氧化钙溶液中溶质含量少,实验中常用氢氧化钠溶液吸收多余的氯气,②错,排除
A、B项;HCl气体与AgNO 溶液可产生沉淀,④错;将气体通入饱和食盐水中,除
3
去的是HCl气体,而不是Cl ,⑤错,排除D项。
2
答案 C
3.(2018·山东淄博模拟)下列对氯气及其化合物的说法正确的是( )
A.通过化合反应不能制得氯化亚铁
B.用pH试纸测得氯水的pH=4
C.溴化钠溶液中加入少量新制氯水振荡,再加入少量四氯化碳振荡,静置后,上层
颜色变浅,下层颜色变橙红色
D.由 Ca(ClO) +CO +H O===CaCO ↓+2HClO 可推出 Ca(ClO) +SO +
2 2 2 3 2 2
H O===CaSO ↓+2HClO
2 3
解析 由Fe+2FeCl ===3FeCl 知,A项错误;氯水中的HClO有漂白性,可漂白
3 2pH试纸,B项错误;NaBr与氯水中的Cl 反应:2NaBr+Cl ===2NaCl+Br ,Br 被
2 2 2 2
CCl 萃取,故上层颜色变浅,下层颜色变为橙红色,C项正确;D项中的CaSO 会
4 3
被HClO氧化为CaSO ,错误。
4
答案 C
4.(2018·开封模拟)溴与氯的单质在性质上具有很大的相似性,但Cl 比Br 的活泼
2 2
性强,下面是根据氯气的性质,对溴单质性质的预测,其中不正确的是( )
A.溴单质可以和烧碱溶液反应
B.溴的单质只具有强的氧化性
C.溴与氢气在一定条件下反应能生成溴化氢
D.溴离子可以用硝酸酸化的AgNO 溶液来检验
3
解析 Br 与Cl 均既有氧化性,又有还原性。
2 2
答案 B
5.下列实验现象描述正确的是( )
A.碘水中加入少量汽油振荡,静置后上层颜色变浅,下层颜色变为紫红色
B.红热的铜丝在氯气中燃烧,产生了棕黄色的雾
C.电解氯化钠饱和溶液,将阴极气体产物通入碘化钾淀粉溶液中,溶液变蓝
D.溴化钠溶液中加入少量新制的氯水振荡,再加入少量四氯化碳振荡,静置后上
层颜色变浅,下层颜色变为橙红色
解析 汽油的密度比水小,上层颜色变为紫红色,下层颜色变浅,A项错误;CuCl
2
是固体应为烟而不是雾,B项错误;电解NaCl饱和溶液,阳极产生的Cl 能使碘化
2
钾淀粉溶液变蓝,C项错误。
答案 D
6.下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
用双氧水滴定KI淀粉
A 溶液变蓝 达到滴定终点
溶液
向食用加碘盐中加入食
该食用加碘盐中含有
B 醋和KI溶液,再加入 下层呈紫红色
KIO
CCl 振荡,静置 3
4
用湿润的淀粉碘化钾试
C 试纸变蓝 该气体为溴蒸气
纸鉴别NO 、溴蒸气
2最后试管有浅黄色沉
D 有机物中含有溴原子
淀
解析 A项,KI淀粉溶液一般作为指示剂,设计用双氧水滴定KI淀粉溶液无法判
定终点,实验不合理;B项,在酸性环境中,KIO 与KI反应生成I ,正确;C项,NO
3 2 2
溶于水变为硝酸,硝酸也具有强氧化性,也可使淀粉碘化钾试纸变蓝,错误;D项,
加入AgNO 溶液之前要用硝酸中和溶液中的碱,错误。
3
答案 B
7.海藻中含有丰富的、以离子形式存在的碘元素。如图是实验室从海藻里提取碘的
流程中的一部分。
下列判断正确的是( )
A.步骤①③的操作分别是过滤、萃取分液
B.可用淀粉溶液检验步骤②的反应是否进行完全
C.步骤③中加入的有机溶剂是裂化汽油
D.步骤④的操作是过滤
解析 通过过滤除去海藻灰悬浊液中难溶性杂质而得到含有I-的溶液,向该溶液
中通入Cl 将I-氧化为I ,经萃取、蒸馏等操作后即得晶体I ,A正确,D错误;淀
2 2 2
粉只能检验生成了I ,而不能说明I-已反应完全,B错误;裂化汽油中含有不饱和
2
烃,能与I 发生反应,C错误。
2
答案 A
8.下列从海洋中获取物质的方案不合理的是( )解析 电解MgCl 溶液发生反应:MgCl +2H O INCLUDEPICTURE "F:\\方正文
2 2 2
件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\反应通电.TIF"
\* MERGEFORMATINET Mg(OH) ↓+H ↑+Cl ↑,得不到金属Mg,制备
2 2 2
金属Mg应电解熔融的MgCl ,D项错误。
2
答案 D
9.(2018·齐齐哈尔五校期末联考)二氧化氯(ClO )是国际上公认的安全、无毒的绿
2
色消毒剂,对酸性污水中的Mn2+也有明显的去除效果,其反应原理为ClO +Mn2
2
+→MnO ↓+Cl-(部分反应物和产物省略、未配平),下列有关该反应的说法正确
2
的是( )
A.工业上可用更为廉价的Cl 来代替ClO
2 2
B.利用该原理处理含Mn2+的污水后溶液的pH升高
C.该反应中氧化产物和还原产物的物质的量之比为2∶5
D.理论上处理含1 mol Mn2+的污水,需要标准状况下的ClO 8.96 L
2
解析 氯气是有毒的气体,所以不能代替ClO ,则A项错误;用ClO 处理酸性污
2 2
水中的Mn2+,反应的离子方程式为2ClO +5Mn2++6H O===5MnO ↓+2Cl-+
2 2 2
12H+,所以处理后溶液的pH是减小的,故B项错误;该反应的氧化产物为MnO ,
2
还原产物为Cl-,由反应方程式可知,二者的物质的量之比为5∶2,故C项错误;由反应的离子方程式可知,处理1 mol Mn2+,需要0.4 mol的ClO ,在标准状况下
2
的体积为8.96 L,故D项正确。
答案 D
10.海洋中有大量的宝贵资源。被称为“海洋元素”的溴,其工业制法为把海水浓
缩得盐卤,然后加热到363 K,控制pH为3.5,通入氯气把溴置换出来,然后用一
种气体X把溴吹出,再用纯碱溶液吸收,这时,溴转化为溴离子和溴酸根,最后用
硫酸酸化,单质溴可从溶液中析出。
(1)把溴吹出的气体X,最可能用下面的________(填选项字母)。
A.乙烯 B.空气 C.氩气 D.CO
2
(2)某同学对上述工艺提出改进意见,认为氧化后直接用有机溶剂萃取出溴即可,
你认为其建议是否合理。________(填“是”或“否”),并说出理由:
_____________________________________________________________________
_____________________________________________________________________
。
(3)提取溴的工厂往往会因为溴的挥发而造成空气污染,某实验小组准备收集工厂
的空气测定溴的含量,提供乙醇溶液、蒸馏水、饱和Na SO 溶液、饱和NaBr溶液,
2 3
请 你 为 他 们 设 计 收 集 一 瓶 工 厂 的 空 气 的 方 法 :
______________________________________________________________________
______________________________________________________________________
_____________________________________________________________________
。
(4) 纯 碱 溶 液 吸 收 溴 的 化 学 方 程 式 为
______________________________________________________________________
_____________________________________________________________________
;
硫 酸 酸 化 得 到 单 质 溴 的 离 子 方 程 式 为
______________________________________________________________________
_____________________________________________________________________
。
解析 (1)吹出的溴单质用 Na CO 吸收,不能用 CO 吹出 Br ,是因为 CO 与
2 3 2 2 2Na CO 能发生反应,乙烯与溴单质发生加成反应,氩气的使用在工业上成本较高,
2 3
因此用的是空气。(2)直接萃取单质溴不仅需要大量的萃取剂,而且还造成一部分
溴流失,使从萃取剂中分离出液溴成本增加。(3)收集工厂内的空气,只需把装满饱
和NaBr溶液的试剂瓶带到工厂后,把其中的液体倒出,然后密封试剂瓶,即得一
瓶工厂内的空气。(4)根据题中提供的信息,Br 与Na CO 反应的化学方程式为
2 2 3
3Br +3Na CO ===5NaBr+NaBrO +3CO ↑,然后用硫酸酸化得单质溴的离子方
2 2 3 3 2
程式为5Br-+6H++BrO===3Br +3H O。
2 2
答案 (1)B (2)否 需大量萃取剂,污染大,利用率低
(3)把装满饱和NaBr溶液的试剂瓶带到工厂,在工厂内把其中的液体全部倒出,然
后加盖密封
(4)3Br +3Na CO ===5NaBr+NaBrO +3CO ↑
2 2 3 3 2
5Br-+6H++BrO===3Br +3H O
2 2
11.(2017·专家原创)PCl 是一种重要的化工原料,实验室用如图装置制取PCl 。已
3 3
知PCl 的熔点是-112 ℃,沸点是75.5 ℃,极易水解,受热易被氧气氧化。
3
请回答下列问题:
(1)B仪器的名称是___________________________________________。
(2)实验开始前的操作依次是:①组装仪器,②________,③加药品,
④__________________________________________________________________,
⑤最后点燃酒精灯。
(3) 导 管 a 的 作 用 是
______________________________________________________
_____________________________________________________________________
;
E装置的作用是______________________________________________________。
(4)F 装 置 中 的 药 品 是 ________ ; F 装 置 不 能 换 成 C 装 置 , 理 由 是
_____________________________________________________________________。解析 由于PCl 遇水会水解,所以氯气必须干燥,C装置中可盛装浓硫酸干燥氯
3
气。利用二氧化碳排尽装置中的空气,防止PCl 被氧化。根据PCl 的沸点数据,利
3 3
用E装置收集PCl 。因尾气中含有有毒气体氯气且空气中的水蒸气可能进入装置,
3
所以用F装置中的碱石灰可吸收多余的氯气及少量的HCl,同时防止空气中的水
蒸气进入烧瓶与PCl 反应。
3
答案 (1)恒压分液漏斗
(2)检验装置的气密性 打开弹簧夹K通一段时间的CO ,然后关闭弹簧夹K
2
(3)平衡三颈烧瓶与分液漏斗上方的气压,使B仪器中的液体能够顺利滴下 冷凝
并收集PCl
3
(4)碱石灰 C装置只能吸收水,而F装置还可以吸收多余的氯气及少量的HCl
[B级 拔高选做题]
12.ClO 是一种高效安全的绿色杀菌剂,下列有关ClO 制备与杀菌的说法或解释
2 2
存在错误的是( )
A.可用Cl 和NaClO 制备ClO ,其中n(氧化剂)∶n(还原剂)=1∶2
2 2 2
B.ClO 在强碱性环境中使用失效:2ClO +2OH-===ClO+ClO+H O
2 2 2
C.ClO 处理饮用水时残留的ClO,可用FeSO 来除去:ClO+2Fe2++4H+===
2 4
2Fe3++Cl-+2H O
2
D.等物质的量的ClO 杀菌效果比Cl 、HClO强
2 2
解析 Cl 和NaClO 制备ClO 的反应为2NaClO +Cl ===2NaCl+2ClO ,NaClO
2 2 2 2 2 2 2
作还原剂,Cl 作氧化剂,n(氧化剂)∶n(还原剂)=1∶2,A正确;ClO 在强碱性环境
2 2
中发生反应:2ClO +2OH-===ClO+ClO+H O,B正确;Fe2+具有还原性,可将
2 2
ClO还原为无毒的Cl-,离子反应方程式书写错误,应为ClO+4Fe2++
4H+===4Fe3++Cl-+2H O,C错误;ClO ~5e-~Cl-,Cl ~2e-~2Cl-、HClO~2e
2 2 2
-~Cl-,D正确。
答案 C
13.(2019·湖南湘中名校联考)已知H SO +I +H O===H SO +2HI,将0.1 mol Cl
2 3 2 2 2 4 2
通入100 mL含等物质的量的HI与H SO 的混合溶液中,有一半的HI被氧化,则
2 3
下列说法正确的是( )
A.物质的还原性HI>H SO >HCl
2 3
B.HI与H SO 的物质的量浓度为0.6 mol·L-1
2 3C.通入0.1 mol Cl 发生反应的离子方程式为:5Cl +4H SO +2I-+4H O===4SO
2 2 2 3 2
+I +10Cl-+16H+
2
D.若再通入0.05 mol Cl ,恰好能将HI和H SO 完全氧化
2 2 3
解析 由题意可知氧化性Cl >I >H SO ,故还原性HCl<HI<H SO ,A错;B项,
2 2 2 4 2 3
设n(HI)=n(H SO )=x,
2 3
则H O+Cl +H SO ===2HCl+H SO ,
2 2 2 3 2 4
x x
Cl +2HI===2HCl+I ,
2 2
x+=0.1 mol,解得x=0.08 mol,c(HI)=c(H SO )==0.8 mol/L;C项,Cl 先与
2 3 2
H SO 反应,再与HI反应且HI消耗了一半,故反应方程式中H SO 和HI的化学
2 3 2 3
计量数之比为2∶1;D项,若将H SO 和HI完全消耗需n(Cl )=n(H SO )+=0.12
2 3 2 2 3
mol。
答案 C
14.(2018·湖北八校第二次联考,26)卤素单质在碱性溶液中容易发生歧化反应,歧
化的产物依反应温度的不同而不同。
Cl +2OH-=====Cl-+ClO-+H O
2 2
3Cl +6OH-=====5Cl-+ClO+3H O
2 2
下图为制取氯气、氯酸钾、次氯酸钠和检验氯气性质的微型实验装置:
装置中盛装的药品如下:①多用滴管中装有5 mL浓盐酸;②微型具支试管中装有
1.5 g KMnO ;③微型具支试管中装有2~3 mL浓硫酸;④U形反应管中装有30%
4
KOH溶液;⑤U形反应管中装有2 mol·L-1 NaOH溶液;⑥、⑦双U形反应管中分
别装有 0.1 mol·L-1 KI淀粉溶液和 KBr 溶液;⑧尾气出口用浸有 0.5 mol·L-1
Na S O 溶液的棉花轻轻覆盖住。
2 2 3
(1) 整 套 装 置 气 密 性 检 查 的 方 法 :
__________________________________________________________________________________________________________________________________________。
(2)为了使装置④、⑤中的反应顺利完成,应该控制的反应条件分别为
____________________________________________________________________。
(3) 装 置 ⑥ 、 ⑦ 中 能 够 观 察 到 的 实 验 现 象 分 别 是
_____________________________________________________________________
____________________________________________________________________。
(4)如果把装置⑥、⑦中的试剂互换位置,还能否证明氧化性:Cl >I ,________(填
2 2
“ 能 ” 或 “ 不 能 ” ) , 理 由 是 :
_____________________________________________________________________
_____________________________________________________________________
。
(5)已知氯酸钾和氯化钾的溶解度曲线如下图所示,反应结束后,从装置④中提取
氯酸钾晶体的实验操作是________。
(6) 尾 气 处 理 时 发 生 反 应 的 离 子 方 程 式 为
______________________________________________________________________
_____________________________________________________________________
。
(7) 选 择 微 型 实 验 装 置 的 优 点 有
_____________________________________________________________________
(至少写两点)。
解析 (2)装置④中盛放30%KOH溶液,用于制备KClO ,发生的反应为3Cl +
3 2
6KOH=====KClO +5KCl+3H O;装置⑤中盛放2 mol·L-1 NaOH溶液,用于制
3 2
备NaClO,发生的反应为Cl +2NaOH===NaCl+NaClO+H O;根据题给信息,为
2 2
使装置④中反应顺利完成,装置④应放入348 K热水浴中;为使装置⑤中反应顺
利完成,装置⑤应放入冰水浴中。(3)装置⑥中盛放KI淀粉溶液,通入Cl 发生反应Cl +2KI===2KCl+I ,淀粉遇I
2 2 2 2
呈蓝色,装置⑥的实验现象是:溶液变蓝。装置⑦中盛放KBr溶液,通入Cl 发生反
2
应Cl +2KBr===2KCl+Br ,装置⑦的实验现象是:溶液变成橙色。
2 2
(4)如果把装置⑥、⑦中的试剂互换位置,装置⑥中盛放KBr溶液,装置⑥中发生
反应Cl +2KBr===2KCl+Br ,由此得出氧化性:Cl >Br ;装置⑦中盛放KI淀粉溶
2 2 2 2
液,无论是Cl 还是装置⑥中挥发出来的Br (g)都能与KI反应生成I ,能说明Cl
2 2 2 2
或Br (g)的氧化性强于I ,结合装置⑥中结论也能证明Cl 的氧化性强于I 。
2 2 2 2
(5)根据溶解度曲线,KClO 的溶解度随温度升高明显增大,KCl在低温时溶解度大
3
于KClO ,高温时溶解度小于KClO ,从装置④中提取KClO 晶体的实验操作是将
3 3 3
溶液冷却结晶、过滤、洗涤、干燥。
(6)尾气用0.5 mol·L-1 Na S O 溶液吸收,Cl 将S O氧化成SO,Cl 被还原成Cl-,
2 2 3 2 2 2
反应的离子方程式为4Cl +S O+5H O===2SO+8Cl-+10H+。
2 2 2
答案 (1)连接好实验装置,由⑧导管向装置⑦中加水,若能形成一段稳定的水柱,
则装置的气密性良好(其他合理答案也可)
(2)装置④放入348 K(或75 ℃)热水浴中;装置⑤放入冰水浴中
(3)装置⑥中溶液变蓝;装置⑦中溶液变成橙色
(4)能 若互换装置⑥、⑦中的试剂,Cl 与KBr反应生成Br ,挥发出来的Br 与KI
2 2 2
反应,也可以证明Cl 的氧化性强于I
2 2
(5)冷却结晶、过滤、洗涤、干燥
(6)S O+4Cl +5H O===2SO+8Cl-+10H+
2 2 2
(7)简化实验装置、节约成本;试剂用量少、能源消耗少;节省空间,缩短实验时间;
减少污染等(任选两点,合理即可)