文档内容
考点 07 元素周期律和元素周期表
(好题冲关)
【基础过关】
1.下列事实不能说明氮和氧非金属性相对强弱的是( )
A.热稳定性:HO>NH B.常温下水为液体而氨为气态
2 3
C.NO中N为+2价,氧为-2价 D.NH 在纯氧中燃烧可生成N
3 2
【答案】B
【解析】A项,简单气态氢化物的热稳定性可以说明非金属性强弱,A不符合题意;B项,水、NH
3
的状态反应的是物质熔沸点,即物理性质,而非金属性属于化学性质,两者不能相互说明,B符合题意;
C项,NO中O显负价,N显正价,说明吸引电子能力O大于N,即非金属性O大于N,C不符合题意;D
项,NH 与O 反应生成N,说明O 可以置换出N,可以说明非金属性O大于N,D不符合题意;故选
3 2 2 2 2
B。
2.下列性质的比较,不能用元素周期律解释的是( )
A.原子半径:S>Cl B.热稳定性:HCl>HS
2
C.非金属性:Cl>S D.酸性:HClO>HSO
3 2 3
【答案】D
【解析】A项,同一周期从左往右主族元素的原子半径依次减小,故原子半径:S>Cl可以用元素周
期律解释,A不合题意;B项,同一周期从左往右主族元素的非金属性增强,其简单气态氢化物的热稳定
性也依次增强,故热稳定性:HCl>HS可以用元素周期律解释,B不合题意;C项,同一周期从左往右主
2
族元素的非金属性增强,故非金属性:Cl>S符合元素周期律,C不合题意;D项,非金属元素的最高价
氧化物对应的水化物的酸性与元素的非金属性一致,但HClO、HSO 不是Cl、S的最高价氧化物对应水
3 2 3
化物,故酸性:HClO>HSO 不能用元素周期律解释,D符合题意;故选D。
3 2 3
3.(2023·上海市高三模拟)短周期元素X、Y,若原子半径X>Y,则下列选项中一定正确的是( )
A.若X、Y均在IVA族,则单质熔点X>Y
B.若X、Y均在VIA族,则气态氢化物的热稳定性X>Y
C.若X、Y均属于第二周期非金属元素,则简单离子半径X>Y
D.若X、Y均属于第三周期金属元素,则元素的最高正价X>Y
【答案】C
【解析】A项,若X、Y均在ⅣA族,原子半径X>Y,则X为Si,Y为C,金刚石的熔点高于单质硅,
A错误;B项,若X、Y均在ⅥA族,原子半径X>Y,X为S,Y为O,非金属性O>S,则气态氢化物的
热稳定性HO>HS,B错误;C项,若X、Y均属于第二周期非金属元素,原子半径X>Y,则X的原子序
2 2
资料收集整理【淘宝店铺:向阳百分百】数小于Y,X、Y的简单离子电子层结构相同,核电荷数越小,离子半径越大,则简单离子半径X>Y,C
正确;D项,若X、Y均属于第三周期金属元素,原子半径X>Y,则原子序数XX>Z
B.气态氢化物的热稳定性:W>Z
C.Y与Z形成的化合物可能具有强氧化性
D.常温下,W单质的分子间作用力小于T单质
【答案】C
【解析】Z和W最外层电子均为6,且Z原子半径小,所以Z为O;W为S;T元素最外层电子书为
7,其原子半径介于Z和W之间,所以T为F;X和Y最外层电子均为1,且半径均大于Z,Y元素半径大
于W;所以X为Na,Y为K。A项,据分析可知,Y为K;Z为O;X为Na,电子层结构相同的离子,随
着核电荷数的增大,离子半径减小;所以简单离子的半径:Y>Z>X;故A错误;B项,W为S;Z为O;
电负性大小为Z>W,所以气态氢化物的热稳定性:Z>W;故B错误;C项,Y为K;Z为O;K和O形成
的过氧化钾即可以做氧化剂又可以做还原剂;故C正确;D项,W为S;T为F;S单质为分子晶体;F单
质为分子晶体;分子晶体之间作用力与分子量大小有关,S是以S 存在,F以F 存在,所以W单质的分子
8 2
间作用力大于T单质;故D错误;故选C。
6.短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半
资料收集整理【淘宝店铺:向阳百分百】径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色
沉淀析出,同时有刺激性气体产生。下列说法正确的是
A.原子半径:Y>Z>X>W
B.简单氢化物的热稳定性:W>X>Z
C.Y、Z形成的化合物溶于水会促进水的电离
.
D 上述刺激性气体通入紫色石蕊溶液,溶液先变红后褪色
【答案】C
【解析】氨可作制冷剂,所以W是氮;钠是短周期元素中原子半径最大的,所以 Y是钠;硫代硫酸
钠与稀盐酸反应生成黄色沉淀硫单质和刺激性气味的气体二氧化硫,所以 X、Z分别是氧、硫。A项,由
分析可知,Y是钠、X是氧、Z是硫、W是氮,N、O同周期,Na、S同周期,自左而右原子半径减小,故
原子半径:N>O,Na>S,S电子层多,原子半径较大,S>N;故原子半径Na>S>N>O,A错误;B项,
非金属性O>N,故氢化物稳定性HO>NH ,即WZ>Y
B.原子半径:ZZ>Y,A项正确;B项,Z、
Y、M分别是N、C、Na,同周期从左到右,原子半径逐渐减小,同主族从上到下,原子半径逐渐增大,
所以原子半径:ZY>W
D.简单气态氢化物的稳定性:X>Z
【答案】A
【解析】W的原子半径在短周期主族元素中最大,W为Na;X的质子数是Z核外最外层电子数的2
倍,分情况讨论:若Z核外最外层电子数为7,则Z为Cl、X为Si,由化合物中元素化合价代数和为0可
知,Y元素化合价为-3,Y为P;若Z核外最外层电子数为6,则Z为S、X为Mg,Y元素化合价为+7,不
合理;若Z核外最外层电子数为5,则X的质子数为10,不合理;可知Z为Cl、X为Si、Y为P。A项,
氢氧化钠为强碱,硅酸为弱酸,磷酸为中强酸,高氯酸为强酸,A项正确;B项,氯化钠水溶液呈中性,
B项错误;C项,核外电子排布相同的离子,原子序数大的半径小,磷离子的半径大于氯离子的,C项错
误;D项,同周期主族元素从左到右,非金属性依次增强,则简单气态氢化物的稳定性Cl>Si,D项错误;
故选A。
12.原子序数依次增大的W、X、Y、Z四种短周期主族元素,W、Y同周期且价电子数之和为10,
W、Y可形成结构如图所示的阴离子,Z原子最外层有2个电子,下列说法错误的是( )
资料收集整理【淘宝店铺:向阳百分百】A.常见简单氢化物沸点:
B.简单离子半径:
C.WY2-中两种元素的原子 离子 最外层均达到8电子结构
2 4
D.Z2+、WY2-均能促进水的电离
2 4
【答案】B
【解析】A项,由图可知W形成四个共价键,所以为碳,Y形成了2个共价键,再结合W、Y价电子
数关系可推出Y是氧。易推出X是氮,Z是镁。常温下水是液体、NH 易液化而CH 难液化,A项正确;
3 4
B项,简单离子半径:N3- >O2- > Mg2+,B项错误;C项,原子最外层有4个电子,通过形成四个共价键而
使自已最外层达到8个电子,O原子最外层有6个电子,形成2个键后最外层也达到8个电子,C项正确;
D项,Mg2+能水解,C O2-是弱酸的酸根,也能水解,D项正确;故选B。
2 4
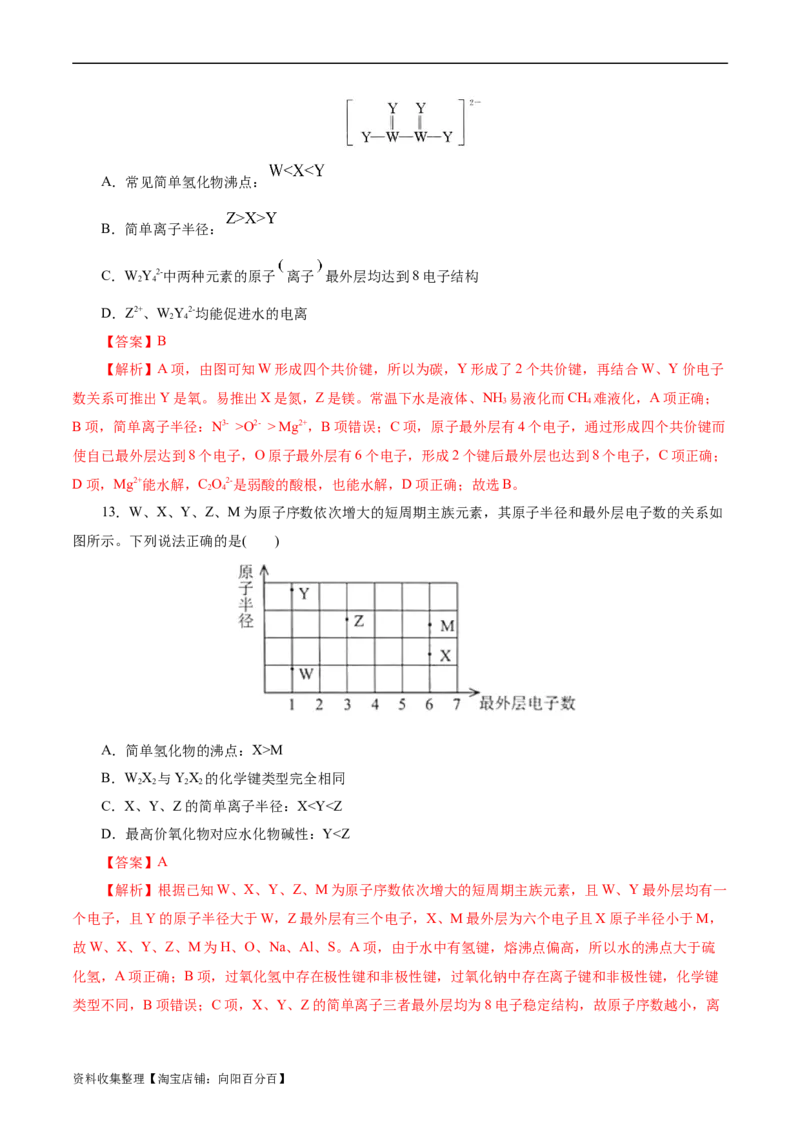
13.W、X、Y、Z、M为原子序数依次增大的短周期主族元素,其原子半径和最外层电子数的关系如
图所示。下列说法正确的是( )
A.简单氢化物的沸点:X>M
B.WX 与YX 的化学键类型完全相同
2 2 2 2
C.X、Y、Z的简单离子半径:XY>Z;C项错误;D项,氢氧化钠为强碱,氢氧化铝为弱碱,故碱性:氢氧化钠>氢氧化
铝,D项错误;故选A。
14.(2023·江西省南昌市质检)短周期主族元素W、X、Y、Z、Q原子序数依次增大,形成的化合物是
一种重要的食品添加剂,结构如下图。下列正确的是( )
A.原子半径大小:Y>Z>Q
B.该化合物中Z原子不满足8电子稳定结构
C.Y是第ⅢA族元素
D.W和Z可形成三种10电子微粒
【答案】D
【解析】五种元素均为短周期元素,且原子序数依次增大,Q显+1价,即Q为Na,W形成一个共价
键,则W为H,Y形成三个共价键,即Y为N,X形成四个共价键,则X为C,Z形成2个共价键,则Z
为O,W为H,X为C,Y为N,Z为O,Q为Na。A项,一般电子层数越多,原子半径越大,同周期从
左向右原子半径依次减小,因此原子半径:Na>N>O,故A错误;B项,其中一个O与C形成碳氧双键,
该氧元素满足8电子稳定结构,另一个O与C形成一个C-O单键,同时该氧元素又得到Na失去的一个电
子,因此该氧元素也满足8电子稳定结构,故B错误;C项,Y为N,位于第二周期ⅤA族,故C错误;
D项,H和O形成10电子微粒分别为HO、HO+、OH-,故D正确;故选D。
2 3
15.(2023·四川省乐山市高三第三次调研考试)我国科学家分析月壤成分发现含有X、Y、Z、W、M五
种主族元素,其原子序数依次增大且都不大于20,Y、Z、W同周期且Z、M同主族;X与W形成的化合
物是光导纤维的基本原料,在潜水艇中YX 可以用作供氧剂。下列说法正确的是( )
2 2
A.离子半径的大小顺序:Z>Y>X
B.最简单气态氢化物稳定性X>W
C.最高价氧化物对应水化物碱性Y>Z>M
D.工业上用电解ZX来制备Z的单质
【答案】B
【解析】光导纤维的主要成分是SiO,X与W形成的化合物是光导纤维的基本原料,则X是O,W
2
是Si。YX 可以用作供氧剂则Y元素是Na,再根据原子序数依次增大且都不大于20,Y、Z、W同周期且
2 2
Z、M同主族,可推断Z元素是Mg,M元素是Ca。A项,据分析可知X、Y、Z元素分别为O、Na、
Mg,离子半径的大小顺序:O2- >Na+ > Mg2+,故A错误; B项,X、W元素分别为O、Si,最简单气态氢
化物稳定性:HO>SiH,故B正确;C项,Y、Z、M元素分别为Na、Mg、Ca,最高价氧化物对应水化物
2 4
资料收集整理【淘宝店铺:向阳百分百】碱性Ca (OH)> Mg (OH) ,故C错误;D项,Z是Mg元素,工业上用电解MgCl 来制备Mg的单质,故D
2 2 2
错误;故选B。
16.(2023·四川省成都市警蓉城名校联盟三模)X、Y、Z、W是原子序数依次递增的短周期主族元素,
其最外层电子数之和为21。其中X、W同族,Y、Z相邻,W与X、Y、Z位于不同周期。下列说法正确的
是( )
A.原子半径:W > X > Y > Z
B.简单氢化物的沸点:Y < Z
C.最高价含氧酸的酸性:Z > W
D.X、Y、W在自然界中均存在游离态
【答案】A
【解析】X、Y、Z、W是原子序数依次递增的短周期主族元素,其最外层电子数之和为21,而X、W
同族,可知X、W不能处于IA族,因为若处于IA族,Y、Z的最外层电子数平均为 =9.5>7,而
Y、Z相邻,且W与X、Y、Z位于不同周期,结合原子序数可知四种元素在周期表中位置关系如图所示:
,设X、W最外层电子数为a,Y的最外层电子数为b,可知Z原子最外层电子数为b+1,
则有2a+b+b+1=21,整理可得a+b=10,只能是a=4,b=6,可知X为C元素、W为Si元素、Y为O元
素、Z为F元素。A项,同周期主族元素自左而右原子半径减小,同主族自上而下原子半径增大,则原子
半径:Si>C>O>F,故A正确;B项,Y、Z的简单氢化物依次为HO、HF,常温下水是液体,而HF是
2
气体,则沸点:HO>HF,故B错误;C项,Z是氟元素,不存在最高价含氧酸,故C错误;D项,硅是
2
亲氧元素,自然界中没有游离态的硅,以化合态形式存在,故D错误;故选A。
17.(2023·安徽省亳州市期中)W、X、Y、Z、N、M六种主族元素,它们在周期表中位置如图所示,
请用对应的的化学用语回答下列问题:
(1)N元素在周期表中的位置___________,根据周期表,推测N原子序数为___________
(2)比较Y、Z、W三种元素形成简单离子的半径由大到小的顺序___________(用元素符号表示)
(3)M最高价氧化物的水化物在水中的电离方程式:___________
(4)以下说法正确的是___________
资料收集整理【淘宝店铺:向阳百分百】A.单质的还原性:X>Y,可以用X与YM 溶液发生反应置换出Y来证明
2
B.Y与同周期的ⅢA元素的原子序数相差1
C.硅主要用于半导体器件的研制,目前用硅研发出的太阳能光伏电池,如我校的路灯
D.元素N位于金属与非金属的分界线附近,可以推断N元素的单质可与氨水反应放出氢气
(5)由X、W元素构成的原子个数比为1:1的化合物所含化学键类型为___________,将一定量此化合
物投入到足量的水中,产生2.24L气体(标准状况下),转移电子的物质的量为________。
【答案】(1) 第四周期ⅣA族 32
(2)S2->O2->Mg2+ (3)HClO =H++ClO -
4 4
(4)BC
(5) 离子键、非极性共价键 0.2mol
【解析】(1)由周期表可知,N元素在周期表中的位置为第四周期ⅣA族,原子序数为32;(2)Y和W
的简单离子电子层数相同,而Y的原子序数大于W,所以Y的简单离子的半径小于W,Y和W的简单离
子电子层数小于Z,所以Y和W的简单离子的都半径小于Z,所以Y、Z、W三种元素形成简单离子的半
径由大到小的顺序为S2->O2->Mg2+;(3)由周期表可知,M元素为Cl,其最高价氧化物的水化物为
HClO,在水中的电离方程式为HClO=H++ClO -;(4)A.X和Y同周期,同周期元素从左往右金属性依次
4 4 4
减弱,金属性越强,其单质的还原性越强,所以X>Y,但X是元素Na,在YM (MgCl )溶液中优先与水反
2 2
应,不会置换出Mg,A错误;B.Y属于第三周,所以与同周期的ⅢA元素的原子序数相差1,B正确;
C.硅主要用于半导体器件的研制,目前用硅研发出的太阳能光伏电池,可用于路灯,C正确;D.元素N
位于金属与非金属的分界线附近,其性质与Al近似,但Al只能与强碱溶液反应生成氢气,而氨水是弱碱
溶液,不能与Al反应生成氢气,D错误;故选BC。(5)由X、W元素构成的原子个数比为1:1的化合物
为NaO,所含化学键类型为离子键、非极性共价键;讲NaO 投入水中,发生反应为2 Na O+2H O=4
2 2 2 2 2 2 2
NaOH+ O↑,该反应中每生成1mol O,转移电子数为2mol e-,产生2.24L气体(标准状况下),则产生
2 2
0.1mol O ,转移电子数为0.2mol e-。
2
18.如图为元素周期表的一部分。请回答下列问题。
(1)图中阴影部分所示区域的元素称为____元素,下列元素属于该区域的是____(填字母)。
A.Ba B.Fe C.Br D.Rb
(2)已知A、B、C、D、E、F六种短周期元素的原子半径和某些化合价如表:
资料收集整理【淘宝店铺:向阳百分百】元素 A B C D E F
化合价 -2 +5、-3 +4、-4 +6、-2 +2 +1
原子半径/nm 0.074 0.075 0.077 0.102 0.160 0.186
写出D元素在元素周期表中的位置____。
(3)C的最高价氧化物与E的单质在点燃条件下发生反应的化学方程式为____;由F的化合物生成A的
单质的化学方程式为____。
(4)C与氢元素可组成一种气体,该气体在标准状况下的密度为1.25g•L-1,该气体的摩尔质量为____。
(5)下列说法不正确的是____。A.元素最高正价与最低负价绝对值相等的元素一定处于第ⅣA族
B.第5周期第ⅤA族元素的原子序数为65
C.②形成的最简单氢化物比①形成的最简单氢化物的稳定性高
D.周期表中当某元素的周期序数大于其族序数时,该元素可能属于金属或非金属
(6)BrCl属于卤素互化物,性质与Cl 相似。写出BrCl与氢氧化钠溶液反应的化学方程式____。
2
【答案】(1) 过渡金属 B (2)三周期第ⅥA族
(3)CO +2Mg 2MgO+C 2Na O+2H O=2NaOH+O ↑
2 2 2 2 2
(4)28g/mol (5)ABD (6)BrCl+2NaOH=NaCl+NaBrO+H O
2
【解析】(1)如图中阴影部分所示区域为副族和VIII族元素,又称为过渡金属元素;选项中Ba、Br、
Rb为主族元素,Fe为过渡金属元素,所以 B正确;(2)A、D主要化合价为-2价,其中A无正化合价,则
A为0元素、D为S元素;B化合价有+5、-3价,则B位于VA族,由于B的原子半径大于O、小于S,则
B为N元素;C的化合价为+4、-4价,则C位于IVA族,C的原子半径大于O、小于S,则C为C元素;E
为+2价, E的原子半径大于S,则E为Mg元素;F的化合价为+1价,原子半径大于Mg,则F为Na元素,
根据分析可知,D为S元素,在元素周期表中的位置是第三周期第ⅥA族;(3)C为C元素,C的最高价氧
化物为二氧化碳,E为Mg,镁与二氧化碳点燃生成氧化镁和C,反应的化学方程式为:CO+2Mg
2
2MgO+C ;F为Na元素,A为氧元素,其单质为氧气,由钠的化合物生成A单质,即过氧化钠与水反应
生成氢氧化钠和氧气,反应的化学方程式为: 2NaO+2H O=2NaOH+O ↑;(4)该气体的摩尔质量为:
2 2 2 2
;(5)A项,H元素化合价范围为-1~+1,其最高正价与最低负价绝对
值相等,但处于IA,故A错误;B项,第五周期第0族,原子序数为54,第五周期第VA族,其原子序数
应为:54-3=51,故 B错误;C项,②和①同周期,且在①右边,同周期元素越往右,非金属性越强,故
非金属性更强,②形成的最简单氢化物比形成的最简单氢化物的稳定性高,故C正确;D项,周期表中当
某元素的周期序数大于其族序数时,该元素处于左下方,属于金属元素,故D错误;故选ABD;(6)BrCl
属于卤素互化物,性质与Cl 相似,氯气与氢氧化钠溶液反应的化学方程式:
2
资料收集整理【淘宝店铺:向阳百分百】