文档内容
考点 07 元素周期律和元素周期表
(核心考点精讲)
一、3年真题考点分布
考点内容 考题统计
元素周期律
2023天津卷5题,4分;2021北京卷4题,4分
2023全国甲卷11题,6分;2023全国乙卷10题,6分;2023广东
卷14题,3分;2023浙江1月10题,3分;2023浙江6月11题,3
分;2023湖北卷6题,3分;2023湖南卷6题,3分;2022浙江1
文字叙述型元素推断 月16题,2分;2022浙江6月16题,2分;2022海南卷10题,4
分;2022辽宁卷5题,3分;2021全国甲卷11题,6分;2021全国
乙卷11题,6分;2021海南卷7题,2分;2021山东卷4题,2
分;2021天津卷12题,4分;2021海南卷12题,4分
周期表片段型元素推断 2022年广东7题,2分;2021浙江1月15题,2分
2023辽宁卷9题,3分;2022全国乙卷11题,6分;2022湖南卷5
物质结构式型元素推断 题,3分;2021河北卷12题,4分;2021广东卷13题,4分;2021
辽宁卷14题,3分;2021湖北卷8题,3分
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,是历年高考的必考内容。元素周期律能对物质的结构性质进行推理和预测,
元素周期表更是直观明了地显示出所有化学元素间的位置、结构关系。应用元素周期律和元素周期表,既
能推断原子的结构,又能预测元素的性质,如金属性、非金属性的变化,半径的变化,同时还可进行性质、
实验考查。
【备考策略】
元素“位”“构”“性”三者关系的题型会继续以元素及其化合物知识为载体,用物质结构理论,解
释现象、定性推断、归纳总结相结合。可集判断、实验、计算于一体,题型稳定。要想在高考中化学取得
高分,就必须掌握元素同期表命题特点和解题方法。通过编排元素周期表考查的抽象思维能力和逻辑思维
能力;通过对元素原子结构、位置间的关系的推导,培养学生的分析和推理能力。。
【命题预测】
预测2024年该知识将是一个必考点,题型依然会以选择题为主,难度不会有大的变化。重点掌握同周
期、同主族元素性质的递变规律,理清元素“位—构—性”的关系,用好元素周期表这一工具,通过结构
理论来解释现象、定性推断、归纳总结。特别是金属性、非金属性强弱以及原子或离子半径大小判断更是
资料收集整理【淘宝店铺:向阳百分百】考点的重点,复习时加以关注。
考法 1 元素周期表的结构
1.世界上第一张元素周期表是在1869年由俄国化学家门捷列夫绘制完成的,随着科学的不断发展,
已逐渐演变为现在的常用形式。
2.编排原则
(1)周期:把电子层数相同的元素,按原子序数递增的顺序,从左至右排成的横行。
(2)族:把最外层电子数相同的元素,按电子层数递增的顺序,从上至下排成的纵行。
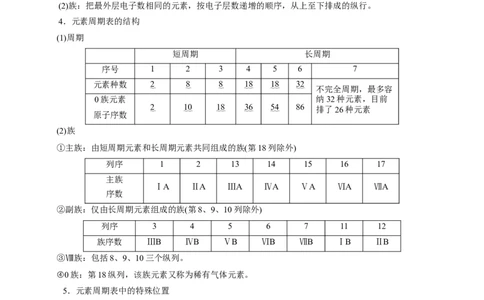
4.元素周期表的结构
(1)周期
短周期 长周期
序号 1 2 3 4 5 6 7
元素种数 2 8 8 18 18 32
不完全周期,最多容
0族元素 纳32种元素,目前
2 10 18 36 54 86 排了26种元素
原子序数
(2)族
①主族:由短周期元素和长周期元素共同组成的族(第18列除外)
列序 1 2 13 14 15 16 17
主族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
序数
②副族:仅由长周期元素组成的族(第8、9、10列除外)
列序 3 4 5 6 7 11 12
族序数 ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB
③Ⅷ族:包括8、9、10三个纵列。
④0族:第18纵列,该族元素又称为稀有气体元素。
5.元素周期表中的特殊位置
(1)分区
①分界线:沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条斜线,即为金属
元素区和非金属元素区分界线(氢元素除外)。
②各区位置:分界线左面为金属元素区,分界线右面为非金属元素区。
③分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
(2)过渡元素:元素周期表中部从ⅢB族到ⅡB族10个纵列共六十多种元素,这些元素都是金属元素。
(3)镧系:元素周期表第6周期中,57号元素镧到71号元素镥共15种元素。
(4)锕系:元素周期表第7周期中,89号元素锕到103号元素铹共15种元素。
(5)超铀元素:在锕系元素中92号元素铀(U)以后的各种元素。
资料收集整理【淘宝店铺:向阳百分百】元素周期表的结构
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)元素周期表中位于金属与非金属分界线附近的元素属于过渡元素( )
(2)第ⅠA族全部是金属元素( )
(3)元素周期表中镧系元素和锕系元素都占据同一格,它们是同位素( )
(4)两短周期元素原子序数相差8,则周期数一定相差1( )
(5)随着原子序数的递增,元素原子的核外电子数逐渐增多,原子半径逐渐减小( )
(6)若两种元素原子的最外层电子数相同,则元素最高正价一定相同( )
(7)原子的最外层有2个电子的元素一定是第ⅡA族元素( )
(8)原子及离子的核外电子层数等于该元素所在的周期数( )
(9)最外层电子数等于或大于3(小于8)的元素一定是主族元素( )
(10)原子的最外层有1个或2个电子,则可能是ⅠA、ⅡA族元素,也可能是副族、Ⅷ族元素或0族元
素氦( )
(11)最外层电子数比次外层电子数多的元素一定位于第二周期( )
(11)元素周期表是按元素的相对原子质量由小到大排列而形成的( )
(12)3、4周期同主族元素的原子序数相差8( )
(13)元素周期表中从第ⅢB族到第ⅡB族10个纵行的元素都是金属元素( )
(14)同周期第ⅡA族和第ⅢA族的原子序数相差1( )
(15)元素周期表中镧系元素和锕系元素都占据同一格,它们是同位素( )
(16)元素周期表中位于金属与非金属分界线附近的元素属于过渡元素( )
答案:(1)× (2)× (3) (4) √ (5)× (6)× (7)× (8)× (9)√ (10) √ (11)× (12)× (13)√ (14)×
(15)× (16)×
例1 X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y、Z为地壳中含量前三的元素,
资料收集整理【淘宝店铺:向阳百分百】X、W同主族。下列说法错误的是( )
A.单质的导电性:YW
C.最简单气态氢化物的热稳定性:X>W
D.最高价氧化物对应水化物的酸性:W>Y
【答案】A
【解析】X、Y、Z为地壳中含量前三的元素,其原子序数依次增大,推出X、Y、Z分别为O、Al、
Si,X和W同主族,W为S。A项,Si是半导体材料,Al是金属,金属的导电性强于非金属,故A说法错
误;B项,同周期从左向右原子半径减小,即Al的半径大于S的半径,故B说法正确;C项,O的非金属
性强于S,HO比HS稳定,故C说法正确;D项,非金属性越强,其最高价氧化物对应水化物酸性越强,
2 2
即HSO 的酸性强于Al(OH) ,故D说法正确;故选A。
2 4 3
例2 (2023·河北省邯郸市高三联考)W、X、Y、Z是周期表中前20号原子序数依次增大的的主族元素,
部分性质如下表,下列说法正确的是( )
W 某种单质被称为地球生物的保护伞
X X、W形成的化合物中阴阳离子个数比为1:2
Y Y的最外层电子数是X、W的最外层电子数之和
Z X和Z不在同一主族
A.简单离子半径:Z>Y>X>W
B.X的最高价氧化物对应水化物为弱碱
C.W与X、Y、Z形成的化合物均有离子键
D.Z的单质能与水反应生成氢气
【答案】D
【解析】W、X、Y、Z是周期表中前20号原子序数依次增大的的主族元素,臭氧层能吸收紫外线被
称为地球生物的保护伞,W为O,X、W形成的化合物中阴阳离子个数比为1:2,该化合物为NaO,X是
2
Na,Y的最外层电子数是X、W的最外层电子数之和,Y是Cl,X和Z不在同一主族,、Z是Ca。A项,
Z、Y、X、W分别为Ca、Cl、Na、O,离子半径为Cl->Ca2+>O2->Na+,A错误;B项,X是Na,最高价
氧化物对应水化物是强碱NaOH,B错误;C项,O与Na、Cl、Ca形成的化合物中,O与Cl形成的是共价
化合物,没有离子键,C错误;D项,Z是Ca,单质能与水反应生成氢气,D正确;故选D。
对点1 下列事实或实验能作为判断依据的是( )
A.盐酸是强酸,氢硫酸是弱酸,判断氯与硫的非金属性强弱
资料收集整理【淘宝店铺:向阳百分百】B.热稳定性:HSe<HS<HO,判断氧、硫与硒的非金属性强弱
2 2 2
C.沸点:HO>NH >CH,判断碳、氧与氮的非金属性强弱
2 3 4
D.在MgCl 与AlCl 溶液中分别加入过量的氨水,判断镁与铝的金属性强弱
2 3
【答案】B
【解析】A项,盐酸和氢硫酸均不是相应元素的最高价态氧化物对应水化物,不能作为判断氯与硫的
非金属性强弱依据,A错误;B项,非金属性越强的元素其单质越容易与氢气化合,得到的氢化物越稳定,
故可依据热稳定性:HSe<HS<HO,判断氧、硫与硒的非金属性强弱,B正确;C项,HO、NH 、CH
2 2 2 2 3 4
物质的沸点与分子间作用力强弱有关,沸点:HO>NH >CH,不能判断碳、氧与氮的非金属性强弱,C
2 3 4
错误;D项,镁与铝的金属性强弱可用其跟酸反应的剧烈程度判断,在MgCl 与AlCl 溶液中分别加入过量
2 3
的氨水,不能判断镁与铝的金属性强弱,D错误;故选B。
对点2 M、X、Y、Z为原子序数依次增大的短周期主族元素,其中M、Z位于同一主族,Z的最高
价含氧酸为强酸。M、Z的原子序数之和是X的2倍,Y的最外层电子数等于Z和X的最外层电子数之差。
下列叙述正确的是( )
A.氢化物沸点:M<Z B.原子半径:M<X<Y<Z
C.工业上用电解法制备单质X D.华为芯片的主要成分为Y的氧化物
【答案】C
【解析】M、X、Y、Z为原子序数依次增大的短周期主族元素,M、Z位于同一主族,Z的最高价含
氧酸为强酸, M、Z可能是O、S或者F、Cl;M、Z的原子序数之和是X的2倍,Z可能为Mg或者Al;
Y的最外层电子数等于Z和X的最外层电子数之差,若Z和X为S和Mg,则Y为Si,若Z和X为Cl和
Al,则Y为Si;所以M、X、Y、Z分别为O、Mg、Si、S或者F、Al、Si、Cl。A项,由于分子间氢键,
氢化物沸点:HO>HS、HF>HCl,A错误;B项,同主族,原子半径自上而下依次增大,同周期,原子半
2 2
径从左至右依次减小,所以原子半径M