文档内容
考点 42 分子结构与性质
【基础过关】
1.下列关于σ键和π键的理解不正确的是( )
A.含有π键的分子在进行化学反应时,分子中的π键比σ键活泼
B.在有些分子中,共价键可能只含有π键而没有σ键
C.有些原子在与其他原子形成分子时只能形成σ键,不能形成π键
D.当原子形成分子时,首先形成σ键,可能形成π键
2.下列反应中既有离子键、极性共价键、非极性共价键的断裂又有其形成的反应是( )
A.NH Cl NH ↑+HCl B.2NaO+2H O = 4NaOH+O ↑
4 3 2 2 2 2
C.2Al+2NaOH+2H O=2NaAlO +3H ↑ D.2NaOH+Cl =NaCl+NaClO+H O
2 2 2 2 2
3.下列有关化学键知识的比较肯定错误的是( )
A.键能:C—N<C===N<C≡N
B.键长:I—I>Br—Br>Cl—Cl
C.分子中的键角:HO>CO
2 2
D.相同元素原子间形成的共价键键能:σ键>π键
4.NF 是微电子工业中一种优良的等离子蚀刻气体,可通过电解熔融氟化氢铵(NH HF )制得。下列有
3 4 2
关说法错误的是( )
A.NF 的空间构型为平面三角形
3
B.相关元素电负性由大到小的顺序为F>N>H
C.NF 和NH HF 中N原子的杂化方式均为sp3
3 4 2
D.NH HF 晶体中微粒间的作用有离子键、共价键、配位键、氢键
4 2
5.一定条件下发生反应:Fe+6HCN+2KCO=K [Fe(CN) ]+H↑+2CO↑+2HO。下列说法正确的是
2 3 4 6 2 2 2
( )
A.K[Fe(CN) ]的中心原子的核外电子排布式为[Ar]3d5
4 6
B.该反应中只存在离子键和共价键的断裂和形成
C.HCN、CO、CO2-中碳的杂化方式和空间构型均相同
2 3
D.HCN 水溶液中存在 4 种氢键
6.甲醛分子式为CHO,有强烈刺激性气味,甲醛在常温下是气态,已被世界卫生组织确定为致癌和
2
致畸形物质。下列关于其结构及性质的分析正确的是( )
A.C原子采取sp3杂化,O原子采取sp杂化
B.甲醛分子中中心原子价层电子对数为4,含有一对孤电子对,是三角锥形结构
C.一个甲醛分子中含有3个σ键和1个π键
D.甲醛分子为非极性分子
资料整理【淘宝店铺:向阳百分百】7.CHOH、NH 和(CH)NNH 均为常见的燃料,关于这三者的结构与性质,下列说法错误的是(
3 2 4 3 2 2
)
A.CHOH的电子式为
3
B.NH 空间结构为平面形
2 4
C.CHOH、NH 和(CH)NNH 都易溶于水
3 2 4 3 2 2
D.CHOH和(CH)NNH中C、O、N杂化方式均相同
3 3 2
8.徐光宪在《分子共和国》一书中介绍了许多明星分子,如 HO 、CO 、BF 、CHCOOH等。下列
2 2 2 3 3
说法正确的是( )
A.HO 分子中的O为sp2杂化 B.CO 分子中C原子为sp1杂化
2 2 2
C.BF 分子中的B原子为sp3杂化 D.CHCOOH分子中C原子均为sp2杂化
3 3
9.了解有机物分子中化学键特征以及成键方式是研究有机物性质的基础。下列关于有机物分子成键
方式的描述不正确的是( )
A.烷烃分子中碳原子均采取sp3杂化成键
B.炔烃分子中的碳碳三键由1个σ键、2个π键组成
C.苯分子中所有碳原子均采取sp2杂化成键,苯环中存在6个碳原子共有的大π键
D.甲苯分子中所有碳原子均采取sp2杂化成键
10.NF 是微电子工业中一种优良的等离子蚀刻气体,可通过电解熔融氟化氢铵(NH HF )制得。下列
3 4 2
有关说法错误的是( )
A.NF 的空间构型为平面三角形
3
B.相关元素电负性由大到小的顺序为F>N>H
C.NF 和NH HF 中N原子的杂化方式均为sp3
3 4 2
D.NH HF 晶体中微粒间的作用有离子键、共价键、配位键、氢键
4 2
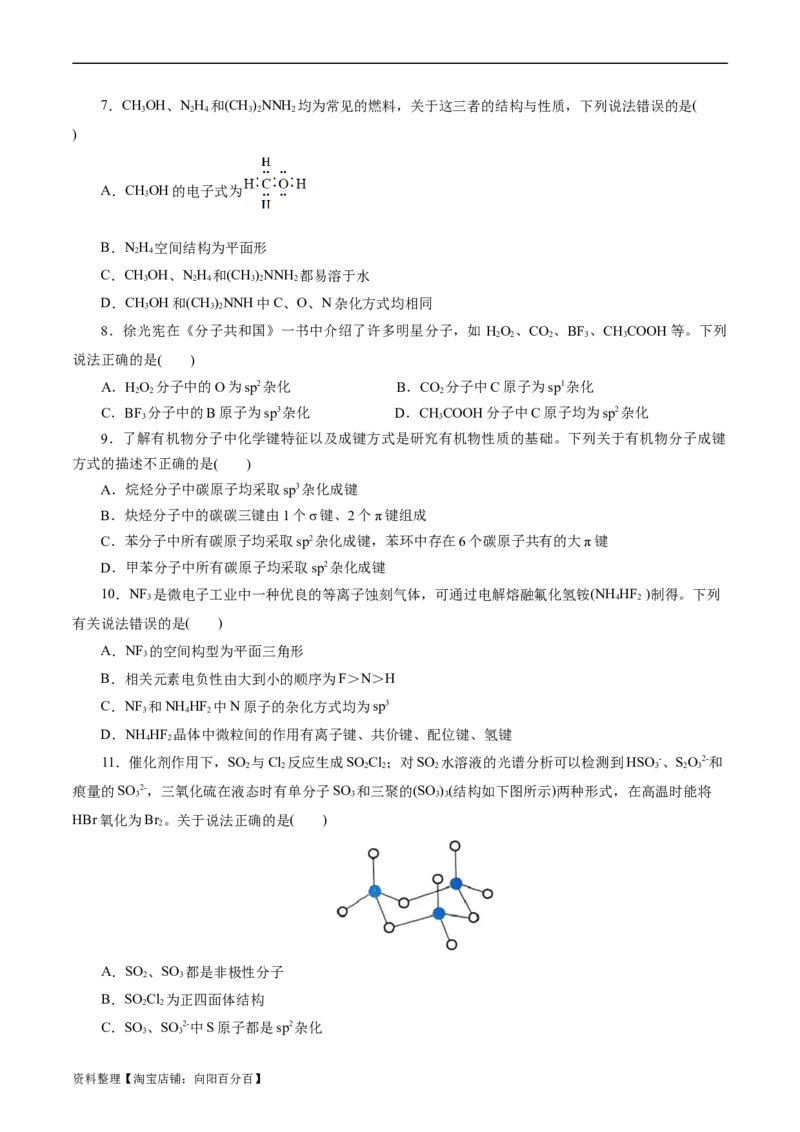
11.催化剂作用下,SO 与Cl 反应生成SO Cl;对SO 水溶液的光谱分析可以检测到HSO -、SO2-和
2 2 2 2 2 3 2 3
痕量的SO 2-,三氧化硫在液态时有单分子SO 和三聚的(SO )(结构如下图所示)两种形式,在高温时能将
3 3 3 3
HBr氧化为Br 。关于说法正确的是( )
2
A.SO 、SO 都是非极性分子
2 3
B.SO Cl 为正四面体结构
2 2
C.SO 、SO 2-中S原子都是sp2杂化
3 3
资料整理【淘宝店铺:向阳百分百】D.1 mol (SO ) 分子中含有12 mol σ键
3 3
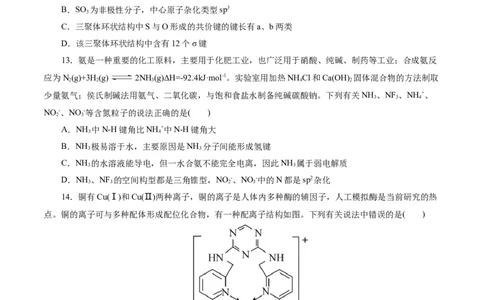
12.(2023·浙江省衢州市期末)SO 及其三聚体环状结构如图所示。下列说法不正确的是( )
3
A.SO 与CO2-、NO -互为等电子体,空间结构都为平面三角形
3 3 3
B.SO 为非极性分子,中心原子杂化类型sp3
3
C.三聚体环状结构中S与O形成的共价键的键长有a、b两类
D.该三聚体环状结构中含有12个σ键
13.氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反
应为N(g)+3H(g) 2NH (g)ΔH=-92.4kJ·mol-1。实验室用加热NH Cl和Ca(OH) 固体混合物的方法制取
2 2 3 4 2
少量氨气;侯氏制碱法用氨气、二氧化碳,与饱和食盐水制备纯碱碳酸钠。下列有关NH 、NF 、NH +、
3 3 4
NO -、NO -等含氮粒子的说法正确的是( )
2 3
A.NH 中N-H键角比NH +中N-H键角大
3 4
B.NH 极易溶于水,主要原因是NH 分子间能形成氢键
3 3
C.NH 的水溶液能导电,但一水合氨不能完全电离,因此NH 属于弱电解质
3 3
D.NH 、NF 的空间构型都是三角锥型,NO -、NO -中的N都是sp2杂化
3 3 2 3
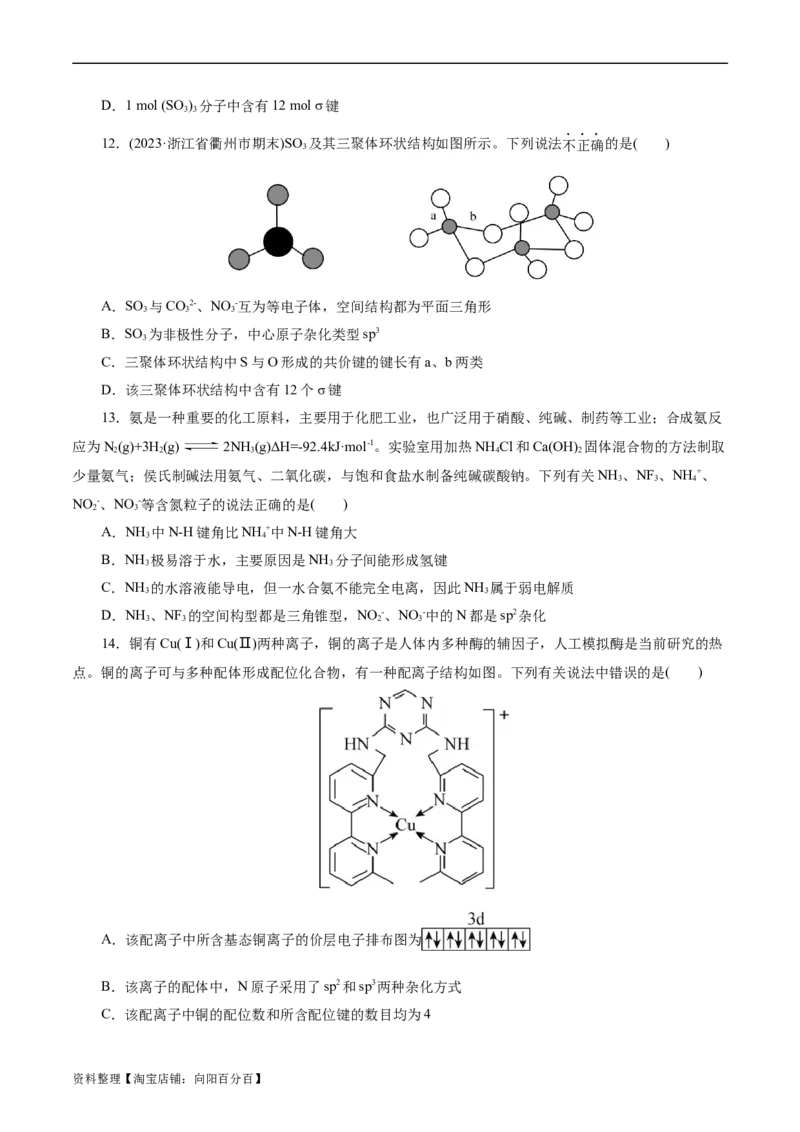
14.铜有Cu(Ⅰ)和Cu(Ⅱ)两种离子,铜的离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热
点。铜的离子可与多种配体形成配位化合物,有一种配离子结构如图。下列有关说法中错误的是( )
A.该配离子中所含基态铜离子的价层电子排布图为
B.该离子的配体中,N原子采用了sp2和sp3两种杂化方式
C.该配离子中铜的配位数和所含配位键的数目均为4
资料整理【淘宝店铺:向阳百分百】D.从核外电子排布角度分析,稳定性:Cu(Ⅰ)<Cu(Ⅱ)
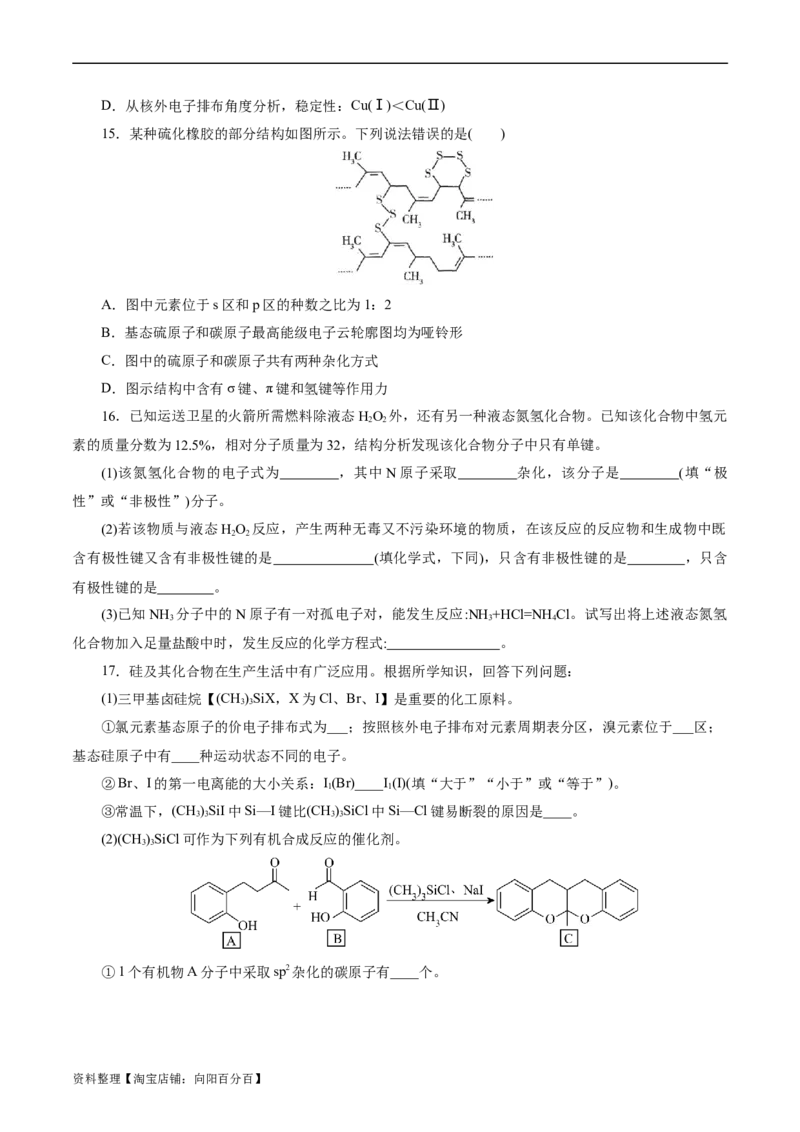
15.某种硫化橡胶的部分结构如图所示。下列说法错误的是( )
A.图中元素位于s区和p区的种数之比为1:2
B.基态硫原子和碳原子最高能级电子云轮廓图均为哑铃形
C.图中的硫原子和碳原子共有两种杂化方式
D.图示结构中含有σ键、π键和氢键等作用力
16.已知运送卫星的火箭所需燃料除液态HO 外,还有另一种液态氮氢化合物。已知该化合物中氢元
2 2
素的质量分数为12.5%,相对分子质量为32,结构分析发现该化合物分子中只有单键。
(1)该氮氢化合物的电子式为 ,其中N原子采取 杂化,该分子是 (填“极
性”或“非极性”)分子。
(2)若该物质与液态HO 反应,产生两种无毒又不污染环境的物质,在该反应的反应物和生成物中既
2 2
含有极性键又含有非极性键的是 (填化学式,下同),只含有非极性键的是 ,只含
有极性键的是 。
(3)已知NH 分子中的N原子有一对孤电子对,能发生反应:NH+HCl=NH Cl。试写出将上述液态氮氢
3 3 4
化合物加入足量盐酸中时,发生反应的化学方程式: 。
17.硅及其化合物在生产生活中有广泛应用。根据所学知识,回答下列问题:
(1)三甲基卤硅烷【(CH)SiX,X为Cl、Br、I】是重要的化工原料。
3 3
①氯元素基态原子的价电子排布式为___;按照核外电子排布对元素周期表分区,溴元素位于___区;
基态硅原子中有____种运动状态不同的电子。
②Br、I的第一电离能的大小关系:I(Br)____I (I)(填“大于”“小于”或“等于”)。
1 1
③常温下,(CH)SiI中Si—I键比(CH)SiCl中Si—Cl键易断裂的原因是____。
3 3 3 3
(2)(CH )SiCl可作为下列有机合成反应的催化剂。
3 3
①1个有机物A分子中采取sp2杂化的碳原子有____个。
资料整理【淘宝店铺:向阳百分百】②有机物B的沸点低于对羟基苯甲醛( )的沸点,其原因是____。
③CHCN中σ键与π键的个数比为____。
3
【能力提升】
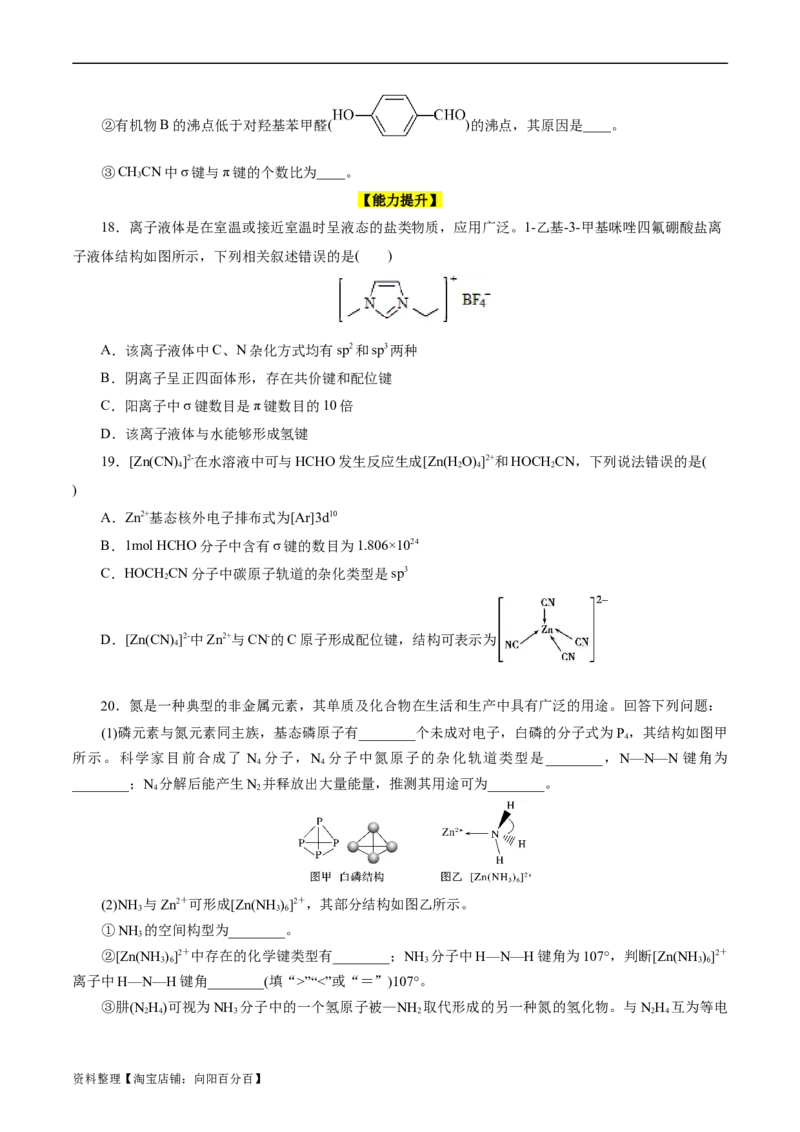
18.离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。1-乙基-3-甲基咪唑四氟硼酸盐离
子液体结构如图所示,下列相关叙述错误的是( )
A.该离子液体中C、N杂化方式均有sp2和sp3两种
B.阴离子呈正四面体形,存在共价键和配位键
C.阳离子中σ键数目是π键数目的10倍
D.该离子液体与水能够形成氢键
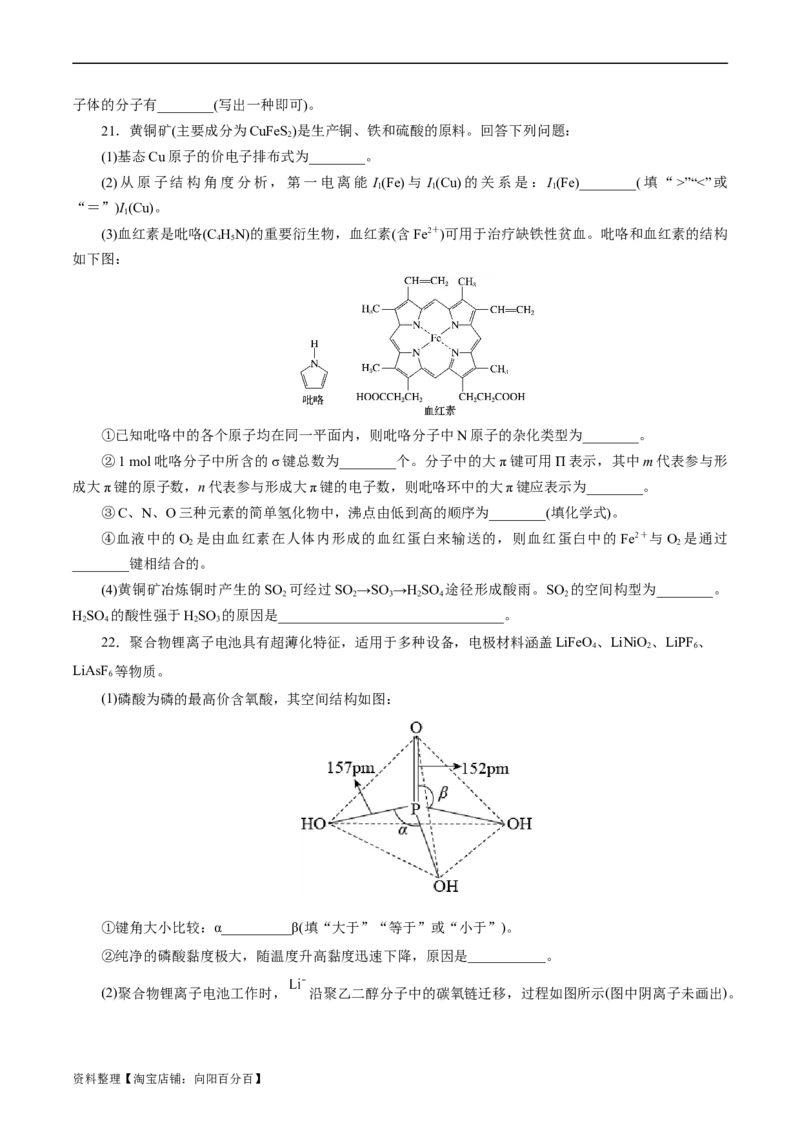
19.[Zn(CN) ]2-在水溶液中可与HCHO发生反应生成[Zn(HO) ]2+和HOCH CN,下列说法错误的是(
4 2 4 2
)
A.Zn2+基态核外电子排布式为[Ar]3d10
B.1mol HCHO分子中含有σ键的数目为1.806×1024
C.HOCH CN分子中碳原子轨道的杂化类型是sp3
2
D.[Zn(CN) ]2-中Zn2+与CN-的C原子形成配位键,结构可表示为
4
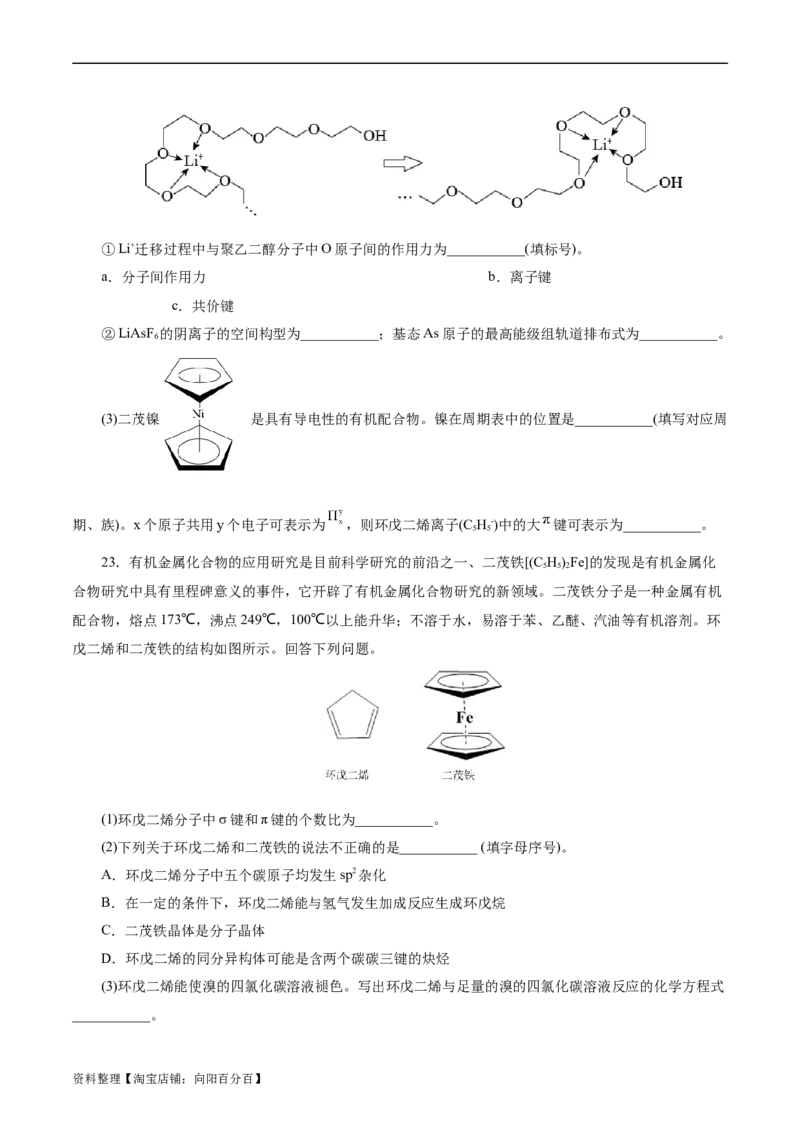
20.氮是一种典型的非金属元素,其单质及化合物在生活和生产中具有广泛的用途。回答下列问题:
(1)磷元素与氮元素同主族,基态磷原子有________个未成对电子,白磷的分子式为P ,其结构如图甲
4
所示。科学家目前合成了 N 分子,N 分子中氮原子的杂化轨道类型是________,N—N—N 键角为
4 4
________;N 分解后能产生N 并释放出大量能量,推测其用途可为________。
4 2
(2)NH 与Zn2+可形成[Zn(NH )]2+,其部分结构如图乙所示。
3 3 6
①NH 的空间构型为________。
3
②[Zn(NH )]2+中存在的化学键类型有________;NH 分子中H—N—H键角为107°,判断[Zn(NH )]2+
3 6 3 3 6
离子中H—N—H键角________(填“>”“<”或“=”)107°。
③肼(N H)可视为NH 分子中的一个氢原子被—NH 取代形成的另一种氮的氢化物。与NH 互为等电
2 4 3 2 2 4
资料整理【淘宝店铺:向阳百分百】子体的分子有________(写出一种即可)。
21.黄铜矿(主要成分为CuFeS)是生产铜、铁和硫酸的原料。回答下列问题:
2
(1)基态Cu原子的价电子排布式为________。
(2)从原子结构角度分析,第一电离能 I(Fe)与 I(Cu)的关系是:I(Fe)________(填“>”“<”或
1 1 1
“=”)I(Cu)。
1
(3)血红素是吡咯(C HN)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构
4 5
如下图:
①已知吡咯中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类型为________。
②1 mol吡咯分子中所含的σ键总数为________个。分子中的大π键可用Π表示,其中m代表参与形
成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为________。
③C、N、O三种元素的简单氢化物中,沸点由低到高的顺序为________(填化学式)。
④血液中的O 是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的 Fe2+与O 是通过
2 2
________键相结合的。
(4)黄铜矿冶炼铜时产生的SO 可经过SO →SO →HSO 途径形成酸雨。SO 的空间构型为________。
2 2 3 2 4 2
HSO 的酸性强于HSO 的原因是________________________________。
2 4 2 3
22.聚合物锂离子电池具有超薄化特征,适用于多种设备,电极材料涵盖LiFeO 、LiNiO 、LiPF 、
4 2 6
LiAsF 等物质。
6
(1)磷酸为磷的最高价含氧酸,其空间结构如图:
①键角大小比较:α__________β(填“大于”“等于”或“小于”)。
②纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是___________。
(2)聚合物锂离子电池工作时, 沿聚乙二醇分子中的碳氧链迁移,过程如图所示(图中阴离子未画出)。
资料整理【淘宝店铺:向阳百分百】①Li+迁移过程中与聚乙二醇分子中O原子间的作用力为___________(填标号)。
a.分子间作用力 b.离子键
c.共价键
②LiAsF 的阴离子的空间构型为___________;基态As原子的最高能级组轨道排布式为___________。
6
(3)二茂镍 是具有导电性的有机配合物。镍在周期表中的位置是___________(填写对应周
期、族)。x个原子共用y个电子可表示为 ,则环戊二烯离子(C H-)中的大 键可表示为___________。
5 5
23.有机金属化合物的应用研究是目前科学研究的前沿之一、二茂铁[(C H)Fe]的发现是有机金属化
5 5 2
合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。二茂铁分子是一种金属有机
配合物,熔点173℃,沸点249℃,100℃以上能升华;不溶于水,易溶于苯、乙醚、汽油等有机溶剂。环
戊二烯和二茂铁的结构如图所示。回答下列问题。
(1)环戊二烯分子中σ键和π键的个数比为___________。
(2)下列关于环戊二烯和二茂铁的说法不正确的是___________ (填字母序号)。
A.环戊二烯分子中五个碳原子均发生sp2杂化
B.在一定的条件下,环戊二烯能与氢气发生加成反应生成环戊烷
C.二茂铁晶体是分子晶体
D.环戊二烯的同分异构体可能是含两个碳碳三键的炔烃
(3)环戊二烯能使溴的四氯化碳溶液褪色。写出环戊二烯与足量的溴的四氯化碳溶液反应的化学方程式
___________。
资料整理【淘宝店铺:向阳百分百】(4)已知环戊二烯阴离子(C H )的结构与苯分子相似,具有芳香性。二茂铁[(C H)Fe]晶体中存在的微
5 5 5 2
粒间的作用力有___________(填字母序号)。
a.离子键 b.σ键 c.π键 d.氢键 e.配位键
(5)钴的一种配位聚合物的化学式为{[Co(bte) (H O) ](NO )}。其中bte的分子式为C HN,其结构简
2 2 2 3 2 n 6 8 6
式为 。
①[Co(bte) (H O) ]2+中,与Co2+形成配位键的原子是____和____(填元素符号)。
2 2 2
②C、H、N的电负性从大到小顺序为____。
③bte分子中碳原子轨道杂化类型为____和____。
④1mol bte分子中含 键的数目为____mol。
资料整理【淘宝店铺:向阳百分百】